壳聚糖镍配合物对尿素吸附性能研究
李小芳,冯小强,伏国庆,杨 声,*
(1.天水师范学院生命科学与化学学院,甘肃天水 741001; 2.天水市中医医院化验科,甘肃天水 741001)
壳聚糖镍配合物对尿素吸附性能研究
李小芳1,冯小强1,伏国庆2,杨 声1,*
(1.天水师范学院生命科学与化学学院,甘肃天水 741001; 2.天水市中医医院化验科,甘肃天水 741001)
合成了壳聚糖和金属元素Ni的配合物,通过红外光谱(I R)和紫外吸收光谱做了表征,并研究了壳聚糖-Ni对尿素的吸附性能,探讨了尿素初始质量浓度、反应pH、温度及时间对吸附量的影响。结果发现,壳聚糖-Ni配合物对尿素具有很好的吸附能力,当尿素溶液的初始浓度为 3.5mg/mL,反应温度为 20℃,pH为 6.0,反应时间为 10h时,壳聚糖-Ni对尿素的吸附性能最好。
壳聚糖镍,尿素,吸附
1 材料与方法
1.1 材料与仪器
壳聚糖 水溶性,60目,济南海德贝海洋生物工程有限公司;氯化镍、尿素、对二甲氨基苯甲醛 均为分析纯;显色剂 称取 2.00g对二甲氨基苯甲醛,溶于 100mL无水乙醇中,再加入 10mL浓 HCl,混匀;尿素标准溶液 准确称取尿素 0.5000g,溶于 1000mL容量瓶内,用蒸馏水稀释至刻度,此溶液尿素含量为0.5000mg/mL。
UV-2450紫外吸收仪 日本岛津;9200型UV-vis分光光度计 北京瑞利;PHS-3D精密 pH计 上海精科;Spectrum One傅立叶红外光谱仪 Perkin E lmer;RF-5301PC型荧光分光光度计。
1.2 壳聚糖-N i配合物的制备
将 0.5g壳聚糖、0.5g氯化镍加入到 50mL 1.0%乙酸中,用氨水调 pH至 4.5左右,磁力搅拌器上80℃恒温搅拌 3h,冷却至室温,混合物倒入200mL丙酮中,过滤,沉淀用 200mL 95%乙醇洗涤,再用200mL去离子水洗涤,60℃真空干燥至恒重。
1.3 配合物对尿素的吸附
1.3.1 标准曲线的绘制[7]准确吸取 0.5000mg/mL的尿素标准溶液 0.00、2.00、4.00、6.00、8.00、10.00、12.00mL于 25mL比色管中,分别准确加入显色剂10.00mL,用蒸馏水稀释至刻度,充分摇匀;放置20min,待气泡完全消失后,用 1cm比色皿,在波长420nm处,以试剂空白作参比,用分光光度计进行比色测定。以所含尿素质量为横坐标,对应的吸光度为纵坐标,绘制标准曲线。
1.3.2 配合物对尿素的吸附 称取 1.0g壳聚糖-Ni于一定质量浓度的 100mL尿素溶液中,调节溶液的pH,在一定温度下搅拌反应一定时间后,用移液管吸取 1.0mL上清液置于 5.0mL容量瓶中,准确加入2.0mL对二甲氨基苯甲醛显色剂。以试剂空白作参比,测定 420nm处的吸光度值,计算尿素含量。
1.3.3 吸附量的计算 在 100mL尿素溶液中加入1.0g吸附剂,搅拌反应一段时间,测定吸附前后溶液中尿素质量浓度的变化,按下式计算吸附量Q:

式中:V为尿素溶液的体积,mL;W为吸附剂的干重,g;C0为吸附前溶液的质量浓度,mg/mL;C为吸附后溶液的质量浓度,mg/mL;Q为吸附量,mg/g。
2 结果与讨论
2.1 壳聚糖-N i配合物表征2.1.1 红外光谱 采用 KBr压片法测定壳聚糖和壳聚糖 -Ni的红外光谱,如图 1所示。壳聚糖在3445.74cm-1处的强吸收峰是-OH和-NH的特征吸收部分重叠结果;在 1152.84、1083.04、1664.51cm-1处产生了-O-、C-O和乙酰基中C=O的伸缩振动吸收峰;在 893.48cm-1处的吸收峰是伯胺-NH2的吸收带;1599.46cm-1是伯胺 N-H面内弯曲振动强吸收峰;1028.84cm-1归属为伯醇的吸收峰;1325.13cm-1处的较弱的吸收峰是由C-N键的伸缩振动引起的。壳聚糖-Ni在 1634.12cm-1有新的吸收峰出现,表明 C2上的胺基或乙酰胺基与 Ni发生了配位;壳聚糖1421.15cm-1处-OH的弯曲振动逐渐消失,表明-OH也参与了配位。
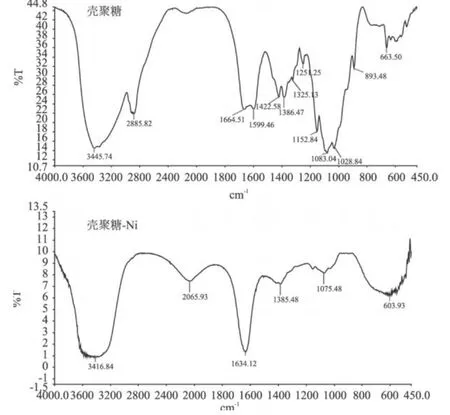
图 1 壳聚糖和壳聚糖-Ni配合物的红外光谱
2.1.2 壳聚糖-Ni(II)配合物的紫外吸收光谱 用1.0%HCl溶解壳聚糖和壳聚糖-Ni(II)配合物,进行紫外光谱扫描。由图 2可知,壳聚糖在 222nm有吸收,而 CS-Ni(II)配合物有三个吸收峰,分别在 220、245、392nm,这是由于配合物中 n-p*跃迁及氧氮孤对电子发生 n-S*跃迁的结果。紫外吸收光谱说明,壳聚糖与镍发生了配位作用。

图 2 壳聚糖和壳聚糖-Ni(II)配合物的紫外吸收光谱
2.2 配合物对尿素的吸附
2.2.1 标准曲线的绘制 尿素的质量和 OD420nm满足线性关系:Y=-0.171+0.25457X(R=0.99908),其中,Y是 OD420nm,X是尿素的质量 (mg)。

图3 尿素吸附的标准曲线
2.2.2 尿素初始质量浓度对吸附量的影响 取尿素初始质量浓度分别为 0.5、1.0、1.5、2.0、2.5、3.0、3.5mg/mL,在 pH为 5.0,40℃搅拌吸附 6h的条件下,研究尿素初始质量浓度对吸附量的影响,结果如图 4所示。吸附量随尿素起始质量浓度的增大而增加,这是因为可供配合物中Ni(II)的空余 d轨道吸附尿素的量在逐渐增加的缘故。当尿素起始浓度为3.5mg/mL时,吸附量达到最大,这表明配合物中已基本没有空余 d轨道存在,吸附已基本达到饱和。故本文选择最佳的尿素起始浓度为 3.5mg/mL。
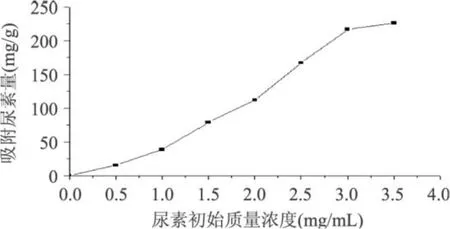
图 4 尿素初始质量浓度对吸附量的影响
2.2.3 pH对吸附量的影响 取 pH分别为 3.5、4.0、4.5、5.0、5.5、6.0、6.5,尿素初始质量浓度为 3.5mg/mL,在 40℃搅拌吸附6h的条件下研究pH对吸附量的影响,结果如图 5所示。可以看出,当 pH从 3.5增大至6.0时,吸附量达到最大值 169.58mg/mL,而后随着pH的继续增加,吸附量反而降低,因此确定最佳 pH为6.0。

图5 pH对吸附量的影响
2.2.4 反应温度对吸附量的影响 取反应温度分别为 20、30、40、50、60、70℃,在尿素初始质量浓度为3.5mg/mL,pH为 6.0,搅拌吸附 6h的条件下,研究反应温度对吸附量的影响,结果如图 6所示。可以看出,随温度升高,对尿素的吸附量减小,这是由于壳聚糖-Ni随着温度的升高其溶解性增加,导致吸附量下降,因此确定最佳反应温度为 20℃。

图6 反应温度对吸附量的影响
2.2.5 反应时间对吸附量的影响 取反应时间分别为1、2、4、6、7、8、10h,在尿素初始质量浓度为 3.5mg/mL, pH为 6.0,20℃搅拌吸附的条件下,研究反应时间对吸附量的影响,结果如图 7所示。可以看出,随反应时间的延长,对尿素的吸附量逐渐增加,10h时吸附量基本趋于稳定,因此选择最佳反应时间为 10h。

图7 反应时间对吸附量的影响
3 结论
壳聚糖-Ni配合物对尿素具有很好的吸附能力,当尿素溶液的初始浓度为 3.5mg/mL,反应温度为20℃,pH为 6.0,反应时间为 10h时,壳聚糖-Ni对尿素的吸附性能最好。
由于壳聚糖-Ni配合物吸附尿素后,配合物的颜色没有发生变化,实验也表明,在吸附尿素的过程中金属离子并不脱落,说明壳聚糖-Ni吸附尿素后,形成 CS-Ni-Ureal配合物,而不是配体完全取代过程,其配位方式有待于进一步研究。壳聚糖-Ni对尿素的吸附容量大,吸附效果较好,主要原料壳聚糖是从生物体内提取的天然高分子化合物,具有良好的生物活性和医药价值,且生物及血液相容性好,因此该产品具有实际应用价值,不但可用于生物医药领域,也可用于食品保健品生产领域,但将其应用于人工肾或作为口服尿素吸附剂还需进一步在人体血液或体内环境下实验各种因素的影响。
[1]Chung Y C,Chen CY.Antibacterial characteristics and activity of acid-soluble chitosan[J].Bioresource Technology,2008,99:2806-2814.
[2]Seyfarth F,Schliemann S,Elsner P.Antifungal effect of highand low-molecular-weight chitosan hydrochloride,carboxymethyl chitosan,chitosan oligosaccharide and N-acetyl-d-glucosamine against Candida albicans,Candida krusei and Candida glabrata [J].International Journal of Phar maceutics,2008,353:139-148.
[3]周永国,齐印阁,王秀娟 .壳聚糖金属离子配合物吸附尿素性能研究[J].中国生物化学与分子生物学报,1999,15(4):677-679.
[4]郎惠平,张秀军 .不同分子量的壳聚糖亚铁配合物的合成及其对尿素的吸附性能[J].食品科学,2005(3):31-34.
[5]任玉兰,马天慧,刘玉敬 .壳聚糖锰配合物对尿素的吸附性能研究[J].化学与生物工程,2005(10):20-22.
[6]杨滋,许牡丹,王亚娟,等 .壳聚糖铜配合物对尿素的吸附性能研究[J].陕西科技大学学报,2008,26:92-94.
[7]丁雪红,刘柏智,牛进 .缓释尿素中尿素含量的测定[J].化肥工业,2005,33(3):35-36.
Study on the adsorption perform ance of chitosan-N i for urea
L I Xiao-fang1,FENG Xiao-qiang1,FU Guo-qing2,YANG Sheng1,*
(1.College ofBiology and Chemistry,TianshuiNor malUniversity,Tianshui 741001,China; 2.Tianshui Traditional ChineseMedical Hospital,Tianshui 741001,China)
Chitosan-N i(II)comp lex was p rep a red,cha rac te rized by FT-IR and UV-Vis absorbance sp ec tra.The adsorp tion of chitosan-N i for urea was s tud ied,the influentia l fac tors such as initia tion concentra tion of urea,pH, reac tion temp e ra ture and reac tion t im e we re d iscussed.The results showed tha t chitosan-N i had good adsorp tion for urea.
chitosan-N i;urea;adsorp tion
TS201.2
A
1002-0306(2010)03-0169-03
尿素是肾功能衰竭和尿毒症患者血液中积蓄的主要毒性成分,高效率的清除尿素一直是生物医学工程领域中人工肾和口服尿素吸附剂研究的重要课题。对尿毒症患者,目前普遍采用的治疗措施是对其进行定期的血液透析以缓解病情,但由于这些常规的吸附剂存在吸附容量低、选择吸附性差、生物和血液相容性不好等缺点,使人工肾和口服尿素吸附剂的应用受到限制,因此研制一种高吸附性、无毒副作用、生物相容性好、选择性高的新型尿素吸附剂成为人们关注的热点。壳聚糖 (CS)是从虾、蟹壳中提取的无毒天然高分子材料,能有效抑制细菌和真菌的生长[1-2],在生物医学领域具有广阔的应用前景。壳聚糖与过渡金属反应形成的配合物也可用于尿素的吸附,这是由于尿素分子的-CO-和-NH2可在过渡金属的 d轨道上配位,比壳聚糖自身大大提高了吸附尿素的容量和选择性。壳聚糖 -Zn(II)[3], Fe(II)[4],Mn(II)[5],Cu(II)[6]金属配合物对尿素吸附的研究已经有报道,但是,壳聚糖-Ni配合物对尿素吸附性能的研究几乎没有报道,且金属镍离子具有抗炎、杀菌、抗癌、抗凝血、镇痛等药理作用,将两种具有生物活性的物质通过共价键键联,得到的目标化合物能发挥两者的独特性能或协同效应。因此,本文合成了壳聚糖-Ni配合物,通过红外光谱、紫外光谱等方法对配合物进行了表征,研究了它对尿素的吸附性能,为进一步开发壳聚糖和新型尿素吸附剂提供了重要的科学依据。
2009-04-28 *通讯联系人
李小芳 (1983-),女,硕士研究生,从事天然高分子活性研究。
甘肃天水师范学院物理无机化学重点学科基金资助。

