载Fe(Ⅲ)树脂除氟性能的研究
吴程程, 田浩廷, 赵雅萍
(华东师范大学 环境科学系,上海 200062)
载Fe(Ⅲ)树脂除氟性能的研究
吴程程, 田浩廷, 赵雅萍
(华东师范大学 环境科学系,上海 200062)
研究了Fe(Ⅲ)改性大孔磺酸型树脂对饮用水中氟离子的吸附特性.氟在载Fe(Ⅲ)树脂上的吸附不随pH的变化而变化,该吸附剂对氟的饱和吸附量随温度的升高而增加,吸附热力学方式符合Langmuir和Freundlich吸附等温式,吸附动力学符合Elovich和准二级动力学模型,而且代表性竞争离子对氟在树脂上的吸附无明显影响.在动态实验中,吸附剂展示了良好的动力学性能.结果表明载Fe(Ⅲ)树脂是一种很有前景的除氟吸附剂.
氟离子; 吸附; 载Fe(Ⅲ)树脂; 影响因素
0 引 言
世界上的许多地方都存在高氟地下水,严重威胁着人类的健康.长期饮用含氟高于1.5 mg·L-1的水,易患斑齿病[1];如水中含氟量高于4mg·L-1时,可导致氟骨病;世界卫生组织对饮用水中氟含量的建议值为1.5 mg·L-1[2],我国饮用水卫生标准规定为1.0mg·L-1.
随着人类对环境和健康的重视,含氟饮用水越来越受到人们的关注,国内外对如何处理含氟饮用水进行了大量的研究.常用的去除含氟水中氟离子(F-)的方法有吸附法、离子交换法[3]、化学沉淀法[4]、电絮凝法[5]和电渗析法[6].在这些方法中,吸附法操作简便,故应用最为广泛.最常见的吸附剂为活性氧化铝[7,8],由于其成本低廉在国内外被广泛应用.但活性氧化铝的处理能力较低,对pH值的要求较高,易受干扰离子的影响,再生后对F-的去除率有所降低,再生时间长,且易产生污泥[9].近年来,许多学者致力于寻找附着在活性氧化铝上的低成本物质,能够对F-有很好的吸附效果.Shihabudheen等[10]在活性氧化铝上载氧化镁,合成一种新颖的吸附剂,虽然克服了处理能力低等缺点,但是对pH的要求仍然较高.为此人们又研究开发另一种改性后的吸附剂——载金属鳌合离子交换剂.目前已经有专利文献[11]研究了作为氟离子选择性吸附剂的载金属(La和Al)的离子交换树脂,其中载La(Ⅲ)螯合树脂对氟的饱和吸附容量为3.78 mg·g-1,且pH对除氟率无影响.结合相关学者的研究结果,本文提出用载Fe(Ⅲ)的大孔钠离子磺酸型树脂通过配位体交换原理去除饮用水中的氟离子.实验研究表明,载Fe(Ⅲ)树脂对铁的负荷量大,具有良好的稳定性,作为净水材料不会改变原水水质,且对氟具有强烈的选择性吸附,显示出在饮用水除氟方面独特的应用前景.
1 实验部分
1.1 试剂与仪器
大孔Na型磺酸树脂20~60目,购自Sigma Aldrich公司,其它试剂均为分析纯,所用水为去离子水.F-标准储备液的配制:称取2.210 g NaF溶于去离子水中,在容量瓶中定容至1 L,此时溶液中F-浓度为1 000 mg·L-1,将其转移至聚四氟乙烯瓶中0℃保存.
1.2 载铁(Ⅲ)树脂的制备
将500 mL10%的FeCl3溶液转移至1L的容量瓶中,量取50 mL树脂加入瓶中,将其置于恒温振荡器中,45℃振荡48 h,振速为190 r·min-1(HZS-H型,哈尔滨东明医疗仪器厂).称取60.740 7 g乙酸钠再加入到该瓶中,使得Fe3+与CH3COO-的摩尔比为1∶4,继续置于恒温振荡器中振荡24 h.然后将其取出,过滤,用去离子水多次清洗,直至溶液中检测不到Fe3+,放入烘干箱中100℃烘干,装入锥形瓶中待用.
1.3 吸附实验
吸附试验采用静态批次实验完成.称取0.4 g载Fe(Ⅲ)树脂于100 mL锥形瓶,并加入10 mL20 mg·L-1的F-溶液,在室温条件下将其置于恒温振荡器中震荡,震速为190 r·min-1,然后分别考察吸附时间、吸附剂投加量、pH值、F-初始浓度、温度和共存离子等因素对F-去除率的影响.pH和F-的浓度分别用PHS-3C精密pH计(上海雷磁仪器厂)和pH-1型氟离子选择性电极测定(上海罗素科技有限公司).
动态吸附试验采用下向流吸附柱实验完成.量取5 mL3.40 g吸附剂装入层析柱(H×D=22 cm×1.5 cm)中,填装高度为2.87 cm,进水为去离子水配置的F-浓度为20 mg·L-1的NaF溶液,由上而下流经床层.每隔一段时间取样,测定出水中F-浓度,直至床层完全穿透,绘制穿透曲线.室温下研究不同流速(分别为20,30和40 BV·h-1)对氟离子吸附的影响.
2 结果和讨论
2.1 pH值的影响
pH对载Fe(Ⅲ)树脂吸附F-的影响见图1.在pH2~9的范围内,载Fe(Ⅲ)树脂对F-的去除率均高于80%,滤液中剩余的F-浓度均小于0.5 mg·L-1,表明在饮用水的pH范围内,该吸附剂能有效去除饮用水中的高氟,符合饮用水标准1 mg·L-1(GB5749-85).与此对照的是空白树脂对氟离子的去除率可以忽略不计,说明负载的铁对F-有很高的亲和性.另外还考察了不同pH条件下树脂吸附剂上铁的泄漏率,经检测表明,在pH值为2.24~3.38时,铁的泄漏量分别为0.137 8~0.091 3 mg·L-1,pH 值在4~9范围内的铁的泄漏量可忽略不计.铁的泄漏率小于生活饮用水卫生标准规定的铁限值,不会影响处理水的水质.一些研究表明,pH值对活性氧化铝的吸附有显著影响[7,8],活性氧化铝吸附氟在pH值为5~6范围内吸附容量最大.
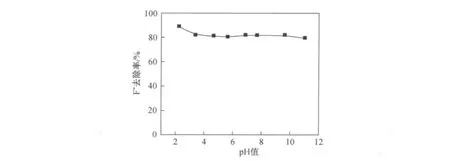
图1 pH值对F-去除率的影响Fig.1 Effect of pH on fluoride removal
2.2 动力学研究
树脂对F-的吸附分两个阶段.第一阶段与F-的外表面吸附相关,吸附速率很快;第二阶段为渐进式吸附,吸附速率变慢直至达到平衡.因为吸附初始阶段树脂表面有大量的活性位点,浓度差造成的传质推动力高,F-可以很容易被树脂吸附.随时间推移,树脂表面堆积大量F-,提供的活性位点减少,阻碍了F-的分子运动,造成非线性吸附[12].298 K时树脂对初始F-浓度为10 mg·L-1的溶液吸附20 min,基本达到吸附平衡,吸附量达0.200 4 mg·g-1;而在初始F-浓度为100 mg·L-1的溶液中,需要120 min左右树脂才能基本达到吸附平衡,吸附量达1.609 1 mg·g-1.这是因为初始F-浓度提高提供了克服液—固相之间传质阻力的推动力,增大了吸附质与吸附剂表面碰撞的机率[13],因此提高了吸附量.常用来描述吸附动力学的模型有Elovich动力学模型、准一级反应模型和准二级反应模型.
Elovich表面反应动力学模型常用于土壤及矿物吸附反应的动力学研究,其表面吸附速率随着吸附量(或覆盖量)的增加呈指数减少,其最简单的形式为[14,15]
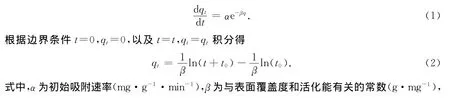

载Fe(Ⅲ)树脂吸附在298 K下不同F-的初始浓度,以及温度为298 K、308 K和318 K时,F-初始浓度为20 mg·L-1.F-的3种动力学拟合结果如图2~7,表1和表2(表中R2为相关系数).Elovich动力学拟合参数中时间常数t0在一定程度上与树脂表面的液膜厚度有关,随着温度的升高,水溶液的粘度减小,从而使得树脂表面的液膜变薄,因此t0逐渐减小.初始吸附常数α随着温度的升高而略有增加,说明初始吸附速率对温度敏感度不是很强.在不同温度下,与表面覆盖度和活化能有关的常数β变化很小,即F-在树脂表面的吸附活化能几乎不随温度而变化[19].
表2中准二级动力学方程计算所得qe与实验测定值更为接近,且相关系数更高,可推测吸附过程符合准二级动力学模型.大多数情况下,准一级动力学方程只能应用于吸附过程的初始阶段而不是整个阶段;而准二级反应动力学模型假定限速步骤可能为化学吸附,适用于很多吸附研究[20].当温度从298 K升到318 K时,准一级和准二级反应的速率常数从0.484 8和1.603 7分别增加到0.603 6和1.925 2.温度升高加快了F-在树脂表面的吸附速率,说明树脂吸附F-为吸热反应.
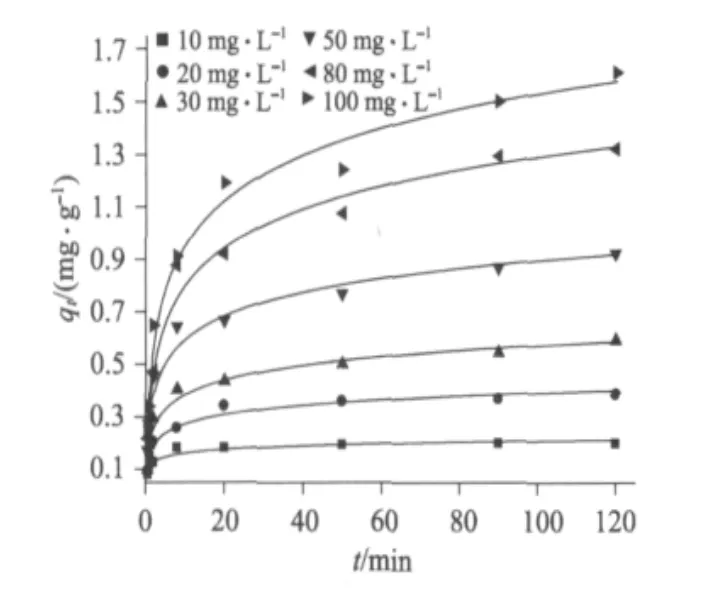
图2 不同初始浓度的Elovich模型Fig.2 Adsorption kinetics described by Elovich equation at various initial fluoride concentrations
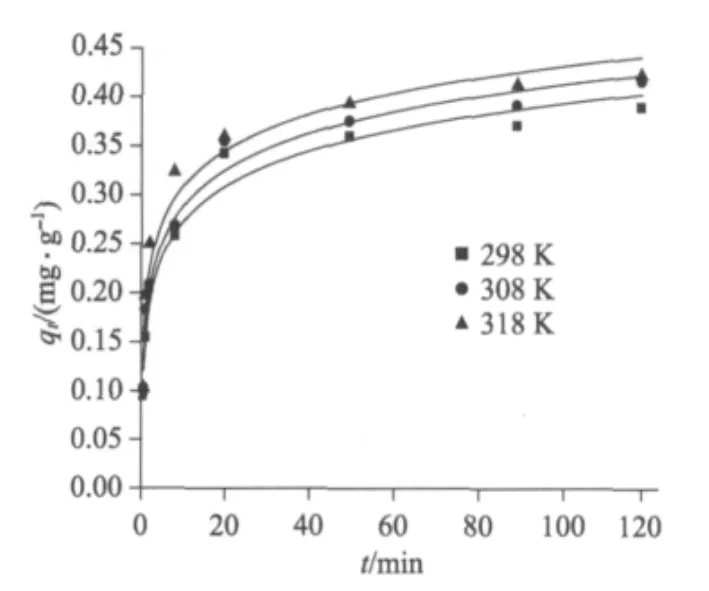
图3 不同温度下的Elovich模型Fig.3 Adsorption kinetics described by Elovich equation at various temperatures
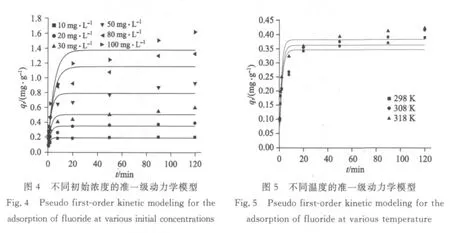
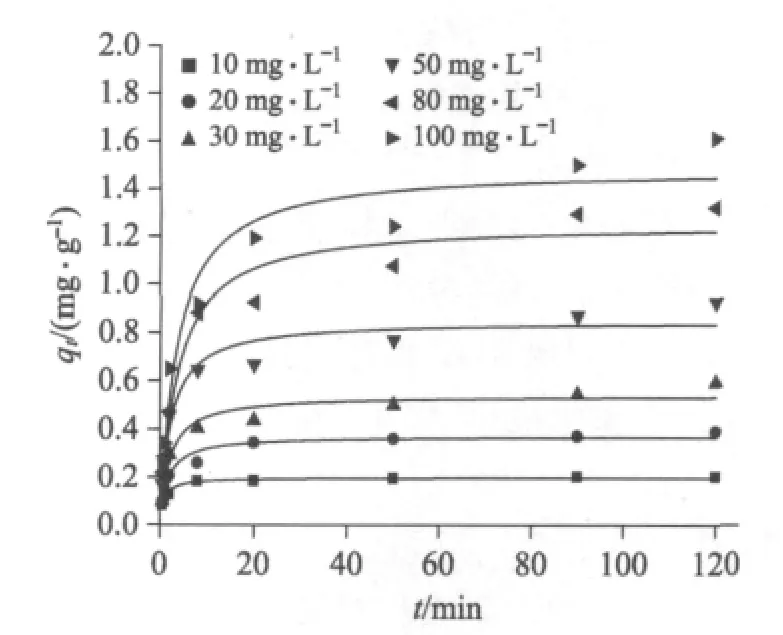
图6 不同初始浓度的准二级动力学模型Fig.6 Pseudo second-order kinetic modeling for the adsorption of fluoride at various initial concentrations

图7 不同温度的准二级动力学模型Fig.7 Pseudo second-order kinetic modeling for the adsorption of fluoride at various temperature
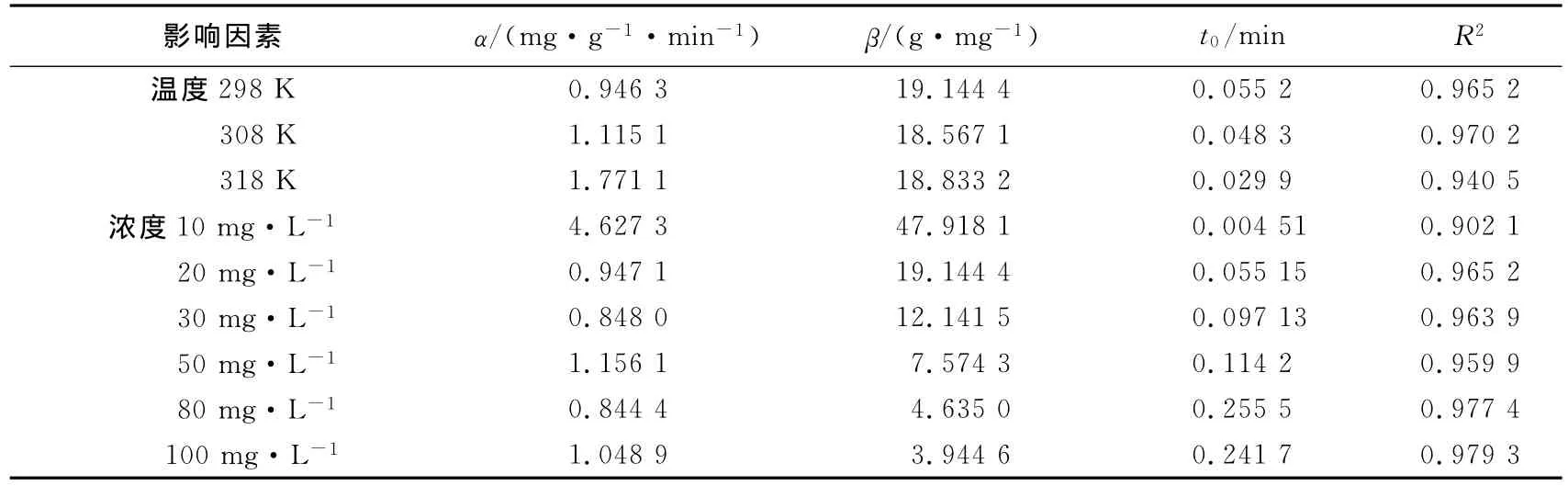
表1 Elovich模型的动力学参数Tab.1 Kinetic parameters of Elovich equation
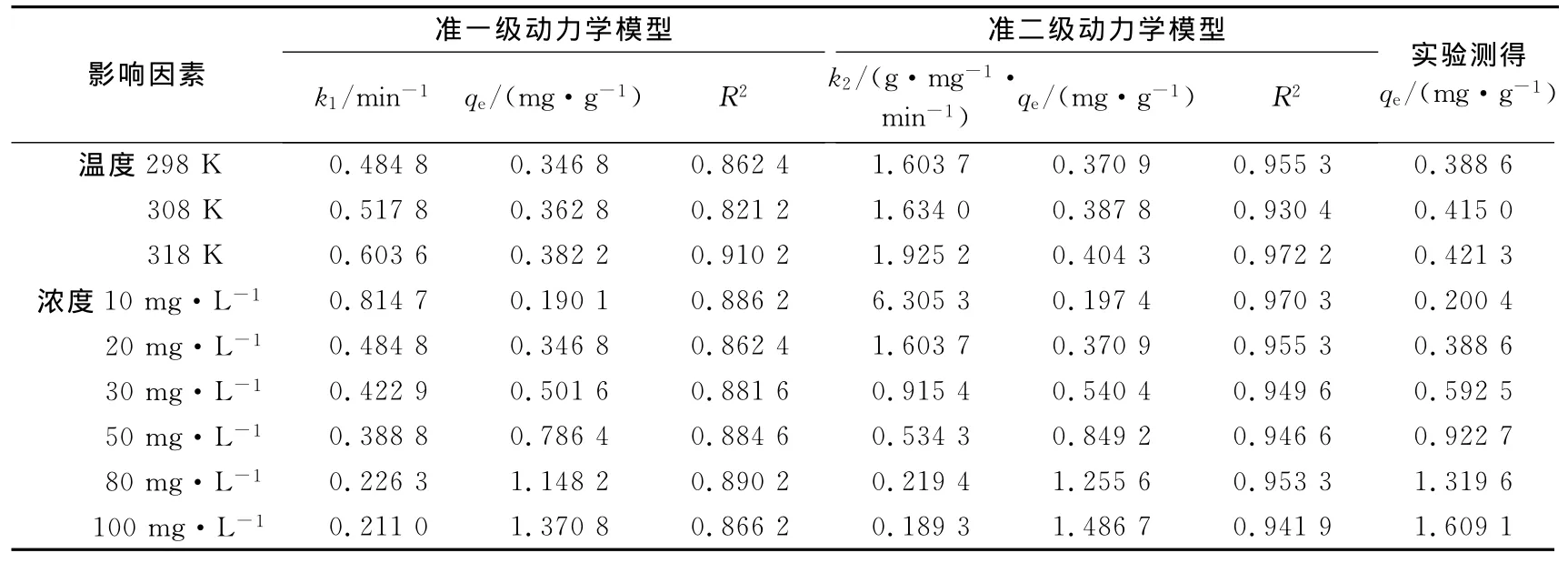
表2 准一级和准二级动力学参数Tab.2 Kinetic parameters of pseudo first and pseudo second-order equations
吸附剂的吸附过程一般认为是由3个连续的步骤完成的.①吸附质通过固体表面液膜向固体外表面的扩散,称为膜扩散(film diffusion).液膜是固体表面的滞留边界层,其厚度和搅拌强度或流速有关.②吸附质在颗粒内部的扩散,由孔隙内溶液中的扩散(pore diffusion)和孔隙内表面上的二维扩散(interior surface diffusion)两部分组成.③吸附质在微孔表面上的吸附反应.吸附过程的总速率按照上述顺序取决于最慢的一步(速率控制步),通常在物理吸附中,第三步“吸附反应”速率很决,迅速在吸附表面各点吸附位点上建立吸附平衡,因此总吸附速率由膜扩散或颗粒内扩散控制.
颗粒扩散控制在很多情况下是有限制条件的,颗粒内扩散方程定义为

式中,ki为颗粒内扩散速率常数(mg·(g·min0.5)-1).其与颗粒内扩散系数D的关系为)

式中,r为颗粒半径(cm).另外,C为截距,C值的大小反映了边界层的厚度,即C值(截距)越大,边界层效应越大.
如果曲线qt对t0.5做图为一条直线且通过原点(即C=0),那么颗粒内扩散过程则是唯一的吸附速率控制步骤.若吸附机理符合颗粒内孔扩散方程,将qt对t0.5作图应为直线,所得直线的斜率即孔扩散速率常数,孔扩散模型拟合曲线如图8所示.由图8可以看出,不同浓度下qt对t0.5呈良好的线性关系,表明孔内扩散过程是树脂吸附氟离子吸附速率的控制步骤,但是直线未通过原点,表明孔内扩散过程并不是该吸附速率唯一的控制步骤,吸附同时受其它因素,如液膜扩散(外扩散)的影响[22].
为了进一步判断膜扩散控制是否是吸附过程的主要限制步骤,用以下Boyd模型对动力学数据进行分析.Boyd动力学表达式如下所示[23]:
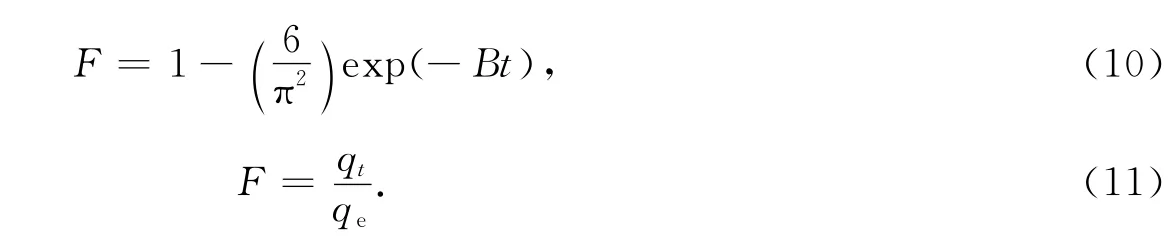
qt为t时的吸附量(mg·g-1);qe为平衡时的吸附量(mg·g-1),F为时间t时的溶质分数.
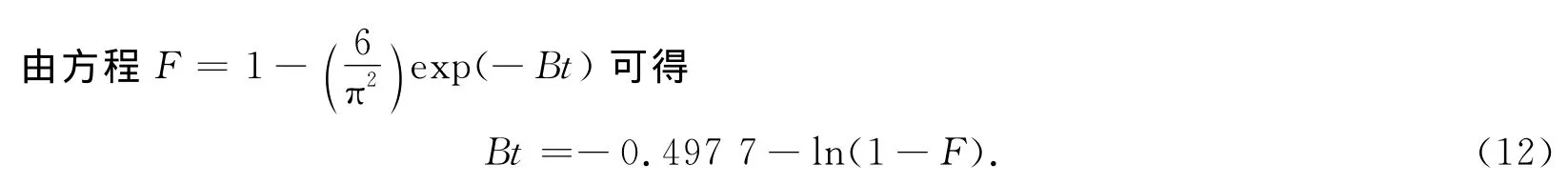
Bt可由上式计算得出.Bt与时间t的关系如图9所示,Bt与t在不同的浓度下呈折线关系,由图8可知,不同浓度下qt对t0.5呈良好的线性关系,表明孔内扩散过程是树脂吸附氟离子吸附速率的主要控制步骤[24].载Fe(Ⅲ)树脂对F-的吸附过程中化学作用非常迅速,一般不是控速步骤,而是受物质传输步骤所控制.由图8可以得知,颗粒内扩散也并不是该吸附速率的唯一控制步骤,吸附同时可能受颗粒外扩散过程(如表面吸附和液膜扩散)的影响[25].
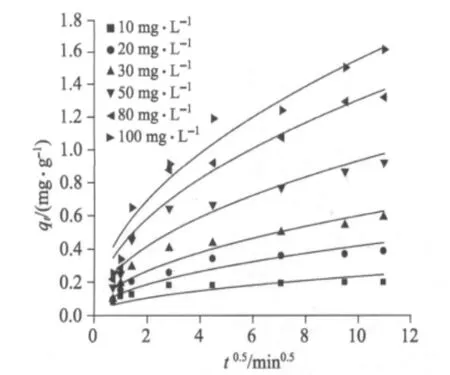
图8 不同浓度的孔扩散模型Fig.8 Intraparticle mass transfer plots for the adsorption of fluoride
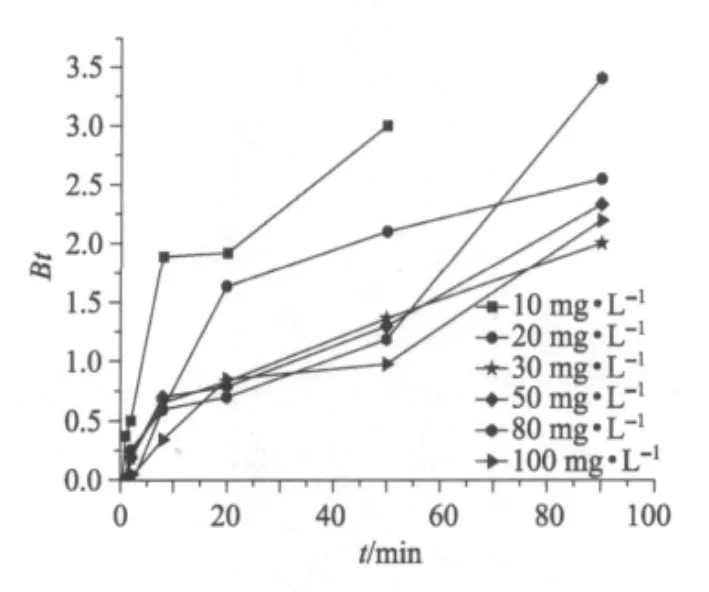
图9 吸附F-的Boyd曲线Fig.9 Boyd plots for the adsorption of fluoride
2.3 热力学研究
不同温度下,载Fe(Ⅲ)树脂对不同初始浓度F-的平衡吸附量见图10.随着温度的升高,氟离子在吸附剂上的吸附容量不断上升.吸附平衡可以采用吸附等温线来描述.在温度固定的条件下吸附达到平衡,吸附剂在固—液两相浓度的关系曲线称为吸附等温线.在吸附平衡研究中,描述吸附等温线的最常用的表达式是Langmuir方程和Freundlich方程.
对单一组份的溶质,水处理中常见的吸附等温线有两种形式,一种是Langmuir吸附等温式,Langmuir吸附等温线[26]的试验数据可写成公式的形式:

q0为每克吸附剂所吸附溶质的极限值,表示单分子层饱和吸附量,mg·g-1;b为与温度、吸附过程焓变有关的常数,L·mg-1.
另一种常用的等温式为Freundlich公式[27],这是一个经验公式,表示为

k是与温度、吸附剂比表面积等因素有关的常数;n是一个与温度等因素有关的常数,通常n>1.
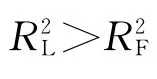

图10 不同浓度的吸附等温线Fig.10 Isotherm plots on various initial concentrations
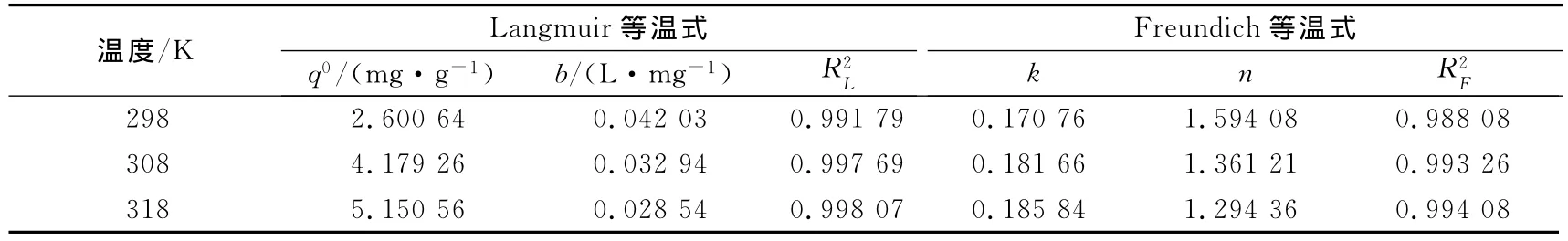
表3 Langmuir和Freundlich吸附常数和相关系数Tab.3 Langmuir and Freundlich constants for fluoride removal
吸附过程的吉布斯自由能变ΔG采用下列方程计算[28]:

式中,ΔG是标准的吸附自由能变化(kJ·mol-1),T 是开尔文温度,R是气体常数(8.314 J·mol-1·K-1).K0是吸附平衡常数,以lg(qe/Ce)对Ce作图,得到的直线斜率即为不同温度下的吸附平衡常数,由此可计算出吉布斯自由能,如表4所示.

表4 热力学参数Tab.4 Thermodynamic parameters for fluoride adsorption
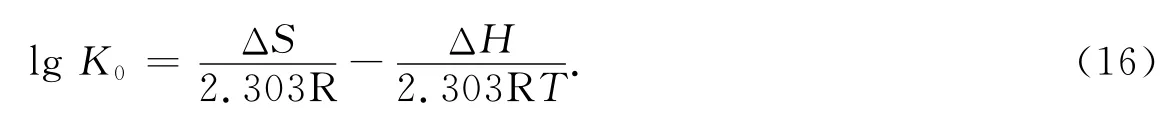
式中,ΔS是吸附过程的熵变(kJ·mol-1·K-1),ΔH 是吸附过程的焓变(kJ·mol-1),以lg K0对1/T×1 000作图.由此可以得到ΔS和ΔH的值,如表4所示.
由表4中的数据可知,ΔG均小于0,说明吸附质倾向于从溶液中吸附到吸附剂表面,反应过程是自发进行的.而且水溶液中的F-在树脂上的吸附焓变ΔH>0,说明此吸附为吸热过程,提高温度有利于吸附的进行.由表4可以看出ΔS>0,这说明F-在树脂上的吸附是熵推动过程,固/液相界面上分子运动更为混乱[31].对于以水为溶剂的体系,由于大多数有机
吸附过程熵变ΔS和吸附焓变ΔH是通过Van’t Hoff方程计算的[30]:物的分子体积远大于水,水分子解吸引起的熵增加远大于F-吸附引起的熵减小[32],故而它们的吸附过程ΔS常常大于0.同时随着温度的提高,吸附熵的绝对值减小,整个体系的自由度增加.
2.4 共存离子的影响
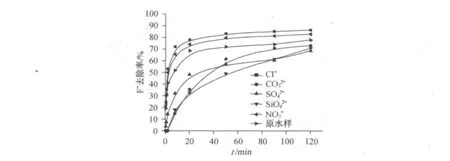
图11 共存离子对F-去除率的影响Fig.11 Effect of common ions on fluoride removal
2.5 动态实验
动态实验中,流速(分别为20,30和40 BV·h-1)对载Fe(Ⅲ)树脂吸附F-的效果见图12.由图可知,其他条件不变的情况下,随着流速的增大,吸附柱床层穿透加快.所以,当进水水质一定时,流速越大,所需床层越大.当流速为20 BV·h-1,床层体积22 BV时出水F-浓度超过1 mg·L-1,102 BV时吸附床层完全穿透,达吸附终点.流速从20 BV·h-1升至40 BV·h-1时,床层完全穿透体积从102 BV降至92 BV.在动态试验初始期阶段,出水中F-浓度小于1 mg·L-1时,符合国家饮用水卫生标准,这是因为在动态试验初期,含氟溶液单向非循环流经树脂床层,树脂的新鲜表面对F-有很强的吸附能力,出水中F-浓度很低.随着树脂表面吸附位为F-占据,出水浓度逐渐升高.之后随着处理时间的延长,出水中F-浓度逐渐升高,逐渐达到稳定,穿透曲线缓慢上升,甚至出现平台,随后吸附剂完全穿透,出水浓度与进水浓度相同,当树脂孔隙填充到一定程度时,毛细管力减弱,孔表面和富集在表面的氟对水中F-的引力也随之减弱,导致氟吸附量减少,水中含氟增加,吸附床层逐渐完全穿透,由于树脂有诸多孔隙,表面吸附的减弱与毛细管浓缩达到平衡,导致出水中F-浓度稳定.陈志刚等人在用膨胀石墨处理含油废水时出现相似的吸附“平台”[33].
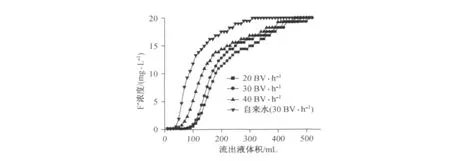
图12 流速对穿透曲线的影响Fig.12 Effect of flow rate on the breakthrough curve
3 结 论
通过Fe(Ⅲ)改性大孔磺酸型树脂吸附含氟饮用水的实验,探讨了此吸附剂的可行性,揭示其动力学反应机理并研究其热力学参数.主要得到以下结论.
(1)该吸附剂在298 K时的静态饱和吸附量达到2.600 6 mg·g-1,约为原沸石除氟容量(0.03 mg·g-1)的86倍,约为活性氧化铝除氟容量(0.8 mg·g-1)的3倍.
(2)吸附动力学结果表明Elovich动力学模型和准二级反应模型都能很好的描述Fe(Ⅲ)改性大孔磺酸型树脂氟吸附过程;孔内扩散拟合结果表明孔内扩散不是吸附速率唯一控制步骤,吸附速率同时受孔内扩散和液膜扩散的影响;通过Boyd动力学方程传质分析可知孔内扩散是主要控制步骤.
(3)Langmuir等温方程能够很好地描述氟吸附平衡特征,吸附是按照单分子吸附模式进行的.
(4)Fe(Ⅲ)改性树脂对氟离子吸附为吸热过程,提高温度有利于吸附的进行.吉布斯自由能△G均小于0,说明反应过程可自发进行的.
(5)通过动态实验可以得知,在其他条件不变的情况下,随着流速的增大,吸附柱床层穿透加快.
致谢:感谢国家自然科学基金(20707006)对本文研究工作的资助.
[1] FAN X,PARKER D J,SMITH M D.Adsorption kinetics of fluoride on lowcost materials[J].Water Res,2003,37:4929-4937.
[2] WHO.Chemical Fact Sheets:Fluoride[M]//Guidelines for Drinking Water Quality(Electronic Resource):Incorporation First Addendum,Recommendations,2006(1):375-377.
[3] VAARAMAA K,LEHTO J.Removal of metals and anions from drinking water by ion-exchange[J].Desalination,2003,155:157-170.
[4] 李雪玲,刘俊峰,李培元.石灰沉淀法除氟的应用[J].水处理技术,2000,26(6):359-361.
LI X L,LIU J F,LI P Y.Principle and application of fluoride removal by lime sedimentation method[J].Technology of Water Treatment,2000,26(6):359-361.
[5] 李静波,赵璇,李福志.电絮凝—微滤去除饮用水中的氟[J].清华大学学报:自然科学版,2007,47(9):1495-1497.
LI J B,ZHAO X,LI F Z.Defluoridation of drinking water using electrocoagulation-microfiltration[J].Journal of Tsinghua University:Science and Technology,2007,47(9):1495-1497.
[6] AMOR Z,BARIOU B,MANERI N,et al.Fluoride removal from brackish water by electrodialysis[J].Desalination,2001,133(3):215-223.
[7] WU Y C,ASCE M.Avtivated alumina removes fluoride ions from water[J].Water and Sewage Works,1978,125:76-82.
[8] CHOI W W,CHEN K Y.The removal of fluoride from waters by adsorption[J].Journal American Water Works Association,1979,71:562-570.
[9] MEENAKSHI,MAHESHWARI R C.Fluoride in drinking water and its removal[J].Journal of Hazardous Materials,2006,B137(1):456-463.
[10] MALIYEKKAL S M,SHUKLA S,PHILIP L,et al.Ehanced fluoride removal from drinking water by magnesiaamended activated alumina granules[J].Chemical Engineering Journal,2008,140(1-3):183-192.
[11] 赵雅萍,祁旭,徐斌.载La(Ⅲ)和载Fe(Ⅲ)氨基膦酸酸型鳌合树脂对氟吸附性能的比较[J].上海环境科学,2004,23(3):96-99.
ZHAO Y P,QI X,XU B.Comparison of fluoride adsorption of La(Ⅲ)and Fe(Ⅲ)carried phosphonoamidic chelating resins[J].Shanghai Environmental Sciences,2004,23(3):96-99.
[12] KENNEDY L J,VIJAYA J J,SEKARAN G,et al.Equilibrium,kinetic and thermodynamic studies on the adsorption of m-cresol onto microand mesoporous carbon[J].Journal of Hazardous Materials,2007,149(1):134-143.
[13] WAN NGAH W S,HANAFIAH M A K M.Adsorption of copper on rubber(Hevea brasiliensis)leaf powder:Kinetic,equilibrium and thermodynamic studies[J].Biochemical Engineering Journal,2008,39(3):521-530.
[14] CHEUNG C W,PORTER J F,MCKAY G.Sorption kinetics for the removal of copper and zinc from effluents using bone char[J].Separation and Purification Technology,2000,1990(1-2):55-64.
[15] ZHANG J S,STANFORTH R.Slow adsorption reaction between arsenic species and goethite(α-FeOOH):Diffusion or heterogeneous surface reaction control[J].Langmuir,2005,21(7):2895-2901.
[16] NATHALIE C,RICHARD G,ERIC D.Adsorption of Cu(Ⅱ)and Pb(Ⅱ)onto a grafted silica:isotherms and kinetic models[J].Water Research,2003,37(13):3079-3086.
[17] HO Y S,MCKAY G .Pseudo-second order model for sorption processes[J].Process Biochem,1999,34(5):451-65.
[18] ÖZACAR M.Equilibrium and kinetic modeling of adsorption of phosphorus on calcined alunite[J].Adsorption,2003,9(2):125-132.
[19] 邓军,施周,许光眉.IOCS吸附锑的动力学及其吸附机理研究[J].工业用水与废水,2009,40(5):19-23.
DENG J,SHI Z,XU G M.Adsorption of antimony on IOCS:kinetics and mechanisms[J].Industrial Water and Wastewater,2009,40(5):19-23.
[20] PRASANNA KUMAR Y,KING P,PRASAD V S R K.Equilibrium and kinetic studies for the biosorption system of Copper(Ⅱ)ion from aqueous solution using Tectona grandis L.f.leaves powder[J].Journal of Hazardous Materials,2006,137(2):1211-1217.
[21] JASSON-CHARRIER M,GUIBAL E,ROUSSY J,et al.Vanadium(Ⅳ)sorption by chitosan:kinetics and equilibrium[J].Water Research,1996,30(2):465-475.
[22] LAZARIDIS N K,ASOUHIDOU D D.Kinetics of sorption removal of chromium(VI)from aqueous solutions by calcined Mg-Al-CO3hydrotalcite[J].Water Research,2003,37(12):2875-2882.
[23] GUPTA V K,ALI I.Removal of DDD and DDE from wastewater using bagasse fly ash,a sugar industry waste[J].Water Research,2001,35(1):33-40.
[24] VADIVELAN V,KUMAR K V.Equilibrium,kinetics,mechanism,and process design for the sorption of methylene blue onto rice husk[J].Journal of Colloid and Interface Science,2005,286(1):90-100.
[25] YANG X Y,OTTO S R,AL-DURI B.Concentration-dependent surface diffusivity model(CDSDM):Numerical development and application[J].Chemical Engineering Journal,2003,94(3):199-209.
[26] LANGMUIR I.The constitution and fundamental properties of solids and liquids[J].J Am Chen Soc,1916,38(11):2221-2295.
[27] FREUNDLICH H M F.Uber die adsorption in losungen[J].Z Phys Chem (Leizig),1906,57A:385-470.
[28] BEHERA S K,KIM J H,GUO X J,et al.Adsorption equilibrium and kinetics of polyvinyl alcohol from aqueous solution on powdered activated carbon[J].Journal of Hazardous Materials,2008,153(3):1207-1214.
[29] SEKAR M,SAKTHI V,RENGARAJ S.Kinetics and equilibrium adsorption study of lead(Ⅱ)onto activated carbon prepared from coconut shell[J].Journal of Colloid and Interface Science,2004,279(2):307-313.
[30] JAGTAP S,THAKER D,WANJARI S,et al.New modified chitosan-based adsorbent for defluoridation of water[J].Journal of Colloid and Interface Science,2009,332(2):280-290.
[31] 刘福强,陈金龙,费正皓,等.复合功能超高交联吸附树脂对氨基萘酚磺酸的静态吸附热力学及动力学[J].应用化学,2003,20(12):1123-1128.
LIU F Q,CHEN J L,FEI Z H,et al.Thermodynamics and kinetics of the adsorption of amino-naphthol sulfonic acid onto a new bi-functional hypercrosslinked polymeric adsorbent[J].Chinese Journal of Applied Chemistry,2003,20(12):1123-1128.
[32] 解建坤,岳钦艳,于慧,等.污泥活性炭对活性艳红K-2BP染料的吸附特性研究[J].山东大学学报:理学版,2007,42(3):64-70.
XIE J K,YUE Q Y,YU H,et al.Adsorptive properties of sludge activated carbon to brilliant red K-2BP[J].Journal of Shandong University:Natural Science,2007,42(3):64-70.
[33] 陈志刚,刘成宝,张勇,等.膨胀石墨对油田含油废水的动态吸附[J].机械工程材料,2006,30(5):81-83.
CHEN Z G,LIU C B,ZHANG Y,et al.Dynamic adsorption of expanded graphite for oil in waste water of oil field[J].Materials for Mechanical Engineering,2006,30(5):81-83.
Performance of fluoride removal by Fe(Ⅲ)-modified resin
WU Cheng-cheng, TIAN Hao-ting, ZHAO Ya-ping
(Department of Environment Science,East China Normal University,Shanghai 200062,China)
Fluoride adsorption on Fe(Ⅲ)modified macroporous sulfonic acid resins has been investigated through batch experiments.The adsorption of fluoride on Fe(Ⅲ)-modified resins is independent of pH value,and the saturated adsorption capacity increase with the increase of temperature.The adsorption thermodynamics follows the Langmuir and Freundlich isotherm.The adsorption kinetic follows Elovich kinetic and the pseudo-second-order kinetic equation.The common foreign ions in drinking water do not obviously influence on the adsorption capacity of fluoride.The adsorbent shows good dynamic performance in column experiments.Results show that the Fe-modified resins would be a promising adsorbent for fluoride removal from drinking water.
fluoride ion; adsorption; Fe(Ⅲ)-modified resin; influence factor
X523
A
10.3969/j.issn.1000-5641.2011.06.005
1000-5641(2011)06-0036-11
2010-11
国家自然科学基金(20707006)
吴程程,女,硕士研究生.E-mail:wccxfkl@126.com.
赵雅萍,女,副教授,研究方向为环境化学.E-mail:ypzhao@des.ecnu.edu.cn.

