用HPLC-MS/MS法同时测定Caco-2细胞单层转运介质中吗替麦考酚酯和麦考酚酸的浓度
余自成,江 涛,瞿江媛,田薇薇,马明华,陈红君,陈红专
(1.上海市杨浦区中心医院临床药学和药理学研究室,上海200090;2.上海交通大学医学院药理学教研室,上海200025)
吗替麦考酚酯(mycophenolate mofetil,MMF)是一种重要的免疫抑制药物,已获准用于预防肾脏、肝脏和心脏移植器官排异反应,作为免疫抑制首选药物在临床广泛应用[1]。MMF为前体药物,口服给药后转变为活性产物麦考酚酸(mycophenolic acid,MPA),发挥免疫抑制作用。本研究建立了HPLC-MS/MS法同时测定转运介质中MMF和 MPA的浓度,用于研究MMF和MPA穿透Caco-2细胞单层的跨膜转运机制,评价P-糖蛋白(P-glycoprotein,P-gp)在两者肠道吸收转运中的作用。
1 仪器和试药
1.1 仪器 Agilent 1200型HPLC仪,包括Quat Pump G1311A四元泵、G1329A自动进样器、G1314B可变波长紫外检测器、G1322A在线真空脱气机和G1316A柱温箱;6410三重串联四极杆LC/MS仪和Mass Hunter工作站软件(美国Agilent公司);BS224S型精密电子天平(北京赛多利斯仪器系统有限公司);Delta 320型pH计(梅特勒-托利多仪器有限公司);XW-80A旋涡混合器(原上海医科大学仪器厂);M型移液器(法国Gilson仪器有限公司);Milli-Q超纯水系统(美国Millipore公司)。
1.2 药品和试剂 吗替麦考酚酯对照品(纯度99.0%,德国罗氏诊断有限公司);麦考酚酸对照品(纯度99.8%,罗氏生物科技公司);吲哚美辛对照品(纯度99.2%美国Sigma-Aldrich公司);D-葡萄糖(英国Biotech Bio Basic公司);4-羟乙基哌嗪乙磺酸(HEPES,高纯度,上海生工生物工程有限公司);甲醇(色谱纯,美国Tedia公司);其他试剂均为分析纯;水为超纯水(上海交通大学医学院自制)。
2 方法和结果
2.1 溶液的配制 (1)MMF储备液:精密称取MMF对照品9.4mg,加二甲亚砜(DMSO)216.8μl溶解,混匀,即得浓度为100mmol/L的MMF对照品储备液。(2)MPA储备液:精密称取MPA对照品6.8mg,加DMSO 212μl溶解,混匀,即得浓度为100mmol/L的MPA对照品储备液。(3)Hank平衡盐溶液(Hanks balanced salt solution,HBSS):精密称取CaCl2140mg、KCl 400mg、KH2PO460mg、MgCl2·6H2O 100mg、NaCl 8g、Na2HPO4、MgSO4·7H2O 100mg、NaHCO3350mg、48mg、D-葡萄糖4.5g和HEPES 5.95g,加超纯水溶解并稀释至1 000ml,用1mol/L的NaOH溶液调节pH至7.4,经0.22μm微孔滤膜过滤,分装,置于4℃冰箱储存备用。(4)吲哚美辛(内标)储备液:精密称取吲哚美辛对照品3.0mg,加DMSO 1.0ml溶解,摇匀,即得浓度为3mg/ml的吲哚美辛储备液。精密移取吲哚美辛储备液50μl,加HBSS溶液稀释至5ml,摇匀,即得30μg/ml的吲哚美辛对照品溶液。(5)样品溶液:取转运介质样品0.1ml,置于1.5ml塑料离心管中,加入内标溶液(30μg/ml)5μl,涡旋振荡30s,混匀,吸取上清液作为样品溶液。上述溶液均置-40℃低温冰箱中储存备用。
2.2 色谱条件 色谱柱:Zorbax Eclipse XDB-C18柱(50mm×2.1mm,3.5μm);流动相:A相(甲醇,含0.05%甲酸),B相(水,含0.05%甲酸);梯度洗脱:0~3.60min,40%A,流速:0.3ml/min,3.61~7.00min,65%A,流速:0.6ml/min,7.01~10.00min,40%A,流速:0.6ml/min;柱温:30℃。2.3 质谱检测条件 采用电喷雾离子源(ESI),离子源温度100℃,毛细管电压4.0kV,去溶剂气温度350℃,去溶剂气流速9.0L/min,碰撞气为N2,雾化气压力206.9kPa,离子驻留时间均为200ms。检测方式为多种反应监测(MRM),用于定量分析监测的离子反应为MMF:m/z 433.8→194.8,离子极性为正离子,锥孔电压150V,碰撞能量35eV;MPA:m/z319.1→191.0,离子极性为负离子,锥孔电压165V,碰撞能量30eV;吲哚美辛:m/z 356.0→312.1,离子极性为负离子,锥孔电压80V,碰撞能量5eV。
2.4 色谱-质谱行为 在2.2项色谱条件和2.3项质谱条件下,取HBSS溶液,添加MMF对照品、MPA对照品和吲哚美辛对照品的HBSS溶液,以及样品溶液分别进样,在各自的离子通道上采集数据。结果MMF、MPA和内标物的保留时间分别为4.16、6.38和8.49min,色谱峰形较好,能够完全分离,色谱图见图1。

图1 吗替麦考酚酯和麦考酚酸的HPLC-MS/MS谱图Figure 1 HPLC-MS/MS photograms of mycophenolate mofetil and mycophenolic acid
2.5 方法学验证
2.5.1 离子抑制实验 将MMF和MPA分别用甲醇、流动相和HBSS溶液溶解后进样测定,考察离子化过程中由HBSS溶液残留介质效应产生的离子抑制作用。结果发现,不同溶剂对MPA的质谱检测信号影响相似,用甲醇和流动相溶解质谱检测信号强度相同,用HBSS溶液溶解较甲醇和流动相溶解质谱检测信号强度略有下降,但差别不明显,而将HBSS溶液中盐份切换与不切换至废液的质谱检测信号强度相同。但溶剂不同对MMF的质谱检测信号影响差异较大,信号强度由大到小依次为:流动相>甲醇>HBSS溶液。用流动相溶解,质谱检测信号约为用HBSS溶液溶解时的两倍,而将HBSS溶液中盐份切换至废液可以提高检测信号强度。
2.5.2 标准曲线的制备和最低检测浓度 用空白HBSS溶液将MMF和MPA对照品储备液稀释,分别配制成系列浓度为0.01、0.05、0.10、0.50、1.00、5.00、10.00、20.00μmol/L的溶液,按照样品测定方法操作,以内标法定量。以MMF、MPA与内标物峰面积之比(As/Ai)为纵坐标,浓度(c)为横坐标,绘制标准曲线,计算标准曲线方程。MMF和MPA在0.01~20μmol/L范围内有良好线性关系,MMF的标准曲线方程为:As/Ai=-0.035 2+0.394 5 c(r=0.999 1),MPA为As/Ai=0.005 5+0.050 8 c(r=0.999 5)。以信噪比(S/N)≥3为标准,测得MMF和MPA的最低检测浓度分别为0.005、0.001μmol/L。
2.5.3 精密度和回收率实验 用适量空白HBSS溶液将MMF和MPA对照品储备液稀释,配成浓度为0.10、1.50和15.00μmol/L的对照品质控样品,按照2.2项下色谱条件和2.3项下质谱条件,在同一天重复测定5份,计算日内RSD。每天测定1份,连续测定5d,计算日间RSD。利用标准曲线方程计算浓度,以测得浓度与配制浓度的比值计算方法回收率。结果表明,MMF的日内RSD<6.02%,日间RSD<7.27%;3种浓度的回收率分别为(103.2±7.5)%、(97.3±3.1)%和(96.0±3.4)。MPA的日内RSD<8.85%,日间RSD<9.25%;3种浓度的回收率分别为(106.9±1.0)%、(106.0± 5.7)%和(108.4±3.2)(n=5)。
2.5.4 稳定性实验 将MMF和MPA标准质控样品于室温(20℃)放置48h、37℃培养箱放置4h、4℃冰箱放置1周,以及-20℃冰箱放置3个月,测定浓度,评价样品稳定性,结果见表1。
表1 吗替麦考酚酯和麦考酚酸稳定性实验结果Table 1 Results of stability tests of mycophenolate mofetil and mycophenolic acid(n=3,±s,cB/μmol·L-1)
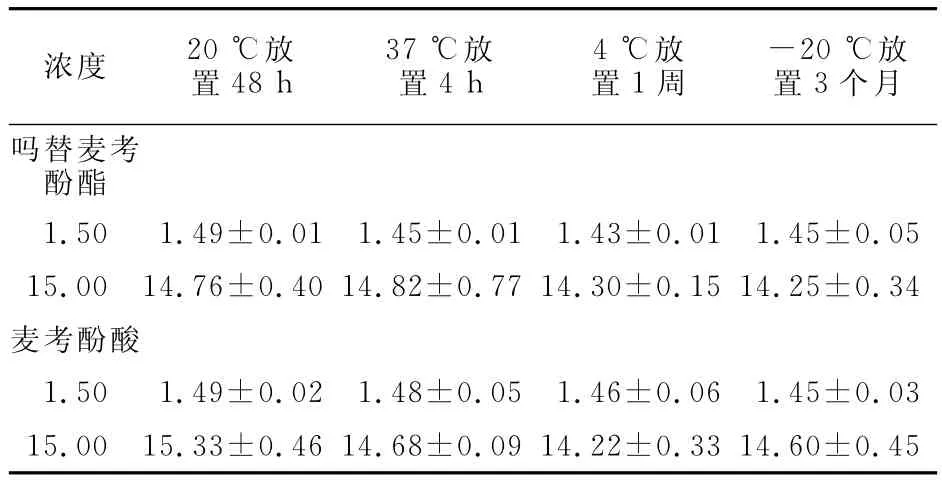
表1 吗替麦考酚酯和麦考酚酸稳定性实验结果Table 1 Results of stability tests of mycophenolate mofetil and mycophenolic acid(n=3,±s,cB/μmol·L-1)
个月吗替麦考酚酯浓度 20℃放置48h 37℃放置4h 4℃放置1周-20℃放置3 1.50 1.49±0.01 1.45±0.01 1.43±0.01 1.45±0.05 15.00 14.76±0.40 14.82±0.77 14.30±0.15 14.25±0.34麦考酚酸1.50 1.49±0.02 1.48±0.05 1.46±0.06 1.45±0.03 15.00 15.33±0.46 14.68±0.09 14.22±0.33 14.60±0.45
3 讨 论
对Caco-2细胞单层转运实验样品的分析通常采用HPLC法[2,3],但是这些检测器灵敏度较低,特别是紫外检测器对多数化合物的检测灵敏度均不够。MS法作为一种新的检测技术,在药物代谢研究中正发挥着越来越重要的作用,特别是HPLC-MS/MS法因具有更好的专属性和灵敏度而被公认为是目前用于生物样品定性和定量分析最为理想的方法。研究者将HPLC-MS/MS法用于Caco-2细胞单层转运实验样品的分析[4,5]。本研究建立了一种具有较高灵敏度和准确度的HPLC-MS/MS方法用于测定Caco-2细胞单层转运实验样品中MMF和MPA的浓度,MMF和MPA理化性质差异较大。通过梯度洗脱的方法,优化梯度条件,实现了在同一色谱条件下对两者的同时检测。本方法测定的线性范围为0.01~20.00μmol/L,能够包括转运实验中所有样品的MMF和MPA浓度,精密度、回收率和稳定性等均能满足分析测定的要求。本研究使用吲哚美辛作为内标物,而未使用与MPA结构相近的丁氧羧基醚化麦考酚酸(MPAC),主要原因是MPAC的离子碎片会给MMF和MPA的含量测定带来离子污染,干扰MMF和MPA低浓度时的测定。由于对照品的量较少,本研究以对照品直接加入二甲亚砜中配制对照品储备液。
转运介质中高浓度盐会导致离子抑制作用,影响检测灵敏度。因此,在分析测定时需要脱盐处理,应在样品进入质谱离子源之前去除无机盐,以避免出现检测信号抑制及离子源污染[6]。离子抑制实验结果表明,HBSS溶液中无机盐的存在对MMF检测有较大影响,对MPA检测影响较小。通过软件系统控制,在样品进入质谱离子源之前使用切换阀可以将HBSS溶液中大部分的盐份切换至废液,显著提高检测信号强度,但残留的少量盐份仍然会导致一定的离子抑制作用。因此为了获得有关MMF、MPA穿过Caco-2细胞单层转运的准确信息,所有样品应维持相同的无机盐含量。
[1] Allison A C,Eugui E M.Mechanisms of action of mycophenolate mofetil in preventing acute and chronic allograft rejection[J].Transplantation,2005,80(2Suppl):S 181-S 190.
[2] Ucpinar S D,Stavchansky S.Quantitative determination of saquinavir from Caco-2cell monolayers by HPLC-UV.High performance liquid chromatography[J].Biomed Chromatogr,2003,17(1):21-25.
[3] Zhou S,Li Y,Kestell P,et al.Determination of thalidomide in transport buffer for Caco-2cell monolayers by high-performance liquid chromatography with ultraviolet detection[J].J Chromatogr B Analyt Technol Biomed Life Sci,2003,785(1):165-173.
[4] Wang Z,Hop C E,Leung K H,et al.Determination of in vitro permeability of drug candidates through a caco-2cell monolayer by liquid chromatography/tandem mass spectrometry[J].J Mass Spectrom,2000,35(1):71-76.
[5] Smalley J,Kadiyala P,Xin B,et al.Development of an on-line extraction turbulent flow chromatography tandem mass spectrometry method for cassette analysis of Caco-2cell based bi-directional assay samples[J].J Chromatogr B Analyt Technol Biomed Life Sci,2006,830(2):270-277.
[6] Hakala K S,Laitinen L,Kaukonen A M,et al.Development of LC/MS/MS methods for cocktail dosed Caco-2samples using atmospheric pressure photoionization and electrospray ionization[J].Anal Chem,2003,75(21):5969-5977.

