用HPLC法测定黄麦合剂中淫羊藿苷含量的不确定度分析
孙 黎,苏克剑,金冠钦(上海交通大学医学院附属仁济医院药剂科,上海200001)
不确定度分析是判定测量结果可信度的依据,有助于评定各种不确定度来源对实验结果的影响,对药物分析检测具有重要意义。测量不确定度是由于测量误差的存在而造成的对被测量值不能确定的程度,是表征合理地赋予被测量值的分散性,与测量结果有关联的参数。作者根据国家质量技术监督局批准发布的JJF1059-1999计量技术规范《测量不确定度评定与表示》与《测量不确定度评定与表示指南》[1],以及有关参考文献,对HPLC法测定黄麦合剂中淫羊藿苷含量的不确定度进行了评估,现报道如下。
1 材 料
1.1 仪器 Waters 1525型HPLC仪、Waters 2487紫外检测器、Waters breeze色谱工作站(美国Waters公司);Mettler AE 240电子天平(Mettler-Toledo公司);5ml移液管,10ml、100ml容量瓶(上海申立玻璃仪器销售有限公司),经检定均为A级。
1.2 药材和试剂 淫羊藿苷对照品(中国食品药品检定研究院,批号121032-200501);黄麦合剂(200ml/支,上海上联药业有限公司,批号20101101);乙腈、乙酸(色谱纯,美国Merck公司);乙酸乙酯(分析纯,江苏省苏州市振亚化工厂,批号20110124);无水碳酸钠(江苏省太仓市美达试剂有限公司,批号20101209);冰乙酸和甲醇均为色谱纯,由美国Tedia公司提供。
2 方法和结果
2.1 色谱条件 色谱柱:Diamonsil-C18柱(250mm× 4.6mm,5μm);流动相:乙腈∶水∶冰乙酸(30∶70∶1);流速:1ml/min;检测波长:270nm;柱温:30℃;进样量:20μl[2]。
2.2 溶液的配制 (1)对照品溶液:精密称取1.0mg淫羊藿苷对照品,置于10ml容量瓶中,用甲醇溶解并定容,配制成浓度为0.1mg/ml的对照品溶液。(2)供试品溶液:取批号为20101101的黄麦合剂20ml,用乙酸乙酯振摇提取3次,乙酸乙酯用量第一次60ml,第二次和第三次均为40ml,合并乙酸乙酯层。取25ml的5%碳酸钠溶液洗涤两次,取乙酸乙酯层,在90℃水浴蒸干,残渣用甲醇溶解并定容至10ml,用0.45μm微孔滤膜过滤,取续滤液,即得供试品溶液。
2.3 标准曲线的制备 取适量0.1mg/ml的淫羊藿苷对照品溶液,倍比稀释,得到系列浓度为3.125、6.250、12.50、25.00和100.0μg/ml的淫羊藿苷对照品溶液,各取20μl,按2.1项下色谱条件测定峰面积。以淫羊藿苷的峰面积(A)对浓度(c)进行线性回归,得到标准曲线方程:A=1.832× 10-5c+0.812(r=0.999 9),表明淫羊藿苷在3.125~100μg/ml浓度范围内线性关系良好。
2.4 方法学考察
2.4.1 精密度实验 精密吸取2.2项下浓度为0.1mg/ml的对照品溶液20μl,连续进样6次,结果测得淫羊藿苷峰面积的RSD为2.45%(n=6)。2.4.2 重复性实验 取2.2(2)项下方法配制的黄麦合剂供试品溶液6份,测定淫羊藿苷峰面积,计算得到RSD=1.13%(n=6)。
2.4.3 加样回收率实验 用移液管精密吸取淫羊藿苷含量已知的黄麦合剂20ml置100ml容量瓶中,分别加入低、中、高3个浓度(9.299、10.299、11.299mg/ml)的淫羊藿苷对照品溶液适量,每个浓度制备3个样品,按2.2项下方法(2)配制得到混合供试品溶液,测定淫羊藿苷的含量并计算回收率。结果低、中、高浓度的淫羊藿苷回收率分别为90.33%、92.54%和95.09%(n=3),平均回收率为(92.65±2.38)%(n=9),符合测定方法学要求。

图1 不确定度分量因果图Figure 1 Causality diagram of uncertainty components
2.4.4 稳定性实验 取2.2(2)项下方法配制的黄麦合剂供试品溶液,分别于配制后0、2、4、6、8h进样测定淫羊藿苷的峰面积,计算得到RSD=2.45%(n=5),表明供试品溶液在配制后8h内稳定性良好。
2.5 样品含量测定 精密量取黄麦合剂样品(批号20101101)20ml,按2.2项下方法(2)制备供试品溶液,连续进样3次,测得其中淫羊藿苷的含量分别为5.350、5.233和5.315μg/ml,均值±标准差为(5.299±0.060)μg/ml(n=3)。
2.6 不确定度分析 根据《测量不确定度评定与表示》(JJF1059-1999)[1],以对照品溶液配制(Cr)、样品制备(Cs)、重复性(R)、拟合回归模型(L)[3]和其他影响因素(F),作为影响HPLC法测定黄麦合剂中淫羊藿苷含量的不确定度的主要因素。根据实验步骤、方法学验证数据、影响结果的因素等,对各不确定分量分别进行计算,流程详见图1。
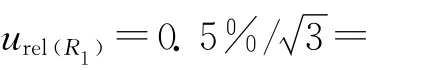



2.6.5 其他影响因素(F)引入的不确定度 由于本实验室的环境处于正常质量控制程序中,温度和湿度波动较小,所以环境温度和湿度的变化对称量和仪器设备稳定性带来的不确定度可忽略不计。
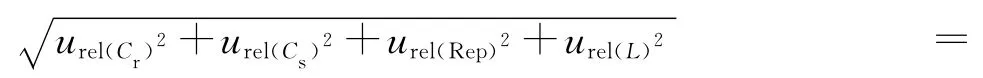
2.6.7 扩展不确定度 测定结果符合正态分布,取置信概率为95%,选择包含因子k=2,得到u=k× urel=2×0.019 3=0.038 6μg/ml。因此HPLC法测得黄麦合剂中淫羊藿苷的含量为(5.299± 0.039)μg/ml,k=2。
3 讨 论
不确定度测量的重要性已得到了广泛的认可,将不确定度测定方法应用于中药材有效成分的定量分析,有助于推动中药标准化的发展。本研究以HPLC法测定黄麦合剂中淫羊藿苷的含量,探讨了此方法不确定度的评定步骤。由计算结果可以看出,检测过程中对不确定度影响最大者是来自于重复性引入的不确定度,其值由精密度测定的不确定度表示,与样品提取步骤较多有密切关系。由此提示研究者在含量测定过程中,需要考虑精化样品提取方法,以提高测定结果的准确性。
[1] 国家质量技术监督局计量司组.测量不确定度评定与表示指南[M].北京:中国计量出版社,2000:1-3.
Measure Department of State Quality and Technology Supervision Bureau.Guide to the evaluation and expression of uncertainty in measurement[M].Beijing:China Metrology Press,2000:1-3.In Chinese.
[2] 马秀建.RP-HPLC法测定气血双生合剂中淫羊藿苷、蛇床子素、五味子甲素与五味子乙素的含量[J].药学与临床研究,2009,17(2):112-114.
Ma XiuJian.Determination of icariin,osthole,deoxyschizan-drin,γ-schizandrin in Qixueshuangsheng mixtures by RP-HPLC[J].Pharm Clin Res,2009,17(2):112-114.In Chinese with English abstract.
[3] 张忠华,陈 玟,许美娟,等.LC-MS/MS法测定人血浆中石杉碱甲浓度的不确定度分析[J].中国药房,2011,22(38):3582-3585.
Zhang ZhongHua,Chen Min,Xu MeiJuan,et al.Analysis of uncertainty measurement of huperzine A content in human plasma by LC-MS/MS[J].China Pharmacy,2011,22(38):3582-3585.In Chinese with English abstract.

