三高调和丸质量标准研究
刘文龙 黄余燕
三高调和丸由丹参、三七、天花粉、泽泻、甘草等组成,其功效为活血消瘀、消食化积、清热生津、扶正驱邪。适用于高血压、高血脂、糖尿病、及脉管炎等症。此次试验的目的是完善三高调和丸质量标准,薄层色谱法(TCL)对处方中的丹参、三七这两种主要药材进行定性鉴别,并采用用高效液相色谱法(HPLC)测定丹参含量。
1 仪器与试药
1.1 仪器 Agilent1100高效液相色谱仪。
1.2 试药 硅胶G由青岛海洋化工有限公司提供批号:080222丹参酮ⅡA对照品(批号:110766-200518,中国药品生物制品检验所)。甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。三高调和丸的制备:三高调和丸为嘉应学院医学院制剂室生产(生产批号:20081118;20081125;20081129)
2 方法与结果
2.1 薄层鉴别
2.1.1 丹参的鉴别
2.1.1.1 供试品溶液的制备 取本品研细,称取细粉10 g,加乙醚30 ml,超声处理10 min,振摇,放置1 h,滤过,滤液挥干,残渣加乙酸乙酯1 ml使溶解,作为供试品溶液。
2.1.1.2 对照品溶液的制备 另取丹参对照药材1 g,同法制成对照药材溶液。再取丹参酮ⅡA对照品,加乙酸乙酯制成2 mg/ml的溶液,作为对照品溶液。
2.1.1.3 阴性对照溶液的制备:取相当于样品量10 g的缺丹参阴性对照样品,按上述供试品溶液制备方法制备丹参阴性对照溶液。
2.1.1.4 薄层色谱分析 照薄层色谱法(《中国药典》(2010年版一部附录VI B)试验[1],吸取上述三种溶液各10 μl,分别点于同一硅胶G薄层板上,以苯-乙酸乙酯(19:1)为展开剂,展开,取出,晾干。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点,在与对照品色谱相应的位置上显相同的暗红色斑点,并且丹参阴性对照未出现斑点。结果见图1。
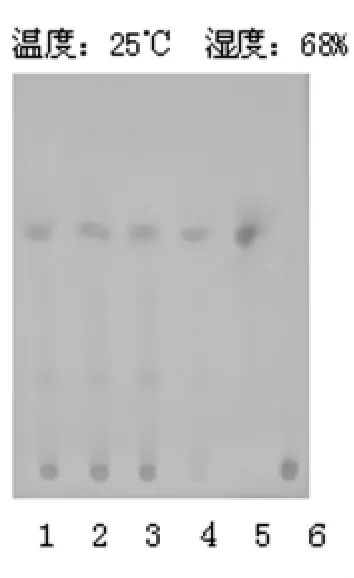
图1
2.1.2 三七的鉴别
2.1.2.1 供试品溶液的制备 取本品研细,称取细粉10 g,加水10 ml使其润湿,搅匀,再加水饱和的正丁醇30 ml,超声处理30 min,滤过,滤液用正丁醇饱和的水洗涤3次,每次10 ml,弃去水层,取正丁醇提取液,蒸干,残渣加甲醇1 ml使溶解,作为供试品溶液
2.1.2.2 对照品溶液的制备 另取三七对照药材0.5 g,同法制成对照药材溶液。再取三七皂苷R1对照品及人参皂苷Rb1、人参皂苷Rg1对照品,加甲醇制成每1 ml各含1 mg的混合溶液,作为对照品溶液。
2.1.2.3 阴性对照溶液的制备 取相当于样品量10 g的缺三七阴性对照样品,按上述供试品溶液制备方法制备三七阴性对照溶液。
2.1.2.4 薄层色谱分析 照薄层色谱法(《中国药典》(2010年版一部附录VI B)试验[1],吸取上述三种溶液各2 μl,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15∶40∶22∶10)10℃以下放置的下层溶液为展开剂,展开,取出,晾干,喷以硫酸乙醇液(1→10),在105℃加热至斑点显色清晰。供试品色谱中,在与对照药材和对照品色谱相应的位置上,显相同颜色的斑点,并且三七阴性对照未出现斑点。结果见图2。
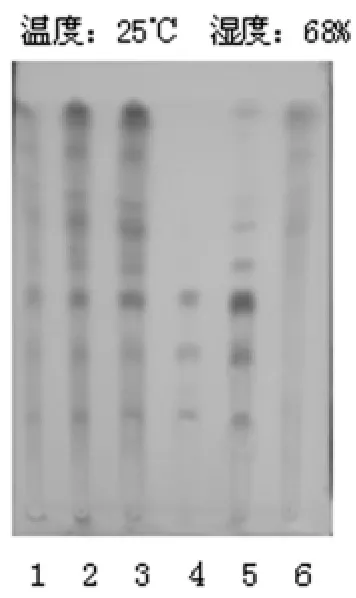
图2
2.2 含量测定
2.2.1 色谱条件与系统适应性试验 色谱柱:Agilent ZORBAX C18 柱(250 mm ×4.6 mm,5μm);流动相:甲醇-水(73∶27);检测波长:270nm;柱温:30℃;理论板数按丹参酮ⅡA峰计算应不低于2000,进样量10 μl。该条件丹参酮ⅡA分离度好,丹参阴性对照无干扰[2]。色谱图见图3。
2.2.2 对照品溶液的制备 取丹参酮ⅡA对照品约10 mg,精密称定,置50 ml棕色容量瓶中,加甲醇制成每1 ml含40 μg的溶液,即得[3]。
2.2.3 供试品溶液的制备 取本品适量研细,取约1 g,精密称定,置具塞棕色瓶中,精密加入甲醇25 ml,密塞,称定重量,超声处理(功率205W,频率33kHz)15 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,置棕色瓶中,即得[4-6]。
2.2.4 阴性对照溶液的制备 取相当于供试品量1 g的缺丹参阴性对照样品,同法制成丹参阴性对照溶液。
2.2.5 标准曲线的制备 精密吸取对照品溶液1、2、5、10、15、20 μl,依次进样测定。以质量Y为纵坐标,峰面积X为横坐标,绘制标准曲线,并进行线性回归。其回归方程和相关系数为:Y=227.22X+1.3829,r=0.9999,丹参酮ⅡA在0.04032~0.8064 μg范围内与峰面积线性关系良好。
2.2.5 精密度试验 精密吸取同一份对照品溶液10 μl,重复测定6次,丹参酮ⅡA的峰面积RSD为0.55%。
2.2.6 重复性试验 取同一批样品(20081129)6份,分别按“2.2.3”项下方法制备,精密吸取10 μl进样,测得样品中丹参酮ⅡA平均含量0.52,RSD为0.74%。
2.2.7 稳定性试验 精密吸取同一份样品溶液10 μl,分别0、2、4、6、8、10 h 测定,RSD 为 0.59%,说明被测溶液在 10 h内基本稳定。
2.2.8 加样回收试验 取已知含量三高调和丸的样品粉末约0.5 g,精密称取共6份,置棕色瓶中,分别精密加入丹参酮ⅡA对照品溶液25 ml,按2.2.3项下方法制备,分别测定,计算回收率,结果见表1。
2.2.9 样品测定 取三高调和丸样品3批,按2.2.3项下方法制备供试品溶液,按上述色谱条件测定。结果见表2。

图3 HPLC色谱图
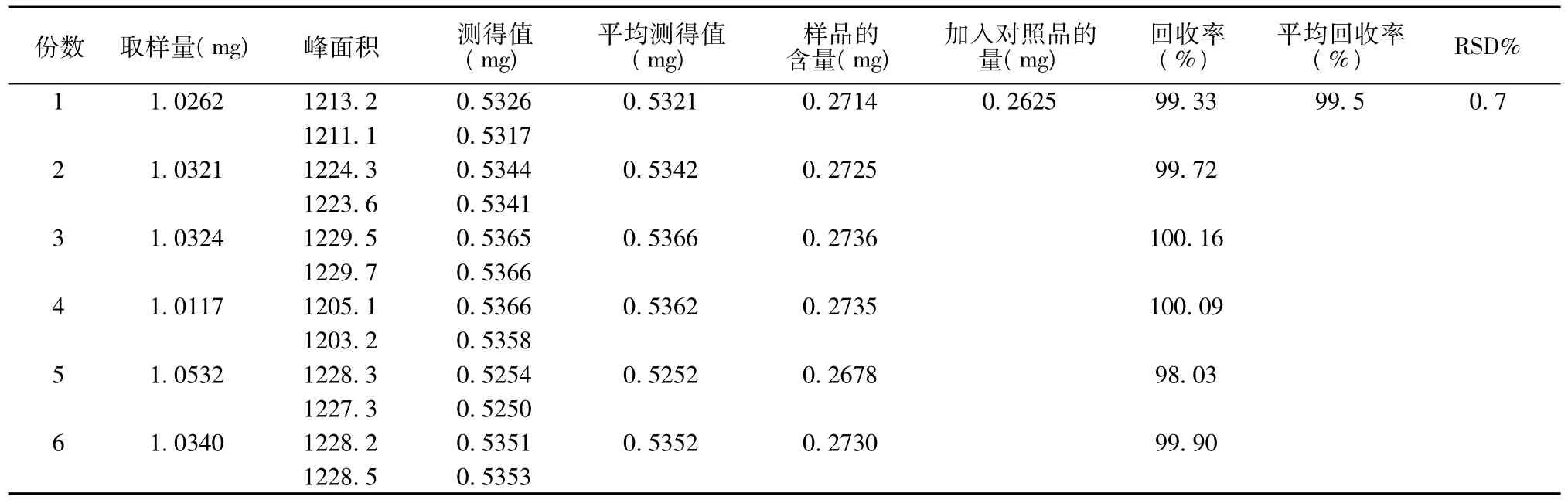
表1 加样回收率试验结果

表2 样品测定结果
4 讨论
4.1 丹参和三七的薄层色谱鉴别操作简单,结果斑点对应性好,阴性对照均无干扰,具有专属性。在不同温度10℃、20℃、30℃及不同湿度,不用同厂家硅胶G薄层板实验结果均一致。
4.2 定量测定参照《中国药典》2010年版一部复方丹参片的方法,简便准确。实验中考察了超声提取时间5、10、15、30 min的提取效果,结果3个超声提取时间含量测定结果基本一致,为保证提取完全同时节省实验时间,最后选择超声时间为15 min。
[1] 国家药典委员会.中国药典(一部).北京:中国医药科技出版社,2010:附录ⅥB.
[2] 张英锋,王燕革,马子川,等.丹参活性化学成分的研究.化学世界,2009,50(10)
[3] 邱丽丽,容蓉,蒋海强,等.高效液相色谱法同时测定丹参提取物中4种成分的含量.分析试验室,2009,28(21).
[4] 蓝天凤.丹参中丹参酮类成分及其含量测定方法研究.山东中医药大学,2011.
[5] 杨东风.丹参药材HPLC指纹图谱及其质量评价研究.西北农林科技大学,2007.
[6] 曹冬.中药丹参及其制剂的质量控制方法研究.河北医科大学,2006.

