安肾丸质量标准研究
谭洪泉,马玉梅,李岩
(1.四平市食品药品检验所,吉林 四平 136000;2.深圳市泰康制药有限公司,广东 深圳 518110;3.吉林省脑科医院,吉林 四平 136000)
安肾丸质量标准研究
谭洪泉1*,马玉梅2,李岩3
(1.四平市食品药品检验所,吉林 四平 136000;2.深圳市泰康制药有限公司,广东 深圳 518110;3.吉林省脑科医院,吉林 四平 136000)
目的:为了更好地控制安肾丸质量,建立了新的安肾丸质量标准。方法:采用HPLC测定安肾丸中苦杏仁苷的含量。采用TLC对制剂中的肉苁蓉、补骨脂、白术分别进行定性鉴别。结果:苦杏仁苷在10.25~512.5 μg线性关系良好,r=0.999 9,平均回收率98.91%,RSD=0.48%。TLC可以鉴别出肉苁蓉、补骨脂、白术的特征斑点。结论:实验方法专属性强、重复性好、准确、简便,可有效地控制安肾丸的质量。
安肾丸;HPLC;TLC;苦杏仁苷
安肾丸收载于《中华人民共和国卫生部药品标准·中药成方制剂》第二册,由巴戟天、肉苁蓉、补骨脂、白术、山药、桃仁等12味中药组成,具有补肾散寒功效。用于肾不纳气,湿寒侵袭引起的梦遗滑精,肾囊湿冷,遗淋白浊,脐腹作痛,精神倦怠,健忘失眠,腰腿酸痛,头晕耳鸣,二便不利[1]。为控制该制剂的内在质量,参照文献[2-4],采用TLC对本制剂中的肉苁蓉、补骨脂、白术分别进行了鉴别。处方中的桃仁主要有活血祛瘀,润肠通便,止咳平喘的功效[5]。桃仁中苦杏仁苷的含量测定方法有高效液相色谱法[6-8]。本研究通过索氏提取器提取出有效成分苦杏仁苷后采用高效液相色谱法测定,本方法专属性强、准确、快速,使产品的质量得到有效的控制,保证了临床疗效。
1 材料
1.1 仪器
Agilengt 1100高效液相色谱仪(配Agilengt 1311A泵、Agilengt 1313A自动进样器、G1314A VWD检测器、G1316A柱温箱);ChemStation色谱工作站;BK-360A超声波清洗机(360 W,济南巴克超声波科技有限公司);梅特勒AG135型电子天平;薄层层析用硅胶G薄层板(青岛海洋生物制品厂),薄层层析用硅胶GF254薄层板(青岛海洋化工厂)。
1.2 试药
安肾丸(北京同仁堂制药有限公司,批号:20120201,20120301,20120601)。苦杏仁苷对照品(批号:110820-201004,含量:93.6%),松果菊苷对照品(批号:111670-200503),毛蕊花糖苷对照品(批号:111530-200706),补骨脂素对照品(批号:110739-200511),异补骨脂素对照品(批号:110738-200309),白术对照药材(批号: 120925-201109),均购自中国食品药品检定研究院。甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 薄层鉴别
2.1.1 肉苁蓉 取安肾丸粉末5 g,加甲醇30 mL,超声处理15 min,滤过,滤液浓缩至近干,残渣加甲醇2 mL使溶解,作为供试品溶液。另取松果菊苷对照品、毛蕊花糖苷对照品,加甲醇分别制成每1 mL含1 mg的溶液,作为对照品溶液。将安肾丸方中去掉肉苁蓉,同法制备和处理作为阴性对照液。照《中国药典》2010版一部附录ⅥB试验,分别吸取上述3种溶液各10 μL,分别点于同一聚酰胺薄层板上,以甲醇-醋酸-水(2∶1∶7)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点,阴性对照中无此荧光斑点,见图1。

1.松果菊苷、毛蕊花糖苷对照品;2~4.安肾丸供试品;5.阴性对照品图1 肉苁蓉薄层鉴别图
2.1.2 补骨脂 取安肾丸研细,称取粉末5 g,加乙酸乙酯20 mL,超声处理15 min,滤过,滤液蒸干,残渣加乙酸乙酯1 mL使溶解,作为供试品溶液。另取补骨脂素对照品、异补骨脂素对照品,加乙酸乙酯制成每1 mL各含2 mg的混合溶液,作为对照品溶液。将安肾丸方中去掉补骨脂,同法制备和处理作为阴性对照液。照《中国药典》2010版一部附录ⅥB试验,吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板上,以正己烷-乙酸乙酯(4∶1)为展开剂,展开,取出,晾干,喷以10%氢氧化钾甲醇溶液,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同的两个蓝白色荧光斑点,而阴性样品溶液在与对照药材和对照品色谱相应的位置上无荧光斑点,见图2。
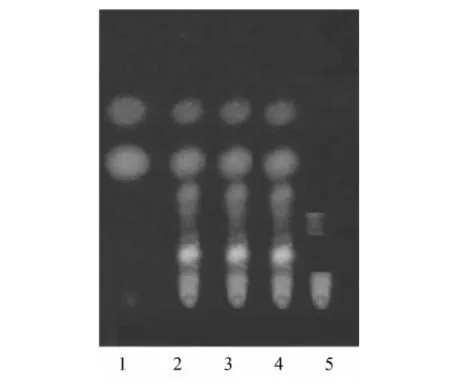
1.补骨脂素、异补骨脂素对照品;2~4.安肾丸供试品;5.阴性对照品图2 补骨脂薄层鉴别图
2.1.3 白术 取安肾丸,研细,称取粉末5 g,加正己烷2 mL,超声处理15 min,滤过,取滤液作为供试品溶液。另取白术对照药材0.5 g,同法制成对照药材溶液。将安肾丸方中去掉白术,同法制备和处理作为阴性对照液。照《中国药典》2010版一部附录ⅥB试验,吸取上述新制备的3种溶液各10 μL,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)乙酸乙酯(50∶1)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,加热至斑点显色清晰。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点,并应显有一桃红色主斑点(苍术酮),而阴性样品溶液在与对照药材色谱相应的位置上无斑点,见图3。

1.白术对照药材;2~4.安肾丸供试品;5.阴性对照品图3 白术薄层鉴别图
2.2 苦杏仁苷的含量测定
2.2.1 色谱条件与系统适用性试验 色谱柱:Agilent TC-C18(250 mm×4.6 mm,5μm)。温度:30℃。流动相:甲醇-水(20∶80)。检测波长:210 nm。进样量:10 μL。理论板数按苦杏仁苷峰计算应不低于3 000。
2.2.2 对照品溶液的制备 精密称取苦杏仁苷对照品10.25 mg,置100 mL容量瓶中,加70%甲醇溶解并稀释至刻度,摇匀,即得每1 mL含苦杏仁苷100 μg的对照品溶液。
2.2.3 供试品溶液的制备 取安肾丸研细,精密称取3.023 6 g,置索氏提取器中,加石油醚(60~90 ℃)50 mL,加热回流3 h,放冷,滤过,弃去石油醚液,药渣及滤纸挥干溶剂,加入70%甲醇50 mL,加热回流3 h,提取液浓缩至5 mL,用50%甲醇定容至100 mL容量瓶中,摇匀,用微孔滤膜(0.45 μm)滤过,即得。
2.2.4 空白试验 按处方比例制成缺桃仁的阴性样品,照2.2.3项下方法制备缺桃仁的阴性对照品溶液,精密吸取10 μL,注入液相色谱仪,按2.2.1项下的色谱条件对阴性对照品溶液进行测定,结果在苦杏仁苷保留时间位置上阴性对照品溶液均未见色谱峰,表明其他药物不干扰指标成分的含量测定,见图4。
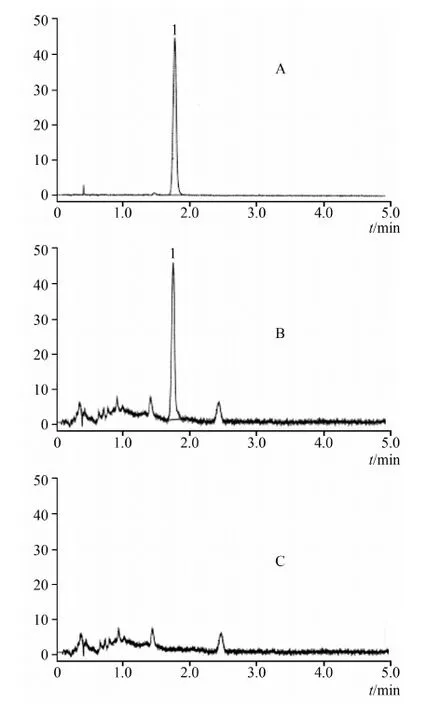
A.苦杏仁苷对照品;B.供试品;C.阴性对照品图4 安肾丸及对照品HPLC图谱
2.2.5 线性关系考察 分别精密量取2.2.2项下的苦杏仁苷对照品溶液1,2,5,10,15,50 μL,注入液相色谱仪,按2.2.1项下的色谱条件,记录峰面积,并以峰面积(Y)对进样量(X)绘制标准曲线,得回归方程Y=14 449X+5.143 8(r=0.999 9),表明苦杏仁苷在10.25~512.5μg与峰面积呈良好的线性关系。
2.2.6 重复性试验 取同一批号(20120201)的安肾丸,平行操作取6份,精密称定,按2.2.3项下供试品溶液的制备方法制备,按2.2.1项下的色谱条件,记录峰面积,以外标法计算含量,结果苦杏仁苷的平均含量为1.83 mg·g-1,RSD=0.58%。
2.2.7 稳定性试验 精密吸取2.2.3项下的样品溶液10 μL,注入液相色谱仪,按2.2.1项下的色谱条件,每隔2 h测量1次,记录峰面积值,得出苦杏仁苷的RSD=0.59%,表明溶液在12 h内保持稳定。
2.2.8 精密度试验 取2.2.2项下的对照品溶液,分别进样6次,每次10 μL,按2.2.1项下的色谱条件进行测定,测得峰面积值,得出苦杏仁苷的RSD=0.98%,表明实验所用仪器精密度良好。
2.2.9 加样回收率试验 取同一批号(20120201)的安肾丸细粉约3.3 g(苦杏仁苷的含量为1.83 mg·g-1)平行操作取6份,精密称定,分别精密加入苦杏仁苷对照品6.04 mg,按2.2.3项下供试品溶液的制备方法制备,记录峰面积,以外标法计算回收率,结果见表1。

表1 苦杏仁苷加样回收率试验
2.2.10 样品含量测定 按上述方法测定3批样品(20120201,20120301,20120601),按上述方法测定苦杏仁苷的含量,结果分别为1.83,1.80,1.85 mg·g-1。
3 讨论
选择有特征斑点和对照品的中药进行定性鉴别,保证了检验结果具有代表性。比较了多种含量测定用供试品的处理方法,参考《中国药典》2010年版一部进行了提取,但由于还有其他中药,样品分析时分离度没有达到要求,说明没有有效地除去杂质,分离不完全。为了目标成分提取完全,我们采用了索氏提取,先用石油醚(60~90 ℃)溶液除去一些杂质,再用70%甲醇提取目标成分,以除去极性强的杂质。建立的高效液相色谱对处理好的样品进行分析,整个样品分析过程杂质峰较少,分离度好,精密度高,重现性及稳定性都很好。
[1] 卫生部.卫生部药品标准·中药成方制剂[S].第二册.1990:105.
[2] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:75.
[3] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:174.
[4] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:95.
[5] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:261.
[6] 王友兰,李红兵,华玉琴.HPLC法测定桃仁中苦杏仁苷的含量[J].中国药师,2002,5(9):550-551.
[7] 韦志英,杨志丽,陆海琳,等.HPLC法测定桃仁配方颗粒中苦杏仁苷的含量[J].广西中医学院学报,2010,13(4):49-50.
[8] 叶晶晶.HPLC法测定不同产地桃仁中苦杏仁苷的含量[J].中华中医药学刊,2011,29(1):206-208.
StudyonQualityStandardforAnshenWan
TAN Hong-quan1,MA Yu-mei2,LI Yan3
(1.SipingInstituteforFoodandDrugControl,Siping136000,China; 2.ShenzhenTaiKangPharmacyCo.,Ltd,Shenzhen518110,China;3.JilinBrainHospital,Siping136000,China)
Objective:To better control the quality of Anshen Wan,establish a new quality standard.Methods:The contents of amygdalin in Anshen Wan were deterrmined by HPLC.Cistanches Herba, Psoraleae Fructus and Atractylodis Macrocephalae Rhizoma were identified by TLC.Results:The resolutons of the determined peaks of Amygdalin were fine at the lineatity range of 10.25~512.5 μg.The average recoveries were 98.91% with RSD 0.48%,for Amygdalin respectively.The characteristic spots of Cistanches Herba, Psoraleae Fructus and Atractylodis Macrocephalae Rhizoma could be detected by TLC.Conclusion:The method is simple,accurate and good in stability,specificity and repeatability,can be used to control quality of Anshen Wan.
Anshen Wan;HPLC;TLC;Amygdalin
2012-10-09)
*
谭洪泉,E-mail:16048034@qq.com

