盐酸克林霉素的核磁共振波谱研究
崔雪红
(天津市捷威动力工业有限公司,天津 300384)
盐酸克林霉素 (Clindamycin Hydrochloride),又称氯林可霉素,氯洁霉素等,于20世纪70年代上市,其抗菌活性强,抗菌谱广,对革兰氏阳性菌有明显抗菌活性。目前国内主要用于人医临床和应用,但在兽药临床上具有广阔的应用前景。该药物化学名为6-(1-甲基-反-4-丙基-L-2-吡咯烷甲酰氨基)-1-硫代-7(S)-氯-6,7,8-三脱氧-L-苏式-α-D-半乳辛吡喃糖苷盐酸盐,已有文献[1]对其进行了结构归属,但部分数据值得商榷,而且所用溶剂为DMSO-d6,对部分信号有掩盖。因此我们选择氘代吡啶作为溶剂(化合物为盐酸盐,吡啶做溶剂较DMSO溶解性更好)重新对其进行了比较全面的波谱表征,并做了详尽的解析和谱峰归属,以期为同类型的有机药物分子的结构鉴定提供一点借鉴。
1 实验部分
1.1 试剂与仪器
盐酸克林霉素由新乡瑞特精细化工有限公司提供(结构式见图1),Pyr-d5为美国CIL公司产品。
核磁共振波谱数据用BRUKER Avance-300核磁共振波谱仪测试,1H和13C NMR及DEPT-135用QNP四核探头检测,1H和13C NMR观测频率分别为300.13MHz和75.47MHz。二维图谱用BBI探头测定。溶剂为 Pyr-d5,兼做1H NMR(δ=8.74ppm)和13C NMR(δ=150.3ppm)内标(均为最低场信号位移数值)。1H NMR谱采样脉冲宽度30°,扫描次数16;13C NMR谱采样脉冲宽度90°,扫描次数10K;DEPT-135扫描次数5K;1H-1H COSY扫描次数为8,采样数据点阵 t2×t1=1024×256;HMQC 和 HMBC 扫描次数均为 8,采样数据点阵 t2×t1=1024×256。(伯)远程偶合相关,归属为C-18,通过HMQC确定δ2.25×10-4为H-18。由此,剩余的一个甲基δ2.98(3H,s)×10-4为 H-16,通过 HMQC 确定 δ41.5×10-4(伯)为 C-16。H-13和 H-14均与 δ37.7(叔)×10-4远程偶合相关,归属为 C-11,HMQC确认 δ2.27×10-4为H-11。
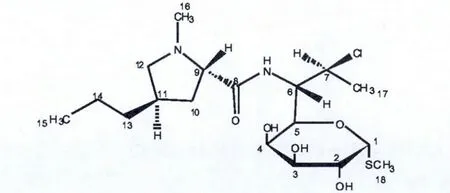
图1 盐酸克林霉素的化学结构
HMBC 谱中,C-13和 C-16均与 δ2.64×10-4远程偶合相关,归属为H-12,通过HMQC,确认δ62.3(仲)×10-4为 C-12,并确认 δ3.64×10-4为 H-12的另一个质子。则剩余的 δ37.2(仲)×10-4为 C-10,HMQC 确认 δ2.12×10-4为 H-10,H-10 的一个质子与H-11叠加在一起较H-11稍低场一些。C-16和C-10与δ4.48×10-4远程偶合相关,归属为H-9,HMQC 确认 δ69.2(叔)×10-4为 C-9。
至此全部谱峰归属完毕,具体数据见表1。
2 结果与讨论
2.1 盐酸克林霉素的1H和13C NMR谱信号的归属
氢谱显示该化合物有30个质子,碳谱显示化合物有18个碳,DEPT-135显示化合物中有4个仲碳,1个季碳,其余13个碳为伯碳和叔碳。
氢谱中由化学位移及偶合常数可以辨认出δ5.83×10-4%(1H,d)为 H-1(异头质子),δ0.73×10-4(3H,t)为H-15,δ1.64×10-4(3H,d)为H-17。结合1H-1H COSY 可以辨认出 H-2(5.02×10-4)、H-3(4.40×10-4)、H-4(4.78×10-4),H-14(1.03×10-4)、H-13(1.20×10-4)及 H-6(5.25×10-4)。结合 HMQC 可确定C-1、C-2、C-3、C-4、C-6、C-13、C-14、C-15 及 C-17。13C NMR中,由化学位移可以知道δ172.0×10-4为 C-8 酰胺羰基碳,HMBC 中,C-8 和 δ9.18(1H,br)远程偶合相关,且δ9.18ppm处质子经重水交换后消失,确认为NH。
HMBC 谱中,H-6和 H-1与 δ71.0(叔)×10-4处碳远程偶合相关,H-6和H-17与δ60.3(叔)×10-4处碳远程偶合相关,分别归属为 C-5(δ71.0×10-4)和C-7(δ60.3×10-4)。通过 HMQC 谱可确定H-5(δ4.87×10-4) 和 H-7(δ4.92×10-4)。H-1 与 δ13.7×10-4
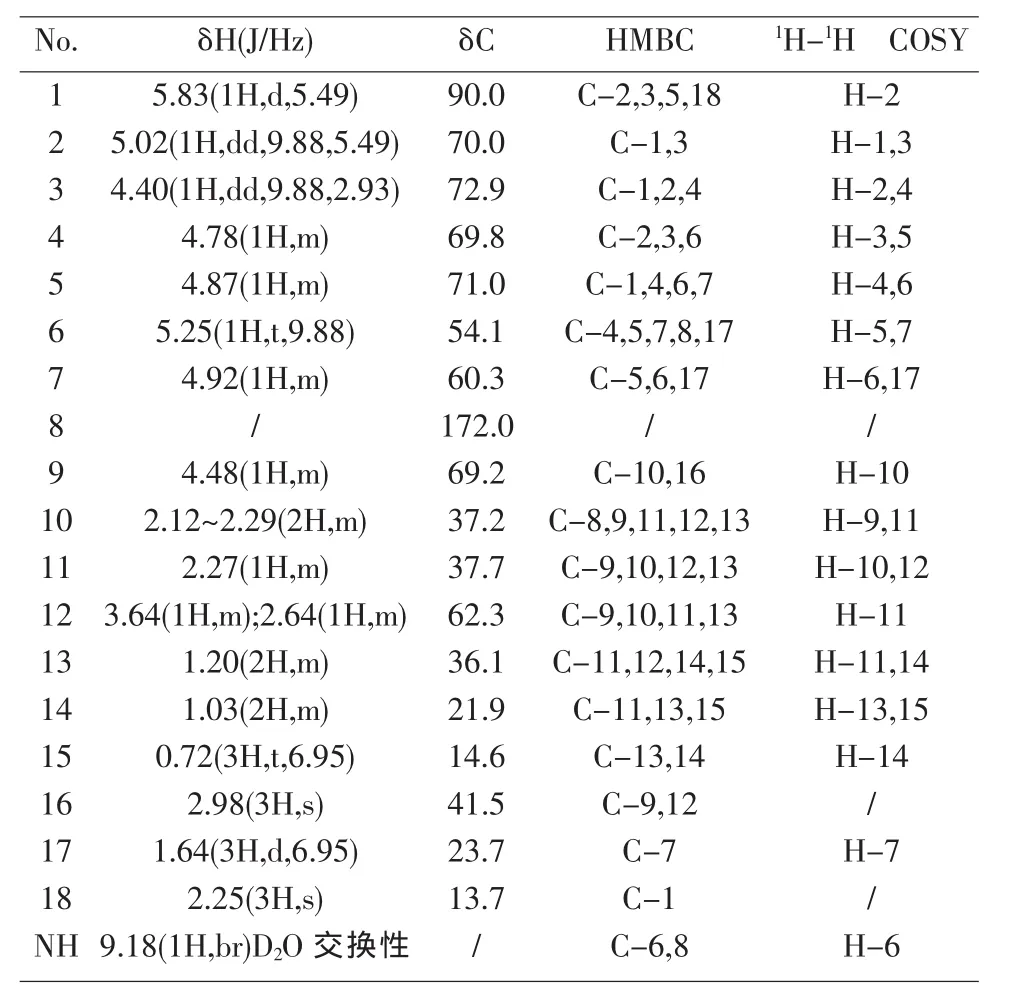
表1 盐酯克林霉素中1H和13C的核磁共振值(溶剂:Pyr-d5)
2.2 讨论
选用吡啶做溶剂,溶剂对信号无掩盖,仅氢谱中质子峰有部分重叠,且HMBC中氨基与C-6、C-8的相关信号及1H-1H COSY中NH与H-6的信号均清晰可辨,较DMSO-d6为好,但羟基峰未能显示。
1H NMR显示H-12的两个质子化学位移相差很大(1×10-4),这是由于五元环的影响,使得 H-12的两个质子不能自由旋转,导致化学环境不同而致。
H-16、H-12及H-9的化学位移较正常值均向低场位移了0.5×10-4左右,这是因为盐酸与该化合物中H-16连接的氮成盐酸盐的原因[2]。H-16的甲基信号较H-18宽,这是由于C-16连接在与盐酸成盐的氮原子上,受14N核电四极矩驰豫效应影响所致[3],H-9、H-12也是此原因,同时此效应导致H-9和H-12的信号变宽,耦合裂分看不到。
[1]李建军,丁元晨,王璐.检验检疫科学[J].2004,14(3):42-44.
[2]梁晓天.核磁共振高分辨氢谱的解析和应用)[M].北京:Science Press(科学出版社),1982,177-184.
[3]R.M.Silverstein,G.C.Bassler,Terence C.Morrill,Spectrometric Identification of Organic Compounds 5th ed.[M],New York:John Wiley&Sons,1991:185.

