外源添加物对海底沉积物微生物燃料电池性能的影响*
英 明 柳昭慧 赵阳国 付玉彬①
(1. 中国海洋大学材料科学与工程研究院 青岛 266100; 2. 中国海洋大学环境科学与工程学院 青岛 266100)
微生物燃料电池(MFCs)是一种利用产电微生物作为催化剂, 催化氧化有机物和无机物并产生电能的生物电化学系统。目前, MFCs的应用集中在污水处理方面, 由于输出功率低和装置放大困难等, 使得MFCs的实际应用受限(Bond et al, 2003; Logan et al,2006)。海底沉积物微生物燃料电池(BMFCs, 以下简称海泥电池)是利用溶氧的海水和厌氧的海泥间的电势差产生电能的装置。其阳极埋入海泥, 阴极浸入海水; 海泥中微生物直接或间接代谢有机物或无机物产生电子(e–)和质子(H+), H+扩散到阴极表面区域; e–从胞内转移到胞外并传递到阳极表面, 通过外电路转移到阴极, 与H+和溶解氧发生还原反应生成水。氧化还原反应持续进行, BMFCs连续输出电能(Lowy et al, 2006; Nielsen et al, 2009)。BMFCs以其底物丰富、结构简单(无人工质子交换膜, 无添加物)和产物无污染(H2O)等优点, 在海底监测仪器电源长期供给应用方面, 展现出广阔的应用前景。
研究表明, 海泥中存在多种产电微生物并可在阳极表面附着(Bond et al, 2002; Dumas et al, 2007)。Lovley等指出 MFCs中微生物通过使用产电呼吸的方式进行产能, 并从电子传递过程获得能量支持(Lovley et al, 2006; Lovley, 2006)。胞外电子传递方式包括直接电子传递机制(如膜蛋白、纳米导线等)和间接电子传递机制(如电活性化合物等)(Zhao et al, 2009;刘敏等, 2010)。微生物的产电呼吸和胞外电子传递是MFCs产电性能的重要影响因素。微生物活性低, 产电呼吸速率降低, MFCs产电能力下降; 电子传递过程受到阻碍, MFCs产电能力下降。本项目组曾通过对海泥电池电极进行改性, 如阳极表面金属化、表面羧基化和电极表面修饰导电高分子材料等方法, 增加微生物附着量或提高电子传递速率, 以提高电极抗极化能力, 进而提高海泥电池产电性能(Li et al,2009; 李建海, 2010; Fu et al, 2011)。项目组还利用该电池装置成功驱动小型电子装置长期运行(付玉彬等,2012)。
人们大量开展了外源添加物在微生物燃料电池中的应用研究, 通过向阳极室添加外源物质改变有机质含量和微生物数量及活性, 进而研究外源添加物对微生物燃料电池性能的影响(Oh et al, 2014; Ren et al, 2014)。不同海域底泥中的有机质含量和微生物数量及活性不同, 为模拟不同海域底泥的区别而直接向海泥中添加两种外源物质(葡萄糖为微生物直接底物(徐金球等, 2012), 用以增加有机质含量和微生物数量; 丹皮酚为抑菌物质(朱传喜等, 2013), 用以减少微生物数量), 而后分析和讨论添加物对海泥电池阳极及电池性能的影响, 并提出相应的机理模型。结果表明: 以外添加葡萄糖海泥作为底物的BMFC-1的产电性能明显高于以外添加丹皮酚海泥作为底物的 BMFC-2的产电性能, 同时根据独特的电容理论(Fradler et al, 2014; Peng et al, 2013a, 2013b), 分析其阳极性能差异的原因。
1 材料与方法
1.1 海泥处理
A 组海泥(250g/组, 取自李村河入海口)中加入60mL海水(取自李村河入海口), B、C组海泥中分别加入60mL 1g/L的葡萄糖溶液和5g丹皮酚粉末, 机械搅拌 25min(DSC-12恒速数显电动搅拌机, 杭州仪表电机有限公司)。自然沉降后待用。
1.2 电池组装
钛丝(Φ1mm)穿过 30mm×30mm×3mm 碳毡连接成电极(表观面积取 San=1800mm2)。将碳毡电极埋入海泥(距离海泥/海水界面 3—5cm)作为阳极; 三个碳刷(Φ50mm×350mm/个)并联浸入海水作为共用阴极(Sca>>3San), 且阴极室连续泵入空气。对照组以天然海泥作为底物(图 1A)构建海泥电池 BMFC-0的阳极室, 实验组分别以外添加葡萄糖和丹皮酚的海泥作为底物构建海泥电池 BMFC-1(图 1B)和 BMFC-2(图1C)的阳极室。
1.3 电极电位及连续放电测试
万用电表(MY60, 深圳华谊仪表有限公司)直接测量断路状态下阳极电位φan(mV.vs.SCE)和阴极电位φca(mV.vs.SCE)。电极电位达到稳定值后, 阳极室通过盐桥连接阴极室, 外接 R=1000Ω 的定值电阻, 形成共用阴极海泥电池组(图 1)。万用电表直接测量输出电压U(mV)和阴极电位φca(mV.vs.SCE)。电流密度i和功率密度 P分别通过公式 i=U/(R·San)和 P=U2/(R·San)计算得到。阳极电位由公式φan=φcat-U计算得到。

图1 海底沉积物微生物燃料电池结构示意图Fig. 1 Diagram of BMFCs structure
1.4 荧光显微镜观察计数
取阳极附近40g海泥(湿重), 加入灭菌PBS缓冲液(0.2mol/L, pH=7), 25°C恒温振荡20min(恒温振荡器, SHA-C, 金坛市新航仪器厂)后滤掉泥沙颗粒, 将滤液中细菌通过抽滤富集到微孔滤膜(孔径 0.22μm)表面。滤膜表面微生物使用 0.01%吖啶橙进行染色,5min后在荧光显微镜下放大400倍观察(Leica DM IL LED倒置显微镜), 在 2500μm2的范围内计数并按比例估算总滤膜面积内细菌数量。
1.5 电化学测试
断路状态下阳极电位稳定后, 分别在3组电池的阳极室中进行循环伏安扫描(LK2005B电化学工作站,天津市兰立科化学电子高技术有限公司), 对照组碳毡以过滤海水、外添加葡萄糖海水和外添加丹皮酚海水(0.22μm滤膜)作为电解质。连续放电 14天后再进行 CV和 Tafel扫描。三电极体系: 碳毡阳极作为工作电极, 30mm×30mm铂片电极(天津艾达恒晟科技发展有限公司)作为对电极, 饱和甘汞电极(SCE)作为参比电极。扫速为: 1mV/s; 扫描范围为: –0.8V—0.3V; 5次循环。
2 结果与讨论
2.1 外源添加物对海泥中微生物的影响
图2表示阳极附近海泥中微生物的相对数量。在相同的视窗范围内, 含葡萄糖海泥(b)中微生物数量多于天然海泥(a); 含丹皮酚海泥(c)中微生物数量最少, 计数结果表明, a、b、c中微生物数量分别为9.1437×107、3.1044×109、5.0241×106(个)。葡萄糖为营养底物, 使微生物总数量增加(徐金球等, 2012);丹皮酚对革兰氏阴性菌具有较强抑制作用, 使得含丹皮酚的海泥中产电菌数量减少(Zhao et al, 2009;刘敏等, 2010; 徐金球等, 2012)。

图2 阳极表面海泥中微生物荧光显微照片(400×)Fig 2 Pictures of flourescence microscopy for bacteria in the sea mud of nearby the anodes(400×) .

图3 断路状态下海泥电池阳极电位Fig. 3 Anode potentials of BMFCs in open circuit station
2.2 外源添加物对阳极性能的影响
2.2.1 断路状态下阳极电位 通常条件下, BMFCs阳极电位达到正常范围的时间为 10±3天。BMFC-0的阳极电位8天后稳定在–445±10mV, 表明产电菌在阳极表面完成附着过程(Dios et al, 2014)。在前期(0—10天), BMFC-1的阳极电位稳定在–450±10mV,与BMFC-0的结果基本一致, 10天后阳极电位持续增大, 并稳定在–360mV。一方面可能是由于葡萄糖的驯化作用而改变海泥中微生物群落结构(徐金球等,2012), 另一方面可能是葡萄糖对电极表面状态的影响(图 4a(gw)), 使阳极电位增大。在前期(0—15天),BMFC-2的阳极电位稳定在–320±10mV, 后期BMFC-2的阳极电位降低到–490±10mV, 可能是由于C中产电菌数量较少(图4b(pm)), 导致阳极电位增大;后期丹皮酚吸附在阳极表面且其中酚羟基失去电子被氧化(王晔等, 2006), 导致阳极电位变小。此外, 丹皮酚的氧化反应认为是醌类可逆反应, 醌可逆体系的电极电势–170mV(vs.SCE)(迪安, 1991), 实测该准可逆反应的还原电极电势值为–184mV(图 4a(pw)),结合前期阳极电位–320±10mV, BMFC-2后期阳极电位为–490±10mV (图 3)。
2.2.2 循环伏安曲线 碳毡电极在天然海水、外添加葡萄糖的海水和外添加丹皮酚的海水中进行循环伏安扫描。图4a(nw)结果表明碳毡电极在海水中没有明显的氧化峰, 在–0.254V 处出现还原峰, 考虑是因为海水中溶氧的作用; 图 4a(gw)显示葡萄糖在无菌海水中的碳毡表面不能发生氧化还原反应, 表1结果表明曲线gw包围面积小于曲线nw包围面积, 即比表面电容减小(从31.8F/m2降到9.1F/m2), 表明葡萄糖可影响碳毡电极表面形貌而造成表面双电层电容减小(Portet et al, 2009); 图4a(pw)显示丹皮酚在无菌海水中的碳毡表面可发生准可逆的氧化还原反应。在以三种不同的海泥作为底物构建的阳极室内进行原位循环伏安扫描, 对于BMFC-0(图4b, 4c), 连续放电前后其阳极分别在–0.022V(inm=0.665A/m2)和–0.66V(inm=–0.765A/m2)出现氧化还原峰, 表明阳极生物膜内微生物催化底物发生氧化反应且电子的传递过程出现电子中介体的作用(Lovley et al, 2006; Nielsen et al, 2009)。对于BMFC-1(图4b, 4c), 连续放电前其阳极在–0.048V 处出现氧化峰(图 4b, igm=2.875A/m2),连续放电后其阳极在 0.054V处出现氧化峰(图 4c,igm=5.769A/m2), 阳极在连续放电后的氧化峰电流 igm是连续放电前的2倍, 且是BMFC-0阳极的8.7倍, 表明葡萄糖提高了 BMFC-1阳极生物膜内微生物电化学活性, 且连续放电后阳极在–0.318V出现还原峰,还原峰位置相对BMFC-0阳极(φnm=–0.66V)发生改变,进一步表明经过葡萄糖的驯化作用, 生物膜中微生物群落结构发生变化, 导致催化电子传递过程的酶种类发生改变(Lovley et al, 2006; 徐金球等, 2012)。对于 BMFC-2(图 4b, 4c), 连续放电前其阳极在0.058V出现氧化峰(ipm=0.71A/m2), 连续放电后其阳极在 0.084 V处出现氧化峰(ipm=0.886A/m2), 且均与图 4a(pw)氧化峰位置相近(φpw=0V, ipw=0.436A/m2),氧化峰位置的变化和峰电流的变化可能由于丹皮酚与微生物之间的相互作用造成的, 由于含有丹皮酚的海泥中微生物数量少, 表明该氧化峰来自丹皮酚的作用。图 4c显示, 连续放电后阳极未出现明显还原峰, 可能是由于丹皮酚氧化后产生不导电的醚类聚合物膜而不能发生还原反应造成(王晔等, 2006)。
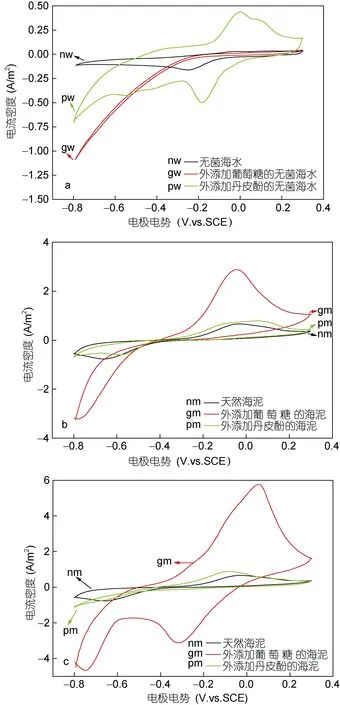
图4 电极在不同海水中循环伏安曲线(a)及连续放电前后不同底泥中阳极循环伏安曲线(b: 连续放电前; c: 连续放电后)Fig. 4 CV curves in different sterile sea water for carbon felt electrodes (a) and anodic curves of cyclic voltammetry in different sediments before (b) and after (c) continuous discharge.
2.2.3 塔菲尔曲线 在连续放电 14天的 BMFCs阳极室内进行原位 Tafel测试, 并根据测试结果绘制Log[i(/mA/cm2)]~E(V.vs.OCP)图(图 5), 在 60—80mV的过电势范围内进行线性拟合并外推出阳极表面氧化反应的交换电流密度i0(mA/cm2)。将交换电流密度i0换算成相对动力学活性, BMFC-1和BMFC-2的阳极相对动力学活性分别是BMFC-0的1.91倍和0.67倍(表2)。葡萄糖显著增加了BMFC-1阳极的动力学和电化学活性(图 4c(gm), 图 5(gm)), 增加了阳极表面微生物数量(图2b), 提高了电子由微生物胞内转移到电极表面的速率, 增大了 BMFC-1的输出电流(图6a); 丹皮酚明显降低阳极表面微生物数量(图2c), 减少微生物产生电子的数量, 且抑制电子由胞内转移到电极的过程(图4c(pm)), Tafel结果进一步证明丹皮酚在阳极表面的氧化反应速率较慢(图 5(pm)), 导致BMFC-2的阳极容易极化且输出电流较小(Lowy et al,2006)。
2.3 外源添加物对电池性能的影响
2.3.1 输出电流密度 BMFCs外接R=1000Ω定值电阻进行连续放电实验, BMFC-1的输出电流密度高于BMFC-0和BMFC-2的输出电流密度。BMFC-0的输出电流密度维持在21.35±3mA/m2; BMFC-1的输出电流密度从46.67mA/m2降低到27.22mA/m2, 然后呈缓慢增加的趋势, 并在 400h后升高到 87.78mA/m2;BMFC-2的输出电流密度从 71.67mA/m2持续降至6.55mA/m2± 1mA/m2。
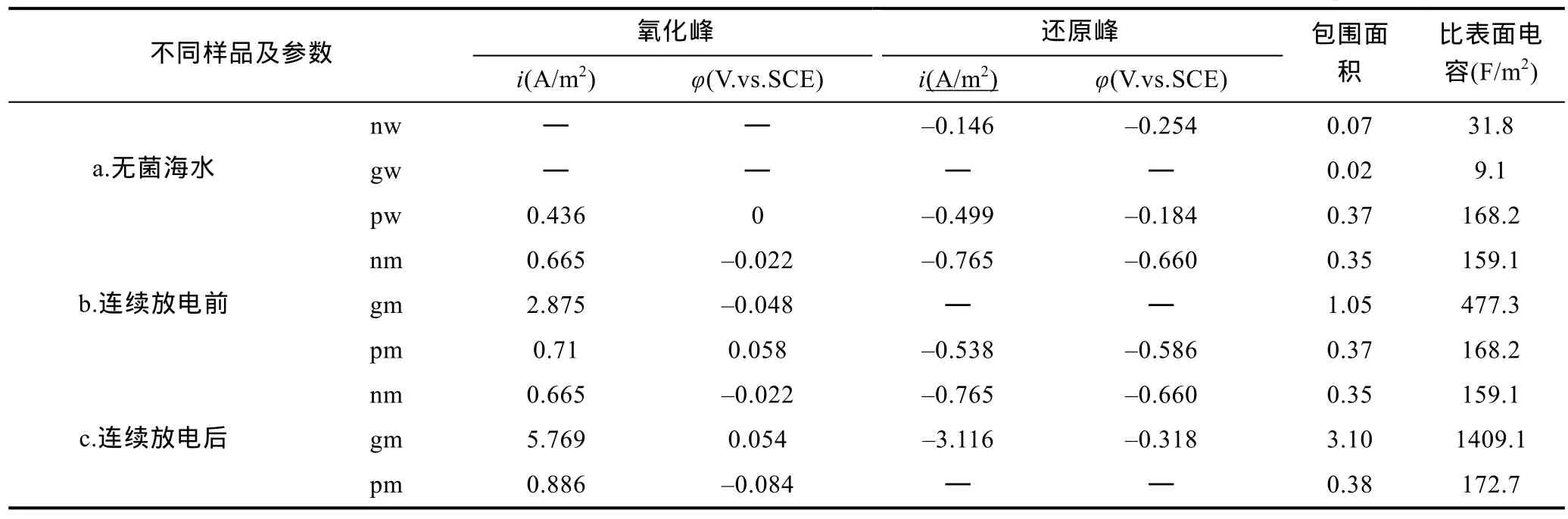
表1 不同底泥中阳极循环伏安曲线参数和不同海水中电极循环伏安曲线参数Tab. 1 Parameters of CV curves in different sediments and sterile sea water for anodes and electrodes respectively.
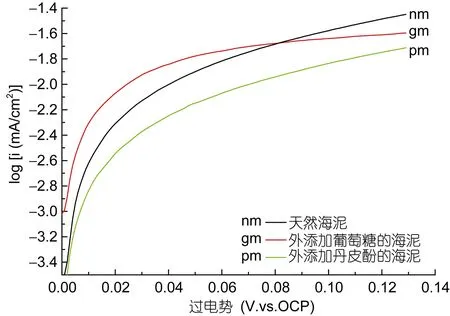
图5 阳极塔菲尔曲线Fig.5 Tafel curves of different anodes

表2 不同底泥中阳极交换电流密度和相对动力学活性Tab. 2 Densities of exchange current and Relative Dynamic Activities of anodes in different sediments
BMFC-0底泥中产电菌未受到外源添加物的影响, 持续放电平稳。经过葡萄糖的驯化后, BMFC-1底泥中优势产电菌数量增多, 电化学和动力学活性提高(图4c(gm), 图5(gm)), 输出电流逐渐变大, 由于阳极附近底物浓度变化对产电微生物的影响而造成输出电流较大的波动。经过丹皮酚处理后, BMFC-2底泥中微生物数量减少, 阳极电化学和动力学活性降低(图4c(pm), 图5(pm)), 输出电流减小(图6a)。
2.3.2 平均输出功率密度 BMFCs在连续放电过程中输出电压和电流受外部环境影响而波动, 通过对比其平均输出功率密度可综合显示BMFCs的产电性能。BMFC-1的平均输出功率密度为7.294mW/m2,分别是BMFC-0(0.875mW/m2)和BMFC-2(0.106mW/m2)的8.3和68.8倍, 且BMFC-0的平均输出功率密度是BMFC-2的 8.3倍。添加葡萄糖后, 平均输出功率密度提高约 8.3倍, 丹皮酚处理后, 平均输出功率密度降低约8.3倍, 说明外源添加物对BMFCs的产电性能具有重要影响, 进一步表明不同底泥中 BMFCs的产电性能不同(图6b)。
2.4 外源添加物对阳极电位影响机理分析及电容模型
BMFCs阳极埋入海泥后, 阳极/海水界面形成双电层电容Cdl和生物膜电容Cbf(图7a, b)。通过氧化还原反应接收和释放电荷的电活性物质附着在电极表面形成法拉第电容, 即赝电容Cp(图7c)。产电菌通过直接电子传递或者间接电子媒介体(电活性氧化还原体等)的方式将电子传递到阳极表面(Bond et al, 2003;Logan et al, 2006; Nielsen et al, 2009), 电子在电极表面电容中存储形成电极电位。BMFC阳极表面总电容值与各个电容值间的数值关系如下式所示:
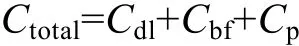
在过滤海水(表 1-a)和外添加葡萄糖的过滤海水(表 1b)中, 碳毡电极表面形成双电层电容 Cdl, 即Ctotal=Cdl; 在外添加丹皮酚的过滤海水(表 1c)中, 碳毡电极表面形成 Cdl和赝电容 Cp, 即 Ctotal=Cdl+Cp。BMFC-0和BMFC-1(表1)阳极表面形成Cdl和生物膜电容 Cbf(图 7 a, b), 即 Ctotal=Cdl+Cp; BMFC-2(表 1)阳极表面形成 Cdl、Cbf和 Cp(图 7c), 即 Ctotal=Cdl+Cbf+Cp。
断路状态下(即连续放电前), 添加葡萄糖后,BMFC-1的阳极比表面电容(表 1) 增大到 477.3F/m2,是 BMFC-0阳极(159.1F/m2, 表 1)的 3倍, 这是由于细菌数量明显增多, 阳极表面附着生物量增多, 生物膜增厚, Cbf增大导致的, 而葡萄糖降低了表面双电层电容Cdl(表1), 造成该状态下阳极电位较正(图3); 添加丹皮酚后, 在海泥和无菌海水中电极比表面电容均为168.2F/m2(表1), 表明BMFC-2阳极表面生物膜电容Cbf非常小或为零; BMFC-2阳极比表面电容(表1, 168.2F/m2)略大于 BMFC-0阳极比表面电容(表 1,159.1F/m2), 可能是由于丹皮酚在电极表面发生氧化反应, Cp增大造成的, 从而导致阳极电位较负(图3)。
通路状态下(即连续放电后), 阳极上电子在电场作用下通过外电路到达阴极并参与阴极还原反应。连续放电后, 经过葡萄糖驯化, 阳极生物膜中产电菌数量和群落结构发生改变, 提高了阳极的电化学和动力学活性(图4c, 图5), 增大生物膜电容Cbf, 使BMFC-1的阳极(表 1)比表面电容增大到 1409.1F/m2, 是连续放电前BMFC-1阳极比表面电容(表1, 477.3F/m2)的3倍, 明显增加BMFC-1的输出电量, 使BMFC-1的平均输出功率密度增大为BMFC-0的8.3倍(图6b)。经过丹皮酚连续作用后, 丹皮酚在阳极表面不断被氧化, 使得 Cp增大,导致 BMFC-2的阳极(表 1)比表面电容达到172.7F/m2,比连续放电前BMFC-2阳极(表1, 168.2F/m2)比表面电容略有增加; 外添加丹皮酚的海泥中细菌数量明显减少, 生物膜厚度减小, Cbf减小, 且形成不导电聚合物膜后使得Cdl减小, 且BMFC-2阳极的动力学和电化学活性较低(图4c, 图5), 减小BMFC-2的输出电量, 使平均输出功率密度减小8.3倍(图6b)。

图6 连续放电曲线(a)及平均输出功率密度(b)Fig. 6 Time discharge curves and average power densities
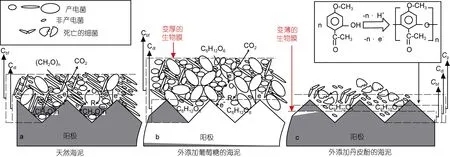
图7 机理模型示意图Fig. 7 Diagram of mechanism model
3 结论
外源添加物对海泥中微生物、阳极电位和电池性能产生重要影响。外添加葡萄糖的底泥中微生物数量增多且阳极电化学和动力学活性提高, 外添加丹皮酚的底泥中微生物数量减少且阳极电化学和动力学活性降低, 这种差异是由于葡萄糖的驯化作用和丹皮酚的抑菌作用引起的。断路状态下, 葡萄糖提高阳极电位至–360±10mV, 丹皮酚降低阳极电位至–490±10mV。通路状态下, 葡萄糖提高输出电流密度,丹皮酚降低输出电流密度。BMFC-1的平均输出功率密度为 7.294mW/m2, 分别是 BMFC-0(0.875mW/m2)和BMFC-2 (0.106mW/m2)的8.3倍和68.8倍。从不同添加物对阳极表面生物膜电容特性的影响出发, 提出阳极表面电容性质对电极及电池性能影响的独特机理。
王 晔, 吴 剑, 李 端等, 2006. 丹皮酚的电化学氧化及其反应机理研究. 分析化学研究简报, 34(9): 1331—1334
付玉彬, 李建海, 赵仲凯等, 2012. 海底生物燃料电池作为电源驱动小型电子器件的应用研究. 中国海洋大学学报,42(6): 93—98
朱传喜, 张维博, 方 强等, 2013. 凝胶型丹皮酚空气清新剂的制备及其抑菌性能评价. 环境化学, 32(10): 1997—1998
刘 敏, 邵 军, 周 奔等, 2010. 微生物产电呼吸最新研究进展. 应用与环境生物学报, 16(3): 445—452
李建海, 2010. 海底沉积物微生物燃料电池阳极表面改性及电极构型研究. 青岛: 中国海洋大学硕士学位论文
迪 安 J A 编著, 尚久方, 操时杰, 辛无名等译, 1991. 兰氏化学手册(第十三版). 北京: 科学出版社, 3—29
徐金球, 梁 波, 王利军等, 2012. 葡萄糖在微生物燃料电池中的应用研究进展. 上海第二工业大学学报, 29(4): 257—265
Bond D R, Holmes D E, Tender L M et al, 2002.Electrode-reducing microorganisms that harvest energy from marine sediments. Science, 295 (5554): 483—485
Bond D R, Lovley D R, 2003. Electricity production by Geobacter sulfurreducens attached to electrodes. Applied and Environmental Microbiology, 69(3): 1548—1555
De Dios F, Iglesias O, Bocos E et al, 2014. Application of benthonic microbial fuel cells and electro-fenton process to dye decolourisation. Journal of Industrial and Engineering Chemistry, 20(5): 3754—3760
Dumas C, Mollica A, Féron D et al, 2007. Marine microbial fuel cell: Use of stainless steel electrodes as anode and cathode materials. Electrochimica Acta, 53(2): 468—473
Fradler K R, Kim J R, Boghani H C et al, 2014. The effect of internal capacitance on power quality and energy efficiency in a tubular microbial fuel cell. Process Biochemistry, 49(6):973—980
Fu Y B, Zhao Z K, Liu J et al, 2011. Sulfonated polyaniline/vanadate composite as anode material and its electrochemical property in microbial fuel cells on ocean floor. Science China Chemistry, 54(5): 844—849
Li J H, Fu Y B, Zai X R, 2009. KMnO4modification of graphite anodes to enhance performance of benthic microbial fuel cell. Beijing: International Conference on Environmental Simulation and Pollution Control and The Second Symposium on Microbial Fuel Cell in China, 12—14
Logan B E, Regan J M, 2006. Microbial fuel cells-challenges and applications. Environmental & Science Technology, 40(17):5172—5180
Lovley D R, Juice B, 2006. Harvesting electricity with microorganisms. Nature Reviews Microbiology, 4: 497—508
Lovley D R, 2006. Taming electricigens: How electricitygenerating microbes can keep going, and going-faster. The Scientist, 7(20): 46
Lowy D A, Tender L M, Zeikus J G et al, 2006. Harvesting energy from the marine sediment-water interface II: Kinetic activity of anode materials. Biosensors and Bioelectronics,21(11): 2058—2063
Nielsen M E, Wu D M, Girguis P R et al, 2009. Influence of substrate on electron transfer mechanisms in chambered benthic microbial fuel cells. Environmental Science &Technology, 43(22): 8671—8677
Oh S E, Yoon J Y, Gurung A et al, 2014. Evaluation of electricity generation from ultrasonic and heat/alkaline pretreatment of different sludge types using microbial fuel cells. Bioresource Technology, 165: 21—26
Peng X H, Yu H, Yu H B et al, 2013a. Lack of anodic capacitance causes power overshoot in microbial fuel cells. Bioresource Technology, 138: 353—358
Peng X H, Yu H B, Ai L et al, 2013b. Time behavior and capacitance analysis of nano-Fe3O4added microbial fuel cells. Bioresource Technology, 144: 689—692
Portet C, Yang Z, Korenblit Y et al, 2009. Electrical double-layer capacitance of zeolite-templated carbon in organic electrolyte. Journal of The Electrochemical Society, 156(1):A1—A6
Ren L J, Ahn Y, Hou H J et al, 2014. Electrochemical study of multi- electrode microbial fuel cells under fed-batch and continuous flow conditions. Journal of Power Sources, 257:454—460
Zhao F, Slade R C T, Varcoe J R et al, 2009. Techniques for the study and development of microbial fuel cells: an electrochemical perspective. Chemical Society Reviews,38(7): 1926—1939

