静电纺MnO2/PAN纳米纤维膜的制备及其催化氧化甲醛性能
陈仁忠,胡 毅,袁菁红,沈 桢,陈艳丽,吕 慧,何 霞
(1.浙江理工大学先进纺织材料与制备技术教育部重点实验室,浙江杭州 310018;2.浙江理工大学生态染整技术教育部工程研究中心,浙江杭州 310018;3.杭州职业技术学院达利女装学院,浙江杭州 310018)
甲醛广泛应用于建筑、皮革、纺织、木材加工等行业,而人或动物长期处于较高浓度的甲醛环境中将对其健康造成极大危害;由此,甲醛消除技术研究一直被广泛关注[1]。传统物理吸附和化学反应可在短时间内有效吸收甲醛[2]。其中,催化氧化法降解甲醛可使最终产品仅有二氧化碳和水;Sekine[3]研究发现,在可催化氧化甲醛的催化剂品种中,二氧化锰(MnO2)对甲醛去除率高,作用明显,且其无有害物质释放,因此MnO2常被用于甲醛消除的活性成分。粉末状MnO2不便直接用于处理甲醛,常用的载体有活性炭[4]、活性炭纤维[5]等。与上述2类载体相比,采用静电纺技术制备的纳米纤维膜具有比表面积大、空隙率高、孔径直径小等优点[6],近来广泛用于催化剂载体[7-8]。
本文通过静电纺将自制二氧化锰颗粒均匀负载于聚丙烯腈(PAN)纳米纤维中,形成功能性复合纳米纤维膜,对其催化氧化甲醛的性能进行了研究,取得了较好的实验效果。
1 实验部分
1.1 材料
聚丙烯腈(PAN,MW=140000)高锰酸钾(KMnO4,分析纯),环己醇(分析纯),N,N-二甲基甲酰胺(DMF,分析纯),氢氧化钠(分析纯),无水乙醇(分析纯),乙酰丙酮(分析纯),冰醋酸(分析纯),醋酸铵(分析纯)。
1.2 MnO2的制备
采用液相沉积法。取一定质量的KMnO4加入到KOH水溶液中。在45℃条件下逐滴加入环己醇,滴加完毕后反应60 min。反应完毕后过滤并用蒸馏水和乙醇分别洗涤至pH值为中性,然后烘干并用行星球磨机(600 r/min)研磨1 h,得到MnO2颗粒[9]。
1.3 静电纺MnO2/PAN纳米纤维膜
将一定比例的MnO2和聚丙烯腈(PAN)共混于N,N-二甲基甲酰胺(DMF)中,配成纺丝溶液,60℃下搅拌48 h,然后采用自制静电纺丝设备进行纺丝,其纺丝参数为:喷丝口与接收板间施加电压15 kV,间距15 cm,流速0.7 mL/h,湿度40%,纺丝时间5 h。
1.4 催化氧化甲醛性能测试
配制一定体积和浓度的甲醛溶液,滴加硫酸调节pH值为酸性。控制反应温度,加入0.03 g MnO2/PAN纳米纤维膜吸收甲醛。每隔2 h取吸收甲醛溶液后的样品,再加入乙酰丙酮,在60℃水浴中显色15 min,冷却至室温,在408~414 nm波长下测试其吸光度。
1.5 结构与性能表征
用扫描电镜(SEM)和透射电镜(TEM)观察MnO2颗粒和纤维表面形貌。采用傅里叶红外光谱仪(FT-IR)对纳米纤维结构组成进行表征。采用热重分析仪(TG)研究纳米纤维膜的热稳定性和组分。
2 结果与讨论
2.1 MnO2形貌分析
图1示出MnO2粉末微观形貌和颗粒直径分布。可以发现:MnO2呈不规则的类球形颗粒状,研磨后粒径分布较集中,通过Nano Measurer 1.2软件测得其平均直径为196.46 nm,表明仍有部分团聚未完全分散。

图1 MnO2的SEM照片和粒径分布直方图Fig.1 SEM image(a)and particle size distribution histogram(b)of MnO2
图2示出MnO2的红外光谱分析图。由图可知,526 cm-1处为 Mn—O 特征峰[10];3425 cm-1附近宽峰为MnO2表面水分中—OH伸缩振动吸收峰,表明MnO2表面吸附有丰富的—OH。1521 cm-1处吸收峰为COO—对称伸缩振动峰,1409 cm-1处吸收峰为COO—伸缩振动峰,表明环己醇被氧化成己二酸。
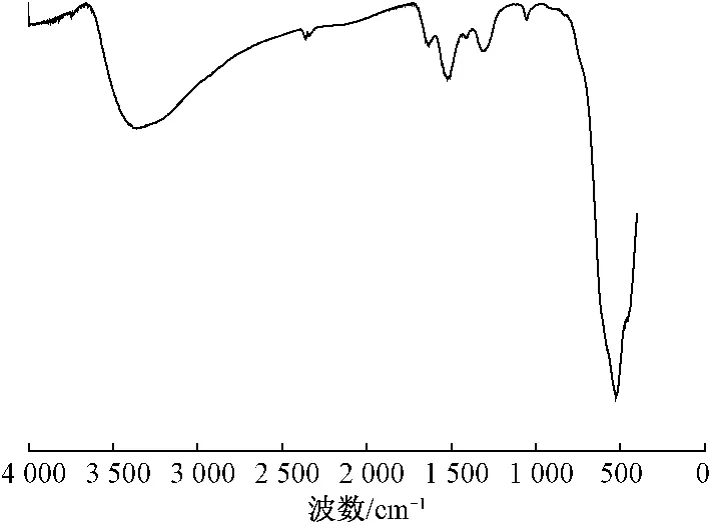
图2 MnO2的FT-IR图Fig.2 FT-IR image of MnO2
2.2 MnO2/PAN纳米纤维膜形貌表征
控制纺丝溶液中MnO2与PAN质量比为1∶2、1∶4、1∶8、1∶16、1∶32,静电纺丝获得不同质量比的MnO2/PAN纳米纤维膜。图3示出不同质量比MnO2/PAN纳米纤维膜的SEM照片。

图3 不同质量比MnO2/PAN纳米纤维膜SEM照片Fig.3 SEM images of fibers with different mass ratios of MnO2to PAN
观察纤维形貌,纤维呈现连续交错的网络状,MnO2颗粒镶嵌在PAN纤维上,在部分单根纤维上出现珠状结构[11]。与静电纺本身产生的珠状表面光滑流畅特点不同,此纤维珠状结构表面呈现不规则的凹凸不平。这是由于PAN包裹较大的MnO2颗粒,易形成珠状结构及MnO2颗粒较大,表面不平整而未能被完全包裹所致。
表1示出MnO2与PAN质量比对PAN纤维的影响。可看出,5种纤维直径分布在150~470 nm之间。随着MnO2含量增加,纤维平均直径出现波动,整体呈现出下降趋势。
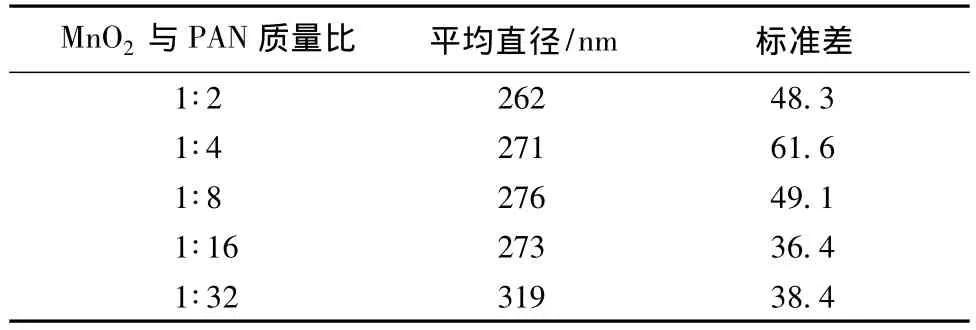
表1 MnO2与PAN质量比对PAN纤维的影响Tab.1 Influence of different mass ratios of MnO2to PAN on fiber diameter
图4示出不同纺丝电压下纳米纤维膜SEM照片。随着纺丝电压增大,纤维直径呈逐渐减小趋势。这是由于在电场中,随纺丝电压增大,纺丝液射流表面电荷密度增大,在电场中所受静电斥力增大,由此,射流受到更大拉伸力,使纤维直径减小[12-13],如表2所示。

图4 不同纺丝电压下纳米纤维膜SEM照片Fig.4 SEM images of fibers at different spinning voltages
纤维直径均匀性与纺丝稳定性可通过标准差判断,电压15 kV时,纤维直径分布范围窄,纺丝稳定性好。考虑纤维形貌均匀、纺丝稳定要求,优选15 kV为最佳纺丝电压。

表2 纺丝电压对PAN纤维的影响Tab.2 Influence of voltage on fiber diameter
图5示出MnO2/PAN纳米纤维膜的TEM照片。图中深色部位是MnO2,浅色部分是PAN。MnO2在纤维中有镶嵌和包含2种分布形式。其中由于MnO2颗粒平均直径为196.46 nm,比表面积大,表面能高,颗粒易发生团聚而使比表面积减小,造成MnO2颗粒易在纤维内团聚,分散不均匀。颗粒较大的MnO2凸出纤维表面,使纤维表面粗糙不平整并出现不规则凸起,与SEM照片表现一致。

图5 MnO2/PAN纳米纤维膜TEM照片Fig.5 TEM image of MnO2/PAN nanofibers
2.3 红外光谱分析
图6示出3种纤维膜材料红外光谱图。2242、1666、1451、1390、1235 cm-1处振动峰(* 标记)是由PAN中C≡N、CO、C—H振动引起[14]。
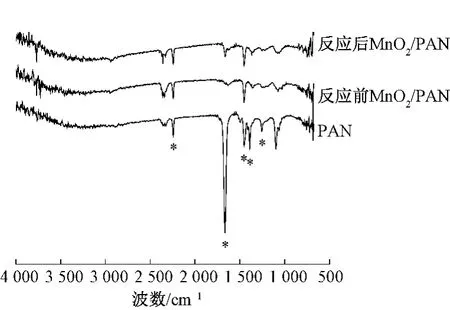
图6 PAN、反应前MnO2/PAN和反应后MnO2/PAN纳米纤维膜的FT-IR图Fig.6 FT-IR images of PAN,MnO2/PAN before reaction and MnO2/PAN nanofibers after reaction
从图 6可看出,加入 MnO2后,1666、1390、1097 cm-1处峰强度明显减弱,其原因在于MnO2作为强氧化剂,影响聚丙烯腈的C≡N键。比较吸收甲醛前后膜的红外光谱图,前后并未发生明显变化,说明反应前后MnO2/PAN纤维膜结构未曾改变。
2.4 热力学性能分析
对PAN纳米纤维膜进行热重分析,升温速率为20℃/min,N2气氛,结果如图7所示。可看出样品的失重行为,经过770℃热处理后曲线趋于平衡,这表明样品中PAN及其杂质完全分解为水、二氧化碳等物质。曲线在100℃之前约有10%质量损失应为样品吸附水分的挥发。在270~430℃之间约有18%的质量损失归因于PAN发生环化反应。430~770℃之间约有65%质量损失归因于PAN完全分解[14]。
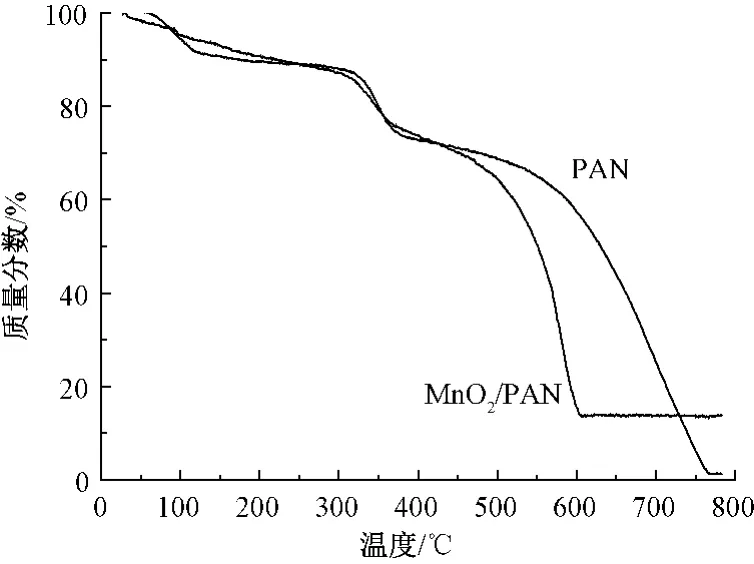
图7 PAN与MnO2/PAN纳米纤维膜TG图Fig.7 TG images of PAN nanofibers and MnO2/PAN nanofibers
比较MnO2/PAN纳米纤维膜热失重曲线,曲线在250℃之前有一个缓慢的质量损失是样品中吸附水和制备MnO2过程中残留有机物(环己醇、己二酸)的挥发导致的。在270~430℃之间约有17%质量损失归因于PAN发生环化反应。430~605℃之间约有55%质量损失归因于PAN完全分解。MnO2加速PAN完全分解致使PAN完全分解温度降低[15]。605~800℃之间质量保持恒定,残余物质应是三氧化二锰[16],约占总质量的13.80%。推算出MnO2占样品的15.20%,占MnO2/PAN总量的16.85%,小于纺丝液配制质量分数20%。这可能是在纺丝过程中,MnO2颗粒发生沉淀而使实际纺丝液浓度降低。
2.5 催化氧化甲醛性能分析
2.5.1 温度影响
图8示出温度-甲醛转化率曲线图,比较反应12 h后的甲醛转化率可发现,随着温度提高,甲醛转化率增加。20~60℃之间转化率提高较快,温度再增加,转化率提高幅度趋缓。说明反应温度提高有利于MnO2对甲醛的催化氧化反应。其原因在于温度增加,分子运动加剧,MnO2与HCHO分子间接触概率增大,相同时间内甲醛转化速率提高较快[10],但随温度升高,60℃后甲醛转化率增加趋缓。从中优选最佳吸收温度为60℃。
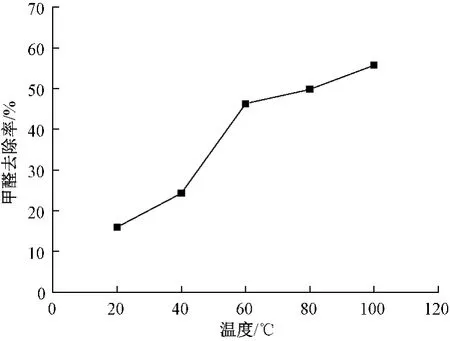
图8 温度对催化氧化甲醛性能的影响Fig.8 Influence of temperature on catalytic oxidation performance on formaldehyde
2.5.2 pH值影响
图9示出pH值对甲醛去除率的影响。比较了反应12 h后甲醛去除率,由图可知:随pH值降低,甲醛去除率快速提高,随后提高速率减缓,pH=2时甲醛去除率最高,随pH值继续降低,甲醛去除率略有下降。其原因在于:MnO2在中性、碱性环境中,氧化性能低,不能降解脱除甲醛;在酸性环境中MnO2氧化性强,且酸性越高,氧化性能越强,甲醛去除率同时提高。但强酸环境会抑制羟自由基生成,降低其催化氧化甲醛性能,因此优选最佳pH值为2。
2.5.3 时间影响
图10示出时间-甲醛去除率曲线图。由图可知:最初1 h,甲醛去除率快速升高,这归因于MnO2表面吸附羟基自由基[9,17]快速氧化甲醛;随后甲醛去除率升高速率减缓,这是由于体系中甲醛浓度下降,使甲醛分子与MnO2接触概率下降,而导致去除率降低。比较2条曲线可知:MnO2/PAN纳米纤维膜甲醛去除率均略高于MnO2粉末,10 h后,甲醛去除率趋于稳定,MnO2纤维膜甲醛去除率为44.0%,MnO2粉末甲醛去除率为37.0%,MnO2纳米纤维膜具有更高的去除速率。12 h后甲醛去除率仍较低,这是由于甲醛去除率与体系中氧含量有关,水溶液中溶解氧含量越高,甲醛最终去除率越高[5]。实际上,水溶液中溶解氧含量较少,限制了甲醛去除率的提高。
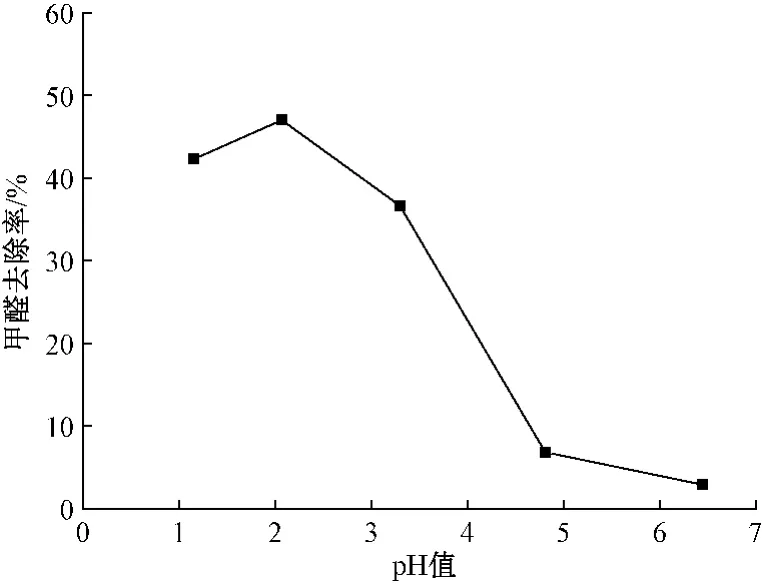
图9 pH值对催化氧化甲醛性能影响Fig.9 Influence of pH on catalytic oxidation performance on formaldehyde
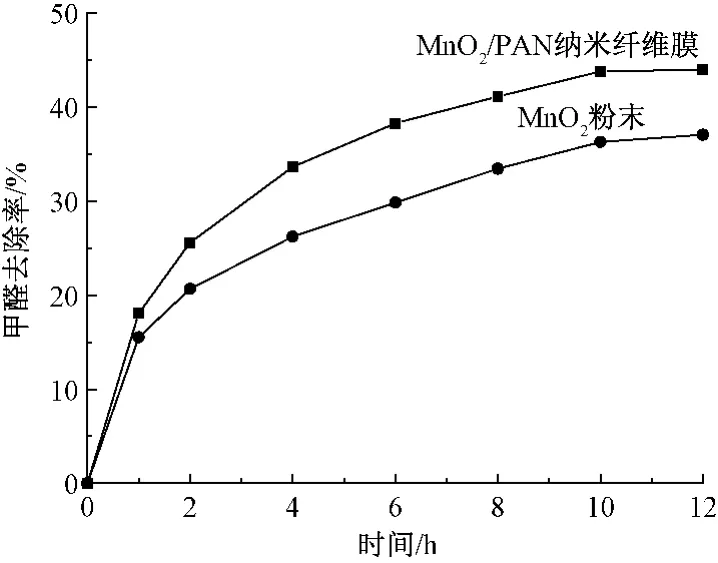
图10 MnO2/PAN纳米纤维膜与MnO2粉末时间-甲醛去除率曲线Fig.10 Time-formaldelyde removal rate curve of MnO2/PAN nanofibers and MnO2powder
3 结论
MnO2与PAN共混静电纺丝制得MnO2/PAN纳米纤维膜,MnO2/PAN纳米纤维膜纤维直径随着MnO2含量增大和纺丝电压提高均减小;MnO2/PAN纳米纤维膜具有催化氧化甲醛的性能。随着反应温度升高,MnO2/PAN纳米纤维膜的甲醛催化氧化性能提高,选择60℃为最适宜温度。pH值在0~7范围内,随pH值下降,MnO2/PAN纳米纤维膜甲醛去除率先升高后下降,最佳pH值为2。与MnO2粉末相比,MnO2纳米纤维膜具有催化速率提高、甲醛去除率提高等优点。
[1] 王燕云.甲醛废气的处理方法及研究进展[J].云南大学学报,2010,32(2):240-245.WANG Yanyun.Methods of formaldehyde waste gas processing and research progress[J].Journal of Yunnan University,2010,32(2):240-245.
[2] 陈雯雯.室内甲醛污染去除方法的研究进展[J].黑龙江科学,2013,4(7):42-44.CHEN Wen wen.Advance on indoor formaldehyde removal[J].Heilongjiang Science,2013,4(7):42-44.
[3] SEKINE Y.Oxidative decomposition of formaldehyde by metal oxides at room temperature[J].Atmospheric Environment,2002,36:5543-5547.
[4] 龙小燕.活性炭负载纳米二氧化钛对水体中砷的去除[J].工业水处理,2012,32(4):29-32.LONG Xiaoyan.Removal of arsenic from water by nano titanium dioxide doped with activated carbon[J].Industrial Water Treatment,2012,32(4):29-32.
[5] 朱舜.活性炭纤维负载金属铂的制备及催化氧化甲醛[J].纺织学报,2014,35(2):1-5.ZHU Shun.Catalytic oxidation of formaldehyde by activated carbon fibers supported platinum[J].Journal of Textile Research,2014,35(2):1-5.
[6] 薛潇.功能性纳米纤维材料在水过滤中的应用[D].武汉:武汉纺织大学,2013:2-3.XUE Xiao.Application of functional nanofiber materials in water filtration[D]. Wuhan:Wuhan Textile University,2013:2-3.
[7] 丁源维.静电纺制备TiO2/PVA复合纳米纤维[J].浙江理工大学学报,2013,30(1):31-35.DING Yuanwei.Photocatalytic performance investigation of TiO2/PVA nanofibers prepared by electros pinning[J].Journal of Zhejiang Sci-Tech University,2013,30(1):31-35.
[8] 王进贤.钇或钕掺杂TiO2纳米纤维的制备及光催化性能研究[J].无机材料学报,2010,25(4):379-380.WANG Jinxian.Preparation and photocatalytic activities of Y3+or Nd3+-doped TiO2nanofibers[J].Journal of Inorganic Meterials,2010,25(4):379-380.
[9] 范栓喜.活性二氧化锰的制备及对亚甲基蓝脱色研究[J].无机盐工业,2009,41(11):15-17.FAN Shuanxi. Study on preparation of activated manganese dioxide and decoloration performance of methylene blue[J].Inorganic Chemicals Industry,2009,41(11):15-17.
[10] ZHOU L.Facile in-situ synthesis of manganese dioxide nanosheets on cellulose fibers and their application in oxidative decomposition of formaldehyde[J]. The Journal of Physical Chemistry C,2011,115:16873-16878.
[11] 程司辰.基于静电纺丝法的PVDF基锂离子电池隔膜的制备与表征[D].上海:东华大学,2013:19-20.CHENG Sichen.Preparation and characterization of electrospun PVDF-based membrane as lithium battery separator[D].Shanghai:Donghua University,2013:19-20.
[12] 李妮.静电纺参数对射流和纳米纤维形态的影响[J].纺织学报,2010,31(12):13-17.LI Ni. Effect of electros pinning parameters on morphologies of nanofibers and jet[J].Journal of Textile Research,2010,31(12):13-17.
[13] 寿大华.静电纺纤维的制备及其应用[D].上海:东华大学,2009:17-20.SHOU Dahua. Preparation and application of electrospun fibers[D].Shanghai:Donghua University,2009:17-20.
[14] 孙新丽.Mn2O3纳米纤维的制备表征及其物性研究[D].吉林:东北师范大学,2008:11-12.SUN Xinli.Preparation and characterization of Mn2O3nanofibers and their properties[D].Jilin:Northeast Normal University,2008:11-12.
[15] 刘水平.PAN基碳纤维原丝的高锰酸钾改性[J].材料工程,2009(2):383-386.LIU Shuiping. Modification ofPAN carbon fiber precursor using potassium permanganate[J].Material Engineering,2009(2):383-386.
[16] 张爱华.锰化合物的热分解动力学[D].武汉:中国地质大学,2010:15-20.ZHANG Aihua.Kinetics for thermal decomposition of manganese compounds[D].Wuhan:China University of Geosciences,2010:15-20.
[17] 田华.氧化锰催化氧化甲醛的研究进展[J].化学通报,2013,76(2):100-106.TIAN Hua.Research progress in catalytic oxidation of formaldehyde by manganese oxides[J].Chemistry,2013,76(2):100-106.

