新型链行走烯烃聚合催化剂的合成及其催化活性*
李翠勤,林治宇,王 俊,宫喜艳,赵 千,王玉茹,邵 楠
(东北石油大学化学化工学院石油与天然气化工省重点实验室,黑龙江大庆 163318)
聚烯烃材料由于具有性价比高、力学性能好、易加工、化学性质稳定和可循环利用等优点,被广泛应用于日常生活、包装行业、汽车、建筑、农业和军事等领域[1-2]。然而,随着社会对材料性能要求的不断提高,原有聚烯烃材料已逐渐不能满足需求。开发具有拓扑结构、低成本和高性能的新型聚烯烃材料成为材料科学追求的目标。
目前,研发用于传统聚合方法的新型催化剂是合成新型通用聚烯烃材料的主要研究方向之一。早期常用的烯烃聚合催化剂为具有多个催化活性中心的Ziegler-Natta催化剂和具有单活性中心的茂金属催化剂。这两类催化剂虽然可用于合成高强度、高透明度和低温热封性良好的高性能聚乙烯[3-4],但合成具有不同支化拓扑结构的聚烯烃时,其支链长度和密度均受外加的昂贵α-烯烃单体的限制[5-6]。
因此,催化工作者对烯烃聚合催化剂展开了大量研究。1998 年,Brookhart[7]发现具有新型结构的吡啶亚胺铁等过渡金属化合物催化剂可制备具有不同支化拓扑结构的支化聚乙烯,并在此基础上提出了“链行走机理”,阐述了该类催化剂催化合成超支化聚乙烯的具体反应历程[8-9]。
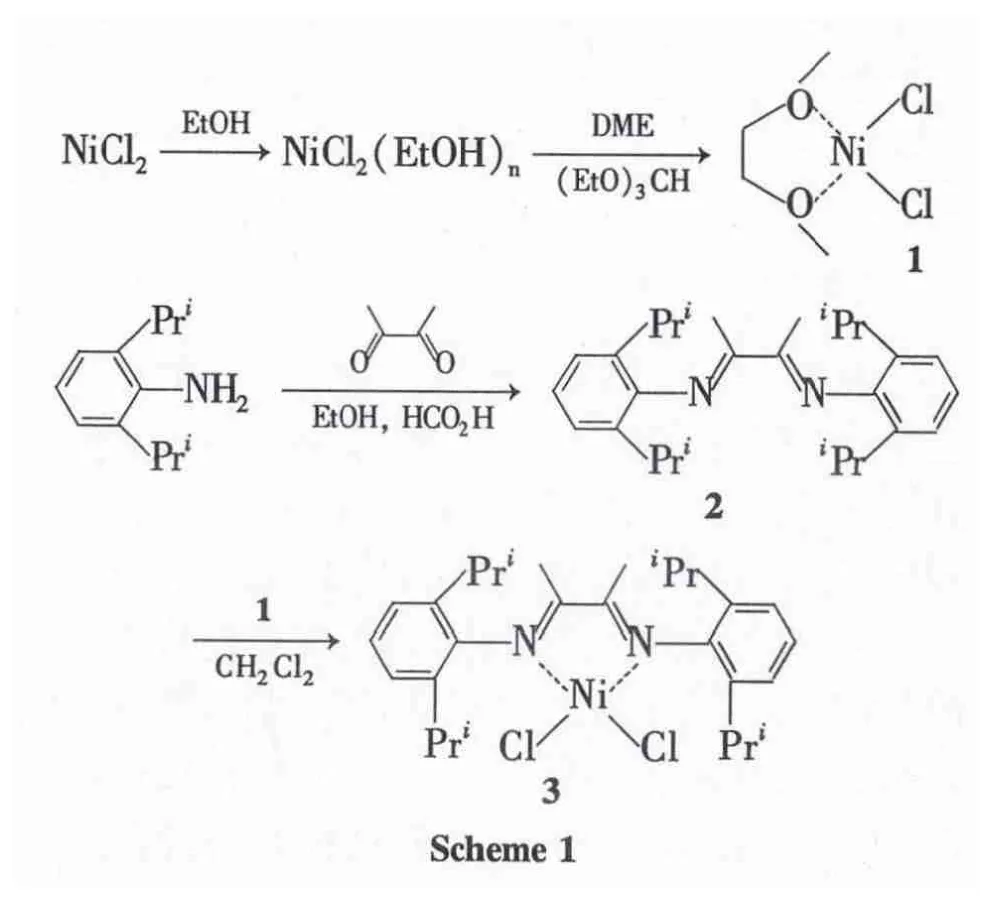
本文根据“链行走”理论,以二氯化镍为原料制得配合物(DME)NiCl2(1);以2,6-二异丙基苯胺和丁二酮为原料,经缩合反应制得α-二亚胺配体(2);1与2经络合反应合成了一种用于乙烯齐聚制备超支化聚乙烯的新型链行走催化剂(3,Scheme 1),其结构经IR,XRD和元素分析表征。以乙烯齐聚为探针反应,考察了助催化剂,反应温度和反应时间对3催化活性的影响。
1 实验部分
1.1 仪器与试剂
HITACHI 260.50型傅立叶变换红外光谱仪(KBr压片);D/max-2200PC型 X-射线衍射仪;CHN-O Rapid型元素分析仪。
所用试剂均为分析纯。
1.2 合成
(1)1的合成
氮气保护,在反应瓶中加入无水二氯化镍0.64 g和无水乙醇30 mL,搅拌使其溶解;于30℃反应12 h。于60℃/133 MPa蒸馏5 h得二氯化镍与乙醇的络合物A。
在反应瓶中加入乙二醇二甲醚15 mL和原甲酸三乙酯1 mL,氮气保护下于30℃搅拌反应0.5 h。加入A,反应12 h;于60℃/133 MPa蒸馏8 h得黄色固体1,收率98.75%。
(2)2的合成
在反应瓶中加入丁二酮8.00 g(90 mmol),2,6-二异丙基苯胺 39.83 g(225 mmol)和无水乙醇80 mL,搅拌使其溶解;缓慢滴加甲酸2 mL,滴毕,氮气保护下于 25℃反应 12 h。冷却至-4℃,静置72 h。过滤,滤饼用0℃无水乙醇(3×20 mL)洗涤,于45℃干燥3 h得荧光黄色针状晶体2,收率83.43%。
(3)3的合成
在反应瓶中加入1 0.69 g(3 mmol)和无水二氯甲烷30 mL,搅拌使其溶解;氮气保护下于25 ℃搅拌0.5 h;加入 2 1.3 g(32 mmol),反应24 h。于20℃/133 MPa蒸馏3 h,残余物于35℃干燥8 h得红棕色晶体3,收率96.4%。
1.3 催化活性
用真空和氮气将Schlenk聚合瓶循环置换三次。在氮气保护下,注入正己烷50 mL,通入乙烯使其充分吸收至饱和。加入助催化剂Al(Et)319.36 g(0.14 mol),于 20 ℃搅拌 10 min;加入 3 150 mg(0.29 mmol)的环己烷溶液,调节乙烯通入量,维持反应瓶内压力为0.134 MPa,反应0.5 h。用5%酸化乙醇溶液100 mL终止反应。静置0.5 h,取上层液体,于60℃/133 Pa减压蒸除环己烷得黏稠液体支化聚乙烯。
2 结果与讨论
2.1 表征
(1)IR
图1为2和3的 IR谱图。由图1可见,2 957 cm-1和2 867 cm-1处强峰为甲基的伸缩振动吸收峰;1 459 cm-1和1 363 cm-1处吸收峰为甲基的变形振动吸收峰;1 638 cm-1处吸收峰为C=N特征吸收峰;1 183 cm-1处吸收峰为Ar-N特征吸收峰[7];这些特征峰证明合成的2结构与理论设计相符。由3的IR谱图还可见,1 640 cm-1处吸收峰为强度减弱的C=N特征吸收峰;736 cm-1处吸收峰为Ni-N特征吸收峰;这表明亚胺基中N和Ni发生了配位作用。

图1 2和3的IR谱图Figure 1 IR spectra of 2 and 3
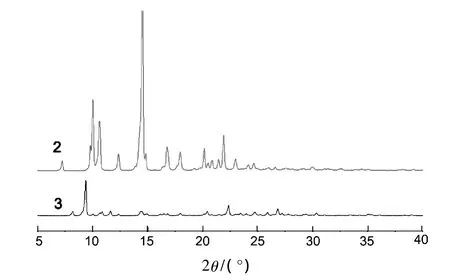
图2 2和3的XRD谱图Figure 2 XRD spectra of 2 and 3
(2)XRD
图2为2和3的XRD谱图。由图2可见,2中14.50处衍射峰较之于3中相同位置弱很多,这表明2与1中的镍进行了络合,使3晶体结构更加无序,晶体粒子更为细小。正是这种无序结构使活性组分发生稳定络合且充分分散。
(3)元素分析
表1为2和3的元素分析结果。由表1可见,2和3中各元素的实测值与理论值基本一致。进一步说明合成的2和3的结构与Scheme 1预期一致。

表1 2和3的元素分析数据Table 1 Elemental analysis of 2 and 3
2.2 催化活性
为优化3催化乙烯聚合工艺,考察了助催化剂Al(Et)3和催化剂3的用量比 r[n(Al)∶n(Ni)],反应温度和反应时间对3催化活性的影响。
(1)r
Al(Et)30.14 mol,其余反应条件同1.3,考察r对3催化活性(α)的影响,结果见表2。

表2 r对3催化活性的影响*Table 2 Effect of r on the catalytic activities of 3

表3 反应温度对3催化活性的影响*Table 3 Effect of temperature on the catalytic activities of 3
由表2可见,随着r增加,3催化活性呈现先上升后下降的趋势。当r=600时,催化活性达到最大值[2.5×106g PE·(mol·Ni·h·MPa)-1]。其原因可能在于,r较低时,Al(Et)3量太少,不足以活化活性中心和去除反应体系中的有害物质[10];r增大,Ni(Ⅱ)配合物活性中心数目增多,催化活性增强;但过量Al(Et)3反而是链转移剂,因此r>600时,3催化活性反而降低。因此,最佳r=600。
(2)反应温度
r=600,其余反应条件同 2.2(1),考察反应温度对3催化活性的影响,结果见表3。由表3可知,随着反应温度升高,催化活性下降。这是由于温度升高,乙烯气体在聚合溶液中的溶解度降低及3失活速率加快所致[11]。因此,最佳反应温度为20℃。
(3)反应时间
r=600,反应温度20℃,其余反应条件同2.2(1),考察反应时间对3催化活性的影响,结果见表4。

表4 反应时间对3催化活性的影响*Table 4 Effect of reaction time on the catalytic activities of 3
由表4可见,随着反应时间延长,催化活性降低。当t=0.5 h时,催化活性为2.5×106g PE·(mol·Ni·h·MPa)-1;当 t=6 h 时,催化活性降低至0.33 × 106g PE·(mol·Ni·h·MPa)-1。这主要是因为随着反应时间延长,3活性中心逐渐分解所致。因此,最佳反应时间为0.5 h。
综上所述,使3达到最佳催化效果的反应条件为:AlEt30.14 mol,n(Al)∶n(Ni)=600,于20 ℃反应0.5 h。
2.3 产物表征
在最佳反应条件[r=600,于20℃反应0.5 h]下合成的支化聚乙烯,其结构经IR表征(谱图略)。由IR分析可见,2 923 cm-1和2 856 cm-1处特征峰为亚甲基不对称伸缩振动和对称伸缩振动吸收峰;1 463 cm-1和1 377 cm-1处特征峰为甲基不对称变形振动和对称变形振动吸收峰;722 cm-1附近特征峰表明分子中有4个以上的亚甲基相连;1 096 cm-1和1 021 cm-1附近的特征峰为支链烷烃的碳-碳骨架振动吸收峰。以上特征峰表明反应产物为支化聚乙烯。
3 结论
合成了一种用于乙烯齐聚制备超支化聚乙烯的新型链行走催化剂(3)。在最佳反应条件[AlEt30.14 mol,n(Al)∶n(Ni)=600,于20 ℃反应0.5 h]下,3催化活性为 2.5×106gPE·(mol·Ni·h·MPa)-1。齐聚产物为支化聚乙烯,部分支链中碳原子数大于4。
[1]Galli P,Vacellio G.Polyolefins:The most promising large-volume materials for the 21st century[J].J Polym Sci Pol Chem,2004,42:396 -415.
[2]刘建.中国聚烯烃工业2009年发展状况及“十二·五”展望[J].中国塑料,2010,24(4):17 -18.
[3]Stewart H.Olefin markets to grow strongly until 2009[J].ICIS Chemical Business,2007,29(7):29.
[4] 刘丰收,伍青.支化及超支化聚乙烯[J].石油化工,2006,35(4):303 -309.
[5]王俊,宫喜艳,李翠勤,等.后过渡金属催化剂催化乙烯制备超支化聚乙烯新进展[J].化工进展,2012,31(12):2729 -2735.
[6] 毛炳权.发展我国聚烯烃技术的一些建议[J].石油炼制与化工,2001,32(2):1 -3.
[7]Small B L,Brookhart M,Bennett A M A.Highly active iron and cobalt catalysts for the polymerization of ethylene[J].J Am Chem Soc,1998,120:4049 -4050.
[8]Johnson L K,Killian C M,Brookhart M.New Pd(Ⅱ)and Ni(Ⅱ)based catalysts for polymerization of ethylene and α-olefins[J].J Am Chem Soc,1995,117:6414-6415.
[9]Guan Z B.Recent progress of catalytic polynerization for controlling polymer topology[J].Chem Asian J,2010,5:1058 -1070.
[10]Usami T,Takayama S.Fine-branching structure in high-pressure,low-density polyethylenes by 50.10-MHz carbon-13NMR analysis[J].Macromolecules,1984,17:1756 -1761.
[11]Petrie K,Docoslis A,Ye Z B,et al.Non-covalent/non-specific functionalization of multi-walled carbon nanotubes with a hyperbranched polyethylene and characterization of their dispersion in a polyolefin matrix[J].Carbon,2011,49:3371 -3391.

