HPLC法测定奥美拉唑镁原料药中醋酸的残留量
李菊平,刘效平,金永亮
(1.山东大学药学院,山东 济南 250012;2.寿光富康制药有限公司,山东 潍坊 262700;3.西北农林科技大学资源环境学院,陕西 咸阳 712100)
在奥美拉唑镁工艺合成中使用了醋酸[1~4]调节pH,醋酸残留在文献中一般采用气相色谱法[5~9]测定醋酸的残留,但在试验过程发现气相色谱GCFID色谱条件下方法的冰醋酸的响应值很小,且重现性受GC色谱条件如溶剂、不同批次的色谱柱、不同品牌的仪器灵敏度影响大。因此我们使用更为稳定的高效液相色谱法(HPLC)系统使用外标法对奥美拉唑镁冰醋酸的残留进行控制,由于奥美拉唑在此波长210 nm下没有吸收,因此对冰醋酸的吸收峰没有干扰,且在实验中发现,若成品中的醋酸残留超过0.05%很容易使奥美拉唑镁降解[2],UV吸光度变化明显,导致药物不稳定,《中国药典》2015年版[10]和人用药品注册技术要求国际协调会(ICH)中均将醋酸列为三类溶剂,因此需要对它的残留量进行检测[11]。文献没有用HPLC法C18色谱柱进行检测原料药中醋酸的报道,相对于已有的离子色谱法[12],C18色谱柱比离子色谱柱更耐用、更稳定。本文建立了HPLC方法C18色谱柱测定醋酸在奥美拉唑镁的残留,方法灵敏,色谱柱耗材易于采购,稳定性好,检测成本低,操作简便、结果准确,方法重现性好 符合《中国药典》2015年版[10]的有关规定。
1 仪器与试药
Agilent 1200液相色谱仪,UV检测器,自动进样器,柱温箱,X -Bridge TM C18(4.6mm ×250mm,5μm)色谱柱;奥美拉唑镁原料药(寿光富康制药有限公司,批号:52111505001、52111505002、52111505003)。
2 方法
2.1 色谱条件 色谱柱:X-Bridge C18(4.6mm×250mm,5μm)检测波长:210nm;流速:1.2mL·min-1;进样量:20μL;柱温:35 ℃;流动相:0.07%磷酸溶液(用氢氧化钠溶液调节pH至3.0):甲醇 =950∶50;溶媒:50%甲醇。
2.2 方法 标准贮备液:取醋酸100mg,精密称定,置于100mL容量瓶中,用溶媒稀释至刻度。
对照品溶液:准确量取5mL标准贮备液置于100mL容量瓶中,用溶媒稀释至100mL。
供试品溶液:称取样品1.0g,精密称定,置于10mL容量瓶中,用溶媒溶解,漩涡振荡器振荡1min,混合均匀,用溶媒稀释至刻度,微孔滤膜过滤。
系统适用性:①对照溶液连续进样6次,RSD≤2%;②分离度溶液中杂质峰与相邻杂质峰的分离度应大于1.5。图谱见图1。
外标法计算:奥美拉唑镁中残留的醋酸不得超过0.05%(即10%的ICH限度)。
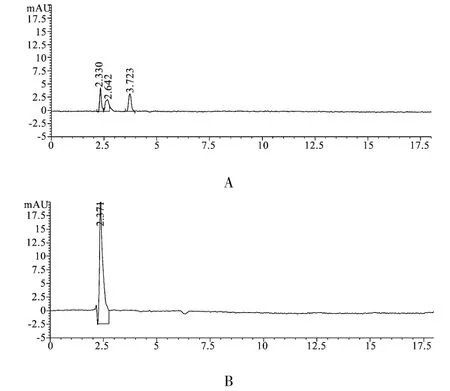
图1 HPLC图谱
2.3 线性关系考察 分别精密量取“2.2”项下的标注贮备液1、2、4、5、6mL 分置于5 个100mL 容量瓶中,分别用溶媒稀释至100mL,摇匀,得系列浓度的溶液,按“2.2”项下的色谱条件测定,分别以浓度X(mg·mL-1)为横坐标,峰面积Y为纵坐标进行线性回归,醋酸在其浓度范围内线性关系良好)。线性方程为:Y=0.01209X+582.94186;相关系数 r=0.999994。结果:冰醋酸检测浓度线性范围为0.01 ~0.06mg·mL-1。
2.4 精密度试验 取对照溶液,按,按“2.1”项下的色谱条件测定,连续进样6次,醋酸峰面积的检测结果为29.82、29.26、28.51、28.74、29.62、28.58,平均值为29.09,RSD 为1.92%,精密度良好。
2.5 检测限定量限试验 将对照品浓溶液逐级稀释后,依法测定,直至信噪比 S/N=10.4 不低于10∶1,所得的最低检测浓度即为定量限度 25.0 μg·mL-1(250 ppm);直至信噪比 S/N=3.1 不低于3∶1,所得的最低检测浓度即为检测限度 5.0 μg·mL-1(50 ppm),且检测限低于定量限的30%。
2.6 回收率试验 分别称取奥美拉唑镁(批号:52111505001)5 g,精密称定,置于9个50mL容量瓶中,按照限度要求对限度浓度的80%、100%、120%3个水平对9份样品进行加标,即加入4、5、6mL标准储备液,每个水平浓度重复3次,按“2.1”项下的色谱条件进行测定,计算醋酸的回收率和RSD,结果见表1。
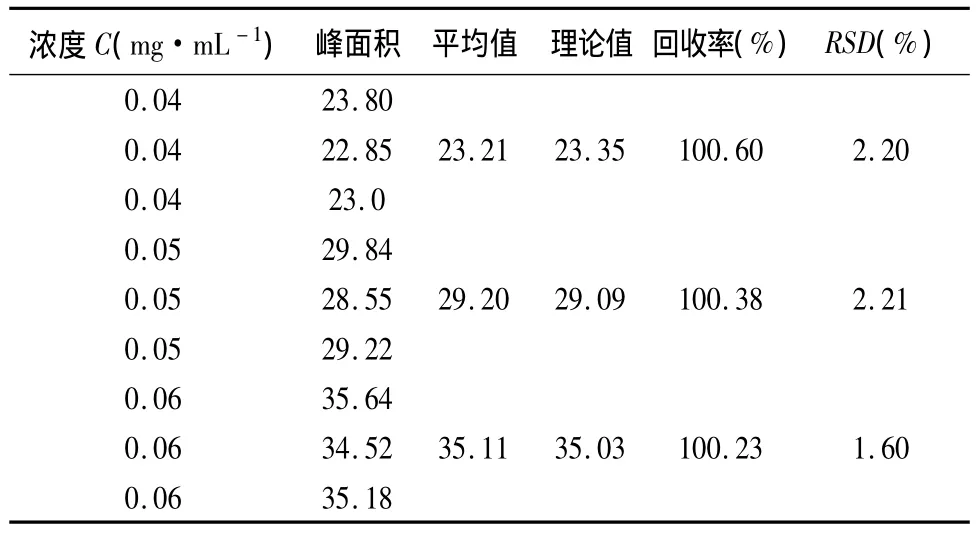
表1 回收率试验结果
结果表明,3个浓度下方法的回收率满足要求。
2.7 样品测定 分别量取对照溶液和供试品溶液按“2.1”项下色谱条件测定,记录色谱图,按外标法以峰面积计算供试品中醋酸的残留,结果3批样品(批号:52111505001、52111505002、52111505003)均未检出。
3 讨论
冰醋酸在奥美拉唑镁的工艺中既是反应物又调节pH值,酸性物质的存在会对奥美拉唑镁的稳定性产生影响,酸性条件下产品很容易降解,为增加产品的稳定性,需要用稳定、经济的方法对冰醋酸在原料药奥美拉唑镁中的残留进行严格控制。《中国药典》2015年版和人用药品注册技术要求国际协调会(ICH)中均将醋酸列为三类溶剂,残留限度是5000 ppm。用常规的顶空-气相色谱(HS-GC)法检测发现其峰面积响应值很小,信噪比S/N低于3.0;而用气相色谱-质谱(GC-MS)检测会增加产品的检测成本。因此我们开发HPLC法对冰醋酸的残留进行控制,冰醋酸能够与奥美拉唑镁中的可检测组分完全分离,准确度高,并且检测成本低。虽然法定限度是NMT 5000 ppm,但我们对冰醋酸制定了更严格的内控标准NMT 500 ppm(10%的ICH限度),保证了产品在整个生命周期内的稳定性。
[1]冯常炜,李振峰,赵治国,等.奥美拉唑镁肠溶片与奥美拉唑胶囊治疗消化性溃疡的临床随机对照研究[J].胃肠病学和肝病学杂志,2004,13(4):414 -416.
[2]楼忠裕,王康达.奥美拉唑镁肠溶片长期维持治疗慢性复发性消化性溃疡临床观察[J].现代实用医学,2008,20(5):362.
[3]刘开明.奥美拉唑治疗消化性溃疡的剂量与疗程分析[J].中国现代药物应用,2010,4(19):20 -22.
[4]英君伍.双氧水催化氧化法合成奥美拉唑的研究[D].大连:大连理工大学,2012.
[5]严欢,唐明清,毛艳,等.毛细管气相色谱法测定氯高铁血红素原料药中的冰醋酸残留量[J].中国药房,2012,23(45):4285 -4286.
[6]孟涛,唐奎山,尤楠.齐多夫定中冰醋酸残留量检测方法研究[J].辽宁医药,2007,22(3):21 -22.
[7]黄京芳,徐沄,彭方,等.毛细管气相色谱法同时测定盐酸氨溴索中乙醇、醋酸和甲苯残留量[J].药物分析杂志,2005,25(4):466 -468.
[8]解艳,吕文博.气相色谱法检查醋酸钾中冰醋酸残留量[J].科技创新与应用,2014,10:15.
[9]井玥,王刚,张爱莲,等.气相色谱法测定磺胺多辛中的冰醋酸和N,N-二甲基甲酰胺残留[J].南京师大学报(自然科学版),2012,35(2):93 -96.
[10]国家药典委员会.中华人民共和国药典2015版(二部)[S].北京:中国医药科技出版社,2015.
[11]王梅.梯度洗脱HPLC法测定尼莫地平原料药中残留醋酸[J].齐鲁药事,2012,31(7):404 -406.
[12]晏菊姣.离子色谱法测定盐酸氨溴索中醋酸残留量[J].中国药品标准,2008,9(3):203-205.

