HPLC法测定出血热预防片中的女贞苷、特女贞苷、哈巴苷和哈巴俄苷
钱永健, 张 超
(1.广州医科大学药学院,广东 广州 510182;2.广州市妇女儿童医疗中心,广东 广州 510623)
HPLC法测定出血热预防片中的女贞苷、特女贞苷、哈巴苷和哈巴俄苷
钱永健1,2,张 超1*
(1.广州医科大学药学院,广东广州510182;2.广州市妇女儿童医疗中心,广东广州510623)
目的 建立高效液相色谱法测定出血热预防片中女贞苷、特女贞苷、哈巴苷和哈巴俄苷的定量测定方法。方法采用依利特Hypersi1C18色谱柱(4.6 mm×200 mm,5μm);体积流量1.0 mL/min;女贞苷和特女贞苷的检测流动相为甲醇-0.1%磷酸(42∶58),检测波长为224 nm;哈巴苷和哈巴俄苷的检测流动相为乙腈-0.03%磷酸溶液,哈巴苷检测波长为210 nm,哈巴俄苷检测波长为280 nm。结果 女贞苷和特女贞苷分别在0.012 6~0.252 0μg(r= 0.999 2)、0.073 2~1.464 0μg(r=0.999 6)范围内进样量与峰面积的线性关系良好,平均回收率分别为97.1%、98.2%,RSD(n=6)分别为1.0%、1.1%。哈巴苷和哈巴俄苷分别在0.095 2~1.904 0μg(r=0.999 5)、0.013 4~0.268 0μg(r=0.999 1)范围内进样量与峰面积呈良好的线性关系,平均加样回收率分别为98.7%、97.0%,RSD(n=6)分别为0.7%、0.9%。结论 本方法简便、快捷,结果准确,重复性好,可应用于出血热预防片的质量控制。
出血热预防片;女贞苷;特女贞苷;哈巴苷;哈巴俄苷
出血热预防片为卫生部药品标准中药成方制剂第十二册收录处方,由女贞子、玄参、地黄、白茅根、丹参、丹皮和板蓝根等七味药物组成。具有凉血化瘀、清热解毒的功效,可用于预防流行性出血热。原质量标准仅对个别药味进行了显微鉴别,未对方中的任何药味进行定性或定量测定[1-2]。为保证产品质量,确保临床疗效,本实验采用高效液相色谱法对女贞子中女贞苷、特女贞苷和玄参中哈巴苷、哈巴俄苷进行了测定。
1 仪器与材料
1.1仪器 Agi1ent 1200高效液相色谱仪;G1322A脱气机、G1329A自动进样器、G1311A四元泵、Chemstation色谱工作站;G1315B可变波长检测器。
1.2材料 女贞苷对照品(批号111918-201102,纯度以88.6%计)、特女贞苷对照品(批号111926-201203,纯度以96.4%计)、哈巴苷对照品(批号111729-201204,纯度以94.5%计)和哈巴俄苷对照品(批号111730-201207,纯度以97.1%计)均购于中国食品药品检定研究院;出血热预防片(每片相当原生药0.667 5 g,素片0.3 g/片,包糖衣后0.5 g/片,批号分别为130719、130725、130729)自制;甲醇、乙腈(色谱纯,安徽时联特种溶剂股份有限公司);磷酸(分析纯,广州化学试剂二厂);水为重蒸馏水。
2 方法与结果
2.1女贞苷和特女贞苷的定量分析
2.1.1色谱条件及系统适应性试验 依利特Hypersi1C18色谱柱(4.6 mm×200 mm,5μm);甲醇-0.1%磷酸(42∶58)为流动相[3-6],检测波长224 nm[6-9];体积流量1.0 mL/min。在上述色谱条件下,女贞苷、特女贞苷与其他组分分离效果良好,理论塔板数以女贞苷计算应不低于3 000。
2.1.2混合对照品及供试品溶液的制备 精密称取女贞苷、特女贞苷对照品适量,加甲醇溶解并定容,制成含女贞苷0.012 6 mg/mL、特女贞苷0.073 2 mg/mL的混合对照品溶液。取适量本品,除去糖衣,研细,取约1.0 g,精密称定,置锥形瓶中,加甲醇50 mL,超声波(300 W,25 kHz)超声25 min,放冷,用甲醇补足减失的质量,摇匀,用微孔滤膜滤过,即得供试品溶液。
2.1.3阴性对照试验 依据出血热预防片处方比例称取除女贞子的其他药味,按出血热预防片的制备工艺制成女贞子空白样品,按照“2.1.2”项下供试品溶液的配制方法制成女贞子空白溶液。分别精密吸取10μL的供试品溶液、混合对照品溶液及女贞子空白溶液,按“2.1.1”项下的色谱条件进行色谱分析,空白溶液对样品测定无干扰,结果见图1。
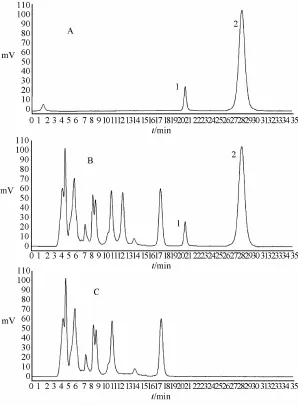
图1 女贞苷和特女贞苷的HPLCFig.1 HPLC of IigustrofIavone and specnuezhenide determ ination
2.1.4线性关系考察 精密量取混合对照品溶液1、5、10、15、20μL,按“2.1.1”项下色谱条件进行测定,以峰面积为纵坐标,女贞苷、特女贞苷量为横坐标进行线性回归,得两种成分的回归方程。女贞苷为Y=2.168 7×106Ⅹ-394.1,r= 0.999 2;特女贞苷为Y=3.154 2×106Ⅹ+631.2,r=0.999 6。结果表明女贞苷、特女贞苷分别在0.012 6~0.252 0μg、0.073 2~1.464 0μg进样量与峰面积呈良好的线性关系。
2.1.5精密度试验 精密吸取混合对照品溶液,按“2.1.1”项下的色谱条件重复进样6次,记录女贞苷和特女贞苷的峰面积,RSD分别为0.7%、0.4%,表明仪器具有良好的精密度。
2.1.6重复性试验 取同一批样品(批号130719),按“2.1.2”项下供试品溶液制备方法制备6份供试品溶液,分别测定,女贞苷和特女贞苷的RSD分别为0.8%、0.3%。结果表明本方法重复性良好。
2.1.7稳定性试验 取同一批样品(批号130719)的同一供试品溶液,在放置0、1、2、4、6、8 h后精密吸取10μL进样,测定其峰面积值,女贞苷和特女贞苷的RSD分别为0.7%、0.4%,供试品溶液8 h内基本稳定。
2.1.8加样回收率试验 取已知含有量(女贞苷0.648 mg/g,特女贞苷3.64 mg/g)的同一批样品(批号130719)适量,除去糖衣,研细,取约0.5 g,精密称定,置具塞锥形瓶中,加混合对照品溶液25 mL、甲醇25 mL,超声波(300 W,25 kHz)超声25 min,放冷,用甲醇补足减失的质量,摇匀,用微孔滤膜滤过,制成加样供试液。精密吸取加样供试液10μL,进样分析,计算回收率,结果见表1。
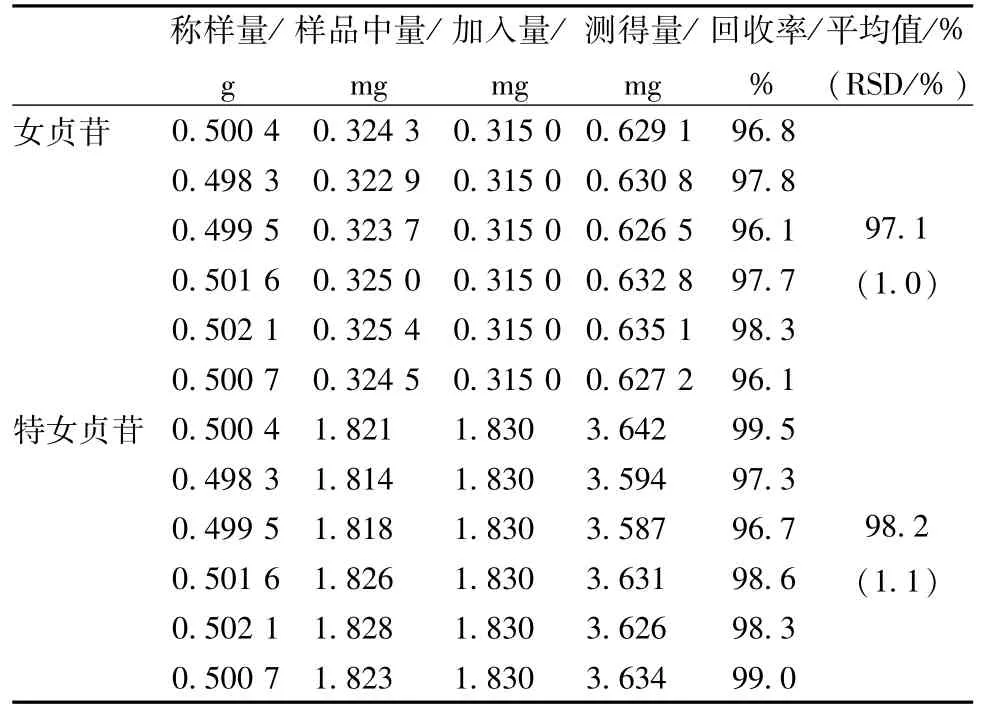
表1 女贞苷和特女贞苷回收率试验结果Tab.1 Resu Its of recovery tests for IigustrofIavone and specnuezhenide
2.2哈巴苷和哈巴俄苷的定量分析
2.2.1色谱条件及系统适应性 Hypersi1C18色谱柱(4.6 mm×200 mm,5μm);流动相A为乙腈,流动相B为0.03%磷酸溶液[10-13],梯度洗脱(0~11 min,40.0%A;11~25 min,40.0%→65.0% A;25~50 min,65.0%A);体积流量1.0 mL/min;检测波长λ1=210 nm(0~25 min),λ2=280 nm(25~50 min)。在上述色谱条件下,哈巴苷、哈巴俄苷与其他组分基线分离良好,以哈巴俄苷计理论塔板数应不低于3 500。
2.2.2混合对照品及供试品溶液的制备 精密称取哈巴苷、哈巴俄苷对照品适量,加50%甲醇溶解并定容,制成含哈巴苷0.095 2 mg/mL、哈巴俄苷为0.013 4 mg/mL的混合对照品溶液。取本品适量,除去糖衣,研细,取约1.0 g,精密称定,置锥形瓶中,加50%甲醇50 mL,超声波(300 W,25 kHz)超声30 min,放冷,用50%甲醇补足减失的质量,摇匀,用微孔滤膜滤过,作为供试品溶液。
2.2.3阴性对照试验 依据出血热预防片处方比例称取除玄参的其他药味,按出血热预防片的制备工艺制成玄参空白样品,按照“2.2.2”项下供试品溶液的配制方法制成玄参空白溶液。分别精密吸取10μL的供试品溶液、混合对照品溶液及玄参空白溶液,按“2.2.1”项下的色谱条件进行色谱分析,空白溶液对测定无干扰,结果见图2。
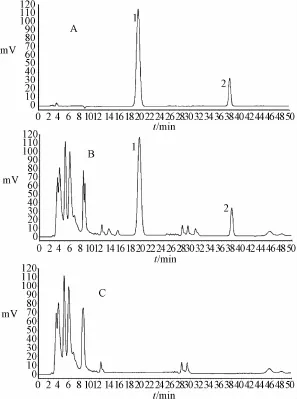
图2 哈巴苷和哈巴俄苷的HPLCFig.2 HPLC chromatograms of harpagide and harpagoside
2.2.4线性关系考察 精密吸取混合对照品溶液1、5、10、15、20μL,按“2.2.1”项下色谱条件进行测定,以峰面积为纵坐标,哈巴苷、哈巴俄苷进样量为横坐标进行线性回归,得两种成分的回归方程。哈巴苷为Y=2.624 9×106Ⅹ+264.7,r= 0.999 5;哈巴俄苷为Y=2.016 2×106Ⅹ-348.3,r=0.999 1。结果表明哈巴苷、哈巴俄苷分别在0.095 2~1.904 0μg、0.013 4~0.268 0μg范围内进样量与峰面积呈良好的线性关系。
2.2.5稳定性试验 取同一批样品(批号130719)的同一供试品溶液,在放置0、1、2、4、6、8 h后精密吸取10μL进样,测定其峰面积值,哈巴苷和哈巴俄苷的RSD分别为0.5%、0.9%,供试品溶液8 h内基本稳定。
2.2.6精密度试验 精密吸取混合对照品溶液重复进样6次,按以上色谱条件测定哈巴苷和哈巴俄苷的峰面积,RSD分别为0.4%、0.8%,表明仪器具有良好的精密度。
2.2.7重复性试验 取同一批样品(批号130719),按上述方法制备6份供试品溶液,分别测定,哈巴苷和哈巴俄苷的RSD分别为0.4%、0.6%。结果表明本方法具有良好的重复性。
2.2.8加样回收率试验 取已知含有量(哈巴苷4.78 mg/g、哈巴俄苷0.682 mg/g)的同一批样品(批号130719),除去糖衣,研细,取约0.5 g,精密称定,置锥形瓶中,加混合对照品溶液25 mL,50%甲醇25 mL,超声波(300 W,25 kHz)超声30 min,放冷,用50%甲醇补足减失的质量,摇匀,用微孔滤膜滤过,制成加样供试液。精密吸取加样供试液10μL,进样分析,计算回收率,结果见表2。
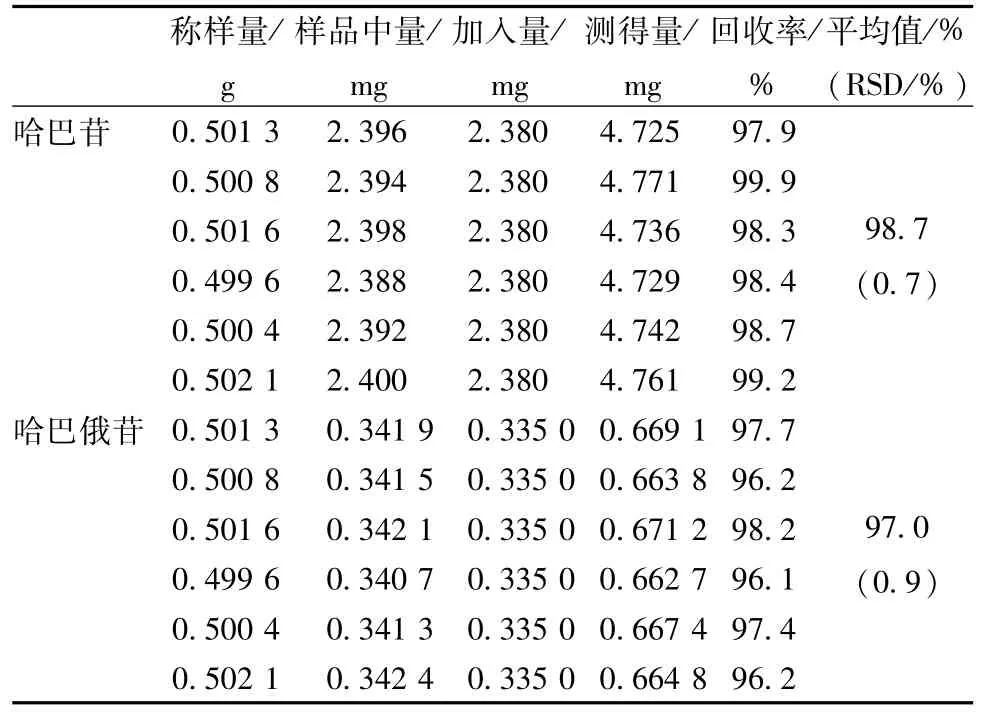
表2 哈巴苷和哈巴俄苷回收率试验Tab.2 Resu Its of recovery tests for harpagide and harpagoside
2.3样品测定 取3批样品按“2.1”项下女贞苷和特女贞苷测定方法和“2.2”项下哈巴苷和哈巴俄苷测定方法测定其中4个成分的量,结果见表3。
3 讨论
3.1流动相的选择 实验中曾采用乙腈与0.03%磷酸溶液、甲醇与0.1%磷酸为流动相以不同比例梯度洗脱同时测定以上4种成分,结果以乙腈与0.03%磷酸溶液为流动相不同比例梯度洗脱时,哈巴苷和哈巴俄苷能达到基线分离,而女贞苷和特女贞苷分离效果差,不能有效分离;以甲醇与0.1%磷酸为流动相不同比例梯度洗脱时,哈巴俄苷达不到有效分离,峰型差,拖尾现象严重,其他3个成分峰型良好。故本实验采用两种不同流动相对处方中的4个主要成分进行了测定,以有效控制产品的质量。
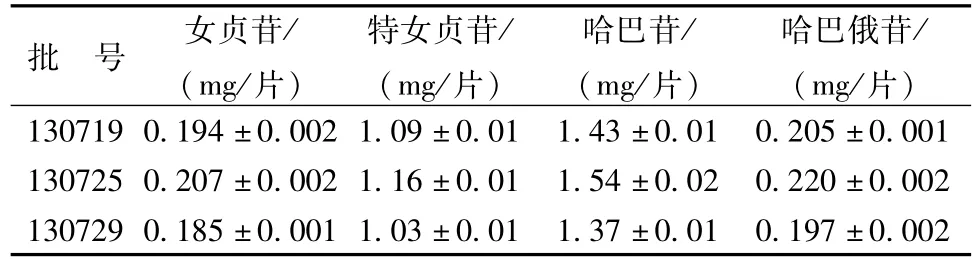
表3 样品测定结果Tab.3 Resu Its of content determ ination
3.2提取方式的选择 考虑到制剂生产时检验的便捷性,采用超声(300 W,25 kHz)提取进行试验,女贞苷和特女贞苷提取时间参考文献分别以20、25、30 min进行考察,哈巴苷和哈巴俄苷提取时间参考文献分别以20、30、40 min进行考察,结果女贞苷和特女贞苷测定时样品提取最佳时间为25 min,哈巴苷和哈巴俄苷测定时样品提取最佳时间为30 min。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:43,108-109,附录30,附录36.
[2]国家药典委员会.国家药品标准中药成方制剂第十二册[S].北京:人民卫生出版社,1998:41.
[3]郭宇洁,任 烨,葛争艳,等.正交试验法比较女贞子中齐墩果酸与特女贞苷的乙醇提取工艺[J].中成药,2013,35(2):277-281.
[4]封丽彬.HPLC测定生新发胶囊中特女贞苷的含量[J].中国中医药信息杂志,2013,20(12):54-55.
[5]姚卫峰,何 睦,蒋叶娟,等.基于多指标加权评分的中药复方二至丸提取工艺研究[J].中成药,2013,35(7):1414-1418.
[6]刘宏明,刘昱霞,徐楠楠.HPLC测定六味五灵片中特女贞苷的含量[J].中国实验方剂学杂志,2013,19(5):147-149.
[7]商桂春,袁大鹏,刘海滨.HPLC测定女珍颗粒中特女贞苷的含量[J].中国实验方剂学杂志,2013,19(4):153-155.
[8]常星洁,刘汉清,邹建荣,等.响应面法优化女贞子有效成分的提取工艺[J].中成药,2012,34(5):839-842.
[9]阮 佳,贺英菊,詹 雁,等.含女贞子复方中药的提取及干燥工艺研究[J].华西药学杂志,2013,28(3):278-280.
[10]黄滔敏,陈念祖,王东蕾,等.红外光辅助萃取-HPLC法测定玄参中肉桂酸和哈巴俄苷的含量[J].中国药房,2011,22(19):1796-1798.
[11]朱海涛,管 群,陈 黎,等.正交试验优选风湿Ⅱ号合剂提取工艺[J].中国药房,2010,21(19):1754-1756.
[12]魏庆华,王 勤.HPLC测定增液承气口服液中哈巴苷和哈巴俄苷含量[J].中国实验方剂学杂志,2012,18(7):81-83.
[13]梁 晨,徐思思,聂诗明.HPLC法测定不同产地微波真空干燥玄参中哈巴苷和哈巴俄苷的含量[J].数理医药学杂志,2012,25(6):688-690.
[14]白云娥,袁鹏飞,王庆辉,等.HPLC-UV波长转换法测定玄参药材及饮片中哈巴苷与哈巴俄苷的含量[J].中国中药杂志,2011,36(19):2697-2702.
[15]李 娟,萧 伟,刘 涛,等.玄参脑保护作用提取物的工艺优化[J].中成药,2011,33(6):1057-1059.
Determ ination of IigustrofIavone,specnuezhenide,harpagide and harpagoside in Chuxuere Yufang
Tab Iets by HPLC
QIAN Yong-jian1,2, ZHANG Chao1*
(1.School of Pharmaceutical Sciences,Guangzhou Medical University,Guangzhou 510182,China;2.Guangzhou Women and Children'sMedical Center,Guangzhou 510623,China)
AIM To deve1op an HPLC method for determining the contents of 1igustrof1avone,specnuezhenide,harpagide and harpagoside in Chuxuere Yufang
Tab1ets.M ETHODS An Hypersi1C18co1umn was used as the chromatographic co1umn,the f1ow rate was 1.0 mL/min.Measurement of 1igustrof1avone and specnuezhenide wasmade usingmethano1-0.1%phosphoric acid(42∶58)as themobi1e phase,and setting UV detection wave1ength at254 nm.Measurementof harpagide and harpagosidewasmade using acetonitri1e asmobi1e phase A and 0.03%phosphoric acid asmobi1e phase B,setting the UV detection wave1ength at 210 nm and 280 nm. RESULTS The good 1inear re1ationships between the concentration and peak area were in the ranges of0.012 6-0.252 0μg(r=0.999 2)for 1igustrof1avone,0.073 2-1.464 0μg(r=0.999 6)for specnuezhenide,respective1y.Their average recoveries were 97.1%(RSD=1.0%)and 98.2%(RSD=1.1%),respective1y.The good 1inear re1ationships between the concentration and peak area va1ue were in the range of0.095 2-1.904 0μg(r=0.999 5)for harpagide、0.013 4-0.268 0μg(r=0.999 1)for harpagoside,respective1y.Their average recoveries were 98.7%(RSD=0.7%)and 97.0%(RSD=0.9%),respective1y.CONCLUSION The method is simp1e,accurate and reproducib1e and can be used for the qua1ity contro1of Chuxuere Yufang
Tab1ets.
Chuxuere Yufang
Tab1ets;1igustrof1avone;specnuezhenide;harpagide;harpagoside
R927.2
A
1001-1528(2015)01-0116-05
10.3969/j.issn.1001-1528.2015.01.023
2014-04-02
钱永健(1980—),男,药师,主要从事临床药学服务。E-mai1:qianyongjian1unwen@163.com
张 超(1964—),男,副教授,主要从事药物化学和天然药物化学研究。E-mai1:zhangchao1unwen1@163.com