基于壳聚糖的分子印迹聚合物的制备和应用
许龙,黄运安,朱秋劲,2,叶春
(1贵州大学酿酒与食品工程学院,贵州 贵阳550025;2贵州大学食品科学工程研究中心,贵州 贵阳550025)
化[5],大多数以丙烯酸及其衍生物为功能单体,聚合发生在有机溶剂中,这限制了生物大分子物质的应用,因此寻求一种能在温和条件下聚合的功能单体是研究者们的一个愿望。壳聚糖是甲壳素脱乙酰基的产物,甲壳素是自然界中含量丰富的氨基多糖化合物且具有无毒、生物可降解以及生物相容性等特点[6]。壳聚糖分子上既有羟基和氨基,又有以半缩醛形式存在的糖苷键等官能团,如图1所示。所以在一定条件下,壳聚糖可以发生O-和N-酰基化、N-烷基化、含氧无机酸的酯化、醚化、氧化及螯合等化学反应,合理地利用这些化学反应可以合成具有特征性能的壳聚糖衍生物,从而扩大了壳聚糖的应用范围。壳聚糖分子中的氨基和羟基是比较活泼的,其中壳聚糖中的羟基有两种:一种为一级羟基,即C6—OH,第二种为二级羟基,即C3—OH;从壳聚糖的空间构型来看,C6—OH的空间位阻小,可以自由旋转,其反应活性高,而C3—OH在壳聚糖的椅式结构中空间位阻大,所以其反应活性比较低,故与壳聚糖羟基官能团的反应基本上都是与C6—OH的反应。壳聚糖已经在生物科学及多个领域包括水处理、膜分离、化妆品、食品以及制药等得到广泛应用[7]。由于壳聚糖链上众多的氨基和羟基为其结构修饰和合成分子印迹聚合物提供了可能,因此,近年来将其用于分子印迹材料合成,开展具有特定吸附功能的聚合物研究成为热点[8],见图2。
基于壳聚糖的分子印迹聚合物的制备和应用
许龙1,黄运安1,朱秋劲1,2,叶春1
(1贵州大学酿酒与食品工程学院,贵州 贵阳550025;2贵州大学食品科学工程研究中心,贵州 贵阳550025)
摘要:壳聚糖具有良好的生物相容性和独特的分子结构,基于其制备的分子印迹聚合物因亲和性和选择性高、应用范围广等特点引起了广泛的关注。本文首先总结了壳聚糖和改性壳聚糖在分子印迹聚合物制备中的作用,然后介绍了壳聚糖分子印迹聚合物在环境污染治理、医药、蛋白质分离与识别、手性物质分离以及吸附功能成分等方面的应用,分析了壳聚糖分子印迹聚合物在各个应用领域的优缺点及发展方向。最后,从发展绿色分子印迹技术以及分子印迹技术与电化学传感器结合等层面对壳聚糖分子印迹聚合物的应用前景进行了展望。
关键词:壳聚糖;分子印迹技术;生物相容性;聚合物
自从20世纪40年代诺贝尔奖获得者PAULING提出分子印迹的思想、德国科学家WULFF等首次报道分子印迹有机高分子材料以来,特别是1993年瑞典科学家MOSBACH在《Nature》上发表有关茶碱分子印迹材料的报道后,分子印迹技术得到了飞速的发展,现已广泛应用于色谱分离、抗体或受体摸拟、生物传感器以及酶的模拟和催化合成等诸多领域[1-4]。
近年来,国内外有关分子印迹的报道很多,但目前分子印迹技术主要用于小分子物质的分离纯
化[5],大多数以丙烯酸及其衍生物为功能单体,聚合发生在有机溶剂中,这限制了生物大分子物质的应用,因此寻求一种能在温和条件下聚合的功能单体是研究者们的一个愿望。壳聚糖是甲壳素脱乙酰基的产物,甲壳素是自然界中含量丰富的氨基多糖化合物且具有无毒、生物可降解以及生物相容性等特点[6]。壳聚糖分子上既有羟基和氨基,又有以半缩醛形式存在的糖苷键等官能团,如图1所示。所以在一定条件下,壳聚糖可以发生O-和N-酰基化、N-烷基化、含氧无机酸的酯化、醚化、氧化及螯合等化学反应,合理地利用这些化学反应可以合成具有特征性能的壳聚糖衍生物,从而扩大了壳聚糖的应用范围。壳聚糖分子中的氨基和羟基是比较活泼的,其中壳聚糖中的羟基有两种:一种为一级羟基,即C6—OH,第二种为二级羟基,即C3—OH;从壳聚糖的空间构型来看,C6—OH的空间位阻小,可以自由旋转,其反应活性高,而C3—OH在壳聚糖的椅式结构中空间位阻大,所以其反应活性比较低,故与壳聚糖羟基官能团的反应基本上都是与C6—OH的反应。壳聚糖已经在生物科学及多个领域包括水处理、膜分离、化妆品、食品以及制药等得到广泛应用[7]。
由于壳聚糖链上众多的氨基和羟基为其结构修饰和合成分子印迹聚合物提供了可能,因此,近年来将其用于分子印迹材料合成,开展具有特定吸附功能的聚合物研究成为热点[8],见图2。
1 壳聚糖在分子印迹聚合物中的作用
1.1 作为功能单体
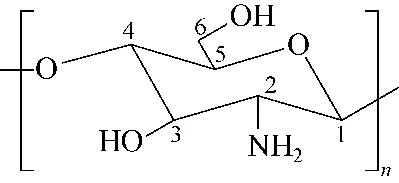
图1 壳聚糖的结构式

图2 壳聚糖分子印迹聚合物的制备原理图
壳聚糖作为功能单体参与分子印迹聚合物的合成时一般具有两种形式。一种是将不经任何化学修饰的壳聚糖直接作为功能单体用于合成分子印迹聚合物[9],常用于金属离子[10-14]、氨基酸[15-17]以及一些功能成分[18-19]的吸附。例如,黄丽梅等[19]以壳聚糖为功能单体,柚皮苷为模板分子,硫酸为交联剂,在水相中制备了水相识别柚皮苷分子印迹壳聚糖膜。红外光谱及紫外光谱分析表明,模板分子柚皮苷与壳聚糖之间产生了氢键相互作用,其作用位点在—OH、C=O和C—O—C。另一种则是将壳聚糖经过物理或化学修饰,在其氨基或羟基上引入化学基团以改善壳聚糖的物理及化学性质,而后将修饰后的壳聚糖作为功能单体合成分子印迹聚合物,常用于金属离子[20-21]、蛋白质[22-23]和某些化合物[24]的吸附以及电化学传感器[25]等领域。例如,童跃进等[23]以壳聚糖为原料,通过羧甲基化和选择甲基丙烯酸缩水甘油酯(GMA)作为功能化试剂,得到了水溶性的含乙烯基功能团的壳聚糖衍生物,而后将其作为功能单体,在水相中合成了血红蛋白印迹聚合物。该印迹聚合物显示了对血红蛋白分子特异的识别能力。此外,近年来还出现了一个新颖的改性方法——磁性壳聚糖,肖玲等[26]使用壳聚糖包埋纳米级四氧化三铁,采用表面印迹技术制备了纳米级Cu2+印迹磁性壳聚糖,改善了分子排布的空间有序性,增加了金属离子与壳聚糖分子的配位点,减小了内传质过程,该吸附剂表现出吸附量大、选择性高、平衡快、操作简单、可重复使用以及廉价高效等特点。磁性分子印迹技术为从复杂基质中选择性分离特定物质提供了更加快捷和方便的方法。
1.2 作为功能载体
将壳聚糖作为载体应用于分子印迹领域主要集中于蛋白质的分子印迹[27-31]。合成此类分子印迹聚合物时,常常将壳聚糖整合到聚丙烯酰胺凝胶中,这样可以制备出相对均匀的分子印迹聚合物,而且用于蛋白质的吸附时吸附量大。此外,可以根据用途将这种复合凝胶制成不同的形态,例如,颗粒和微球常常用于生物吸附,薄膜则常常用于传感器中作识别元件。这类分子印迹聚合物中,常以丙烯酰胺为功能单体,N,N′-亚甲基双丙烯酰胺为交联剂,顺丁烯二酐为改性试剂。例如,GUO等[31]以血红蛋白作为模板分子,丙烯酰胺作为功能单体,顺丁烯二酸酐改性的壳聚糖作为载体,合成的分子印迹聚合物对血红蛋白分子显示出了高选择性,且可作为色谱固定相从混合蛋白样品中分离血红蛋白。
2 壳聚糖分子印迹聚合物的应用进展
2.1 治理环境污染方面
2.1.1 对金属离子的吸附性能
金属离子的污染问题一直是世界的难题[32]。寻找快捷有效的去除污水中重金属离子的方法一直是科研人员探索的热点。大量的研究工作表明,壳聚糖及其衍生物是重金属离子的良好吸附剂[33-35]。但是壳聚糖分子中的游离氨基在酸性环境下易被质子化为NH3+而造成溶解流失,因此,为了使壳聚糖得到广泛应用,需使用特定的交联剂如甲醛、戊二醛(图3)、乙二醛、环氧氯丙烷和乙二醇环氧丙基醚等交联。在这些金属离子印迹聚合物中,金属离子与功能单体的静电、配位等键合作用相比于氢键、范德华力和疏水作用等具有空间结构稳定、定向性强等特点。

图3 戊二醛交联的壳聚糖结构式
NISHAD等[36]以环氧氯丙烷为交联剂制备了Co2+印迹壳聚糖分子印迹聚合物,并考察了该聚合物的吸附量及选择性等性能。壳聚糖对Fe2+的吸附量比Co2+的吸附量高,而合成的此种印迹聚合物对Co2+的吸附量明显高于Fe2+。在pH=4~5的环境下,该聚合物都保持了对Co2+的高选择性吸附性能,为含有强络合剂核反应堆的净化提供了便利。尽管已有壳聚糖[37]和Co2+印迹壳聚糖[38]用于吸附Co2+的报道,但是其并未解决Fe2+和Co2+共同存在的情况下专一性吸附Co2+的问题,而该印迹就显示出了其优良的专一性。LIU等[39]在壳聚糖内嵌入纳米α-Fe2O3,以As3+为印迹离子,合成了一种新型的壳聚糖微球。该种微球在30℃、pH=5的环境下对As3+的最大吸附量达到6.18mg/g,显示了良好的选择特异性和重复利用性。该印迹聚合物的新颖之处在于其利用了壳聚糖以及α-Fe2O3的协同效应,与传统的吸附剂如活性炭和活性氧化铝相比,明显提高了对As3+的吸附效率并且简化了后处理过程。FAN 等[40]首次合成了表面印迹Ag+的磁性硫脲-壳聚糖并将其应用于水溶液中选择性吸附Ag+,该聚合物不仅在30℃、pH=5的环境下对Ag+的吸附量达到4.93mmol/g之多,更是可以重复利用5次以上。LIU 等[41]以铀酰离子为模板分子,用乙二醇二缩水甘油醚将壳聚糖与聚乙烯醇交联制得了互穿网络离子印迹水凝胶。该凝胶对铀酰离子的吸附过程符合Langmuir和Freundlich等温吸附模型,吸附量明显高于非印迹水凝胶。特异性吸附实验表明该离子印迹壳聚糖/聚乙烯醇凝胶能够有效地去除水中的铀酰离子,为从水溶液中特异性去除铀酰离子提供了良好的应用前景。
目前壳聚糖有关的离子印迹技术已经有了很大的进展,涉及Cu、Ni、Co、Zn、Pb、Cd、Cr、Hg 和As等众多金属离子,而针对某些常见阴离子的研究工作有待于进一步展开。进一步的研究发现,金属离子聚合物的应用研究仍然集中于对目标离子的分离及富集等方面,对于金属离子的分析检测领域涉及较少。进一步提高壳聚糖-金属离子印迹聚合物的吸附专一性能,并将离子印迹技术同某些检测技术相结合,通过电信号或光信号的响应来实现对金属离子的定量检测将是未来的发展热点。
2.1.2 对大分子污染物的吸附性能
近年来,全氟辛烷磺酸和它的前体物质相继在水、废水、沉积物甚至于人类的血清和肝脏中以及野生动物体内被检测出来[42-43],其具有环境抵抗性、生物累积性以及潜在毒性,已经在全球范围内造成了严重的环境污染。YU等[44]以全氟辛烷磺酸为模板分子,壳聚糖为功能单体,环氧氯丙烷为交联剂首次制备了可以从水中选择性吸附全氟辛烷磺酸的分子印迹聚合物,该聚合物对全氟辛烷磺酸的吸附量为560μmol/g,而非印迹聚合物的吸附量仅为258μmol/g。该印迹聚合物可以至少反复使用5次以上且不会影响吸附量,为从水及废水中去除全氟辛烷磺酸带来了良好的应用前景。然而,其不足之处在于该印迹聚合物受pH值影响显著,吸附量会随着pH值和离子强度的升高而降低,应用该聚合物作为吸附剂去除全氟辛烷磺酸时,还需调整pH值至一定范围。
问题4 根据上面的总结,在Rt△ABC中,∠C=90°,当∠A取其它一定度数的锐角时,它的对边与邻边的比值会出现什么情况?对此,你有怎样的猜想?
工业废水、地表水、土壤甚至饮用水中相继检测出卡马西平(carbamazepine,CBZ),引起了社会广泛重视。由于其稳定且难于生物降解,传统的污水处理方法很难将其去除。ZHANG等[45]基于壳聚糖-Fe3O4,以甲基丙烯酸为辅助功能单体,乙二醇二甲基丙烯酸酯为交联剂,运用沉淀聚合制备了一种新型的快速分离水样中卡马西平的磁性分子印迹聚合物(MMIP)。该MMIP的优点在于其应用范围广,在不同的水样中包括自来水、河流水以及污水中对卡马西平的吸附量没有明显差别,为解决卡马西平污染问题带来了希望。
工业废水中的色素和颜料如果不能及时去除,排放到环境中势必会造成环境污染,对水生生物造成毒害。由于这些染料分子能够抵抗传统的好氧消化而难以处理,选择一种价格低廉的吸附剂成为目前比较有效的一种方法。FAN等[46]将壳聚糖包裹在磁铁矿(Fe3O4)表面,以茜素红为模板分子,环氧氯丙烷为交联剂,合成的分子印迹聚合物对茜素红的最大吸附量为40.12mg/g,吸附容量明显高于非印迹磁性壳聚糖微球。而且该吸附剂显示了高稳定性和重复利用性,为去除废水中的茜素红提供了一种有效的方法。
目前,污水处理仍然是国内外最受关注的问题之一,分子印迹技术的飞速发展为污水处理提供了新的思路,分子印迹聚合物由于重复利用率高、特异性好及低消耗等特点将会成为污水处理的一种新趋势。将壳聚糖分子印迹聚合物应用于污水处理已经取得了很大的进步,然而关于其在污水处理方面应用的报道还比较少,进一步提高壳聚糖分子印迹聚合物的吸附容量并合成出针对多种污染物的印迹聚合物,将会是壳聚糖分子印迹聚合物在污水治理方面的发展趋势。
2.2 医药方面
目前分子印迹技术在医药方面的应用主要集中于药物缓释及手性分离、模拟天然抗体和酶、作免疫吸附剂以及制成生物传感器用于痕量检测等方面[47]。而壳聚糖又具有良好的生物活性、相容性与可降解性,可用于抗菌、防腐、止血和促进伤口愈合等[48]。因此,将分子印迹技术结合壳聚糖应用于医药领域有着广阔的应用前景。
尿素是肾衰竭病人血液中的主要有毒成分,目前最常用的临床疗法主要是用活性炭吸附或者口服吸附剂[49]。CHENG等[50]运用表面分子印迹技术,以壳聚糖为功能单体,环氧氯丙烷为交联剂合成了尿素分子印迹聚合物,并对合成条件如乙酸体积、模板分子用量、预聚合时间、交联剂用量等进行了优化。在最佳条件下,该MIP对尿素的吸附量达到了9.61mg/g,而非印迹聚合物的吸附量仅有4.37mg/g。将该聚合物用于血清中尿素的吸附时,吸附率达到了54.51%。
目前,对于重型肝炎和肝功能衰竭的主要疗法就是进行肝脏移植和人工肝支持系统。胆红素是亚铁血红素的代谢产物。当肝功能出现异常时,胆红素的含量就会上升。WU等[51]通过反相悬浮法,以胆红素为模板分子,蔗糖为致孔剂,戊二醛为交联剂,1,6-己二胺和聚酰胺为氨基化试剂,合成了壳聚糖多孔微球。该微球在37℃、0.05mol/L的磷酸缓冲溶液(pH=7.20~7.40)对胆红素有良好的吸附量。这种生物相容性的吸附微球为利用人工肝支持系统技术吸附胆红素带来了良好的应用前景。
壳聚糖分子印迹聚合物在医药方面的应用还比较少。虽然壳聚糖分子无毒无害且相容性好,但在选择交联剂及溶剂时也应该尽量选择无毒化合物,且应对合成的聚合物做好安全性评价,以确保将聚合物应用于医药领域时不会因有毒有害物质残留而产生副作用。且用于药物传递的分子印迹聚合物还应具备抵抗各种酶和化学物质侵袭的能力,以适应复杂多变的体内环境。
2.3 蛋白质识别方面
多数蛋白质印迹材料的构建是基于非共价印迹的原理,靠氢键、范德华力、离子键以及疏水相互作用等结合。蛋白质分子受其体积庞大、结构复杂、构象灵活及水溶性等特点的限制,至今仍是分子印迹领域极具挑战性的科研领域。要实现蛋白质大分子印迹需在传统小分子印迹的基础上加以改进和创新。
壳聚糖是一种具有生物相容性的天然多糖,物理或化学改性常常被用来改善其孔径、机械强度、化学稳定性、亲水性及生物相容性,而后将其作为基质,聚丙烯酰胺作为功能单体,N,N′-亚甲基双丙烯酰胺为交联剂,目标蛋白为模板分子,合成的蛋白质印迹聚合物用于蛋白质的分离识别近年来引起了广泛关注。GUO等[62]以壳聚糖为功能性生物高聚物,在其分子中引入醛基后,制备了溶菌酶分子印迹聚合物。去除模板分子后,该聚合物对溶菌酶的吸附量达到12.19mg/g,而非印迹聚合物吸附量仅为6.57mg/g。XIA等[64]以N,N′-亚甲基双丙烯酰胺为交联剂,制备了基于壳聚糖和聚丙烯酰胺的半互穿聚合物网络(semi-IPN)凝胶,该凝胶网络对血红蛋白的吸附量达到36.53mg/g。DAN等[67]以N,N′-亚甲基双丙烯酰胺为交联剂,将壳聚糖分别与丙烯酰胺(AAm)、丙烯酸(AA)、甲基丙烯酸(MAA)以及甲基丙烯酸-2-羟基乙酯(HEMA)4种功能单体接枝共聚,制备出了专一性识别卵清蛋白的分子印迹聚合物。其中壳聚糖与甲基丙烯酸的接枝共聚物(CS-g-MAA)对卵清蛋白的吸附量最大,达到了22.94mg/g。
蛋白质是水溶性大分子,壳聚糖对其识别主要发生在水溶液中,选择合适的交联剂对提高聚合物的吸附性能及特异性识别能力非常重要,且应充分考虑大分子蛋白质的特殊性,保证聚合过程中蛋白质的生物活性及空间构象。但是由于水分子强大的水和能力,氢键的作用能效会被削弱,因此如何增强水环境中的氢键效能是壳聚糖-蛋白质分子印迹技术需要克服的难点。
2.4 手性物质分离方面
目前,手性异构体的拆分方法主要有结晶法和色谱法。然而这两种方法的分离效率还远未达到令人满意的程度。手性物质分离依然是分离领域最难解决但也是最热门的问题之一。壳聚糖作为一种天然的手性物质,生物相容性好,其分子中的氨基和羟基可通过氢键与氨基酸结合[77-78],以对映体的一种异构体为印迹分子,通过一定的化学交联,就可以形成与模板分子空间几何构型和化学基团相匹配的分子印迹聚合物。
吴洪等[15]以L-苯丙氨酸为印迹分子,采用相转化法制备了分子印迹壳聚糖膜,通过渗透实验考察了分子印迹壳聚糖膜和非印迹空白壳聚糖膜对D,L-苯丙氨酸(D,L-Phe)混合物的手性拆分性能,并与空白膜进行了比较。印迹膜的分离因子达到1.43。MONIER等[16]以戊二醛为交联剂,L-谷氨酸为模板分子,制备了壳聚糖交联树脂(LGIC),并将该树脂应用于从水溶液中固相萃取分离L-谷氨酸。吸附等温曲线显示,该树脂对L-谷氨酸和D-谷氨酸的最大吸附量分别为42mg/g±0.80mg/g和26mg/g±1.20mg/g,而非印迹壳聚糖对L-谷氨酸和D-谷氨酸的最大吸附量均为7mg/g±0.60mg/g。MONIER等[71]又以乙二醛作为交联剂,L-天冬氨酸为模板分子,制备了L-天冬氨酸/壳聚糖分子印迹聚合物(LAIC)。吸附等温曲线显示,该印迹聚合物对L-天冬氨酸和D-天冬氨酸的最大吸附量分别为48mg/g±0.70mg/g和27mg/g±1.00mg/g,而非印迹聚合物对L-天冬氨酸和D-天冬氨酸的吸附量均为9mg/g±0.80mg/g。MONIER等[72]以甲醛作为交联剂,S-扁桃酸为模板分子,制备了S-扁桃酸/壳聚糖分子印迹聚合物。吸附等温曲线显示,该印迹聚合物对S-扁桃酸和R-扁桃酸的最大吸附量分别为100mg/g±0.50mg/g和64mg/g±0.80mg/g,而非印迹聚合物对S-扁桃酸和R-扁桃酸的吸附量均为55mg/g±1.00mg/g,该分子印迹聚合物可应用于从水溶液中固相萃取分离S-扁桃酸。
壳聚糖分子印迹聚合物在手性分离上的应用已较成熟,然而其分离因子还不能达到理想的效果。如何更深层次地探索结合位点的作用机理和传质机理,从而更有效地提高壳聚糖分子印迹聚合物的分离效果,提高识别专一性,将会是手性物质印迹聚合物的突破点。
2.5 吸附功能成分方面
由于壳聚糖具有许多独特的生理功能和良好的生物相容性,壳聚糖分子印迹聚合的吸附作用还常常被用于对有效成分的分离上。而且将分子印迹技术结合固相萃取应用于复杂生物或化学样品中的选择性富集成为了近年来比较活跃的研究领域[79-81]。
关怀民等[24]以壳聚糖为原料,通过其活性基团与甲基丙烯酸缩水甘油酯反应,在其C6位引入了乙烯基。在印迹分子鸟嘌呤的存在下,利用该乙烯基壳聚糖衍生物为功能单体和乙二醇二甲基丙烯酸酯为交联剂,合成了可通过非共价自组装法形成多个识别位点的生物碱基——鸟嘌呤的分子印迹聚合物。对不同碱基的分子识别能力评价表明,该聚合物实现了对鸟嘌呤的选择分子识别。段玉清等[75]以大黄酸为印迹分子,大孔壳聚糖为功能载体,甲基丙烯酸为功能单体,制备了大黄酸的分子印迹聚合物。通过固相萃取和HPLC评价了聚合物对大黄酸的选择性分离效果。与非印迹聚合物相比,印迹聚合物表现出快速吸附和高吸附量的优良特性,平衡吸附量为909.50μg/g。通过固相萃取可选择性地从大黄游离蒽醌衍生物中富集分离大黄酸,并获得满意的效果。XIA等[76]以大孔壳聚糖作为功能载体,甲基丙烯酸为功能单体,槲皮苷为模板分子,制备了壳聚糖分子印迹聚合物并考察其吸附效果。该印迹聚合物在黄酮类混合物中显示出对槲皮素的高选择性。
通常所采用的富集分离功能成分的方法具有选择性吸附能力差、难以实现一次性分离等缺点,而将分子印迹技术与固相萃取技术相结合为功能成分的富集、分离及纯化提供了一种有效可行的新方法。目前,壳聚糖分子印迹聚合物对功能成分的富集应用范围还不够,如何制备出选择特异性良好的壳聚糖分子印迹聚合物成为富集功能成分的关键环节。
综上所述,总结壳聚糖分子印迹聚合物的应用实例见表1。

表1 壳聚糖分子印迹聚合物应用实例
3 结论与展望
壳聚糖是天然多糖中唯一的碱性多糖,其多糖链上的活性氨基质子化为NH3+后可以通过静电相互作用或螯合作用吸附一些重金属离子、染料甚至蛋白质等。然而仅仅以壳聚糖或改性壳聚糖作为吸附剂很难达到理想的吸附量和吸附专一性等效果。而且其分子中的游离氨基在pH值较低的条件下被质子化为NH3+后易造成溶解流失,稳定性差,限制了壳聚糖的使用。近年来,将壳聚糖或经过接枝改性、化学及生物修饰的壳聚糖作为功能单体或功能载体,选择合适的交联剂合成对目标分子具有特异性识别能力的分子印迹聚合物,成为了扩大壳聚糖应用范围的亮点。壳聚糖分子印迹聚合物不仅可以达到吸附专一性的效果,也可以扩大吸附容量,更是可以从选择性吸附传统的氨基酸等小分子物质过渡到核苷酸、多肽和蛋白质等生物大分子,与分子印迹技术将来的发展方向相符。此外,壳聚糖因其具有无毒、生物可降解及生物相容性等良好特性,成为了近年来分子印迹领域中常用有毒功能单体的良好替代物,为发展绿色分子印迹技术提供了有利支撑。随着壳聚糖在分子印迹领域研究的不断深入和应用领域的不断拓展,在解决目前壳聚糖分子印迹聚合物所存在的缺点的同时,将壳聚糖分子印迹聚合物结合电化学传感元件制成传感器应用于快速检测,也是今后的研究热点。
参 考 文 献
[1] WULFF G,SARHAN A,ZABROCKI K. Enzyme-analogue built polymers and their use for the resolution of racemates[J]. Tetrahedron Letters,1973,14(44):4329-4332.
[2] NORRLÖW Olof,GLAD Magnus,MOSBACH Klaus. Acrylic polymer preparations containing recognition sites obtained by imprinting with substrates[J]. Journal of Chromatography A,1984,299:29-41.
[3] MOSBACH Klaus,RAMSTRÖM Olof. The emerging technique of molecular imprinting and its future impact on biotechnology[J]. Nature Biotechnology,1996,14(2):163-170.
[4] VLATAKIS George,ANDERSSON Lars I,MÜLLER Ralf,et al. Drug assay using antibody mimics made by molecular imprinting[J]. Nature,1993,361:645-647.
[5] MOSBACH Klaus,HAUPT Karsten. Some new developments and challenges in non-covalent molecular imprinting technology[J]. Journal of Molecular Recognition,1998,11:62-68.
[6] RINAUDO Marguerite. Chitin and chitosan:properties and applications[J]. Progress in Polymer Science,2006,31(7):603-632.
[7] WAN NGAH WS,TEONG L C,HANAFIAH M A K M. Adsorption of dyes and heavy metal ions by chitosan composites:a review[J]. Carbohydrate Polymers,2011,83(4):1446-1456.
[8] LIU Bingjie,WANG Dongfeng,YU Guangli,et al. Adsorption of heavy metal ions,dyes and proteins by chitosan composites and derivatives:a reveiw[J]. Oceanic and Coastal Sea Research,2013,12(3):500-508.
[9] 赵冬艳,乔旭光,徐志祥. 壳聚糖在分子印迹技术中的应用研究进展[J]. 食品与生物技术学报,2014(6):570-575.
[10] 洪英,钟泽辉,郭宾. 壳聚糖印迹聚合物对Zn2+的吸附动力学[J].化工进展,2011,30(6):1296-1301.
[11] 石光,胡小艳,郑建泓,等. Cu(Ⅱ) 印迹壳聚糖交联多孔微球去除水溶液中金属离子[J]. 离子交换与吸附,2010(2):103-110.
[12] 徐文峰. 分子印迹技术改性壳聚糖吸附废水中钴(Ⅱ)[J]. 理化检验(化学分册),2010(7):829-831.
[13] 柯仁怀,关怀民,林妹,等. 离子印迹交联壳聚糖的制备及其对Zn2+的吸附作用[J]. 福建医科大学学报,2007,41(5):440-443.
[14] 王劲松,陈思光,徐华,等. 印迹与交联壳聚糖吸附水中微量 Cr(Ⅵ) 的对比试验研究[J]. 南华大学学报(自然科学版),2010,1:74-77.
[15] 吴洪,赵艳艳,喻应霞,等. 分子印迹壳聚糖膜分离手性苯丙氨酸[J]. 功能高分子学报,2007,19(20):262-266.
[16] MONIER M,EL-SOKKARY A M. Preparation of molecularly imprinted cross-linked chitosan/glutaraldehyde resin for enantioselective separation of L-glutamic acid[J]. International Journal of Biological Macromolecules,2010,47(2):207-213.
[17] MONIER M,AYAD D M,WEI Y,et al. Preparation of cross-linked chitosan/glyoxal molecularly imprinted resin for efficient chiral resolution of aspartic acid isomers[J]. Biochemical Engineering Journal,2010,51(3):140-146.
[18] 常勇慧. 壳聚糖分子印迹槲皮素识别材料的制备[J]. 江西化工,2011(2):98-101.
[19] 黄丽梅,马秀玲. 分子印迹壳聚糖膜和柚皮苷模板分子间相互作用的研究[J]. 广州化学,2009,34(1):27-31.
[20] 杨潇,张朝晖,张华斌,等. 基于壳聚糖修饰碳纳米管表面铅离子印迹材料的制备及其性能研究[J]. 分析化学,2011,39(1):34-38.
[21] BIRLIK Ebru,ERSÖZ Arzu,DENIZLI Adil,et al. Preconcentration of copper using double-imprinted polymer via solid phase extraction[J]. Analytica Chimica Acta,2006,565(2):145-151.
[22] 王艺峰,王立莹,刘洲,等. 壳聚糖与羧甲基壳聚糖蛋白质印迹聚合物的制备及吸附性能[J]. 高分子材料科学与工程,2011,27 (9):126-129.
[23] 童跃进,关怀民. 壳聚糖基蛋白质分子印迹聚合物的制备及识别性能研究[J]. 福建师范大学学报(自然科学版),2010(1):73-76.
[24] 关怀民,童跃进. 壳聚糖乙烯基衍生物的合成及其对鸟嘌呤的印迹识别[J]. 科学技术与工程,2009(8):2038-2041.
[25] 孙兆辉,连惠婷,孙向英,等. 石墨烯掺杂对分子印迹电化学传感器的增敏作用[J]. 华侨大学学报(自然科学版),2012,33(4):401-407.
[26] 肖玲,陈乐英. 表面印迹纳米磁性壳聚糖的制备及对 Cu(Ⅱ)的吸附研究[J]. 离子交换与吸附,2008,24(3):193-199.
[27] 高婷,郭敏杰,樊志,等. 牛血清白蛋白分子印迹壳聚糖树脂的制备[J]. 天津科技大学学报,2010,25(1):20-23.
[28] 张莹,苏立强. 壳聚糖表面胰蛋白酶分子印迹聚合物的制备及性能的研究[J]. 化工时刊,2010,24(8):9-11.
[29] 王华芳,何运华,何锡文,等. 3-氨基苯硼酸为功能单体在壳聚糖上印迹牛血清白蛋白的研究[J]. 高等学校化学学报,2008,29(4):726-730.
[30] 刘秋叶,何锡文,李文友,等. 壳聚糖包裹硅胶载体印迹牛血红蛋白的研究[J]. 高等学校化学学报,2009,30(4):691-696.
[31] GUO Tianying,XIA Yongqing,WANG Jin,et al. Chitosan beads as molecularly imprinted polymer matrix for selective separation of proteins[J]. Biomaterials,2005,26(28):5737-5745.
[32] 黃润华,贾振邦. 环境学基础教程[M]. 北京:高等教育出版社,1997:164-165.
[33] FINDON Ann,MCKAY Gordon,BLAIR Hal S. Transport studies for the sorption of copper ions by chitosan[J]. Journal of Environmental Science and Health,Part A,1993,28(1):173-185.
[34] 黄金明,金鑫荣. 天然高分子壳聚糖作为吸附剂的吸附特性研究[J]. 高等学校化学学报,1992,13(4):535-536.
[35] 陈世清. 甲壳素与壳聚糖在工业水处理中的应用[J]. 工业水处理,1996(2):1-2,26.
[36] NISHAD Padala Abdul,BHASKARAPILLAI Anupkumar,VELMURUGAN Sankaralingam,et al. Cobalt (Ⅱ) imprinted chitosan for selective removal of cobalt during nuclear reactor decontamination[J]. Carbohydrate Polymers,2012,87(4):2690-2696.
[37] MINAMISAWA Hiroaki,IWANAMI Hisayoshi,ARAI Nobumasa,et al. Adsorption behavior of cobalt (Ⅱ) on chitosan and its determination by tungsten metal furnace atomic absorption spectrometry[J]. Analytica Chimica Acta,1999,378(1):279-285.
[38] LIU Yan,GAO Jie,LI Chunxiang,et al. Synthesis and adsorption performance of surface-grafted Co(Ⅱ)-imprinted polymer for selective removal of cobalt[J]. Chinese Journal of Chemistry,2010,28(4):548-554.
[39] LIU Bingjie,WANG Dongfeng,LI Haiyan,et al. As(Ⅲ) removal from aqueous solution using α-Fe2O3impregnated chitosan beads with As(Ⅲ) as imprinted ions[J]. Desalination,2011,272(1/2/3):286-292.
[40] FAN L,LUO C,LV Z,et al. Removal of Ag+from water environment using a novel magnetic thiourea-chitosan imprinted Ag+[J]. Journal of Hazardous Materials,2011,194:193-201.
[41] LIU Yunhai,CAO Xiaohong,HUA Rong,et al. Selective adsorption of uranyl ion on ion-imprinted chitosan/PVA cross-linked hydrogel[J]. Hydrometallurgy,2010,104(2):150-155.
[42] GIESY John P,KANNAN Kurunthachalam. Global distribution of perfluorooctane sulfonate in wildlife[J]. Environmental Science & Technology,2001,35(7):1339-1342.
[43] SCHULTZ Melissa M,BAROFSKY Douglas F,FIELD Jennifer A. Quantitative determination of fluorinated alkyl substances by large-volume-injection liquid chromatography tandem mass spectrometry-characterization of municipal wastewaters[J]. Environmental Science & Technology,2006,40(1):289-295.
[44] YU Q,DENG S,YU G. Selective removal of perfluorooctane sulfonate from aqueous solution using chitosan-based molecularly imprinted polymer adsorbents[J]. Water Research,2008,42(12):3089-3097.
[45] ZHANG Y L,ZHANG J,DAI C M,et al. Sorption of carbamazepine from water by magnetic molecularly imprinted polymers based on chitosan-Fe3O4[J]. Carbohydrate Polymers,2013,97(2):809-816.
[46] FAN L,ZHANG Y,LI X,et al. Removal of alizarin red from water environment using magnetic chitosan with Alizarin Red as imprinted molecules[J]. Colloids and Surfaces B:Biointerfaces,2012,91:250-257.
[47] 张丽丽,彭涛,王林,等. 分子印迹技术在医药化工中的应用[J]. 化学工程师,2004(12):48-50.
[48] 程志,杜娜. 壳聚糖在医药领域应用研究进展[J]. 人民军医,2013,56(2):223-224.
[49] 何炳林,宗芳,马建标. 交联聚丙烯酸固载化氧化β-环糊精的合成及其对尿素的吸附性能[J]. 中国科学 B 辑,1993,23(3):225-229.
[50] CHENG Yuan,XU Kailin,LI Hui,et al. Preparation of urea-imprinted cross-linked chitosan and its adsorption behavior[J]. Analytical Letters,2014,47(6):1063-1078.
[51] WU Liping,WU Weihua,LI Qian,et al. The preparation of functionalized crosslinked macroporous chitosan microspheres and their adsorption properties for bilirubin[C]//Proceedings of the Macromolecular Symposia,2010. Wiley Online Library.
[52] DAI Chenglong,LIU Changsheng,WEI Jie,et al. Molecular imprinted macroporous chitosan coated mesoporous silica xerogels for hemorrhage control[J]. Biomaterials,2010,31(30):7620-7630. [53] HUO Hongyan,SU Haijia,TAN Tianwei. Adsorption of Ag+by a surface molecular-imprinted biosorbent[J]. Chemical Engineering Journal,2009,150(1):139-144.
[54] JIANG W,SU H,HUO H,et al. Synthesis and properties of surface molecular imprinting adsorbent for removal of Pb2+[J]. Applied Biochemistry and Biotechnology,2010,160(2):467-476.
[55] CHEN Chia-Yun,YANG Cheng-Yu,CHEN Arh-Hwang. Biosorption of Cu (Ⅱ),Zn (Ⅱ),Ni (Ⅱ) and Pb (Ⅱ) ions by cross-linked metal-imprinted chitosans with epichlorohydrin[J]. Journal of Environmental Management,2011,92(3):796-802.
[56] SHI Yingying,ZHANG Qianghua,FENG Liangdong,et al. Preparation and adsorption characters of C(Ⅱ)-imprinted chitosan/ attapulgite polymer[J]. Korean Journal of Chemical Engineering,2014,31(5):821-827.
[57] QADDAFI Muhammad,WAHAB Wahid,LA Nafie Nursiah,et al. Imprinted nickel-cobalt chitosan as a specific adsorbent of nickel (Ni 2) and cobalt (Co 2)[J]. Journal of Scientific & Technology Research,2014,3(9):37-42.
[58] TANG Xuejiao,WANG Chengjun. Adsorption of Ni (Ⅱ) from aqueous solution by polyaminated crosslinked Ni (Ⅱ)-imprinted chitosan derivative beads[J]. Environmental Engineering Science,2013,30(10):646-652.
[59] LIU Yunqin,LIU Yunguo,HU Xinjiang,et al. Adsorption of Cr (Ⅵ) by modified chitosan from heavy-metal polluted water of Xiangjiang River,China[J]. Transactions of Nonferrous Metals Society of China,2013,23(10):3095-3103.
[60] TAN Tianwei,HE Xiaojing,DU Weixia. Adsorption behaviour of metal ions on imprinted chitosan resin[J]. Journal of Chemical Technology and Biotechnology,2001,76(2):191-195.
[61] TANG Xuejiao,NIU Dong,BI Chengliang,et al. Hg2+Adsorption from a low-concentration aqueous solution on chitosan beads modified by combining polyamination with Hg2+-imprinted technologies[J]. Industrial & Engineering Chemistry Research,2013,52(36):13120-13127.
[62] GUO Hao,YUAN Dongying,FU Guoqi. Enhanced surface imprinting of lysozyme over a new kind of magnetic chitosan submicrospheres[J]. Journal of Colloid and Interface Science,2015,440:53-59.
[63] YANG SHAN,Wang Yuzhi,XU Minli,et al. Synthesis of modified chitosan-based molecularly imprinted polymers for adsorptive protein separation[J]. Analytical Methods,2013,5(20):5471-5477.
[64] XIA Yongqing,GUO Tianying,SONG Moudao,et al. Hemoglobin recognition by imprinting in semi-interpenetrating polymer network hydrogel based on polyacrylamide and chitosan[J]. Biomacromolecules,2005,6(5):2601-2606.
[65] GUO T,XIA Y,HAO G,et al. Chemically modified chitosan beads as matrices for adsorptive separation of proteins by molecularly imprinted polymer[J]. Carbohydrate Polymers,2005,62(3):214-221. [66] GUO T Y,XIA Y Q,HAO G J,et al. Adsorptive separation of hemoglobin by molecularly imprinted chitosan beads[J]. Biomaterials,2004,25(27):5905-5912.
[67] DAN R,WANG Y,DU L,et al. The synthesis of molecular imprinted chitosan-gels copolymerized with multiform functional monomers at three different temperatures and the recognition for the template ovalbumin[J]. Analyst,2013,138(12):3433-3443.
[68] XI Fengna,WU Jianmin. Preparation of macroporous chitosan layer coated on silica gel and its application to affinity chromatography for trypsin inhibitor purification[J]. Reactive and Functional Polymers,2006,66(6):682-688.
[69] FU Guoqi,ZHAO Jichao,YU Hao,et al. Bovine serum albumin-imprinted polymer gels prepared by graft copolymerization of acrylamide on chitosan[J]. Reactive and Functional Polymers,2007,67(5):442-450.
[70] LI F,LI J,ZHANG S. Molecularly imprinted polymer grafted on polysaccharide microsphere surface by the sol-gel process for protein recognition[J]. Talanta,2008,74(5):1247-1255.
[71] MONIER M,AYAD DM,WEI Y,et al. Preparation of cross-linked chitosan/glyoxal molecularly imprinted resin for efficient chiral resolution of aspartic acid isomers[J]. Biochemical Engineering Journal,2010,51(3):140-146.
[72] MONIER M,EL-MEKABATY A. Preparation of molecularly imprinted resin based on chitosan for chiral recognition of S-mandelic acid[J]. International Journal of Biological Macromolecules,2013,55:207-213.
[73] 魏俊,孙向英,刘斌.手性拆分L-脯氨酸分子印迹聚合物的制备及其性能[J]. 应用化学,2006,23(12):1336-1341.
[74] 农兰平,黄敏,庄玉萍. L-色氨酸分子印迹壳聚糖膜的制备及透过选择性[J]. 化学研究,2009,20(3):15-18.
[75] 段玉清,张海晖,徐菲菲,等. 分子印迹-固相萃取法选择性分离大黄酸的研究[J]. 林产化学与工业,2009,29(5):35-40.
[76] XIA Yongqing,GUO Tianying,SONG Moudao,et al. Selective separation of quercetin by molecular imprinting using chitosan beads as functional matrix[J]. Reactive and Functional Polymers,2006,66 (12):1734-1740.
[77] ABURTO Jorge,LE Borgne Sylvie. Selective adsorption of dibenzothiophene sulfone by an imprinted and stimuli-responsive chitosan hydrogel[J]. Macromolecules,2004,37(8):2938-2943.
[78] SU Haijia,WANG Zhixing,TAN Tianwei. Preparation of a surface molecular-imprinted adsorbent for Ni2+based on Penicillium chrysogenum[J]. Journal of Chemical Technology and Biotechnology,2005,80(4):439-444.
[79] 李礼,胡树国,何锡文,等. 应用分子印迹-固相萃取法提取中药活性成分非瑟酮[J]. 高等学校化学学报,2006,27(4):608-611.
[80] 蔡亚岐,牟世芬. 分子印迹固相萃取及其应用[J]. 分析测试学报,2005,24(5):116-121.
[81] 肖淑娟,李红霞,于守武. 分子印迹固相萃取法提取花生壳中木犀草素[J]. 化工进展,2010,29(2):293-296.
研究开发
Preparation and application of molecularly imprinted polymers based on chitosan
XU Long1,HUANG Yun’an1,ZHU Qiujin1,2,YE Chun1
(1School of Liquor & Food Engineering,Guizhou University,Guiyang 550025,Guizhou,China;2Food Science & Engineering Research Center,Guizhou University,Guiyang 550025,Guizhou,China)
Abstract:Chitosan has excellent bio-degradability and unique molecular structure. The molecularly imprinted polymers prepared based on chitosan usually have high affinity and selectivity and therefore wide applications. This paper summarized the function of chitosan and modified chitosan in the preparation of molecularly imprinted polymers,then reviewed latest development of molecularly imprinted polymers based on chitosan in environmental protection,medicine,separation and identification of protein,chiral compounds and adsorption for functional compounds. Advantages,disadvantages and development directions of these polymers in various fields were analyzed. Additionally,some application prospects of these molecularly imprinted polymers were discussed from the perspectives of green molecular imprinting technology and its combination with electrochemical sensor.
Key words:chitosan; molecular imprinting technique; biocompatibility; polymer
基金项目:国家自然科学基金(31360373)及贵州省优秀科技教育人才省长专项基金[黔省专合字(2010)7号]项目。
收稿日期:2015- 07-21;修改稿日期:2015-09-01。
DOI:10.16085/j.issn.1000-6613.2016.03.030
中图分类号:O 629.12;O 631.3
文献标志码:A
文章编号:1000–6613(2016)03–0847–09
第一作者:许龙(1989—),男,硕士研究生,研究方向为分子印迹技术在食品活性包装材料中的应用。E-mail xulong19891026@163.com。
联系人:朱秋劲,博士,教授,研究方向为食品营养与安全和畜产品加工。E-mail qiujin_z@hotmail.com。

