离子色谱法和毛细管电泳法测定土壤中氯离子、硫酸根及其差异性①
蒋 倩,韩 勇,孙晓丽,龚 华,钱 薇,陆国兴
(1 土壤与农业可持续发展国家重点实验室(中国科学院南京土壤研究所),南京 210008;2 中国科学院大学,北京 100049)
离子色谱法和毛细管电泳法测定土壤中氯离子、硫酸根及其差异性①
蒋倩1,2,韩勇1,孙晓丽1,龚华1,钱薇1,陆国兴1
(1 土壤与农业可持续发展国家重点实验室(中国科学院南京土壤研究所),南京210008;2 中国科学院大学,北京100049)
摘要:分别采用离子色谱法(IC)、毛细管电泳法(CE)两种仪器方法对不同pH土壤中Cl-、�含量进行测定,并对其结果进行差异性分析。结果显示:参照标准物质的参考值(滴定法),IC与CE测定值的准确度、回收率均满足实验分析要求,但精密度差异较大,IC(RSD, 3.61%)的稳定性优于CE (RSD, 8.97%)。据差异性(F与t检验)分析,两种仪器方法测定酸性土壤中 Cl-、含量存在显著性差异,而碱性、中性土壤的测定结果保持一致。对比4个被测样品基本性质发现,酸性土壤的pH与离子强度均低于其他样品,从而影响了石英毛细管的电渗流,最终改变了CE分离过程,这可能是Cl-结果偏离的主要因素。同时,对于IC,酸性土壤较中性、碱性土壤更易由于离子交换效应产生次级保留(拖尾)。此外,采用碱性分离体系分离酸性样品易形成结晶,从而导致含量的偏离。可见,两种方法各有优缺点。但是,IC较经典,而CE是一种新兴的仪器方法。测定像土壤这样基体较复杂的样品(特别是酸性土壤)中阴离子的仪器条件还需要进行更多摸索与优化,以促进这两种方法在土壤领域的推广与应用。
关键词:离子色谱;毛细管电泳;土壤;氯离子;硫酸根
氯离子(Cl-)、硫酸根)是土壤可溶盐的主要组成部分,也是阴离子含量监测的必需指标。它们的测定方法主要有化学滴定法(分别常用硝酸银滴定法、EDTA间接滴定法等)[1-2]和仪器测定法(离子色谱法,以下简称 IC;毛细管电泳法,以下简称CE)[3-5]。前者的不足主要表现为:工作量大、操作繁琐、滴定终点难控制(易受指示剂颜色与自然光线变化的影响)以及试剂引起的环境问题等。相比之下,后者克服了以上不足,并且具有分析速度快、准确度高、精密度高的特点。目前,IC是测定Cl-、SO42-含量的常用方法[6],也较广泛应用于土壤领域[7],但是 CE的报道却相对较少[8-9],更鲜有两种方法的对比研究。本文分别采用 IC与 CE测定了不同pH土壤样品中的Cl-、含量,系统地对比了这两种色谱方法仪器运行参数、准确度、精密度、回收率并对测定结果进行差异性分析。同时,与滴定法的参考值进行对比,以期提供不同分析方法在土壤领域应用上的选择依据,最终促进各种方法的应用推广。
1 实验部分
1.1仪器、试剂和材料
DX-500 离子色谱,美国戴安公司;P/ACE-MDQ毛细管电泳,美国贝克曼库尔特公司;HZ-9310K全温恒温振荡器,江苏太仓市华利达实验设备公司;KQ-600E超声波,昆山市超声仪器有限公司;HH-8数显恒温水浴锅,国华电器有限公司;RJ-TDL-5A低速大容量台式离心机,常州诺基仪器有限公司;CP100W X超高速离心机,日本日立公司;弹性石英毛细管,永年锐沣色谱器材有限公司。
Cl-、标准溶液:1 000 mg/L,购自国家标准物质研究中心;淋洗液:4.5 mmol/L Na2CO3(AR,南京化学试剂有限公司)与1.0 mmol/L NaHCO3(AR,南京化学试剂有限公司)混合溶液;阴离子分析缓冲溶液包(A53537)购自美国贝克曼公司。
供试验的土壤标准样品均购自中国地质科学院地球物理地球化学勘查研究所。其基本性质数据由标准样品附带证书提供(表1)。
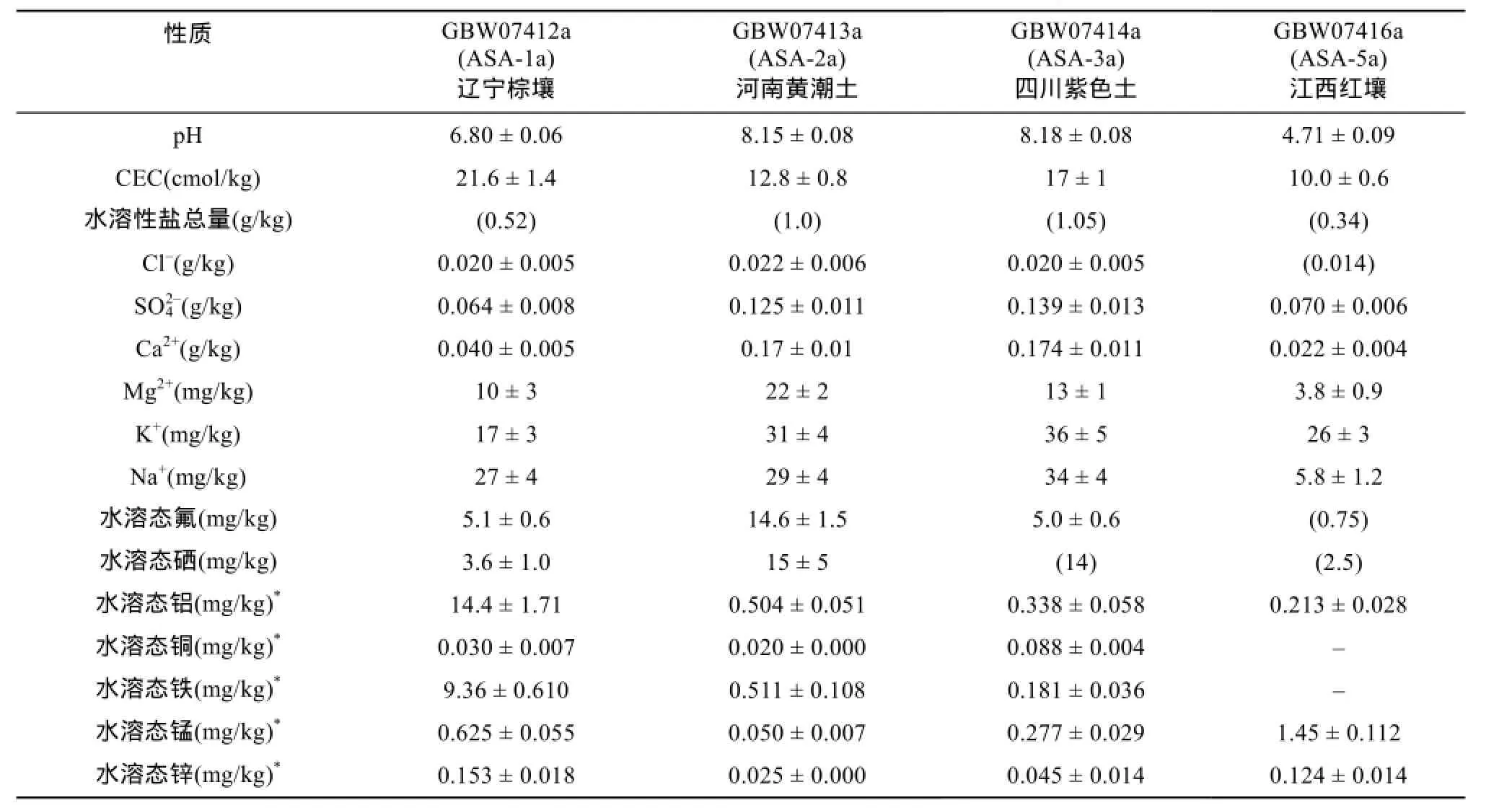
表1 供试土壤标准样品基本性质Table 1 Basic characteristics of standard soils used in this study
1.2色谱条件
IC:电流,50 mA;淋洗流速,1.2 ml/min;进样定量环,25 μl;时间,15 min;色谱柱,Dionex IonPac AS14型分析柱(4 × 250 mm),IonPac AG14型保护柱(4 × 50 mm);抑制器,ASRS-ULTRA II 4-mm;电导检测器。
CE:分离电压,25 kV;分离压力,20 psi;时间,5 min;正电源;熔融石英毛细管,75 µm I.D.× 62 cm;254 nm固定波长;紫外检测器。
1.3样品预处理
1.3.1待测液的浸提称取 50.00 g风干土壤样品(10目)于500 ml塑料提取瓶中,加入无CO2纯水250 ml,盖好瓶盖,放入振荡器振荡210 r/min,3 min。浸提液经离心(4 900 r/min,10 min)、过滤纸,然后经高速离心(15 000 r/min,20 min)、过0.22 μm滤膜,盛装于塑料瓶中[10-11],待测[6]。
1.3.2配制Cl-、SO42-混合标准曲线首先,用纯水稀释Cl-、SO42-标准溶液至100 mg/L。其次,从100 mg/L Cl-标准溶液中分别移取 0.50、1.50、2.50、5.00、7.50 ml至5个50 ml容量瓶中,同时,从100 mg/L SO42-标准溶液中分别移取 2.50、5.00、7.50、10.0、15.0 ml至上述5个容量瓶中。最后,用纯水定容,即得含Cl-1.00、3.00、5.00、10.0、15.0 mg/L系列及含SO42-5.00、10.0、15.0、20.0、30.0 mg/L系列混合标准溶液。
1.4质量控制
本实验质量控制通过测定F-、Cl-、SO42-与NO3-混合标样(GSB 07-1381-2001,204715)来实现,其中Cl-、SO42-的参考值分别为(8.48 ± 0.66) mg/L、(19.9 ± 0.9) mg/L,购自国家环境保护总局标准样品研究所。此标样用于监测在分析测试过程中仪器的稳定性,以确保测定数据的准确性。
1.5数据处理
采用 Excel 2013 和 SPSS 16.0 软件对数据进行统计和方差分析(Duncan),差异显著性水平P<0.05。
2 结果与讨论
2.1两种仪器方法的基本原理与运行基本参数对比
IC基本原理是离子交换平衡,即以低容量的离子交换树脂为固定相,淋洗液为流动相,待测样品溶液的各离子与树脂上能游动的离子之间进行可逆交换,依据各离子对交换剂的亲和力不同而被分离。这种差异通过电导检测器在线连续检测各流出物的保留时间而记录下来,从而实现数据、色谱图的采集[4]。CE亦叫高效毛细管电泳(HPCE)。CE分离过程是典型的差速运动,是离子或带电粒子以石英毛细管为分离通道,以高压电场为驱动力,基于样品中各组分之间的淌度和分配行为上的差异而实现分离[5]。CE是近年发展速度最快的分离技术之一。IC与CE均可以对土壤中Cl-、SO24-进行定量分析。
从表 2数据可知,在本实验条件下,IC与 CE测定Cl-(1.00 ~ 15.0 mg/L)、SO42-(5.00 ~ 30.0 mg/L)具有较好的线性关系,R2均达到0.999,能够满足对样品准确的定量分析。根据公式(3×噪音×浓度/峰高)计算检出限,结果显示:IC较CE具有更灵敏的检出限,这与Stahl[12]报道一致,并且本研究的IC灵敏度较该文报道值更加优异。

表2 两种方法测定Cl-、SO24-基本参数对比Table 2 Comparison of basic parameters of chloride and sulfate determined respectively by IC and CE
2.2两种仪器方法的精密度对比
分别采用IC、CE对同一标准样品新疆灰钙土进行9次测量,其结果见表3。IC测定土壤中Cl-含量的RSD为3.61%,优于CE的8.97%。同时,也分别对同一待测液 SO42-进行了测定,其 RSD分别为2.98%、4.80%。这些结果与李立平等[8]报道相同。据此,两种方法均具有较高的精密度。
2.3两种仪器方法的加标回收率对比
本研究对两种方法测定Cl-、SO42-进行了回收实验,结果见表4。IC测定Cl-、SO42-的回收率分别为105% ~ 110%、104% ~ 108%;CE则分别为83.0% ~91.8%、109% ~ 115%。据此,IC回收率的RSD值同样优于CE。从回收率数据看,两种方法均满足分析要求。
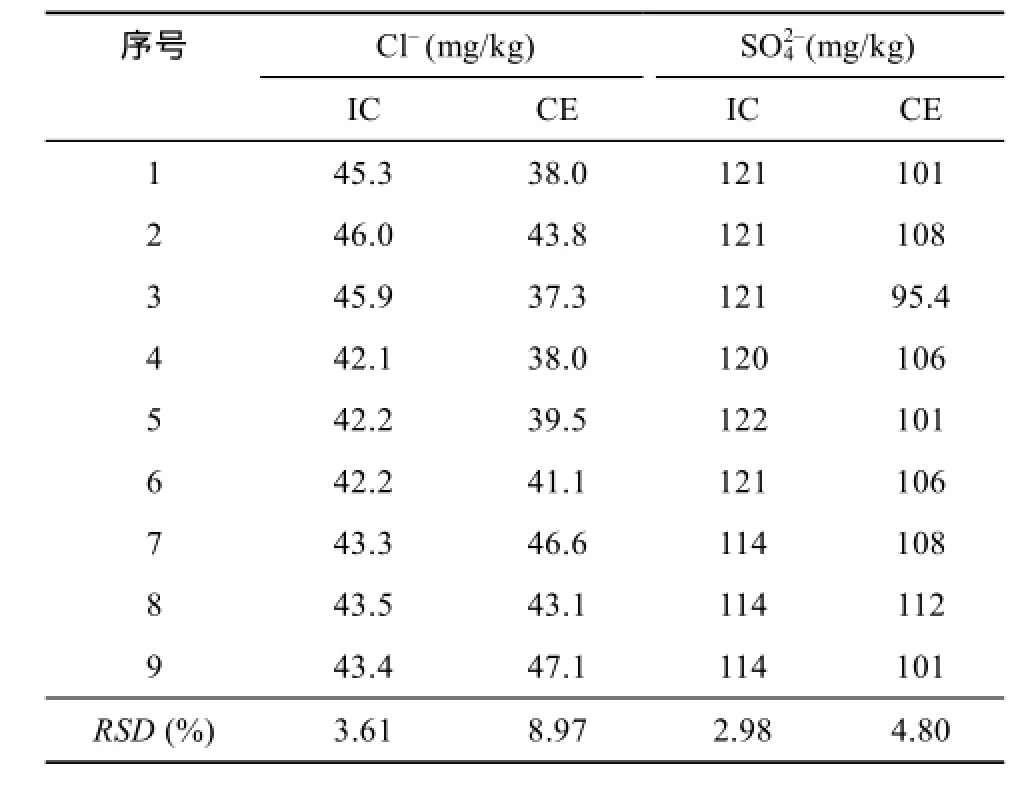
表3 两种方法测定标样(ASA-8)Cl-、SO24-精密度对比Table 3 Comparison of the precision of chloride and sulfate in standard soil (ASA-8) determined respectively by IC and CE
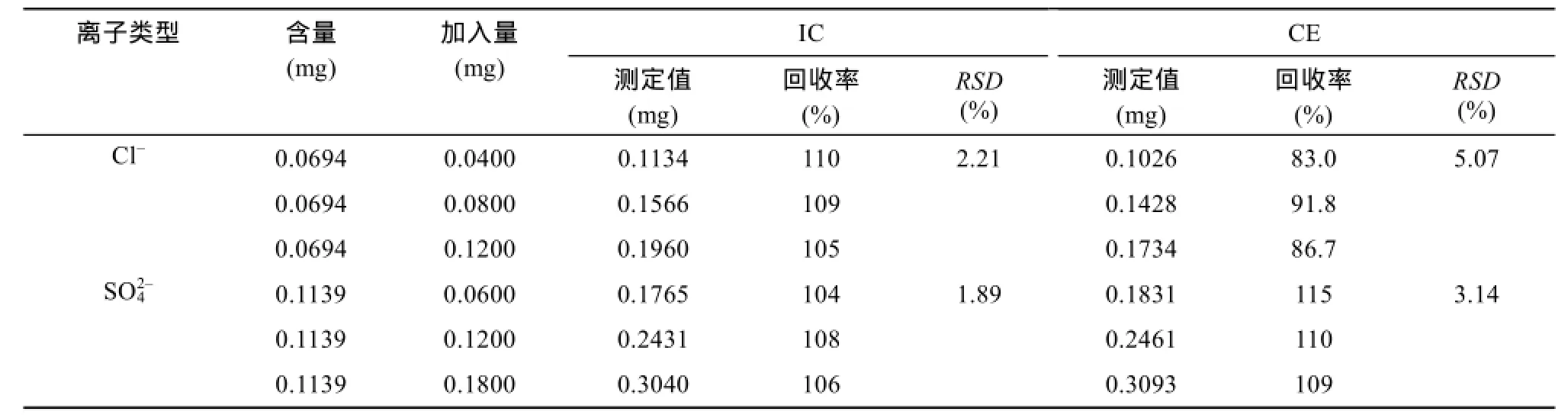
表4 两种方法测定Cl-、SO42-加标回收率对比Table 4 Comparison of recovery of chloride and sulfate in soils determined respectively by IC and CE
2.4两种仪器方法测定结果对比
2.4.1两种仪器方法与标准参考值(以 STD表示)对比图1 ~ 2中,不同pH土壤标准物质中Cl-含量即参考值源自证书提供(表1),分别采用常规的硝酸银滴定法、EDTA滴定法测定[13]。其标准偏差(SD)均比较大,是由于组织定值方统计多家单位检测结果所致。参照此值,本文IC与CE两种仪器法测定结果均在所给定参考值的1 ~ 2倍标准偏差的正负误差范围内,但是测定结果及误差都存在较大差异。显然,IC较CE的仪器稳定性更具有优势。但是两者测定结果是否存在差异则需要进行显著性分析。
2.4.2两种仪器方法的显著性检验采用 F检验法和 t 检验法分别对本研究 IC、CE测定中性土壤(ASA-1a)、碱性土壤(ASA-2a,ASA-3a)以及酸性土壤(ASA-5a) Cl-及SO42-含量进行差异性检验,结果见表5。由表5可知,当两法测定结果的方差齐性Levene检验 P>0.05,可认为两方差齐性,应选用“假设方差相等”(即“Y”)行的t检验结果,按α=0.05显著水平,当P>0.05(双侧),两法测定结果一致,当P<0.05(双侧),两法测定结果不一致;当两法测定结果的方差齐性Levene检验P<0.05,可以认为两方差不齐,应选用“假设方差不相等”(即“N”)行的t检验结果,按α=0.05显著水平,当P>0.05(双侧),两法测定结果一致,当P<0.05(双侧),两法测定结果不一致。
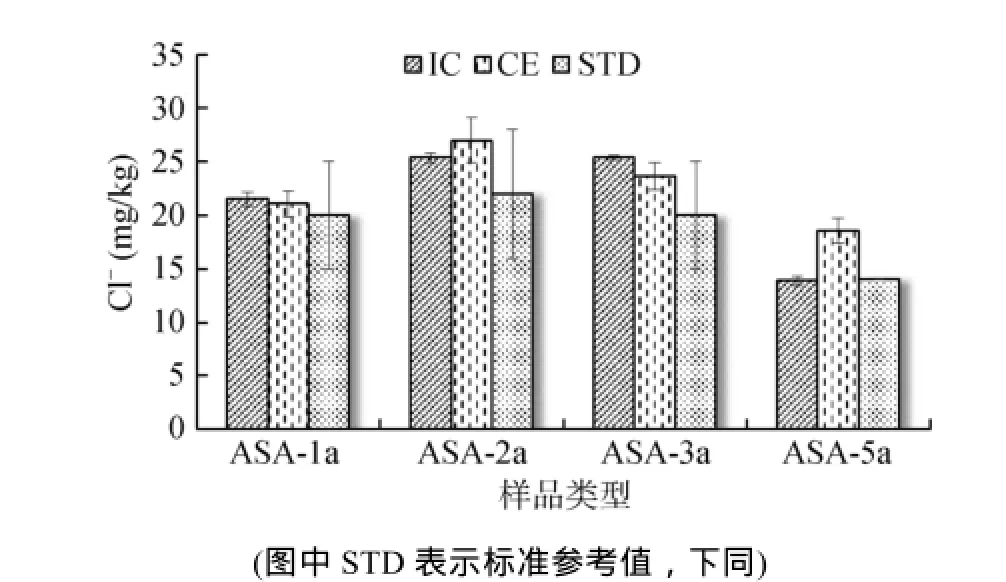
图1 两种方法测定Cl-含量与STD值对比(n = 3)Fig. 1 Comparison of soil chloride contents determined by IC,CE and STD
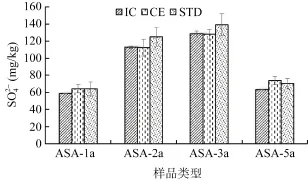
图2 两种方法测定SO24-含量与STD值对比(n=3)Fig. 2 Comparison of soil sulfate content determined by IC,CE and STD
由SPSS输出结果可以看出,两种方法测定中性及碱性土壤Cl-及SO42-含量无显著性差异。但是,对于酸性土壤,其t统计量(在方差相等时)的相伴概率0.003、0.019均小于显著性水平0.05,接受t检验的零假设。可见,两种方法的测定含量存在显著性差异。另外,两个样本均值差的95%置信区间未跨0,这也表明显著性差异的存在。结合图1,CE测定Cl-偏离于IC与参考值。结合图2,IC测定SO42-偏离于CE与参考值。这种差异与李立平等[8]报道的类似。
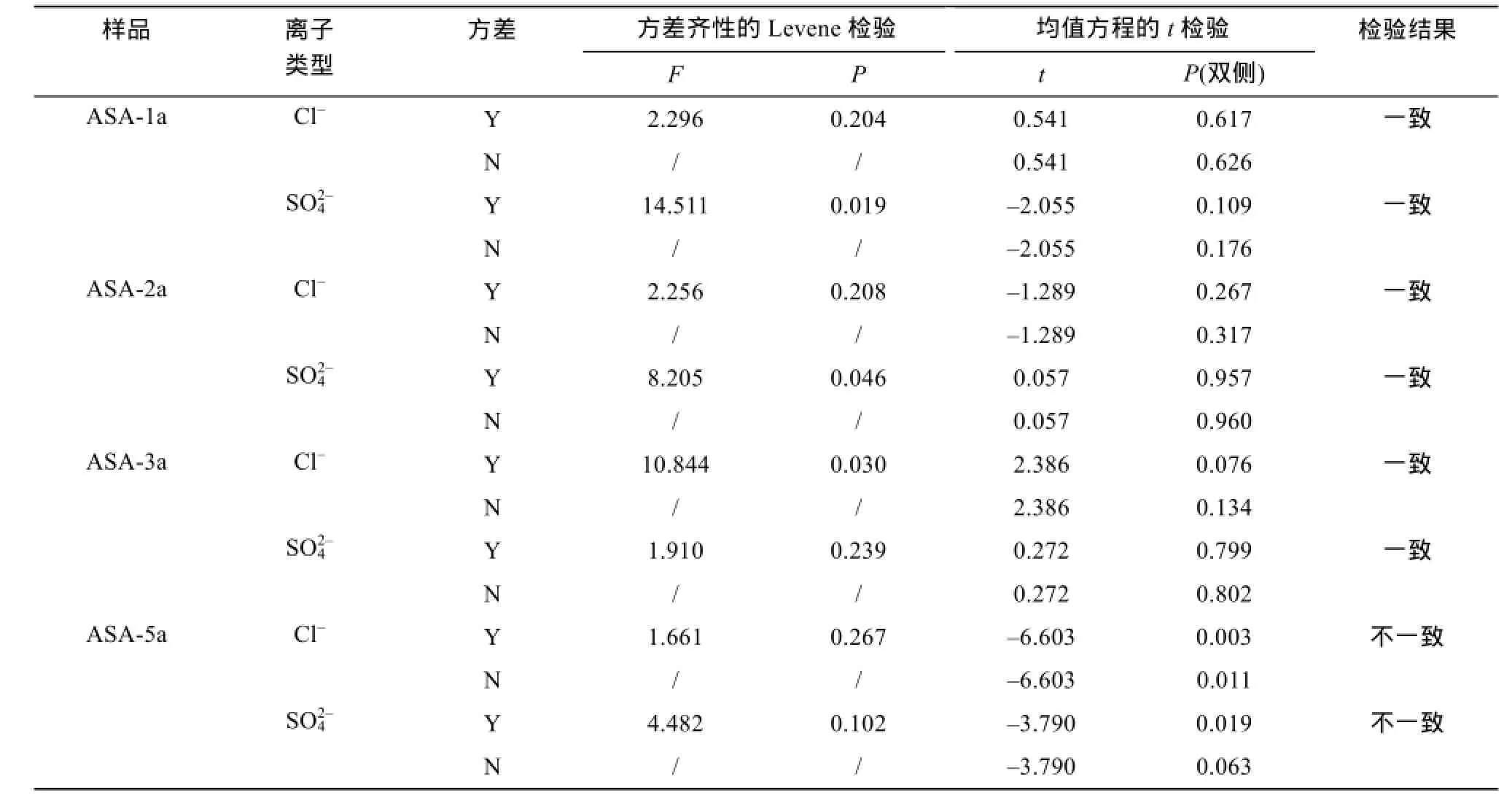
表5 两种方法测定土壤Cl-、SO42-含量的显著性检验(α=0.05)Table 5 Significance analysis of chloride and sulfate contents in soils determined respectively by IC and CE
ASA-5a为取自江西的红壤,其pH、CEC及主要水溶性阴、阳离子均低于其他3个标样(表1)。一方面,对于CE,pH越高,电渗流越大。离子强度越高,电渗流越小,而这两者对电渗流的交互影响是难以定量的[14]。本研究采用仪器公司提供阴离子分析包,表面活性剂CTAB(十六烷基三甲溴化铵)更易溶解于碱性环境。而电渗流的大小及极性不仅依赖于CTAB的浓度,还依赖于分离电解的背景的组成成分,它们之间的相互作用存在竞争性、复杂性及整体性[15]。只有通过具体实验的摸索才能找出最佳条件。这些可能是CE测定酸性土壤Cl-偏离于IC与参考值的主要原因。另一方面,对于IC,引起SO24-定量偏差的因素常有金属离子、离子交换效应以及结晶作用[16]。本研究通过测定振荡提取水溶性金属离子含量(表 1),排除其是引起偏差的主要原因。相反,在本实验中,质子化的样品分子更易与色谱柱中离子化的硅酸发生离子交换产生次级保留(拖尾)。此外,IC采用的碱性分离体系(淋洗液为碳酸钠与碳酸氢钠混合溶液)在分离酸性样品时更易形成结晶。这两者可能是引起 SO42-偏离的主要原因。因此,这两种仪器对酸性土壤Cl-、SO42-的测定结果存在差异是各自不同分离原理所引起,具有必然性。但是,可以通过摸索实验条件来降低这些不利的干扰,这是本研究下一步的工作。
3 结论
参照标准参考值,本研究两种仪器方法的准确度、精密度以及回收率都能够满足实验分析的要求,可广泛应用于中性、碱性土壤中Cl-、SO42-含量的分析,其测定结果保持一致。但是,受酸性土壤基体的影响,其测定结果存在显著性差异。
参考文献:
[1] 鲁如坤主编. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000
[2] 戚冰洁, 汪吉东, 张永春, 等. 甘薯不同氯离子测定方法的比较研究[J]. 土壤学报, 2013, 50 (3): 154-160
[3]王战, 李向全, 王振兴, 等. 青海省鱼卡-大柴旦盆地土壤盐分特征[J]. 土壤, 2015, 47(4): 819-822
[4] 牟世芬, 刘克纳. 离子色谱方法及应用[M]. 北京: 化学工业出版社, 2000
[5] 陈义. 毛细管电泳技术及应用[M]. 北京: 化学工业出版社, 2000: 48-52
[6] 国家环境保护总局. 水质-无机阴离子的测定-离子色谱法(HJ/T 84-2001)[S]. 2001
[7] 高超, 王莹, 杜涛, 康万利, 等. 离子色谱测定土壤中Cl-和SO24-[J]. 光谱实验室, 2010, 27(5): 1 840-1 843
[8] 李立平, 张佳宝, 朱安宁, 等. 土壤无机阴离子的毛细管电泳分析[J]. 土壤学报, 2004, 41(6): 881-888
[9] 李立平, 张佳宝, 邢维芹, 等. 无机离子的毛细管电泳分析及其在土壤上的应用[J]. 土壤, 2004, 36(5): 468-475
[10] 国家农业部. 土壤检测 第 17部分: 土壤氯离子含量的测定(NY/T 1121.17-2006) [S]. 北京: 中国标准出版社,2006
[11] 国家农业部. 土壤检测 第 18部分: 土壤硫酸根离子含量的测定(NY/T 1121.18-2006) [S]. 北京: 中国标准出版社, 2006
[12] Stahl R. Routine determination of anions by capillary electrophoresis and ion chromatography[J]. Journal of Chromatography A, 1994, 686: 143-148
[13] 全国农业技术推广服务中心编. 土壤分析技术规范[M]. 2版. 北京: 中国农业出版社, 2006
[14] Pacáková V, Štulík K. Capillary electrophoresis of inorganic anions and its comparison with ion chromatography[J]. Journal of Chromatography A, 1997, 789: 169-180
[15] Beckers J L, Bocek P. Multiple effect of surfactants used as additives in background electrolytes in capillary zone electrophoresis: Cetyltrimethylammonium bromide as example of model surfactant[J]. Electrophoresis, 2002, 23:1 947-1 952
[16] 吴方迪. 色谱仪器维护与故障排除[M]. 北京: 化学工业出版社, 2001: 174-177
Study on the Determination and Its Difference Analysis of Chloride and Sulfate in Different Soils by Ion Chromatography and Capillary Electrophoresis
JIANG Qian1,2, HAN Yong1, SUN Xiaoli1, GONG Hua1, QIAN Wei1, LU Guoxing1
(1 State Key Laboratory of Soil and Sustainable Agriculture (Institute of Soil Science, Chinese Academy of Sciences), Nanjing 210008, China; 2 University of Chinese Academy of Sciences, Beijing100049, China)
Abstract:Chloride and sulfate in different soil samples with various pH were determined with Ion Chromatography (IC)and Capillary Electrophoresis (CE), respectively. The results showed that these two methods both worked well as the measured values of chloride and sulfate were consistent with these obtained with the standard titration method, but the relative standard deviation in measurements of CE (8.97%) was greater than that of IC (3.61%). The statistical F-test and t-test showed that there was no significant difference on the measurements between the two methods for alkaline and neutral soils, but the significant difference was observed for the acid soil of ASA-5a. The lower pH and ionic strength of ASA-5a affected the electroosmotic flow (EOF) of fused silica capillary and changed the separation process of anions in CE, thus caused bigger deviation of measured chloride than other methods, i.e. IC and titration method. Meanwhile, acid soil samples could bring secondary retention of ions in IC measurements compared with other soils. Moreover, alkali eluent caused the formation of crystallization in separation process of acid soil samples with IC, which led to a bigger deviation of measured Sulfate than other methods, i.e. CE and titration methods. Therefore, CE and IC methods have their own merits and demerits. CE is a new method for measurements of soil chloride and sulfate, and more studies should be conducted to improve experimental conditions in the future, especially for acid soils.
Key words:Ion Chromatography; Capillary Electrophoresis; Soil; Chloride; Sulfate
中图分类号:S151.9
DOI:10.13758/j.cnki.tr.2016.02.020
基金项目:①中国科学院知识创新工程领域前沿项目(12201415143200000)资助。
作者简介:蒋倩(1980—),女,贵州思南人,博士研究生,工程师,主要从事土壤仪器分析及方法研究。E-mail: qjiang@issas.ac.cn.

