羧甲基壳聚糖吸附剂对亚甲基蓝的脱色研究
彭亚娟 王晓雪 路媛媛
(1.遵义师范学院, 贵州 遵义 563000; 2.重庆市南岸区环境监测站, 重庆 401336;3.重庆市大足区环境监测站, 重庆 402360)
羧甲基壳聚糖吸附剂对亚甲基蓝的脱色研究
彭亚娟1王晓雪2路媛媛3
(1.遵义师范学院, 贵州遵义563000; 2.重庆市南岸区环境监测站, 重庆401336;3.重庆市大足区环境监测站, 重庆402360)
摘要:利用自制的羧甲基壳聚糖(CMCTS)对模拟印染废水亚甲基蓝进行脱色处理,并进行了化学动力学和热力学机理的研究。正交实验表明:羧甲基壳聚糖吸附剂对亚甲基蓝的脱色率影响程度大小的次序是:取代度>脱乙酰度>pH>温度。最佳实验条件为取代度为0.9,脱乙酰度为80%,pH为8,反应温度为35℃时,脱色率达到93%。不同温度下,吸附行为满足Freundlich等温式,吸附过程较好的遵循二级反应动力学模型,主要为化学吸附。
关键词:羧甲基壳聚糖;亚甲基蓝;脱色率;吸附动力学;吸附热力学
纺织印染废水是主要的工业废水之一,两大污染指标是色度和COD,污染特点和处理难点是色度高、脱色困难[1-2]。以往用在染料脱色处理中的物理、化学法如膜分离法、光氧化法、絮凝法等,由于处理成本相对较高,或由于光和氧化剂对染料的脱色效果达不到要求,上述方法的应用受到限制[3—5]。吸附法主要用于废水的预处理与深度处理,具有投资小、实用、简便易行,不受被去除物质毒性影响的特点[6],具有广泛的应用前景。壳聚糖由于价廉、生物相容性好、无毒,对染料有较好的脱色作用[7-9],是一种能有效保护环境的天然高分子材料。由于壳聚糖不溶于水和碱溶液,限制了其应用范围。为了增强其实用性,最近研究对壳聚糖分子进行化学改性的报道日趋增多[10]。高浓度的亚甲基蓝对生物有毒害作用,能导致动物中毒甚至死亡[11]。人们之所以关注亚甲基蓝在水中的残留,是由于该染料及降解物有致畸作用[12],因此被禁止用于美国与日本的水产养殖业。本文对壳聚糖进行醚化改性,研究了羧甲基壳聚糖对亚甲基蓝的吸附脱色能力。
1 实验部分
1.1实验材料
羧甲基壳聚糖(自制)。
1.2主要仪器和试剂
SHA-BC水浴恒温振荡箱;离心机TDZ4—WS;pH320-S酸度计;UV1102分光光度计;傅立叶红外光谱仪。
亚甲基蓝(C16H18ClN3S.3H2O)。
1.3实验方法
(1)亚甲基蓝溶液配制
准确称取10 mg亚甲基蓝药品于烧杯中,加水溶解完,转移到1L容量瓶,定容后摇匀,配制成10 mg/L的溶液。
(2)羧甲基壳聚糖对亚甲基蓝的吸附
取一定量的羧甲基壳聚糖放入100 ml浓度为10 mg/L的亚甲基蓝溶液中,在恒温振荡器常温条件下吸附振荡,振荡一定时间,每隔半小时吸取上清液,3 800 r/min离心7 min,在波长665 nm下,测定其吸光度A,计算脱色率。
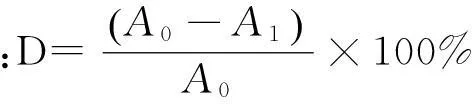
(1)
式中,D为脱色率,A0和A1分别为吸附前后染料废水的吸光度。
2 结果与讨论
2.1红外光谱表征
羧甲基壳聚糖与壳聚糖的红外光谱对比图,见图1。
由图1可见:N,O-羧甲基壳聚糖的红外光谱在3 452~3 000 cm-1处的强吸收峰变尖锐,强度变小。说明羟基和氨基存在的分子间氢键遭到破坏,在壳聚糖的羟基和氨基上发生了衍生反应。羧甲基壳聚糖在1 608 cm-1和1 419 cm-1处出现了羧甲基钠盐的特征吸收峰, 分别为—CO2的不对称和对称伸缩振动吸收峰,而壳聚糖无1 409 cm-1吸收峰,说明壳聚糖发生了羧甲基化反应。1 032 cm-1处的一级羟基的C—O伸缩振动吸收峰明显减弱,有中等强度的吸收峰。在1 080 cm-1处O-H有面外弯曲振动峰,说明壳聚糖已经发生了羧甲基取代。

图1 羧甲基壳聚糖与壳聚糖的红外光谱图
2.2pH的影响
不同pH条件下,羧甲基壳聚糖吸附亚甲基蓝脱色率见表1。

表1 pH对羧甲基壳聚糖吸附亚甲基蓝脱色率的影响
由表1可知:在pH=2时,脱色率基本为0,这是由于羧甲基壳聚糖在强酸环境中完全溶解的缘故。pH逐渐增大,亚甲基蓝的脱色率也随之变大,pH为8时,脱色率最大。pH大于8时,脱色率变小,这是由于亚甲基蓝在水溶液中是呈+ 1价的有机阳离子[13], 在较酸的的条件下,H+与正价的亚甲基蓝溶液产生竞争性吸附导致脱色率低[14]。亚甲基蓝在弱碱性条件下易于脱色,可能因为随着pH的增大,H+越来越少,亚甲基蓝的阳离子基团与羧甲基壳聚糖的带负电的羧基吸附点结合,有利于吸附。在强碱环境下,亚甲基蓝中的N原子电负性减小,染料呈现出来的阳离子性不太明显,所以与羧甲基壳聚糖中的-COOH的静电作用减弱,导致脱色率减小。
2.3取代度的影响
取代度即每个糖单元上平均含有的羧甲基数。当pH=8,羧甲基壳聚糖投加量为0.1g,吸附时间为1h时,考察不同取代度对亚甲基蓝脱色率的影响,其结果见图2。

图2 取代度对脱色率的影响
由图2所知,随着取代度的提高,脱色率逐渐增大,可能由于随着取代度的提高,羧甲基数量增多,使与亚甲基蓝反应的几率大,从而提高了脱色率。
2.4脱乙酰度的影响
脱乙酰度即壳聚糖的活性基团自由氨基的含量。经不同脱乙酰度的壳聚糖改性后的羧甲基壳聚糖,在当pH=8,羧甲基壳聚糖投加量为0.1 g,吸附时间为1 h条件下,考察不同脱乙酰度对亚甲基蓝脱色率的影响,结果见图3。
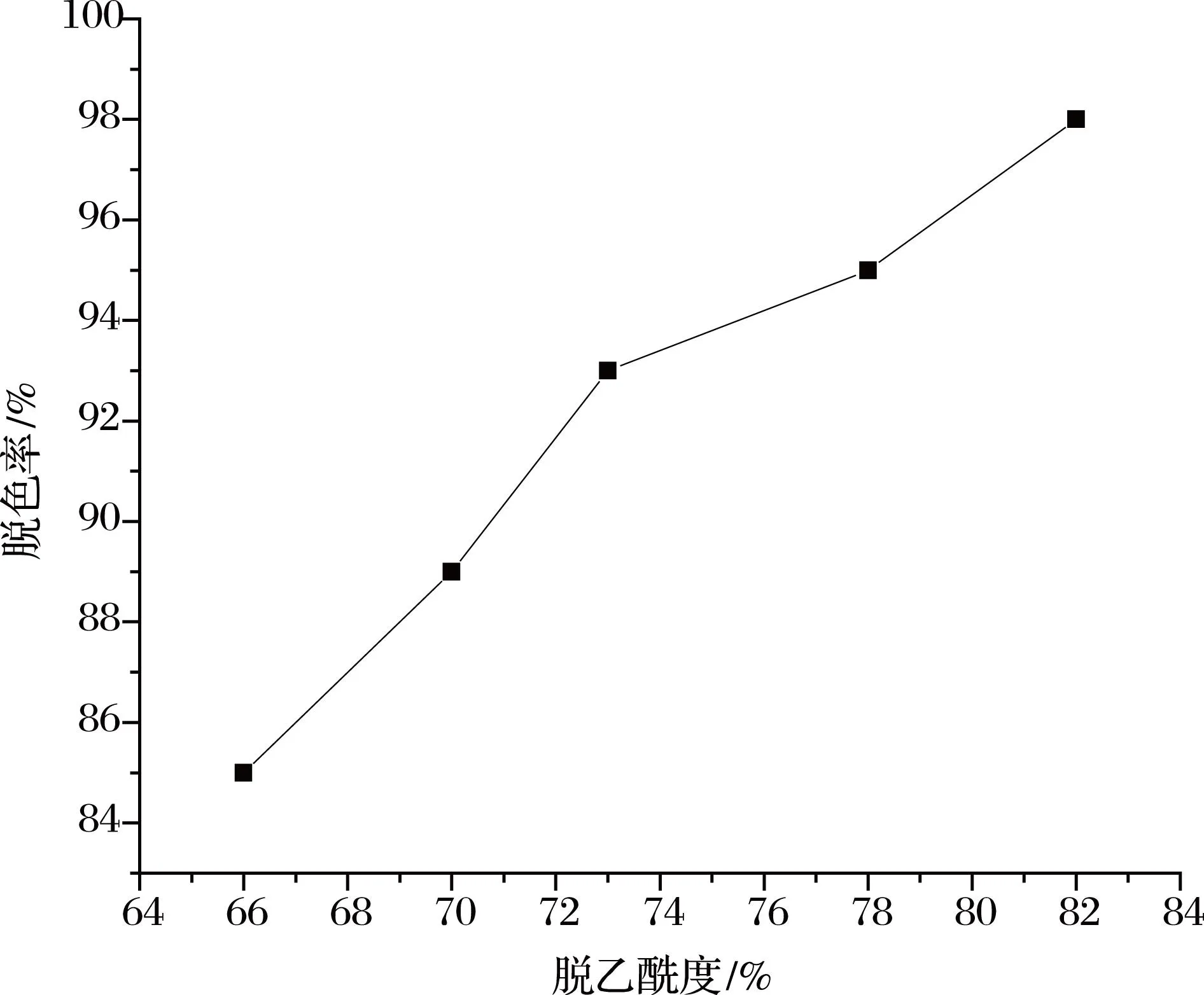
图3 脱乙酰度对脱色率的影响
由图3所知,随着脱乙酰度的提高,脱色率逐渐增大,可能由于随着脱乙酰度的提高,—NH2数量增多,随之在—NH2上的羧甲基反应几率增大,与亚甲基蓝反应的几率大,从而提高了脱色率。
2.5温度的影响
温度对脱色率的影响见图4,由图可知,在一定范围内,升高温度有利于亚甲基蓝的脱色,在25℃时脱色率最大,高于25℃脱色率逐渐减小。可能由于该吸附为放热过程,低温度下有利于对亚甲基蓝的吸附。

图4 脱色率随反应温度的变化
2.6正交优化实验
以pH、脱乙酰度、反应温度、取代度为四因素三水平正交实验,考察对亚甲基蓝脱色率的影响,见表2~3。
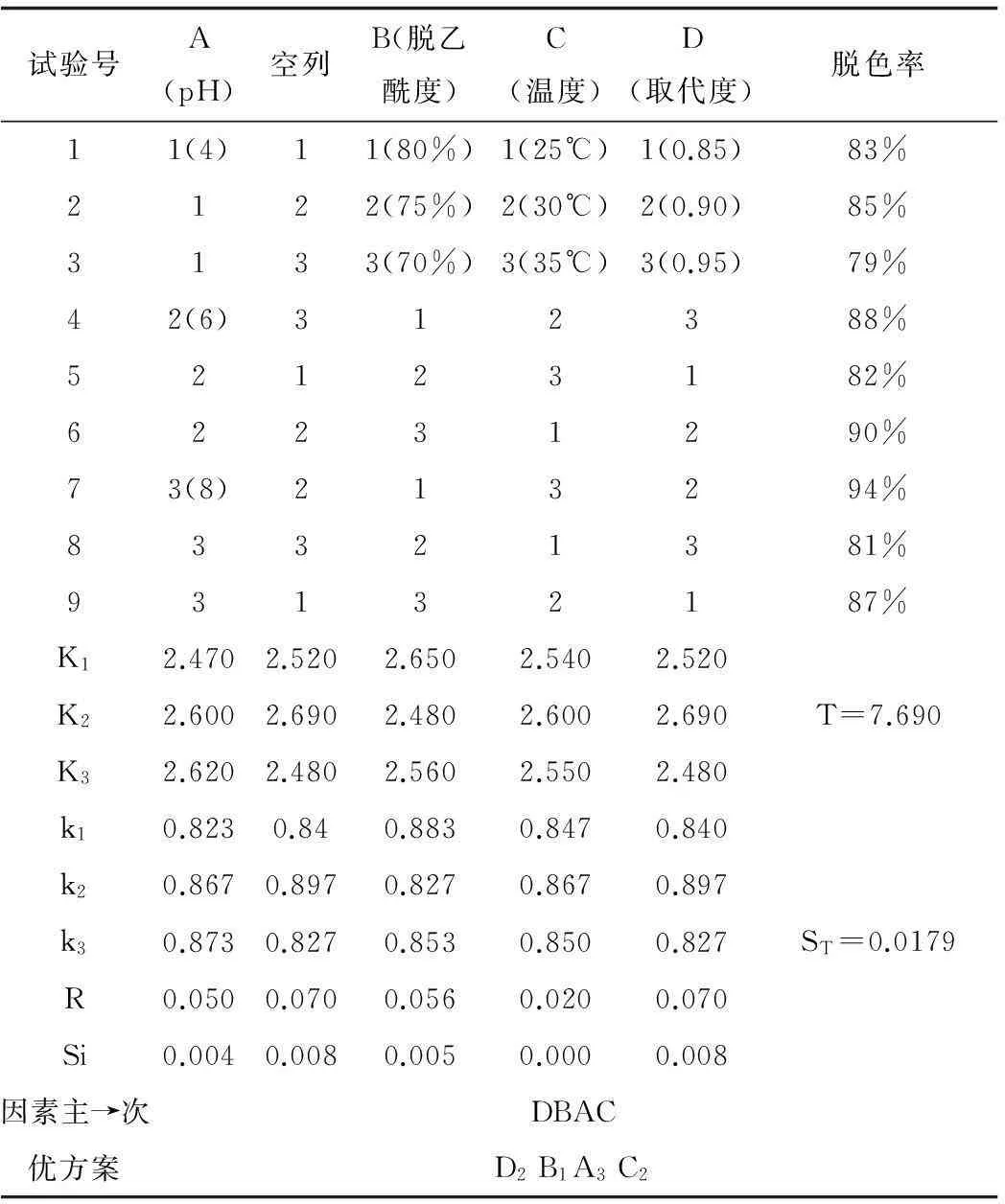
表2 正交实验结果分析
由表2可知:正交表中,脱色率最高为94%的因素水平为D2B1A3C3,与极差分析出来的优化方案D2B1A3C2不一致,所以要再次进行验证实验,结果表明,D2B1A3C3条件下,脱色率为92%。D2B1A3C2条件下,DS=93%。因此,羧甲基壳聚糖吸附剂对亚甲基蓝的脱色率影响程度大小的次序是,取代度>脱乙酰度>pH>温度。最高脱色率的最佳实验条件为D2B1A3C2,即取代度为0.9,脱乙酰度为80%,pH为8,反应温度为35℃。
通过F检验表,查得α=0.05和α=0.01时F1-α的值分别为12.06和5.41,计算结果见表3。
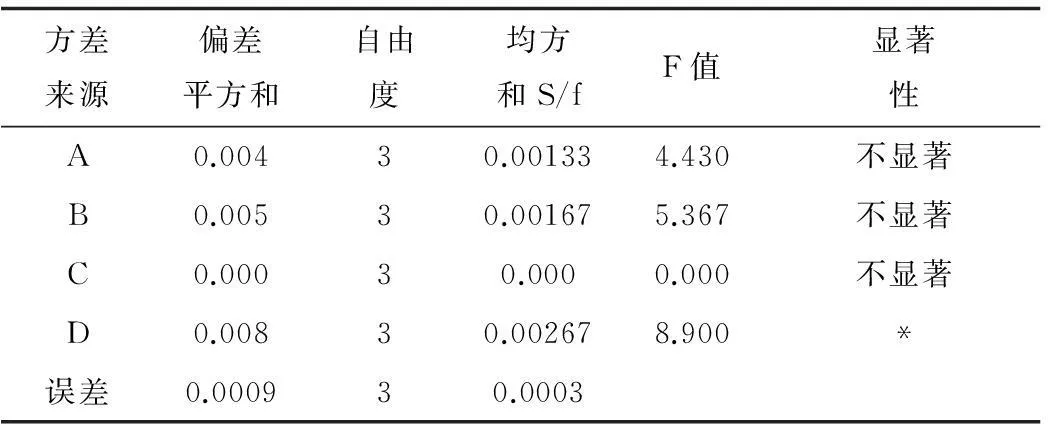
表3 方差分析表
由表3可知,各影响因素均无显著影响,相对来讲,因素D的影响大些。
2.7等温吸附线
图5为羧甲基壳聚糖在不同温度下(25、35、45℃)吸附亚甲基蓝的Freundlich等温吸附线,吸附等温线用式(2)拟合,结果见表4。
Freundlich方程:
(2)

图5 CMCTS在不同温度下吸附亚甲基蓝的Freundlich吸附等温线

1/nKfR20.3867.320.98940.33514.330.99040.24222.540.9912
由图5及表4可知,在不同的实验温度下,羧甲基壳聚糖对亚甲基蓝的吸附符合Freundlich等温吸附方程,吸附等温线模型方程相关系好,R2均在0.99左右。0﹤1/n<1,表明羧甲基壳聚糖表面分布着多种不同能量大小的吸附点[15],吸附比较容易。
2.8吸附动力学
(1)平衡吸附量的测定
不同温度下的平衡吸附量,如图6所示,25oC为8.72 mg/g,35oC为7.34 mg/g,45oC为4.97 mg/g,吸附平衡时间均为60 min。
由图7及表5可知,在298K、308K、318K三个不同温度下,壳聚糖对亚甲基蓝的吸附过程符合伪二级动力学吸附速率模型,因为伪二级动力学模型包含吸附的所有过程,如表面吸附、外部液膜扩散和颗粒内部扩散等[16],该吸附过程是放热反应,降低温度有利于反应的进行,吸附速率常数也相应的减小。因此,吸附过程主要是化学吸附[17-19]。
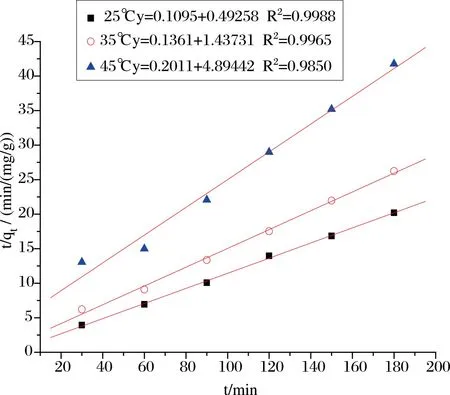
图7 伪二级吸附方程图
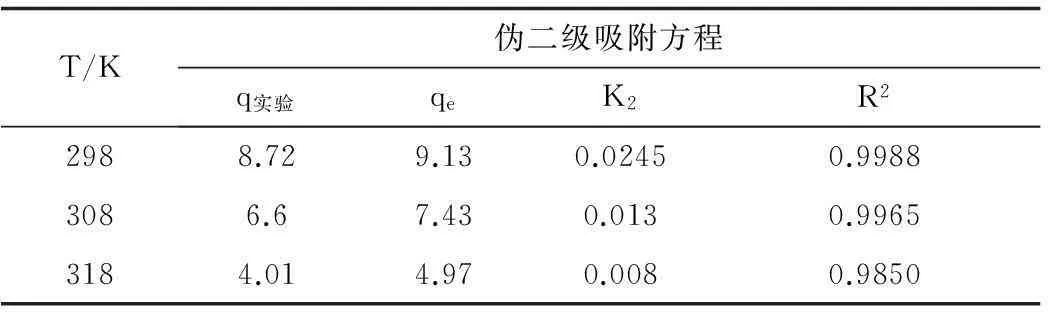
T/K伪二级吸附方程q实验qeK2R22988.729.130.02450.99883086.67.430.0130.99653184.014.970.0080.9850
2.9投资费用简要分析
在羧甲基壳聚糖吸附剂制备过程以及羧甲基壳聚糖吸附剂脱色过程中,采用的原材料为低脱乙酰度的壳聚糖,价格较便宜;实验设备易操作、实验试剂也较少且均为常规试剂、实验操作以及工艺流程简单可行不耗费人力成本。因此,羧甲基壳聚糖吸附剂制备投入成本和脱色运行费用较少,具有一定的市场优势。
3 结论
(1)羧甲基壳聚糖吸附剂对亚甲基蓝的脱色率影响程度大小的次序是,取代度>脱乙酰度>pH>温度。最高脱色率的最佳实验条件为D2B1A3C2,即取代度为0.9,脱乙酰度为80%,pH为8,反应温度为35℃,脱色率达到93%。
(2)吸附行为满足Freundlich等温式。不同温度下,吸附过程符合二级反应动力学,吸附过程以化学吸附为主。
参考文献
[1]黄长盾,杨西昆,汪凯民.印染废水处理[M].北京:纺织工业出版社, 1987 :9-24.
[2]Olcay Tünay, Isik Kabdasli, Gülen Eremektar. Color removal from textile wastewaters [J].Water Science and Technology,1996,34(11) :9-16.
[3]Juang Ruey-Shin, Tseng Ru-Ling, Wu Feng-Chin. Use of chitin and chitosan in lobster shell wastes for color removal from aqueous solutions[J].Environmental Science Health A, 1996, 31(2):325-338.
[4]Adnan Özcan, E. Mine Öncü, A. Safa Özcan. Kinetics, isotherm and thermodynamic studies of adsorption of acid blue 193 from aqueous solutions onto natural sepiolite [J]. Colloids Surfaces A, 2006, 277 :90-97.
[5]Ismail Kiran, Tamer Akar, A. Safa Ozcan, et al. Biosorption kinetics and isotherm studi es of acid red 57 by dried cepha- losporium aphidicola cells from aqueous solution [J]. Biochemical Engineering Journal, 2006, 31 :197-203.
[6]Nikolaos K. Lazaridis, George Z. Kyzas, Alexandros A. Va- ssiliou, et al. Chitosan derivatives as biosorbents for basic dyes[J].Langmuir, 2007, 23 :7634-7643.
[7]袁毅骅,赖兴华,陈纯馨,等.壳聚糖对印染废水的絮凝作用和脱色效果[J].应用化学, 2000,17 (2) :217-218.
[8]杨智宽,袁扬,曹丽芬.羧甲基壳聚糖对水溶性染料废水的脱色研究[J].环境科学与技术, 1999, 85(2) :8-15.
[9]曾德芳,李娟,袁继祖.天然高分子絮凝剂在工业污水处理中的应用[J].工业水处理,2004, 24 (2) :20-22.
[10]蒋挺大.甲壳素[M].北京:化学工业出版社,2003 :194 -210.
[11]Liu Jian-Yong, Peng Shu-Feng. Acute Toxicity Of Methylene Blue To Zoea Mysis And Post Larva Of Penaeus Vannamei [J].Transactions of Oceanology and Limnology,2005(1):49-53.
[12]Hejtmancik M R,Ryan M J,Toft J D, et al.Hematological effects in F344 Rats and B6C3F1 Mice during the 13-Week Gavage Toxicity Study of methylene blue trihydrate[J].Toxicological Sciences, 2002,65 :126-134.
[13]栾文楼.李路明.膨润土的开发应用[M].北京:地质出版社,1998 :32-37.
[14]刘承帅,候梅芳,吴志峰,等.膨润土理化特性对染料废水脱色效果的影响[J].矿产保护与利用,2004 (3) :12-15.
[15]李克斌,张涛,魏红.壳聚糖吸附酸性大红Cu2+对 吸 附 的增强作用[J].环境科学,2009,30(9) :2586-2591.
[16]Chang M Y,Juang R S.Adsorption of tannic aeid,humic acid,and dyes from water using the composite of chitosan and activated clay[J].Colloid and Interface Sci,2004, 278: 18 -25.
[17]Mohanty K, Das D,Biswas M N. Adsorption of phenol from aqueous solutions using activated carbons prepared from Tectona grandis sawdust by ZnCl2activeation[J].Chemical Engineering Journal, 2005,115 :121 -131.
[18]Ho Y S,McKay G. Pseudo-second order model for sorption processes[J].Process Biochemistry, 1999, 34 :451-465.
收稿日期:2016-01-19;2016-03-11修回
作者简介:彭亚娟,女, 1985年生,硕士,助教,研究方向:水污染控制理论与技术。E-mail:lovepyj2005@163.com
中图分类号:X703
文献标志码:A
Study on the decolorization of methylene blue using carboxymethyl chitosan
Peng Yajuan1, Wang Xiaoxue2, Lu Yuanyuan3
(1.Zunyi Normal College, Zunyi 563000;2.Nan’an Dsitrict Environmental Monitoring Station of Chongqing City, Chongqing 401336;3.Dazu District Environmental Monitoring Station of Chongqing City, Chongqing 402360)
Abstract:The decolorization of methylene blue in simulated dyeing wastewater by self made carboxymethyl chitosan(CMCTS) was studied, and the chemical kinetics and thermodynamic mechanism were explored. The results of orthogonal experiments showed that, parameters affecting the degree of decolorization of methylene blue were ranked in descending order as: degree of substitution, degree of acetylation, pH value, and reaction temperature. The optimum experimental condition was substitution degree at 0.9, acetylation degree at 80%, pH at 8, and the reaction temperature at 35℃, under such condition the decolorization rate could reach up to 93%. With different temperatures, the adsorption performance fitted well with the Freundlich Isotherm, and the adsorption process, mainly chemical adsorption, followed the second order dynamic reaction model.
Keywords:CMCTS; methylene blue; decolorization; kinetics of adsorption; thermodynamics of adsorption.

