单分散的二氧化硅微球表面印迹壳层的制备及其对食品包装材料中邻苯二甲酸二苄酯的检测
徐微微,龙泽荣,鹿 毅,王吉德*
(1.新疆大学 石油天然气精细化工教育部自治区重点实验室,新疆 乌鲁木齐 830046;2.新疆维吾尔自治区产品质量监督检验研究院,新疆 乌鲁木齐 830011)
单分散的二氧化硅微球表面印迹壳层的制备及其对食品包装材料中邻苯二甲酸二苄酯的检测
徐微微1,龙泽荣2*,鹿毅2,王吉德1*
(1.新疆大学石油天然气精细化工教育部自治区重点实验室,新疆乌鲁木齐830046;2.新疆维吾尔自治区产品质量监督检验研究院,新疆乌鲁木齐830011)
以邻苯二甲酸二苄酯(DBzP)为模板,以Stöber和“种子生长法”相结合获得的二氧化硅微球为载体,采用表面印迹技术成功制备了纳米印迹壳层(MIPs)。采用红外光谱与扫描电镜对其结构和形貌进行表征,同时进行了一系列的吸附性能实验,结果表明,MIPs达到平衡吸附的时间约为30 min,吸附行为符合伪二级动力学。等温吸附实验结果表明,室温条件下MIPs的最大吸附量达47.35 mg/g。对不同温度条件下的等温实验数据进行拟合发现,Langmuir模型与实验数据的吻合度比Freundlich模型更高;Scatchard拟合结果证实该印迹壳层仅含1种结合位点,且印迹位点为均相分布。选择性吸附实验表明MIPs对DBzP的吸附明显高于其他结构类似物。MIPs经10次循环吸附后,吸附效率为83%,表明MIPs具有较长的使用寿命。采用超高效液相色谱(UPLC)技术,以MIPs为吸附剂提取食品包装材料中的DBzP,其加标回收率为88.8%~93.1%,相对标准偏差低于6%。MIPs可作为食品及其包装材料中DBzP提取的备选材料。
种子生长法;二氧化硅微球;纳米印迹壳层;邻苯二甲酸二苄酯;食品包装材料
邻苯二甲酸酯 (PAEs)是一类广泛应用于塑料制品、玩具、建筑材料、日用品中的增塑剂。由于其分子结构不与塑料晶格结构共价连接,较易迁移到周围环境中,通过人体摄入、接触等方式在体内积累,会干扰人体内分泌系统,导致致畸、致癌等危害[1]。我国的国家标准(GB/T 21928-2008)对16种PAEs的使用对象、用量及检测方法作出了规定[2],但邻苯二甲酸二苄酯(DBzP)的使用及用量未列入其中。Hu等[3]研究发现DBzP的毒性远大于邻苯二甲酸丁苄酯(BBP),并强烈建议DBzP不能作为食品包装材料增塑剂。但DBzP的性质研究、分离和检测等几乎未得到关注。
含有PAEs的实际样品来源广泛,基底复杂,PAEs含量较低,测试前通常需对样品进行前处理,然后再结合气相色谱[4]、液相色谱[5]、气相色谱-质谱联用[6]、液相色谱-质谱联用[7]等仪器方法对PAEs进行检测[8]。目前,实验室常用的样品前处理方法主要有固相萃取 (SPE)、固相微萃取 (SPME)和液液萃取 (LLE),但所用的萃取材料对分析物不具有专一选择性,抗干扰能力差。开发一种能够选择性识别和检测目标分析物的萃取材料成为迫切的任务。
以纳米或微米粒子为载体,采用表面聚合方法在其表面形成分子印迹层的技术是一个日趋重要的研究领域[9]。该聚合粒子在生物传感器、固相萃取、固相微萃取和生物试验等方面具有广泛的应用前景[10-16]。与传统的分子印迹聚合物(MIPs)相比,此类聚合粒子质量传递快,对目标分子具有更显著的结合能力和选择性,模板更易洗脱,并具有亲水性。Fu等[17]以磁性壳聚糖亚微球为载体制备了溶菌酶表面分子印迹聚合物Lyz-MIPs,其Langmuir模型的理论最大吸附量达(129.8±1.2) mg/g,10 min即可达到吸附平衡,采用NaCl溶液即能很方便地将模板洗脱。Xie等[18]制备了虚拟模板的表面分子印迹聚合物(DMIPs)用于9种邻苯二甲酸酯的选择性识别,然而未对DBzP进行研究。目前,以DBzP为模板的表面印迹聚合物尚未见文献报道。
本文以DBzP为模板分子,以Stöber法+“种子生长法”获得的微米二氧化硅微球为载体,采用表面分子印迹技术在其表面接枝形成DBzP印迹聚合层。采用红外光谱和扫描电镜对该聚合物结构进行表征,并对MIPs的平衡吸附时间、饱和吸附量、选择性和使用寿命进行了考察。结合超高效液相色谱(UPLC),以MIPs为吸附材料,对食用油油桶和饮料瓶中的DBzP进行分离、富集和测定,得到了理想的结果。
1 实验部分
1.1仪器与试剂
美国Waters ACQUITY UPLC H-class型超高效液相色谱仪;扫描电镜(ZEISS SUPRA 55VP);傅立叶变换红外光谱仪(Prestige-21,岛津);N-EVAPTM 116氮吹仪(美国Organomation Association INC);DF-2集热式磁力加热搅拌器(金坛市金分仪器有限责任公司);DZF-6050型真空干燥箱(上海博讯实业有限公司);SHZ-82水浴恒温振荡器(金坛市医疗仪器厂);LDZ4-2自动平衡离心机(江苏省金坛市医疗仪器厂)。
邻苯二甲酸二苄酯(DBzP)、邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二环己酯(DCHP)、邻苯二甲酸二辛酯(DOP)、正硅酸乙酯(TEOS)(天津永晟精细化工有限公司);偶氮二异丁腈(AIBN)、甲基丙烯酸(MAA)(天津市光复精细化工研究所);乙二醇二甲基丙烯酸酯(EGDMA,阿拉丁试剂公司);3-甲基丙烯酰氧基丙基三甲氧基硅烷(KH570,西亚试剂公司);无水乙醇、无水甲苯、氨水(天津市富宇精细化工有限公司);氯化钠(天津市致远化学试剂有限公司);冰乙酸、甲醇、异丙醇(天津市百世化工有限公司);以上试剂均为分析纯。乙腈(色谱纯,美国Fisher公司);0.22 μm微孔滤膜(美国Pall公司);蒸馏水由美国Milli-Q纯水系统制备。
1.2液相色谱条件
色谱柱:Waters ACQUITY UPLC HSS T3柱(2.1 mm×150 mm,1.8 μm);进样体积为5 μL,流速0.2 mL/min,柱温30 ℃。检测波长为224 nm。流动相:乙腈-水(95∶5),采用等度洗脱方式。
1.3实验方法
1.3.1二氧化硅微球的合成采用改进的Stöber法[19],分别将16 mL 25%氨水、28 mL水加入250 mL丙醇-甲醇(体积比3∶1,下同)溶液中,剧烈搅拌15 min后,将13 mL TEOS快速加至上述溶液中。30 ℃下,剧烈磁力搅拌17 h。将合成的SiO2离心15 min(3 700 r/min),无水乙醇洗涤多次,离心,直至呈中性,将制得的纳米SiO2粒子分散在无水乙醇中,置于4 ℃冰箱中备用。
采用“种子生长法”[20],以上述合成的SiO2为种子,经两次生长制备大粒径SiO2。准确称取0.067 4 g NaCl至28 mL水中,然后将18 mL 25%氨水、NaCl水溶液(0.067 4 g的NaCl溶于28 mL 水中)加至250 mL丙醇-甲醇(3∶1)溶液中,再加入7 g的种子SiO2,超声10 min,室温磁力搅拌2 h。最后将15 mL TEOS分批次加入(每隔20 min加入1 mL),30 ℃磁力搅拌1夜。再次采用“种子生长法”,合成更大粒径的SiO2,保存至4 ℃冰箱备用。
1.3.2二氧化硅微球的改性将2 g二氧化硅粒子加至80 mL无水甲苯中,超声分散20 min,室温磁力搅拌1 h。加入8 mL KH570,110 ℃氮气保护下磁力搅拌持续回流11 h,得到淡黄色的改性二氧化硅粒子(SiO2-KH570)。
1.3.3DBzP核壳印迹聚合物的制备将50 mL乙腈溶液加至100 mL两口圆底烧瓶中,依次加入242.4 mg DBzP和0.472 mL MAA,室温下氮气保护磁力搅拌12 h。将0.12 g SiO2-KH570、4.375 mL EGDMA和75.0 mg AIBN加至上述溶液中,60 ℃油浴加热,氮气保护下磁力搅拌14 h,然后将温度升至80 ℃,持续10 h。离心10 min得到MIPs,乙腈洗涤两次后,置于索氏提取器中,以甲醇-冰乙酸(体积比85∶15)洗脱模板DBzP。用甲醇多次洗涤至中性,最后用无水乙醇洗涤,离心,40 ℃下真空干燥24 h,备用。非印迹聚合物(NIPs)的制备过程与印迹聚合物完全相同,只是不加模板分子。
1.4吸附特性研究
1.4.1动力学吸附性能测试准确称取20 mg的MIPs或NIPs至10 mL的0.2 mg/mL DBzP-乙腈溶液中,室温下水浴振荡,分别在不同时间点(5,10,15,20,25,30,40,60,80,90 min)依次取出玻璃离心管,3 700 r/min离心10 min,移取上清液,过0.22 μm滤膜,并稀释适当倍数。根据吸附前后稀释溶液中DBzP的浓度变化,求出MIPs和NIPs在不同浓度下的吸附结合量Q(mg/g)[21]。
1.4.2热力学吸附性能测试准确称取20 mg MIPs或NIPs至10 mL玻璃离心管中,分别加入10 mL不同质量浓度(0.02~0.5 mg/mL)的DBzP-乙腈溶液,298 K下水浴振荡40 min。278 K和318 K温度下的实验过程与上述相同。
1.4.3选择性吸附性能测试选取与DBzP结构相似的DMP,DBP,DCHP,DOP为竞争对象。室温下分别将20 mg 的MIPs或NIPs加至浓度均为0.05 mg/mL的含上述5种邻苯二甲酸酯的10 mL乙腈混合溶液中,振荡2 h。
1.4.4吸附-脱附循环吸附性能研究室温下准确称取20 mg MIPs至10 mL玻璃离心管中,加入0.5 mg/mL的DBzP-乙腈溶液,振荡40 min,离心10 min。将聚合物用甲醇-乙酸 (体积比17∶3)溶液充分洗脱处理后,再重复9次上述步骤。
1.5实际样品测定
选取食用油油壶和塑料饮料瓶作为实际样品。实际样品中DBzP的加标浓度分别为12.5,25,50 μg/g。分别准确称取0.5 g样品至25 mL比色管中,加入10 mL乙腈,超声提取30 min,准确移取4 mL萃取液至另一10 mL玻璃离心管中,加入20 mg MIPs聚合物,室温下水浴振荡30 min,离心10 min,加入3×2 mL甲醇-乙酸(85∶15)进行洗脱,离心10 min,收集所有洗脱液至10 mL玻璃离心管中,40 ℃下氮吹近干后,加入1 mL乙腈溶液定容,过0.22 μm 滤膜,待UPLC测定。
2 结果与讨论
2.1分子印迹聚合物的制备
图1为MIPs的合成过程,分别采用Stöber法、“种子生长法”和表面分子印迹技术合成以SiO2为载体的分子印迹聚合壳层。首先,在Stöber方法基础上,30 ℃下通过TEOS的水解缩合作用合成粒径均一的SiO2纳米粒子;再采用“种子生长法”,以Stöber方法合成的SiO2纳米粒子为种子,经过反复两次生长,合成粒径均匀的SiO2微球。在“种子生长法”的过程中,加入微量的电解质NaCl以增大体系中TEOS的分散性,防止SiO2生长过程中的新核密度数,促进SiO2纳米粒子的长大;增加氨水浓度以提高TEOS的水解速率,抑制缩聚速率,防止新核的形成,其作用与电解质NaCl相辅相成;然后,采用硅烷偶联剂KH570修饰SiO2微球表面,引入乙烯基双键,微球表面由亲水性转变为疏水性,大大提高了SiO2微球的分散性。最后,模板分子DBzP和MAA、EGDMA在AIBN引发作用下与SiO2微球表面的乙烯基双键发生表面聚合反应,通过洗脱模板,获得表面分子印迹壳层(MIPs)。同时以上述方法合成了不加模板的印迹壳层(NIPs)。
2.2印迹聚合物的表征
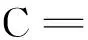
2.2.2扫描电镜分析分别对SiO2种子、SiO2一次生长、SiO2二次生长、SiO2-KH570、MIPs和NIPs的扫描电镜图进行考察(图3)。由图3可见,上述各物质的平均粒径分别为0.912,1.895,2.743,2.776,2.805,2.797 μm。采用“种子生长法”,以SiO2粒子为种子,经两次生长后,合成出的SiO2微球的平均粒径约2.743 μm(图3C);在无水甲苯条件下,SiO2微球经KH570修饰后,表面引入乙烯基双键,其粒径增加(图3D)。然后在修饰后的SiO2微球表面进行表面印迹聚合反应,获得粒径约为2.805 μm的分子印迹二氧化硅微球(图3E),其印迹壳层厚度约为29 nm。采用相似方法制备的非印迹微球,其壳层厚度约为21 nm(图3F)。从图中可以看出,合成的各材料形貌均为球形,且具有良好的分散性和均匀的粒径分布。对比图3E和F可以看出,由于模板分子DBzP的印迹,MIPs的表面比NIPs表面更粗糙。
2.3聚合物的吸附性能研究
2.3.1吸附动力学性能研究对MIPs和NIPs材料进行动力学吸附实验,结果见图4。在吸附过程的前30 min,MIPs和NIPs的吸附速率均较快,但MIPs的吸附速率更快,吸附量更大,这是由于MIPs表面分布有与模板分子DBzP的尺寸、大小和形状相匹配的结合位点,而NIPs表面无与DBzP相匹配的结合位点。30 min后,MIPs的吸附量增加趋缓,吸附趋于平衡。
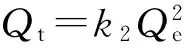
表1MIPs和NIPs的伪一级动力学和伪二级动力学模型参数
Table 1Kinetic adsorption parameters of MIPs and NIPs
2.3.2等温吸附性能研究在动力学吸附实验基础上,还进行了热力学吸附性能实验,考察了不同温度(278,298,318 K)下DBzP在MIPs和NIPs上的吸附性能,结果如图5所示。随着温度的升高,DBzP在MIPs和NIPs上的吸附量Qe均随着初始浓度的增大而增加,直至达到吸附平衡(图5A,B)。从图中可以观察到,在相同温度条件下,DBzP在MIPs上的吸附量明显大于在NIPs上的吸附量,且随着温度升高,MIPs的吸附增加量比NIPs更快。表明随着温度升高,DBzP更易进入印迹壳层的空腔,说明该吸附符合吸热反应的特点。
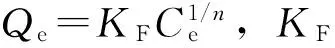
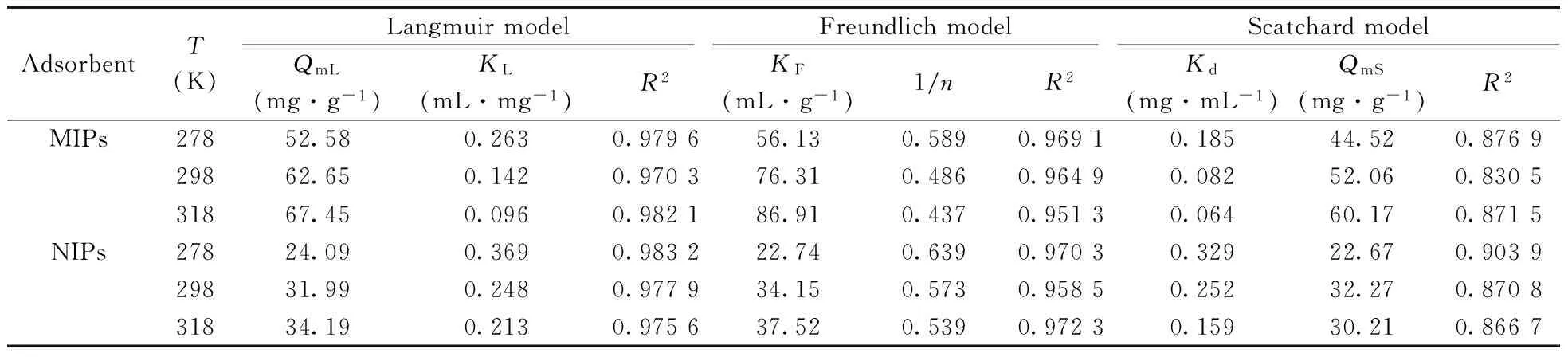
表2 MIPs和NIPs在不同温度下的等温吸附参数Table 2 Adsorption isotherm fitting parameters for MIPs and NIPs at different temperatures
MIPs和NIPs在等温条件下的Scatchard方程拟合曲线显示,在3个不同温度条件下,MIPs和NIPs的Scatchard方程拟合均为一条直线,表明MIPs和NIPs上仅分布1种结合位点,且为均相分布。拟合结果见表2,以298 K温度下的吸附为例,MIPs在Scatchard拟合下的表观最大吸附量QmS为52.06 mg/g,与Langmuir拟合下的理论最大吸附量QmL=62.65 mg/g相比,更接近实测值(47.35 mg/g)。
为更好地评价温度对MIPs吸附DBzP的影响,采用吉布斯自由能(ΔGo)[23]考察了不同温度条件下MIPs的吸附反应趋势。在278,298,318 K温度条件下,ΔGo值分别为-10.05,-11.79,-13.17 kJ/mol。此结果表明DBzP在MIPs上的吸附过程为自发进行,随着温度的升高,ΔGo数值减小,表明升高温度有利于吸附反应的进行,这一结论与实验结果相吻合。
2.3.3选择性吸附研究考察了混标溶液吸附前后的液相色谱图,结果如图6所示。实验结果显示,相比于MIPs吸附前混标溶液的液相色谱图(图6A),经MIPs吸附后,溶液中各物质的浓度有所降低,但DBzP的浓度降低最多,由50 μg/mL降至19.28 μg/mL,DBzP在MIPs上的吸附率达到61.44%(图6B)。对其他结构相似干扰物的吸附率均低于45%,而与DBzP结构极其相似的DCHP在MIPs上的吸附率仅达到46.72%,表明MIPs对DBzP具有显著的识别性能(图6B)。而经NIPs吸附后各物质的浓度变化非常小,吸附率在19.2%~29.5%之间(图6C),表明NIPs对各物质没有识别性。
采用分配系数(Kd)、选择性系数(k)和相对选择性系数(k′)对MIPs和NIPs的选择性吸附性能进行评价[23]。如表3所示,DBzP在MIPs上的吸附量大于其他竞争物(DMP,DBP,DCHP和DOP),而DBzP在NIPs上的吸附量与其他4种结构类似物的吸附量相似,无明显区别。此外,DBzP在MIPs上的Kd(MIPs)也明显高于其他4种结构类似物,各物质的k′均大于1,且k′(DCHP) 2.3.4循环再生吸附性能研究考察了MIPs的循环使用能力及使用寿命,与初始相比,MIPs经过7次使用后,对DBzP的吸附量基本相同,其吸附效率仅降低了9.5%;经过10次吸附后,吸附效率为83%。表明MIPs稳定性强,具有较长的使用寿命。 2.4加标回收实验 以MIPs为吸附材料,结合UPLC技术,富集和测定了食用油油壶与果粒橙塑料瓶中的DBzP。该方法的线性范围为0.5~50 μg/mL,检出限(S/N=3)为0.052 μg/mL。在12.5,25,50 μg/g 3个加标浓度下,油壶中DBzP的回收率分别为88.8%,91.3%,92.9%,果粒橙饮料瓶的回收率分别为90.2%,91.7%,93.1%,相对标准偏差(RSD)均低于6%。该方法能够选择性地萃取和测试塑料产品中的DBzP。 表3 MIPs和NIPs的选择性识别参数Table 3 Selective recognition parameters of MIPs and NIPs -:no data 本文采用Stöber和“种子生长法”相结合获得了粒径均一的二氧化硅微球,并以DBzP为模板分子在改性后的SiO2微球表面进行印迹聚合反应,获得了29 nm的印迹壳层。分别采用红外光谱和扫描电镜对其结构和形貌进行了表征。通过动力学吸附实验、等温吸附实验与选择性吸附实验考察了MIPs的吸附性能,结果发现MIPs的平衡吸附时间为30 min,且对DBzP具有显著识别性,其识别过程为化学吸附过程。同时采用Langmuir,Freundlich和Scatchard模型对等温吸附实验数据进行拟合,结果表明MIPs的吸附行为符合单分子层吸附,在印迹壳层中MIPs只有1种结合位点,且为均相分布。以MIPs作为吸附材料,结合UPLC成功实现了食品包装材料中DBzP的分离、富集与检测,DBzP的平均回收率为88.8%~93.1%,RSD均小于6%,表明MIPs可用于食品包装材料中痕量DBzP的萃取。 [1]Farahani H,Ganjali M R,Dinarvand R,Norouzi P.Talanta,2008,76:718-723. [2]GB/T 21928-2008.Determination of Phthalate Esters in Food Plastic Packaging Materials.Beijing:Standard Press of China(食品塑料包装材料中邻苯二甲酸酯的测定.北京:中国标准出版社),2008. [3]Zhang Z B,Hu Y,Zhao L,Li J,Bai H C,Zhu D S,Hu J Y.Toxicol.Lett.,2011,207:7-11. [4]Lv Y K,Zhang W,Guo M M,Zhao F F,Du X X.Anal.Methods,2015,7:560-565. [5]Su R Y,Zhao X W,Li Z Y,Jia Q,Liu P,Jia J B.Anal.Chim.Acta,2010,676:103-108. [6]Liu F J,Xian Y P,Guo X D,Weng Y B,Peng Y,Chen J W,Lu Y J.J.Instrum.Anal.(刘付健,冼燕萍,郭新东,翁乙斌,彭莺,陈纪文,卢宇靖.分析测试学报),2014,33(4):437-441. [7]Zhan S X,Kuang Y Q,Li X Y,Guo X D.J.Instrum.Anal.(湛社霞,匡耀求,李秀英,郭新东.分析测试学报),2015,34 (8):874-879. [8]Yang J L,Li Y X,Wang Y,Ruan J,Zhang J,Sun C J.TrendsAnal.Chem.,2015,72:10-26. [9]Ding X C,Heiden P A.Macromol.Mater.Eng.,2014,299:268-282. [10]Peng Y Y.J.Instrum.Anal.(彭友元.分析测试学报),2013,32 (12):1427-1432. [11]Huang C N,Duan X J,Ma H P,Yu Y H,Chen L G.J.Instrum.Anal.(黄超囡,段西建,麻海鹏,于嫣涵,陈立钢.分析测试学报),2013,32(3):275-280. [12]Wang X X,Yang J,Xie S Y,Chen Y,Liu F L,Shen H Y,Xia Q H.J.Instrum.Anal.(王新鑫,杨军,谢晟瑜,陈扬,刘芳伶,沈昊宇,夏清华.分析测试学报),2015,34(11):1213-1219. [13]Resmini M.Anal.Bioanal.Chem.,2012,402:3021-3026. [14]Hu Y L,Pan J L,Zhang K G,Lian H X,Li G K.TrAC,TrendsAnal.Chem.,2013,43:37-52. [15]Chen Y,Feng T,Li G K,Hu Y F.J.Sep.Sci.,2015,38(2):301-308. [16]Long Z R,Lu Y,Zhang M L,Qiu H D.J.Sep.Sci.,2014,37(19):2764-2770. [17]Guo H,Yuan D Y,Fu G Q.J.ColloidInterfaceSci.,2015,440:53-59. [18]Hu J H,Feng T,Li W L,Zhai H,Liu Y,Wang L Y,Hu C L,Xie M X.J.Chromatogr.A,2014,1330:6-13. [19]Stöber W,Fink A,Bohn E.J.ColloidInterfaceSci.,1968,26:62-69. [20]Chen S L,Dong P,Yang G H,Yang J J.J.ColloidInterfaceSci.,1996,180:237-241. [21]Wang W,Ma Y,Li A M,Zhou Q,Zhou W W,Jin J.J.Hazard.Mater.,2015,294:158-167. [22]Ma J,Yuan L H,Ding M J,Wang S,Ren F,Zhang J,Du S H,Li F,Zhou X M.Biosens.Bioelectron.,2011,26:2791-2795. [23]Zhang H X,Dou Q,Jin X H,Sun D X,Wang D D,Yang T R.Sep.Sci.Technol.,2015,50:901-910. [24]Zhu J F,Zhang G H,Shang T,Xiong W.Adv.Mater.Res.,2012,549:340-343. Preparation of Monodisperse Molecularly Imprinted Shell Based on Silica Microsphere Surface for Specific Recognition and Determination of Dibenzyl Phthalate in Food Packaging Materials XU Wei-wei1,LONG Ze-rong2*,LU Yi2,WANG Ji-de1* (1.Key Laboratory of Oil and Gas Fine Chemicals,Ministry of Education,Xinjiang University,Urumqi830046,China;2.Product Quanlity Supervision and Inspection Academy of Xinjiang,Urumqi830011,China) A molecularly imprinted nanoshell was prepared successfully by using dibenzyl phthalate (DBzP) as template and silica microspheres as supporter based on the combination of the molecular imprinting technique,sol-gel and seed-mediated growth synthesis.The imprinted microspheres were characterized by FT-IR and SEM.Meanwhile,a series of adsorption experiments were performed to investigate the adsorption characterization of the imprinted particles.The imprinted particles reached an adsorption equilibrium within 30 min,and the adsorption behavior was in accordance with the pseudo-second-order model.The maximum adsorption was up to 47.35 mg/g at ambient temperature.The adsorption isotherms of DBzP onto the imprinted particles were well described by Langmuir isotherm model,Freundlich isotherm model and Scatchard model at different temperature,respectively.The results indicated that the Langmuir isotherm model was more suitable to describe the adsorption process than Freundlich model.The Scatchard analysis suggested that the imprinted particles had only one binding site with homogeneous distribution trait.The imprinted particles also showed an more excellent selectivity to DBzP than other four structural analogues.The rebinding capacities of the imprinted particles remained 83% after 10 cycles of adsorption-desorption under the relatively mild regeneration conditions.Simultaneously,the method for the determination of DBzP in plastic package samples via the imprinted particles coupled with UPLC was developed,it was also successfully applied in the analysis of DBzP in two spiked plastic package samples with average recoveries of 88.8%-93.1% and the relative standard deviation lower than 6%.Thus,the imprinted polymer is one of outstanding candidate materials for extraction of DBzP in food or their packaging materials.Key words:seed-mediated growth synthesis;silica microparticle;imprinting nanoshell;dibenzyl phthalate;food packaging materials 2016-01-05; 2016-03-03 新疆维吾尔自治区自然科学基金(2012211A107);新疆质量技术监督局科技项目(1502) 龙泽荣,博士,高级工程师,研究方向:分子印迹材料的合成及应用,Tel:0991-3191181,E-mail:long8326rong@163.com 王吉德,博士,教授,研究方向:分析化学,Tel:0991-8582807,E-mail:awangjd@126.com 研究报告 10.3969/j.issn.1004-4957.2016.08.001 O657.72;TQ047.9 A 1004-4957(2016)08-0929-08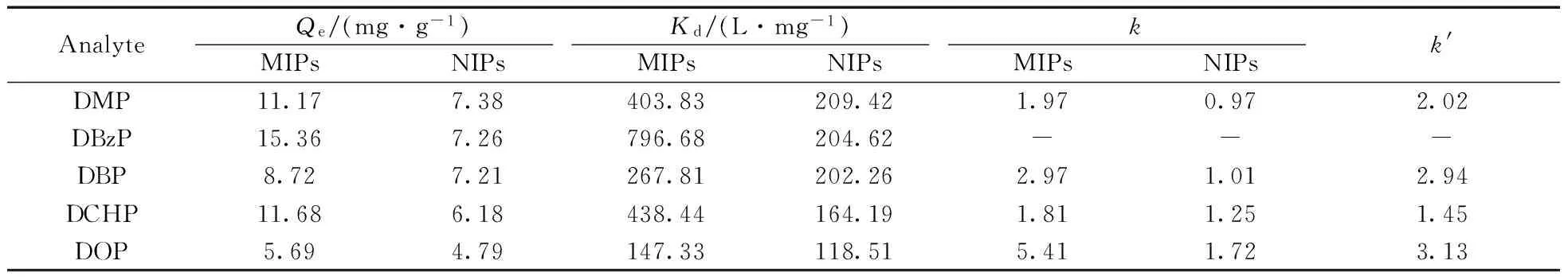
3 结 论

