高中化学一个重要结论的推导及应用
章中华
湖北宜城三中
高中化学一个重要结论的推导及应用
章中华
湖北宜城三中
化学是自然学科中的一门课程,由于高中化学课程知识涉及的面广、内容比较抽象,在高中化学课程的学习上学生们会遇到很多的困难。身为一名高中化学的教师,不仅仅要把教学的内容作为课堂中教学任务,更重要是看学生平时掌握的情况。只有学生及时掌握教师讲授的课程教学内容,才能更好的运用理论。本文以化学课程的一个重要结论为例进行讲解推导,并通过题目加以应用来帮助学生掌握知识要点。所以教师必须对当前高中化学课程教学进行不断探究,寻求学生能够最多的接受教学方法,才能在基础上提高化学课堂教学的整体效果。
化学;溶质;质量
一、结论的内容
同种溶质,不同质量分数的两溶液等体积混合后所得溶液的质量分数,总是介于两溶质质量分数和的一半及原溶液密度大的溶质质量分数之间。
二、结论的推导
1、a%的M的溶液与b%的M的溶液等质量混合后,混合溶液的溶质质量分数为c%;设它们的质量分别为m,由稀释定理可得,
a%·m+b%·m=2m·c%c%=(a%+b%)/2
2、a%的M的溶液与水等体积混合后,混合溶液的溶质质量分数为c%;设它们的体积分别为V,a%的M的溶液的密度为D1,水的密度为D2,则:
由稀释定理可得,
a%·D1·V=c%(D1·V+D2·V)
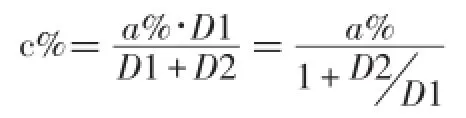
讨论:当D1>D2时,a%>c%>a%/2;当D1<D2时,0<c%<a%/ 2;(注:水中的溶质质量分数可看作为0)。
3、a%的M的溶液与b%的M的溶液等体积混合后,混合溶液的溶质质量分数为c%;设它们的体积分别为V,a%的M的溶液的密度为D1,b%的M的溶液的密度为D2,则:由稀释定理可得,
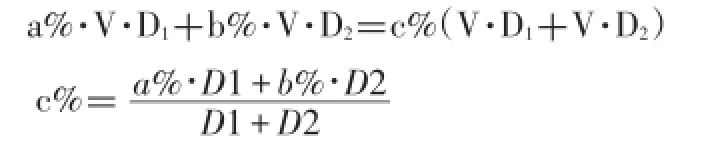
作差有,

讨论:当a%>b%,D1>D2时(即溶液的密度随溶质质量分数增大而增大)。
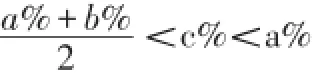
当a%>b%,D1<D2时(即溶液的密度随溶质质量分数增大而减小)。
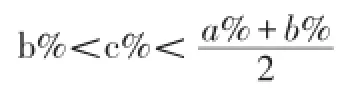
综上所述:以上结论是正确的。
三、结论的应用
1、a%的酒精溶液与(100-a)%的酒精溶液等体积混合后所得酒精溶液的质量分数可能为()
A、<50%B、>50%C、≤50%D、≥50%
分析:当a%=(100-a)%时,即为等质量混合,混合后酒精溶液的质量分数为50%;
当a%≠(100-a)%时,由于酒精溶液的密度是随着其质量分数的增大而减小的,根据上述结论可得,混合后的酒精的质量分数为<50%,所以正确的答案为C。
2、(1997年高考试题)密度为0.91g/㎝3的氨水,质量百分比浓度为25%(即质量分数为0.25),该氨水用等体积的水稀释后,所得溶液的质量百分比浓度为()
A、等于12.5%;B、大于12.5%;C、小于12.5%;D、无法确定;
分析:由上述结论可得,正确的答案为C。
以上就是笔者对一个化学重要理论的讲解过程,通过推导强化对知识点的掌握,突出理论要点,最后通过知识的运用,深化改理论知识的学习,由此反射出化学知识学习运用的讲授。同时在丰富学生课程知识的同时并且提高学生能力,才可以构建出高效可观的化学课堂。新时期,教师必须对当前化学教学进行不断探究,找到适合学生能够接受的教学方案,才能及时提高化学课堂整体的效果。
[1]赵静.研究性学习在高中化学教学中的实践评价[J].科技创新导报,2010(07).
[2]蔺建红.如何提高高中化学教学质量[J].中国教育技术装备,2012(01).
[3]高丽.高中化学教学的几点思考[J].成功(教育),2011(03).
章中华(1972-),男,湖北宜城市人,中学一级教师,现任教于湖北省宜城市第三高级中学,长期处于高中化学一线教学,研究方向:高中化学。

