注射用头孢噻肟钠他唑巴坦钠(6∶1)含量测定方法的研究
陈爱萍,朱雪萍,戴云志
(南京优科生物医药有限公司,南京 210029)
注射用头孢噻肟钠他唑巴坦钠(6∶1)含量测定方法的研究
陈爱萍,朱雪萍,戴云志
(南京优科生物医药有限公司,南京 210029)
目的:建立同时测定注射用头孢噻肟钠他唑巴坦钠(6∶1)中头孢噻肟和他唑巴坦含量的方法。方法:采用反相高效液相色谱法。色谱柱为Agilent Eclipse Plus C18柱(250 mm×4.6 mm, 5 μm),流动相为甲醇-磷酸二氢钾溶液(6.7 g磷酸二氢钾,3 ml磷酸,2 ml四丁基氢氧化铵,用水溶解并稀释至1 000 ml)(27∶73),流速为1.0 ml/min,检测波长为220 nm,柱温为30 ℃,进样量为20 μl。结果:头孢噻肟和他唑巴坦的进样量分别在0.516~4.124 μg和0.083~0.663 μg范围内和各自峰面积积分值呈良好线性关系(r=1);平均加样回收率分别为100.6%和100.4%,RSD分别为0.79%和0.94%(n=9)。结论:该方法操作简便,专属性和耐用性好,结果准确,可同时测定注射用头孢噻肟钠他唑巴坦钠(6∶1)中头孢噻肟和他唑巴坦的含量。
高效液相色谱法,头孢噻肟,他唑巴坦,含量测定
头孢噻肟钠为第三代头孢菌素,抗菌谱广,对大肠埃希菌、克雷伯菌属等革兰阴性菌有强大活性。在临床上头孢噻肟钠主要用于敏感细菌所致的肺炎及其他下呼吸道感染、尿路感染、脑膜炎、败血症、腹腔感染、盆腔感染、皮肤软组织感染、生殖道感染、骨和关节感染等,还可以作为小儿脑膜炎的首选药物。但头孢噻肟易被β-内酰胺酶水解而失去活性,卫生部细菌耐药监测网基础网(MOH National Antimicrobial Resistant Investigation Net,Mohnarin) 近年来对于成人感染患者的调查结果显示[1-3]:常见致病菌,特别是产超广谱β-内酰胺酶(ESBLs)的肠杆菌科细菌对于头孢噻肟的耐药率逐年增高,肠杆菌科主要致病菌对于头孢噻肟的耐药率基本在50%以上,最高已达70%左右。他唑巴坦钠是目前上市的最强的β-内酰胺酶抑制剂[4],二者联用发挥协同抗菌作用。注射用头孢噻肟钠他唑巴坦钠(6∶1)是头孢噻肟和他唑巴坦按6∶1(w/w)组成的复方制剂,可有效克服因ESBLs引起的耐药,并能阻断或延缓耐药的继续发展,是一个安全、有效的复方抗生素,属于化药1.5类新药。本文建立反相高效液相法同时测定头孢噻肟和他唑巴坦含量。
1 仪器与试药
LC-1260高效液相色谱系统(含1260Quat PumpVL泵、1260ALS自动进样器、1260TCC控温箱、1260VWD紫外检测器和OpenLAB色谱工作站,安捷伦);AL204型电子分析天平(德国梅特勒仪器公司);BP211D型电子分析天平(德国赛多利斯仪器公司); 320-S pH计[梅特利-托利多仪器(上海)有限公司]。头孢噻肟对照品(中国药品生物制品检定所,批号130480-200903,含量83.7%);他唑巴坦对照品(中国药品生物制品检定所,批号130511-200402,含量99.1%);注射用头孢噻肟钠他唑巴坦钠粉针剂(6∶1)(南京优科制药有限公司,批号20140401、20140402、20140403)。磷酸二氢钾、10%四丁基氢化铵和磷酸均为分析纯,购自国药集团化学试剂有限公司;甲醇为色谱纯,购自Merck公司;水为娃哈哈纯净水。
2 方法与结果
2.1 色谱条件 色谱柱:Agilent Eclipse Plus C18柱(250 mm×4.6 mm, 5 μm);流动相:甲醇-磷酸二氢钾溶液(6.7 g磷酸二氢钾、3 ml磷酸、2 ml四丁基氢氧化铵,用水溶解并稀释至1 000 ml)(27∶73);流速为1.0 ml/min;波长为220 nm;柱温为30 ℃;进样量为20 μl;运行时间12 min。
2.2 溶液的制备
2.2.1 空白对照溶液 以流动相做为空白对照溶液。
2.2.2 对照品溶液的配制 取头孢噻肟和他唑巴坦对照品适量,精密称定,加流动相溶解并稀释制成每1 ml分别含头孢噻肟100 μg、他唑巴坦17 μg的溶液,作为对照品溶液。
2.2.3 供试品溶液的配制 精密称取注射用头孢噻肟钠他唑巴坦钠(6∶1)适量,加流动相溶解并稀释制成每1 ml分别含头孢噻肟100 μg、他唑巴坦17 μg的溶液,作为供试品溶液。
2.3 系统适用性试验 精密量取对照品溶液、供试品溶液和空白对照溶液各20 μl注入液相色谱仪,记录色谱图。头孢噻肟主峰保留时间为8.515,理论塔板数为9 195,峰纯度为1 000;他唑巴坦主峰保留时间为4.547,理论塔板数为10 461,峰纯度为1 000,两主成分在220 nm均有最大吸收。头孢噻肟和他唑巴坦主峰的分离度符合要求,主峰与各个杂质峰分离度也均符合要求,空白对照对检测没有影响。色谱图见图1。
2.4 线性范围考查 精密称取头孢噻肟对照品和他唑巴坦对照品适量,精密称定,加流动相溶解并稀释制成每1 ml约含头孢噻肟100 μg、他唑巴坦17 μg的溶液,作为线性对照品溶液。分别取溶液5、10、20、30和40 μl依次注入液相色谱仪,记录色谱图。以进样量(μg)为横坐标,以峰面积(Y)为纵坐标,进行线性回归。头孢噻肟回归方程为:Y=1 357.2X+5.215 2(r=1),线性范围为0.516~4.124 μg。他唑巴坦回归方程:Y= 883.65X+ 0.973 2(r=1),线性范围为0.083~0.663 μg。

1.他唑巴坦 2.头孢噻肟
2.5 定量限 取头孢噻肟对照品适量,精密称定,加流动相溶解并稀释制成每1 ml约含头孢噻肟100 μ g的溶液,逐级稀释,进行测定,按信噪比10∶1,确定头孢噻肟的最小定量限为0.11 ng。取他唑巴坦对照品适量,精密称定,加流动相溶解并稀释制成每1 ml约含他唑巴坦17 μ g的溶液,逐级稀释,进行测定,按信噪比10∶1,确定他唑巴坦的最小定量限为0.23 ng。
2.6 精密度试验 取线性试验项下的对照品溶液,精密量取20 μl依次注入液相色谱仪,连续进样6次,记录峰面积,头孢噻肟和他唑巴坦峰面积的RSD分别为0.06%和1.04%。试验结果表明,本法进样精密度良好。
2.7 溶液稳定性试验 取本品(批号20140401),加流动相制成每1 ml含头孢噻肟100 μg、他唑巴坦17 μg的溶液,作为供试品溶液,置于温度为5 ℃自动进样器上,分别于0、2、4、6、8、10和12 h进样测定。头孢噻肟和他唑巴坦峰面积RSD分别为0.53%和0.44%,表明供试品溶液在5 ℃条件下12 h 内相对稳定。
2.8 重复性试验 取本品(批号20140401)适量,精密称定,加流动相溶解并制成每1 ml含头孢噻肟100 μg、他唑巴坦17 μg的溶液,作为供试品溶液,共配制6份,进样测定。结果按无水物计,头孢噻肟和他唑巴坦标示量的含量分别为101.4%和102.1%,RSD分别为0.38%和0.49%。
2.9 回收率试验 按照供试品溶液80%、100%、120%的浓度配制高、中、低三个样品溶液,每个溶液配制三份,进样测定,计算回收率。结果见表1和表2。头孢噻肟和他唑巴坦的平均回收率分别为100.6%和100.4%,RSD分别为0.79%和0.94%。
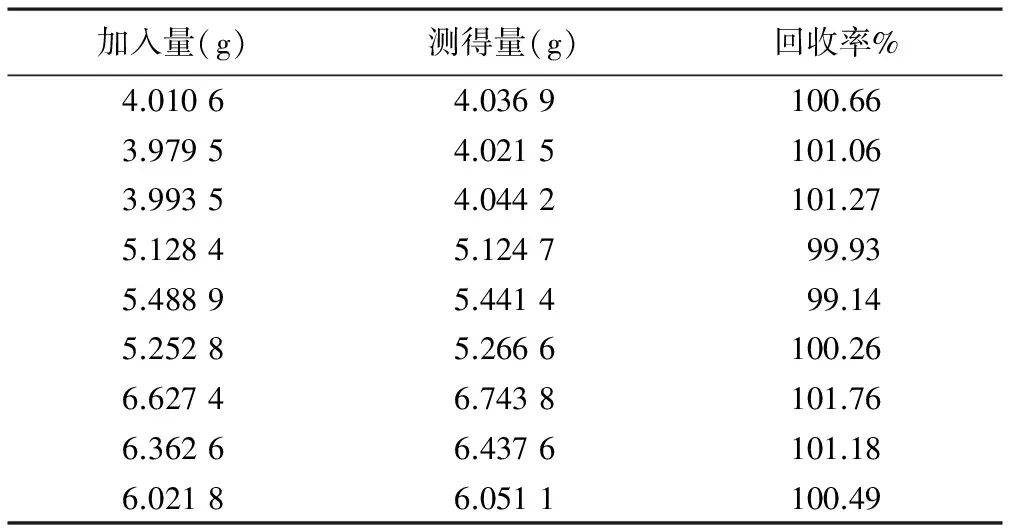
表1 头孢噻肟回收率试验结果(n=9)

表2 他唑巴坦回收率试验结果(n=9)
2.10 耐用性试验 分别考查了盐用量、柱温、流速、pH值、四丁基氢氧化铵用量、流动相比例和波长在±5%范围内变化,及采用不同的色谱柱对本品的含量测定的影响。上述不同条件下,头孢噻肟和他唑巴坦的平均含量分别为100.7%和101.6%,RSD(n=15)分别为0.77%和0.82%。表明本法耐用性良好,微调盐用量、柱温、流速、pH值、四丁基氢氧化铵用量、流动相比例和波长,及更换不同厂家的色谱柱,对本品含量测定结果无影响。
2.11 含量测定 取注射用头孢噻肟钠他唑巴坦钠(6∶1)三批(批号20140401、20140402、20140403),按“2.1”项下色谱条件分别测定头孢噻肟和他唑巴坦的含量,结果见表3。

表3 含量测定结果
3 讨论
头孢噻肟和他唑巴坦都是稳定性较差的内酰胺类化合物,在生产、贮藏、运输和使用过程中易产生较多的杂质,会干扰头孢噻肟和他唑巴坦的含量测定,且在研究过程中发现磷酸盐的离子浓度和四丁基氢氧化铵的浓度对头孢噻肟的保留时间、理论板数和峰型都有很大的影响。本文参考《中国药典》他唑巴坦的含量测定方法进行色谱条件的摸索[5],采用Agilent Eclipse Plus C18柱(250 mm×4.6 mm,5μm),流动相为乙腈-0.03 mol/L磷酸二氢钾溶液-10% 四丁基氢氧化铵溶液(190∶795∶15)(用磷酸调节pH值至4.0);流速为1.0 ml/min;波长为230 nm;柱温为30 ℃,进样量为20 μl。结果头孢噻肟保留时间为29.245 min,理论板数为1 285;头孢噻肟峰较宽,且出现肩峰,峰型很差,柱效低。随后稍微增加磷酸二氢钾的量,减少四丁基氢氧化铵的量,采用报道中的色谱条件,得到了较为满意的分离效果:头孢噻肟峰和他唑巴坦峰在10 min全部洗脱出来,两个主峰之间、两个主峰和杂质之间都达到了基线分离。
在选择检测波长时,因为要同时测定头孢噻肟和他唑巴坦的含量,检测波长需要满足两个成分均有吸收的条件。本文分别取头孢噻肟对照品、他唑巴坦对照品适量,加流动相配制成50 μg/ml的溶液,照紫外分光光度法,在190~400 nm波长范围内进行紫外扫描,头孢噻肟的最大吸收波长为254 nm,由于他唑巴坦在254 nm处无吸收,故选择头孢噻肟和他唑巴坦吸收均较强的220 nm作为检测波长。
综上所述,该方法灵敏度高、专属性强、操作简便,能够同时测定本品中头孢噻肟和他唑巴坦的含量。
1 刘根焰,童明庆,梅亚宁,等. Mohnarin 2009年度报告:青壮年(14-65岁) 来源菌株耐药监测[J]. 中国临床药理学杂志,2011,27(7):508-516
2 梅亚宁,童明庆. 2010年度卫生部全国细菌耐药监测网报告:青壮年来源菌株耐药监测结果[J]. 中华医院感染学杂志,2012,22(1):44-49
3 梅亚宁,童明庆.2011年度卫生部全国细菌耐药监测网报告:成年患者分离菌的耐药监测[J]. 中国临床药理学杂志,2014,30(2):94-99
4 熊自忠,朱德妹,汪复,等.CTX-M-12编码基因的克隆、表达及序列分析[J]. 中国传染病杂志,2003,21(2):110-113
5 中国药典[S].二部.2010:169-170
Determination of cefotaxime sodium and tazobactam sodium in injection
Chen Aiping, Zhu Xueping, Dai Yunzhi
(Nanjin Yoko bio-Pharmaceutical co ltd,Nanjing 210029 )
Objective: To establish a new method for quantitative determination of cefotaxime and and tazobactam simultaneously in the injection preparation with cefotaxime sodium and tazobactam sodium at a ratio of 6 to 1. Methods: An RP-HPLC method was adopted. The analysis was performed on Agilent Eclipse Plus C18column (4.6 mm×250 mm, 5 μm) with a mobile phase consisting of methanol-potassium dihydrogen phosphate buffer (6.7 g potassium dihydrogen phosphate dissolved in water with 3ml of phosphoric acid and 2ml of butyl ammonium hydroxide and diluted to 1 000 ml) (27∶73).The flow rate of of the mobil phase was 1.0 ml/min. The detection wavelength was set at 220nm; and column temperature was 30 ℃;Injection volume was 20ul. Results: Cefotaxime and tazobactam were well-separated with resolution of 7.89. Cefotaxime and tazobactam was also separated from other impurities. The linear range of cefotaxime and tazobactam were 0.516~4.124 μg and 0.083~0.663 μg(r=1) respectively with RSD less than 1.04%; LOQs were 0.11 ng and 0.23 ng, respectively; The average recoveries of cefotaxime and tazobactam were 100.6% (RSD was 0.79%,n=9) and 100.4%( RSD was 0.94%,n=9),respectively. Conclusions: This method was proved to be simple, specific, accurate, and can be used to simultaneous determination of cefotaxime and tazobactam in cefotaxime sodium and tazobactam sodium (6∶1) for injection.
high performance liquid chromatography (HPLC), cefotaxime,tazobactam,content determination
2016-07-19
R927.2
A
1006-5687(2016)05-0023-03

