制药行业药物组分职业接触评估和控制的研究进展
陆业波
摘 要 药物组分的特殊职业健康危害已在部分国家和跨国制药企业得到较深入研究,然而在国内基本还是空白。通过对相关英文文献的检索,从药物组分的职业健康危害、毒理学测试、职业接触限值或职业接触等级的制定、职业接触的控制及其验证等几个方面对该领域的现状进行了综述,并基于国内相关法规标准,就药物组分职业接触评估和控制纳入我国职业卫生管理框架的议题提出了个人的见解。
关键词 药物组分 职业健康危害 毒理学测试 职业接触限值
中图分类号:R135.99 文献标识码:C 文章编号:1006-1533(2017)15-0065-06
Recent progress in research on occupational exposure assessment and control of pharmaceutical ingredients in pharmaceutical industry
LU Yebo*
(Shanghai Xiangyu Environmental Technologies Co., Ltd., Shanghai 200093, China)
ABSTRACT The research of special occupational health hazards of pharmaceutical ingredients has reached a more significant progress in a number of countries and multinational pharmaceutical companies, however, it is basically blank in China. The current status in this area is summarized by English literature retrieval from several aspects such as the occupational health hazard of pharmaceutical ingredients, the toxicological testing, the limit or banding development, and control and verification of occupational exposure. Some personal opinions about the issue how to incorporate the assessment and control of occupational exposure of pharmaceutical ingredients into Chinese framework of occupational health management are proposed based on a review of the relevant domestic regulations and standards.
KEY WORDS pharmaceutical ingredients; occupational health hazard; toxicology testing; occupational exposure limit
制药工业的迅猛发展为全人类生命质量的改善和寿命的延长发挥了至关重要的作用,与此同时,药物对于人群健康的负面效应也受到了关注。然而与审慎的药品开发及严格的审批相比,药物在生产制造过程中对于药厂工人的健康影响直到最近二三十年才得到重视和研究,发达国家和著名跨国公司在此方面是先行者。令人遗憾的是,虽然已有制药过程中工人健康受到影响的事件发生,但中国国内的制药企业以及职业卫生界对于药物组分职业接触评估和控制的研究尚付阙如,相关文献基本处于空白状态。
1 药物组分的职业健康危害
本文中的“药物组分”指的是活性药物成分(API)和药用辅料,不包括药物生产过程中只停留在反应阶段、不能实施分离、不独立出现的中间体[1]。
就API而言,不同于在药品供应链中最终作用的对象(病人),药物生产环境中的人员基本是健康的工人。API对于这些健康工人的作用不但可能是毒理学效应,还可能是药理学效应,且药理学效应无论是副作用还是治疗作用,通常都比毒理学效应发生作用的阈值要低。对于健康的工人而言,API的“治疗作用”所产生的健康影响是主要的方面,需要考虑的因素具体包括:用于严重疾病如癌症治疗、能够抑制免疫系统功能的药物对健康的影响;健康工人的个体易感性;健康工人如果对于某些药物已产生过敏效应,今后将无法接受此药物的治疗;等等[1-2]。
至于药物辅料,相比API,对于职业健康的影响比较轻微;不过,辅料对于活性成分的“稀释作用”需要考虑在检测和控制过程中,活性成分的最大负载量应作为“最坏可信情形”。
2 药物组分的毒理学测试、职业接触限值或职业接触等级的制定
毒理学研究本身是药物临床前安全评估的重要组成部分,其目的是确定该药物是否可以在临床上安全地作用于人体,而整个评估活动也处于药物监管部门的严密监管之下。临床前毒理学研究获得的诸多数据,无论是来自体内試验,还是人体观察,都可以作为职业卫生毒理学家的重要参考信息[3]。
建立毒理学测试项目要求考虑潜在的职业接触、导致不利影响的可能性、待测化学成分的可获取性,以及该药物实现量产的可能性。最后一点对于资源节约尤为重要,因为制药行业的折损率非常之高,仅有极少数的候选新药能最终通过审批。于是便产生了一种与新药开发进程相对应的分层测试方法(图1)[2]。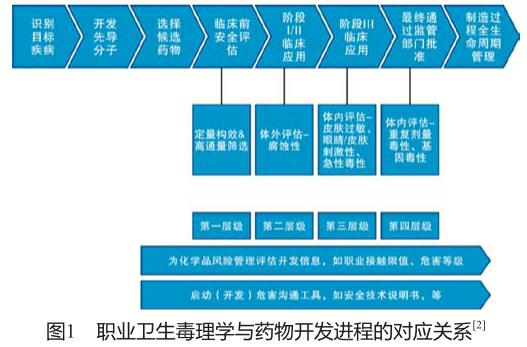
首层测试一般用于化学中间体或补充候选新药的临床前研究,可能包括:对于定量结构—活性关系的计算机研究、物理化学特征界定;自动化高通量细菌致畸性测试;以及预测潜在急性毒性的体外细胞毒性测试。由于这些测试能够快速进行,因此它们能够在研发类中试的早期生产前完成。
第二层级的测试,一般利用初始中试获取的物料,可能包括体外实验以评估潜在的皮肤腐蚀性和眼睛刺激性。仅在候选药物被确认有极大的机会进入市场并且当制造规模实现增长时方可启动第三层级的测试。
第三层级测试基于电脑模拟测试和体外测试的结果,可能包括使用体内哺乳动物细胞对于基因毒性的进一步测试,使用淋巴结测试皮肤过敏性,使用兔模型测试皮肤和眼睛刺激性,以及对于急性毒性的评估。
基于第三层级的测试结果以及对最终制造过程可能接触的了解,可能决定进一步的测试,比如体内基因毒性测试及通过重复剂量研究建立靶器官等。
从职业接触毒理学测试获取的数据将可用于制定相应的职业接触限值或职业接触等级(后者对应相应的危害等级),目前一般是较大的制药公司在其内部从事该实践[4-7],而相关的法定限值则十分罕见。
对于职业接触限值的传统确定方法一般是基于以下公式[6]: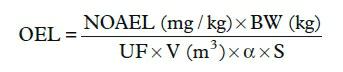
在公式中,NOAEL=未观察到有害作用的水平,BW=平均体重(男性:70 kg;女性:50 kg),UF=不确定性系数,V=一个工作日内呼入的空气(10 m3/d),a=药物组分被吸收的比例,S=达到血浆稳态所需时间(d)。
当然,上述公式中的OEL实际是指TWA,对于部分药物组分而言,还可能涉及到STEL或 Ceiling的制定。
然而,由于制药业的趋势是开发活性越来越高的组分,而对于部分组分而言,无从确认NOAEL水平;此外在药物开发的早期,常缺少制定职业接触限值所需的毒理学和药理学数据;于是,一种“基于效果的接触控制限值”(PB-ECL) [5]或“分级控制”(control banding) [8]方法应运而生。这种方法是一种定性或半定量的方法,根据已获取的毒理学或药理学数据将相应药物组分纳入四个或五个职业控制等级中的其中一个(表1)。与这些等级相对应的是不同保护等级的工程控制措施及相应操作要求(详见本文第3节)。
对应上述药物开发进程及毒理学测试层级,在药物被批准开发之后(这通常对应药物的实验室研发阶段),将会被赋予一个初始的PB-ECL,由于缺少更多的数据,对于不少无从确认PB-ECL等级的药物成分而言,通常将其归为第三级[5]。
在毒理学数据已可搜集的阶段(这通常是在完成90 d的毒理学测试后),该药物组分将会被赋予一个比较精确的PB-ECL等级,甚至是定量的职业接触限值(对于无从确认NOAEL的药物而言,将只能赋予其PB-ECL值)。等到新药通过审批时,一般可最终确认PB-ECL等级或定量的职业接触限值。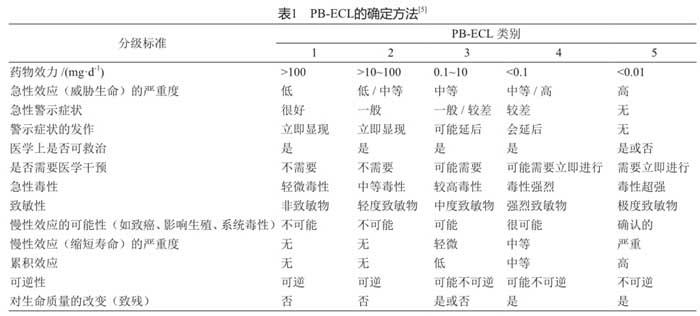
此外,在接触限值要求越来越严格的同时,相比较呼吸接触的控制,对于皮肤接触的控制凸显为重要议题。为了定量评估潜在的皮肤接触造成的风险,“可接受的表面限值(ASL)”概念应时而生[9]。ASL与恰当的分析方法和工业卫生检测方法相结合,将可评估潜在风险并为可能通过皮肤接触到污染表面的人员提供健康和安全保护[10]。
3 药物组分职业接触的控制及其验证
对应于不同等级的PB-ECL,相关专业机构将针对制药工艺(实验室或量产)的密闭措施(containment)也定义为不同的等级(表2)。除了密闭措施外,针对全面通风、局部通风、表面接触、维护、清洁清洗、废弃物处置、污染物去除、个人防护及职业健康监护也有不同等级的要求[11-12]。
然而,这种直接将职业接触等级与控制措施挂钩的方法忽略了职业接触本身的可能性。考虑了这种可能性的“改良版”为英国化学工程师协会(IChemE)的“金字塔”模型(图2),该模型将工艺过程/操作涉及到的物料量级、物料的粉尘分散度(液体的挥发性)以及工艺/操作时长等因素同时列入考虑。
在实际应用该模型以及诸多类似模型的过程中[14-15],制药行业继而发现[16]:①该模型给出的控制方案往往过于保守,在成本上过于高昂,难以实现;②可用的密闭系统类型显然多于资料给出的参考案例,且很多密闭技术还可以组合使用;③就在各种“模型”和“指南”处于撰写或出版阶段的同时,很多新型的或改进型的密闭技术又已经问世了;④具体设备的密闭效果往往依赖具体的工艺条件和不同的制造商。
因此,在工程控制实践方面,除了参考理论模型之外,相关业主、设计人员、设备供应商与咨询机构的经验与背景通常占主导地位。
行业内目前广泛采用的密闭系统(设备)可笼统归纳为这样几个大类,即气流管控型系统、洁净式断开接头、密封式衬垫系统、隔离器和隔离式传送系统等[16-17],对于部分应用较成熟的设备来说,有关其隔离效果的数据范围信息已可获得(图3)。
由于目前所能掌握的各种密闭技术的理论密闭效果也只是区间数据,了解密闭设备所能达到的实际密闭效果对于设备选型及运行监控十分关键。
目前密闭设备效果测試领域的权威标准是国际制药工程协会(ISPE)的Good Practice Guide: Assessing the Particulate Containment Performance of Pharmaceutical Equipment[18]。该导则旨在为制药设备密闭效果的评估提供基本准则与标准化方法,而测试方法则涉及在设备中引入替代物料(粉料)并对该物料经气流造成的逸散和表面污染进行采样和分析。导则可应用于新设备投用前及设备投用运行后的测试和评估,也可用于评估和比较来自不同供应商的类似或不同设备。
4 將药物组分职业接触评估与控制纳入我国的职业卫生管理框架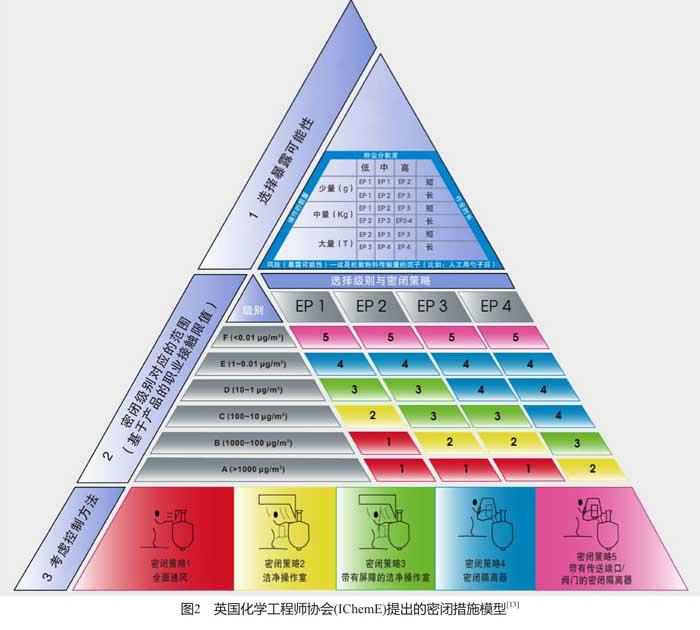
根据相关机构预测,2020年我国有望成为世界排名第二的医药生产大国[19]。提升药物生产过程中的职业卫生管控水平理应成为这一进程中的议题之一。参考药物组分职业接触评估与控制的国际先进实践,基于国内的职业卫生管理现状,作者认为,可从以下三个方面着手:①参考国际劳工组织《职业病目录》(2010年修订)[20],在未来修订国家《职业病分类和目录》[21]时,将职业病病种“药物因素所致的疾病”列入;相应地,在《职业病危害因素分类目录》[22]中,将API或药物粉尘增列于其中。②激活现行《职业病防治法》[23]第二十九条第二款(国内首次使用或者首次进口与职业病危害有关的化学材料,使用单位或者进口单位按照国家规定经国务院有关部门批准后,应当向国务院卫生行政部门、安全生产监督管理部门报送该化学材料的毒性鉴定以及经有关部门登记注册或者批准进口的文件等资料)并予以必要的修订,将包括API在内的新化学材料的毒性鉴定资料用于职业病危害评价,鼓励相关企业(用人单位)开展补充性质的毒理学研究、制定企业内部的职业接触限值/职业接触等级并开发相应的实验室分析方法。③修订AQ/T4255-2015《制药企业职业危害防护规范》[24],或制定其它行业标准(争取制药行业或制药企业的参与),将“基于效果的接触控制限值”(PB-ECL)、相应的控制模型及行业内成熟的密闭措施经验纳入其中。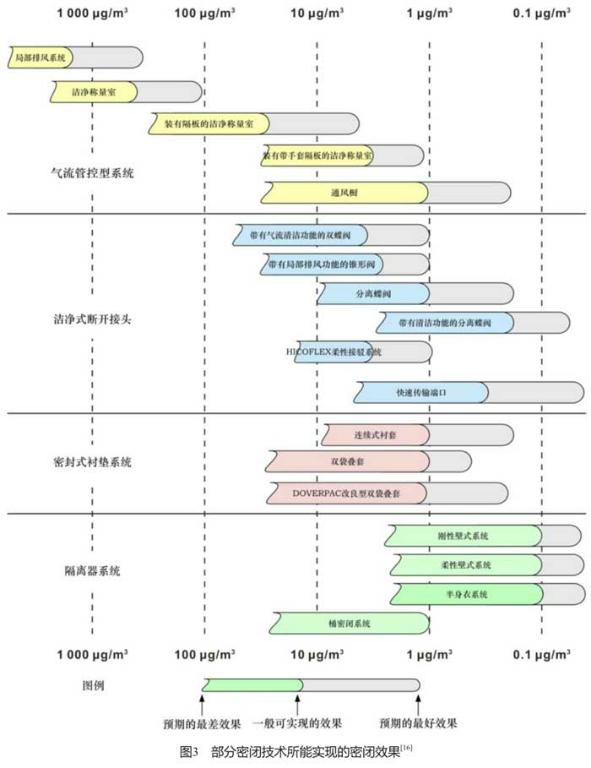
参考文献
[1] Heron RJ, Pickering FC. Health effects of exposure to active pharmaceutical ingredients (APIs) [J]. Occup Med (Lond), 2003, 53(6): 357-362.
[2] Binks SP. Occupational toxicology and the control of exposure to pharmaceutical agents at work[J]. Occup Med(Lond), 2003, 53(6): 363-370.
[3] International Programme on Chemical Safety (2005). Chemical specific adjustment factors for interspecies differences and human variability. Guidance for use of data in dose/concentration - response assessment. World Health Organization, 2005[EB/OL]. [2017-03-07]. http: //www. inchem. org/documents/harmproj/harmproj/harmproj2. pdf.
[4] Association of the British Pharmaceutical Industry (ABPI). Guidance on Setting In-house Occupational Exposure Limits for Therapeutic Substances and their Intermediates[EB/OL].[2017-03-07]. http://www.abpi.org.uk/our-work/library/ guidelines/Documents/Occupational-Exposure-Limits.pdf.
[5] Naumann BD, Sargent EV, Starkman BS, et al. Performancebased exposure control limits for pharmaceutically active ingredients[J]. Am Ind Hyg Assoc J, 1996, 57(1): 33-42.
[6] Sargent EV, Kirk GD. Establishing airborne exposure control limits in the pharmaceutical industry[J]. Am. Ind. Hyg Assoc J, 1998, 49(6): 309-313.
[7] Ku RH. An overview of setting occupational exposure limits(OELs) for pharmaceuticals[J]. Chem Health Saf, 2000, 7(1): 34-37.
[8] Zalk DM, Nelson D. History and evolution of control banding: a review[J]. J Occup Environ Hyg, 2008, 5(5): 330-346.
[9] Kimmel TA, Sussman RG, Ku RH, et al. Developing acceptable surface limits for occupational exposure to pharmaceutical substances[J]. J Astm Internat, 2011, 8(8): 1-6.
[10] National Center for Environmental Assessment, Office of Research and Development. Dermal Exposure Assessment: A Summary of EPA Approaches[M]. Washington, DC: U. S. Environmental Protection Agency, 2007: 7-23.
[11] Ader AW, Farris JP, Ku RH. Occupational health categorization and compound handling practice systems—roots, application and future[J]. Chem Health Saf, 2005, 12(4): 20-26.
[12] Farris JP, Ader AW, Ku RH. History, implementation, and evolution of the pharmaceutical hazard categorization and control system[J]. Chem Today, 2006, 24(2): 5-10.
[13] Hirst N, Brocklebank M, Ryder M. Containment systems: a design guide[M]. Rugby: Institution of Chemical Engineers(IChemE), 2002: 61-76.
[14] Wood JP. Containment in the pharmaceutical industry[M]. New York: Marcel Dekker, 2001: 211-222.
[15] Walker L. Process containment design for development facility—Part 1[J]. Pharm Eng, 2002, 22(4): 72-76.
[16] Gurney-Read P. Containment systems Part 2: Selection, specification and procurement[J]. Clean Air Contain Rev, 2010, 2: 8-12.
[17] Axon MW, Farris JP, Mason J. Handling highly potent active pharmaceutical ingredients-equipment containment performance[J]. Chem Today, 2008, 26(2): 57-60.
[18] ISPE Good practice guide: assessing the particulate containment performance of pharmaceutical equipment, 2nd Edition[M]. Tampa: ISPE, 2012: 1-37.
[19] 曾铮. 中国医药产业发展概况及其趋势研究[J]. 经济研究参考, 2014(32): 4-38.
[20] 国际劳工大会. 关于职业病目录及职业事故和职业病的登记与报告建议书:第194号建议书[EB/OL]. (2002-06-20)[2017-03-07]. http: //www.ilo.org/wcmsp5/groups/public/---ed_norm/---normes/documents/normativeinstrument/wcms_ r194_zh. pdf.
[21] 中华人民共和国国家卫生和计划生育委员会. 关于印发《职业病分類和目录》的通知[EB/OL]. (2013-12-23)[2017-03-07]. http: //www. gov. cn/gzdt/2013-12/30/ content_2557352. htm.
[22] 中华人民共和国国家卫生和计划生育委员会. 关于印发《职业病危害因素分类目录》的通知[EB/OL]. (2015-11-17)[2017-03-07]. http: //www. nhfpc. gov. cn/jkj/s5898b/201511/ 4b286806231a42058d0111aa64053aac. shtml.
[23] 中华人民共和国全国人大常委会. 关于修改《中华人民共和国节约能源法》等六部法律的决定[EB/OL]. (2016-07-02)[2017-03-07]. http: //www. chinasafety. gov. cn/newpage/Contents/ Channel_4111/2016/1130/279089/content_279089. htm.
[24] 国家安全生产监督管理总局. 制药企业职业危害防护规范:AQ/T4255-2015[S]. (2015-03-19)[2017-03-07]. http: // www. chinasafety. gov. cn/newpage/newfiles/AQ4255. pdf.

