焦磷酸测序检测CYP2C19基因多态性方法的建立
杨楠楠+徐琴+罗振元+付雪++黄盛文


[摘要] 目的 建立一种基于焦磷酸测序技术的用于CYP2C19基因多态性快速检测的方法。 方法 选择2016年12月~2017年3月于贵州省人民医院行健康体检者50名,提取其基因组DNA,针对CYP2C19*2(681G>A)、CYP2C19*3(636G>A)、CYP2C19*17(-806C>T)3个单核苷酸多态性(SNP)位点分别设计一套PCR扩增引物和焦磷酸测序引物。将PCR扩增产物制备成单链测序模板,用Qiagen PyroMark Q24焦磷酸测序仪进行测序和基因型分析,采用Sanger一代测序技术对焦磷酸测序结果进行验证。 结果 根据出峰的碱基和峰高可清楚判断出3个SNP位点的不同基因型,检测结果与Sanger测序结果完全一致。50名健康体检者中检出CYP2C19超快代谢型1例,快代谢型22例,中代谢性22例,慢代谢型5例。 结论 本研究建立的焦磷酸测序检测CYP2C19基因多态性的方法具有快速、准确、成本低的特点,适用于临床实验室对CYP2C19基因多态性的分型。
[关键词] CYP2C19;基因多态性;焦磷酸测序;氯吡格雷
[中图分类号] R446.9 [文献标识码] A [文章编号] 1673-7210(2017)10(b)-0011-04
Establishment of genotyping methods for polymorphisms of CYP2C19 gene based on pyrosequencing technology
YANG Nannan1 XU Qin1 LUO Zhenyuan2 FU Xue2 HUANG Shengwen2▲
1.School of Clinical Laboratory Science, Guizhou Medical University, Guizhou Province, Guiyang 550004, China; 2.Department of Clinical Laboratory, Guizhou Provincial People′s Hospital, Guizhou Province, Guiyang 550002, China
[Abstract] Objective To establish a fast detection method for CYP2C19 genotyping based on pyrosequencing technology. Methods Genomic DNA was extracted from 50 blood samples of healthy subjects collected from December 2016 to March 2017 in Guizhou Provincial People′s Hospital, and a set of amplification primers and pyrophosphate sequencing primers were designed according to the single nucleotide polymorphism (SNP) sites of CYP2C19*2 (681G>A), CYP2C19*3 (636G>A), CYP2C19*17 (-806C>T). Single-stranded templates were made from PCR products, then sequencing and genotyping analysis were performed on a Qiagen PyroMark Q24 Sequencer System. The sequencing results were verified via Sanger sequencing. Results Based on the type and peak height of bases of DNA sequence, the genotypes of three SNPs could be identified clearly, which were consistent with Sanger sequencing results. Among the 50 samples of healthy group, 1 case was ultra-rapidmetabolism, 22 cases were rapidmetabolism, 22 cases were medium metabolism and 5 cases were slow metabolism. Conclusion The detection method of CYP2C19 polymorphism based on pyrosequencing technology is quick, accurate and convenient, which can be used to analyze the genotyping of CYP2C19 gene polymorphism.
[Key words] CYP2C19; Gene polymorphism; Pyrosequencing; Clopidogrel
氯吡格雷是臨床上常用的抗血小板聚集的药物之一,冠状动脉介入术(percutaneous coronary intervention,PCI)后患者需长期服用氯吡格雷来进行抗血小板治疗[1-2],但临床上部分患者会出现氯吡格雷抵抗[3]。氯吡格雷的主要代谢酶为细胞色素P4502C19[4-6],其编码基因CYP2C19的多态性是影响氯吡格雷疗效的主要遗传因素[7-8]。CYP2C19的等位基因以CYP2C19*1(野生型)、CYP2C19*2、CYP2C19*3和CYP2C19*17较常见[9]。超快代谢型的基因型为*1/*17、*17*17,快代谢型的基因型为*1/*1,中代谢型的基因型为*1/*2、*1/*3,慢代谢型的基因型为*2/*2、*3/*3和*2/*3[10-11]。本研究采用焦磷酸测序技术建立了一种CYP2C19基因多态性检测方法,并用Sanger测序法对其准确性进行验证。endprint
1 对象与方法
1.1 对象
选择2016年12月~2017年3月贵州省人民医院健康体检成人50名,其中男21名,女29名,平均年龄为(35.7±9.7)岁。
1.2 主要仪器与试剂
NP968核酸自动提取仪(西安天隆科技有限公司);美国ABI Veriti96 PCR仪(美国ABI生物系统公司);Qiagen PyroMark Q24焦磷酸测序仪(德国凯杰公司);PCR擴增引物和焦磷酸测序引物(上海生工生物有限公司)。
1.3 方法
1.3.1 基因组DNA的提取 根据天隆NP968核酸自动提取仪的说明书进行全血DNA提取,对DNA样本进行浓度和纯度检测,置于-20℃保存备用。
1.3.2 CYP2C19多态性位点的引物设计 在NCBI上分别下载CYP2C19*2(681G>A)、CYP2C19*3(636G>A)和CYP2C19*17(-806C>T)3个单核苷酸多态性(single nucleotide polymorphism,SNP)位点上下游各1 kb范围的基因序列,采用PyroMark Assay Design Software 2.0(德国凯杰公司)软件设计PCR引物和焦磷酸测序引物。见表1。
1.3.3 PCR扩增 25 μL PCR反应体系包括:PyroMark PCR Master Mix 12.5 μL,CoraLoad Concentrate 2.5 μL,Q-Solution 5 μL,25 mmol/L MgCl2 1.5 μL,上下游PCR引物各0.5 μL,DNA 1 μL,RNase-free water 1.5 μL。PCR反应条件:95℃预变性15 min,94℃变性30 s,CYP2C19*2 50℃、CYP2C19*3 53℃、CYP2C19*17 49℃退火30 s,72°C延伸30 s,共45个循环,最后72℃延伸10 min。PCR产物经过2%的琼脂糖凝胶电泳检测是否为所需的目的片段。
1.3.4 制备预混液以固定PCR产物 80 μL反应体系包括Beads 2 μL,Binding buffer 40 μL,PCR产物10 μL,高纯水28 μL。
1.3.5 单链的分离 将0.3 μmol/L测序引物分配到q24反应板的每个孔中。打开开关,将真空工具放到PCR管的孔中,持续15 s,以捕获带有PCR产物的sepharose珠。依次用70%乙醇、变性溶液、洗涤液冲洗真空工具10 s,关闭真空开关。将真空工具放到孔中,左右轻柔晃动,以释放含有磁珠的产物。
1.3.6 测序引物与DNA链退火 将q24反应板置于80℃加热块上加热样本2 min,样本冷却至室温(15~25℃)后即可放入焦磷酸测序仪内测序。
1.3.7 基因型分析 通过Qiagen PyroMark Q24(德国凯杰公司)软件对结果进行分析,根据出峰的碱基和峰高分别判断各位点的基因型。
1.3.8 Sanger测序验证 将3个SNP位点的PCR产物送上海生工生物有限公司采用Sanger测序法进行检测,并与焦磷酸测序结果进行比对。
2 结果
2.1 PCR结果
电泳结果显示,3个SNP位点的PCR产物均在相应位置呈单一条带。见图1。
2.2 3个SNP位点的基因型检测结果
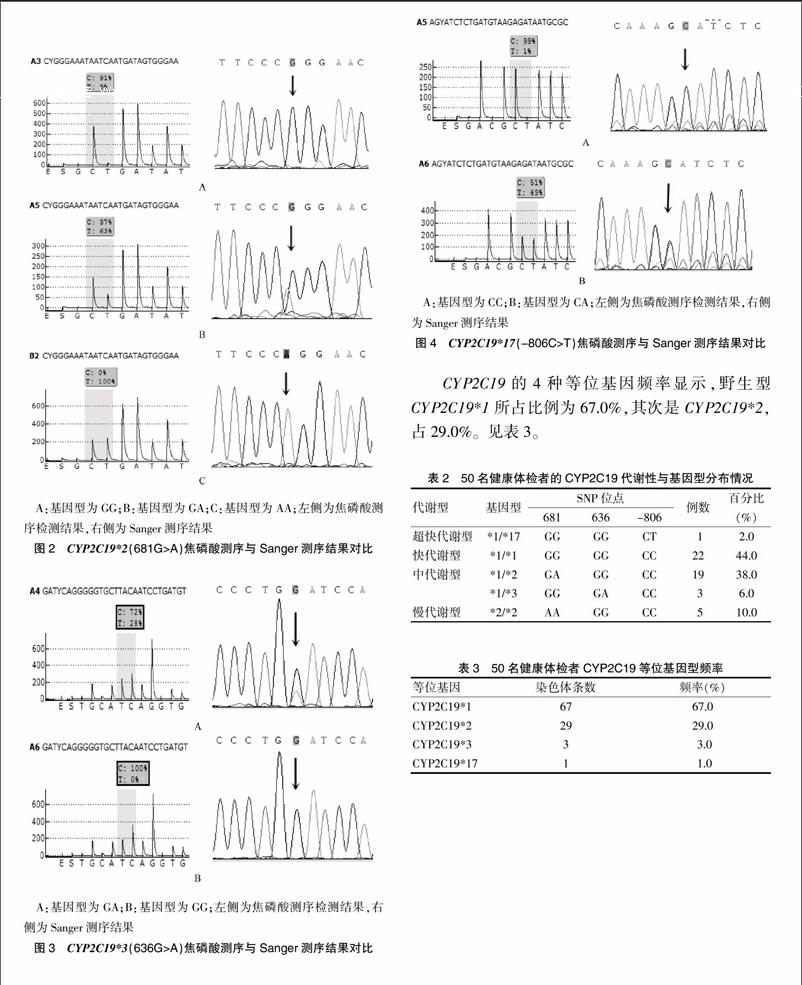
3个SNP位点均可通过出峰的碱基和峰高清楚判断出不同的基因型,信噪比较高,非特异峰的比例均在10%以内。50个样本中3个位点的基因型与Sanger测序结果完全一致。见图2~4(左侧为焦磷酸测序检测结果,右侧为Sanger测序结果)。
2.3 50名样本CYP2C19基因型检测结果
根据3个SNP位点的检测结果,可以得出每个样本的CYP2C19基因型,并判断出其代谢类型。50名健康体检者中检出超快代谢型1例,快代谢型22例,中代谢性22例,慢代谢型5例。见表2。
CYP2C19的4种等位基因频率显示,野生型CYP2C19*1所占比例为67.0%,其次是CYP2C19*2,占29.0%。见表3。
3 讨论
检测CYP2C19多态性的方法除了金标准Sanger测序技术外,常用的还有限制性片段长度多态分析、飞行时间质谱[12]、DNA微阵列芯片、高分辨率熔解曲线分析、Taqman探针等技术[13]。这些技术均具有较高的准确性,但操作步骤较为繁琐,或是需要依赖昂贵的仪器,检测成本较高,不适合规模的推广应用。为适应临床对CYP2C19基因多态性检测的需要,有必要建立一种高效、快速、准确度高、灵敏度好、经济适用的检测方法。
焦磷酸测序是一种基于DNA序列分析的技术,是检测SNP最为准确的方法之一[14]。焦磷酸测序适用于对已知短序列的测序分析,其敏感性和精确性能与金标准(Sanger测序法)相提并论,并能够实时、直观、准确、定量提供待测序列的信息[15-17],已广泛用于基因多态性检测、微生物分型、基因甲基化检测等领域[18]。
本研究建立的焦磷酸测序检测方法可对CYP2 C19基因进行快速、准确的分型,可在20 min内对24个标本进行平行检测,检测结果与Sanger测序结果完全一致,并且检测成本低于Sanger测序法。另外,由于人群中等位基因CYP2C19*17的频率较低,其他方法较少对其进行检测,本研究建立的检测方法包含了对CYP2C19*17的检测,可更为全面地指导氯吡格雷的个体化用药。
本研究共检测到的5种CYP2C19基因型,其中超快代谢型(*1/*17)占2%,快代谢型(*1/*1)占44%,中间代谢型(*1/*2、*1/*3)占44%,慢代谢型(*2/*2)占10%。等位基因CYP2C19*1、CYP2C19*2、CYP2C19* 3、CYP2C19*17的频率分别为67%、29%、3%和1%,与国内其他地区人群的研究结果基本一致[19-21]。endprint
[参考文献]
[1] 马辉,胡增春,吕慧怡,等.CYP2C19基因多态性检测在PCI术后氯吡格雷用药中的研究[J].医学与哲学,2016, 37(8):29-31.
[2] Saydam F,De■irmenci ■,Birdane A,et al. The CYP2C19*2 and CYP2C19*17 Polymorphisms play a Vital Role in Clopidogrel Responsiveness after Percutaneous Coronary Intervention:A Pharmacogenomics Study [J]. Basic Clin Pharmacol Toxicol,2017,37(8):e48.
[3] Bonvini RF,Reny JL,Mach F,et al. Acute coronary syndrome and its antithrombotic treatment:focus on aspirin and clopidogrel resistance [J]. Curr Vasc Pharmacol,2009, 7(2):198.
[4] Christiaens L,Macchi L. Monitoring of the antiplatelet drugs effect in patients with coronary artery disease:what is the real clinical impact?[J]. Curr Vasc Pharmacol,2007, 5(4):293-301.
[5] Lau PS,Leong KV,Ong CE,et al. In Vitro Functional Characterisation of Cytochrome P450(CYP)2C19 Allelic Var?鄄iants CYP2C19*23 and CYP2C19*24 [J]. Biochem Genet,2016,18:1-15.
[6] Collet JP,Hulot JS,Pena A,et al. Cytochrome P450 2C19 polymorphism in young patients treated with clopidogrel after myocardial infarction:a cohort study [J]. Lancet,2008, 373(9660):309-317.
[7] 付良青,黄丰,吴德政,等.中国汉族人群不同性别细胞色素氧化酶CYP2C19基因多态性的比较[J].药学学报,2004,39(3):161-163.
[8] 翟万庆,杨丽娟,宋丽艳,等.缺血性卒中氯吡格雷治疗后病情进展与CYP2C19基因多态性的关系[J].山东医药,2016,56(33):83-85.
[9] Sim SC,Risinger C,Dahl ML,et al. A common novel CYP 2C19 gene variant causes ultrarapid drug metabolism relevant for the drug response to proton pump inhibitors and antidepressants [J]. Clin Pharmacol Ther,2006,79(1):103.
[10] Zou JJ,Xie HG,Chen SL,et al. Influence of CYP2C19 loss-of-function variants on the antiplatelet effects and cardiovascular events in clopidogrel-treated Chinese patients undergoing percutaneous coronary intervention [J]. Eur J Clin Pharmacol,2013,69(4):771.
[11] Sibbing D,Stegherr J,Latz W,et al. Cytochrome P450 2C19 loss-of-function polymorphism and stent thrombosis following percutaneous coronary intervention [J]. Eur Heart J,2009,30(8):916.
[12] 彭文星.急性冠脉综合征患者氯吡格雷抵抗与基因多态性关联性分析[D].北京:首都医科大学,2016.
[13] 贾政军,王华,彭向京,等.焦磷酸测序技术检测LAMA5 rs944895基因多态性方法的建立[J].中国临床药理学与治疗学,2011,16(6):647-651.
[14] 李思勤,邹秉杰,王建平,等.焦磷酸测序测定SNP的常见问题与解决方法[J].现代生物医学进展,2014,14(12):2219-2223.
[15] 万子睿,谢海棠,郭栋,等.焦磷酸测序技术检测SLCO 1B1基因多态性方法的建立[J].中国临床药理学与治疗学,2012,17(5):543-548.
[16] 王谦,杜亚梅,张国军,等.焦磷酸测序法与Sanger测序法检测CYP2C19*17基因多态性方法学对比研究[J].中国医药生物技术,2014,9(3):222-224.
[17] 王谦,杜亚梅,张国军,等.焦磷酸测序法和基因芯片法检测CYP2C19基因多态性的方法学比较[J].中华检验医学杂志,2014,37(8):628-630.
[18] 项铮,刘云龙,邢晓清,等.全血改进线性指数聚合酶链式反应用于焦磷酸测序检测基因多态性[J].分析化学,2015,43(1):55-62.
[19] 吕园,俞杨,张秀梅,等.南京及周边地区冠心病患者CYP2C19基因多态性分析[J].标记免疫分析与临床,2016, 23(10):1139-1143.
[20] 國荣,刘淼,王宇玫,等.北京地区汉族冠心病患者CYP2 C19基因多态性分析[J].医学研究杂志,2015,44(11):101-105.
[21] 王娟,苏明权,杨柳,等.西北地区530例临床患者CYP2 C19遗传多态性分析[J].中华临床医师杂志:电子版,2012,6(22):7395-7397.
(收稿日期:2017-07-02 本文编辑:程 铭)endprint

