功能化锌金属有机骨架对刚果红染料的吸附
张 华 ,李祥鹏 ,张 雯 ,高 燕 ,岳 盼 ,李 伟
(1.天津工业大学材料科学与工程学院,天津 300387;2.天津工业大学省部共建分离膜与膜过程国家重点实验室,天津 300387)
随着科技水平的不断提高,各种染料不断被研发出来,纺织业、食品加工、印刷等行业对染料的需求量日益增大[1-2].然而,印染工业产生的废水有毒且不能被生物降解,对环境和人类的生活健康造成了巨大威胁[3],因此寻找有效的解决方法显得尤为重要.吸附法是印染废水处理技术中的有效方法之一.目前的吸附材料主要有活性炭[4-5]、磁粉[6-7]、粘土[8-9]、粉煤灰[10-11]、珍珠岩[12-13]、碳纳米管[14-15]和聚合物微球[16]等.
金属有机骨架(MOFs)是金属离子与有机配体通过特定的方式形成的杂化新型多孔材料.MOFs具有超高的比表面积、理想的孔隙率、结构可调、制备简单、可化学改性等优点,在选择性吸附领域中展现出广阔的应用前景[17].
1999年,Yaghi等报道了一种新型材料——MOF-5,其是指以Zn2+和对苯二甲酸(H2BDC)分别为中心金属离子和有机配体,通过八面体形式连接而成的具有微孔结构的三维立体骨架[18].目前对MOF-5的研究主要集中在气体吸附领域,而对于液相吸附的报道较少.MOF-5的吸附作用主要是物理吸附,这限制了其作为吸附材料的发展,因此对其化学改性十分必要.乙二胺本身是一种良好的染料溶剂,将乙二胺分子中的氨基基团引入到MOF-5中,使EDA/MOF-5既具有物理吸附,又具备化学吸附的性能.
本研究以制备的MOF-5和EDA/MOF-5作为吸附材料[19],阴离子染料刚果红作为吸附质,探究了刚果红初始质量浓度、温度、pH以及离子强度等对吸附性能的影响,并进一步探究其吸附等温线和吸附动力学,为离子型染料废水的处理提供理论依据.
1 实验部分
1.1 实验材料
对苯二甲酸、刚果红,分析纯,天津市光复精细化工研究所产品;六水合硝酸锌、N,N-二甲基甲酰胺、三氯甲烷、乙二胺、盐酸、无水乙醇,分析纯,天津市光复科技发展有限公司产品;氢氧化钠、氯化钠,分析纯,天津市风船化学试剂科技有限公司产品.
1.2 实验仪器
TU-1901型紫外可见分光光度计,北京普析通用仪器有限公司产品;PHS-25型雷磁pH计,上海仪电科学仪器股份有限公司产品;TD5Z型台式低速离心机,湖南凯达科学仪器有限公司产品;SHA-C型水浴振荡器、DZF-6020型真空干燥箱,巩义市予华仪器有限公司产品;KQ3200DB型超声波清洗器,昆山市超声仪器有限公司产品;101-1AB型电热鼓风干燥箱,天津市泰斯特仪器有限公司产品;JY6002型电子天平,上海衡平仪器仪表厂产品;聚四氟乙烯内衬反应釜,济南祝安信息技术有限公司产品.
1.3 吸附实验
1.3.1 初始浓度调整
将0.02 g MOF-5和0.02 g EDA/MOF-5分别加入到质量浓度为 20 mg/L、40 mg/L、60 mg/L、80 mg/L、100 mg/L的刚果红溶液中,将溶液pH值调为7.0±0.2,置于25℃、震荡速率为120 r/min的水浴振荡器中进行吸附实验,吸附一定时间后,离心分离,取上清液在其最大吸收波长(λ=497 nm)处测量其吸光度,计算刚果红的浓度.
1.3.2 温度调整
分别在18℃、25℃、37℃、45℃、52℃,震荡基率为90 r/min的水浴振荡器中进行振荡吸附,刚果红溶液质量浓度为80 mg/L,固定其他条件不变,按照实验方法,考察温度对吸附的影响.
1.3.3 pH值调整
调节刚果红溶液pH值为4~10,置于25℃,震荡速率为120 r/min的水浴振荡器中进行吸附实验,刚果红溶液质量浓度为80 mg/L,其他条件不变,考察pH对吸附的影响.
1.3.4 离子强度调整
将0.02 g MOF-5和0.02 g EDA/MOF-5分别加入到一系列含有不同质量浓度NaCl(0.001、0.010、0.100 mol/L)的刚果红溶液中,刚果红溶液质量浓度为80 mg/L,其他条件不变,考察离子强度对吸附的影响.
1.3.5 吸附动力学实验
将0.02 g MOF-5和0.02 g EDA/MOF-5加入盛有20 mL质量浓度为80 mg/L的刚果红溶液中,将溶液pH值调为7.0±0.2,置于25℃、震荡速率为90 r/min的水浴振荡器中进行吸附实验,定时取样,离心分离,取上清液在其最大吸收波长(λ=497 nm)处测量其吸光度,计算刚果红的浓度.
1.3.6 染料脱色与吸附测定
根据刚果红染料的标准曲线方程,计算吸附后的染料浓度.由式(1)和式(2)求出脱色率D和吸附量q.
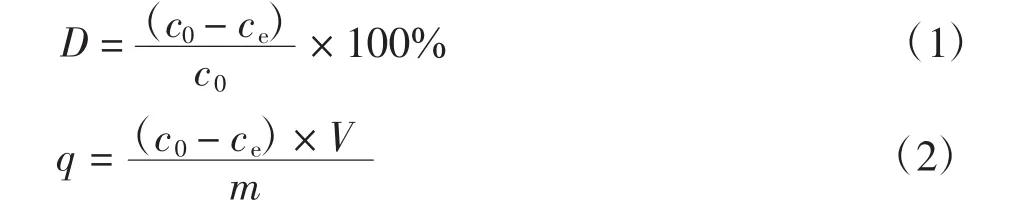
式中:c0为染料初始质量浓度(mg/L);ce为吸附后染料质量浓度(mg/L);V 为吸附染料的体积(L);m 为吸附剂的质量(g).
2 结果与讨论
2.1 初始浓度对吸附的影响
图1和图2分别为吸附量和脱色率随刚果红浓度的变化图.
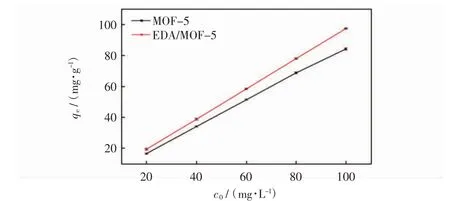
图1 吸附量随刚果红浓度的变化Fig.1 Adsorption capacity varies with concentration of Congo red
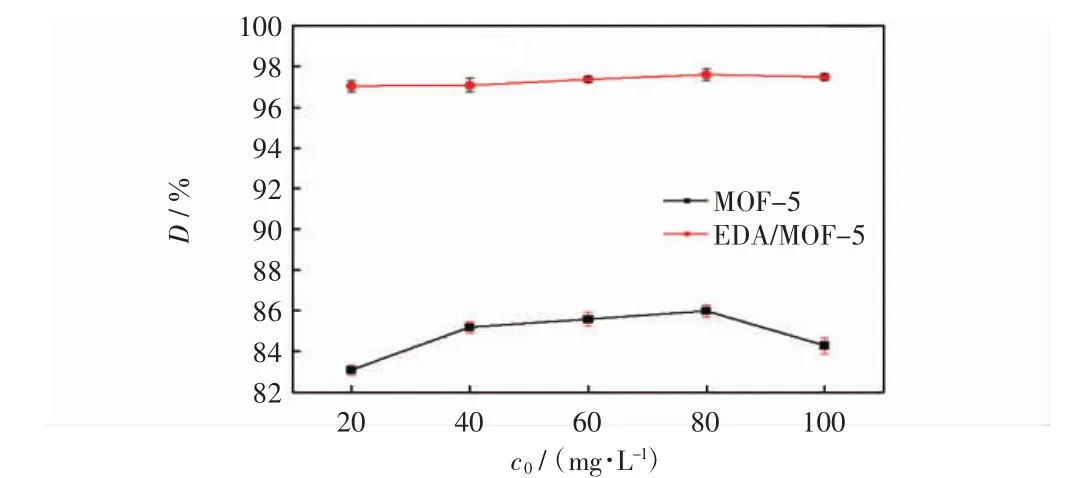
图2 脱色率随刚果红浓度的变化Fig.2 Decolorization rate varies with concentration of Congo red
由图1可见,吸附剂对刚果红的吸附量随着染料浓度的增大而增大,EDA/MOF-5对刚果红的吸附量明显提升.当刚果红质量浓度为100 mg/L时,EDA/MOF-5对刚果红的吸附量为97.49 mg/g.由图2可见,在80 mg/L时,EDA/MOF-5对刚果红的脱色率达到98%.这是由于染料溶液浓度的增大,吸附剂表面和染料溶液之间的浓度差增大,扩散时的动力增大,使更多的染料分子占据吸附剂表面的活性位点,从而增大吸附量[20].由于EDA/MOF-5引入了氨基,而刚果红染料分子中含有磺酸根等阴离子,因此氨基等活性基团可以与染料分子的磺酸根产生静电吸引,通过物理和化学吸附过程,将染料从水溶液中吸附出来,使其对刚果红的脱色率更大.
2.2 温度对吸附的影响
图3为温度对吸附性能的影响.由图3可见,在18~52℃范围内,随温度的升高,吸附材料对染料的吸附量随之增大,在52℃、80 mg/L时,EDA/MOF-5对刚果红的吸附量为78.36 mg/g.MOF-5对刚果红溶液的吸附对于温度更敏感,这主要是因为MOF-5对于刚果红主要是物理吸附,温度影响刚果红溶液分子的运动活性,使染料分子进入到吸附剂空腔的机率降低;而EDA/MOF-5由于化学吸附的作用,使其对温度的敏感度降低,能更好地吸附刚果红溶液.吸附剂与吸附质之间的相互作用与化学键有关,需要克服活化能,因此温度升高对吸附是有利的.另外,在一定范围内,温度升高,溶液的粘度减小,分子运动活跃,分子更容易与吸附剂发生碰撞,进而有利于吸附,使吸附量逐渐增大[21].
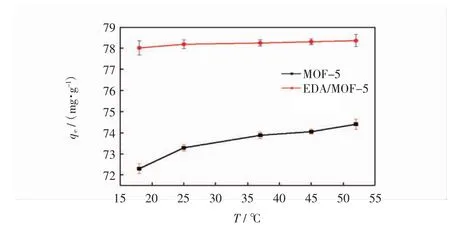
图3 温度对吸附性能的影响Fig.3 Effect of temperature on adsorption performance
2.3 pH值对吸附的影响
pH值是吸附试验重要的探究条件,对材料的吸附性能有很大影响.pH值不仅影响染料分子自身的电离,而且对金属有机骨架的电离也会产生一定影响.图4为pH值对吸附性能的影响.
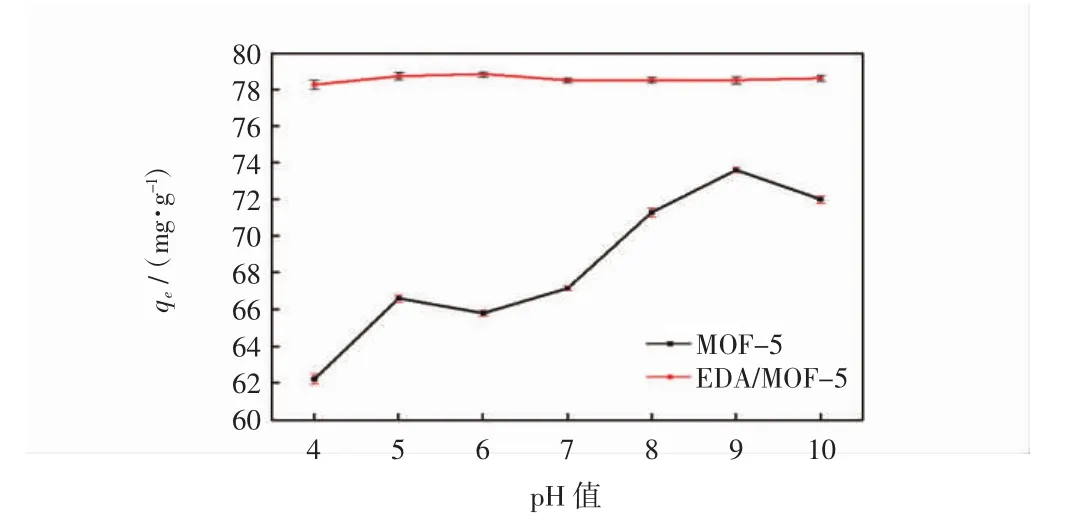
图4 pH值对吸附性能的影响Fig.4 The effect of pH on adsorption performance
由图4可见,较之酸性条件,MOF-5在碱性条件下对刚果红的吸附性能更优,而EDA/MOF-5受pH值的影响较小.随着pH值的增大,MOF-5对刚果红的平衡吸附量先增加后减小,在pH=9时达到最大.刚果红的结构会随着pH值的变化而改变,pH<5.2,刚果红的氨基得到H+而被质子化,刚果红染料表面带正电.
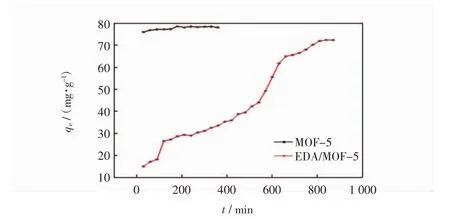
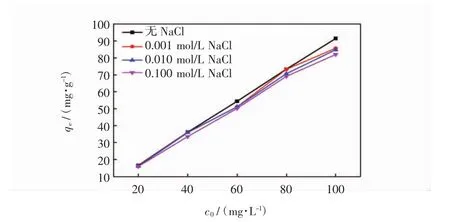
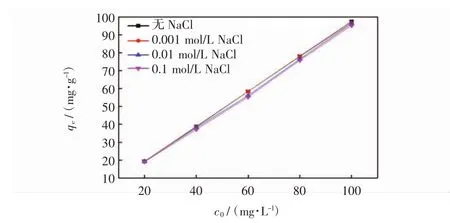
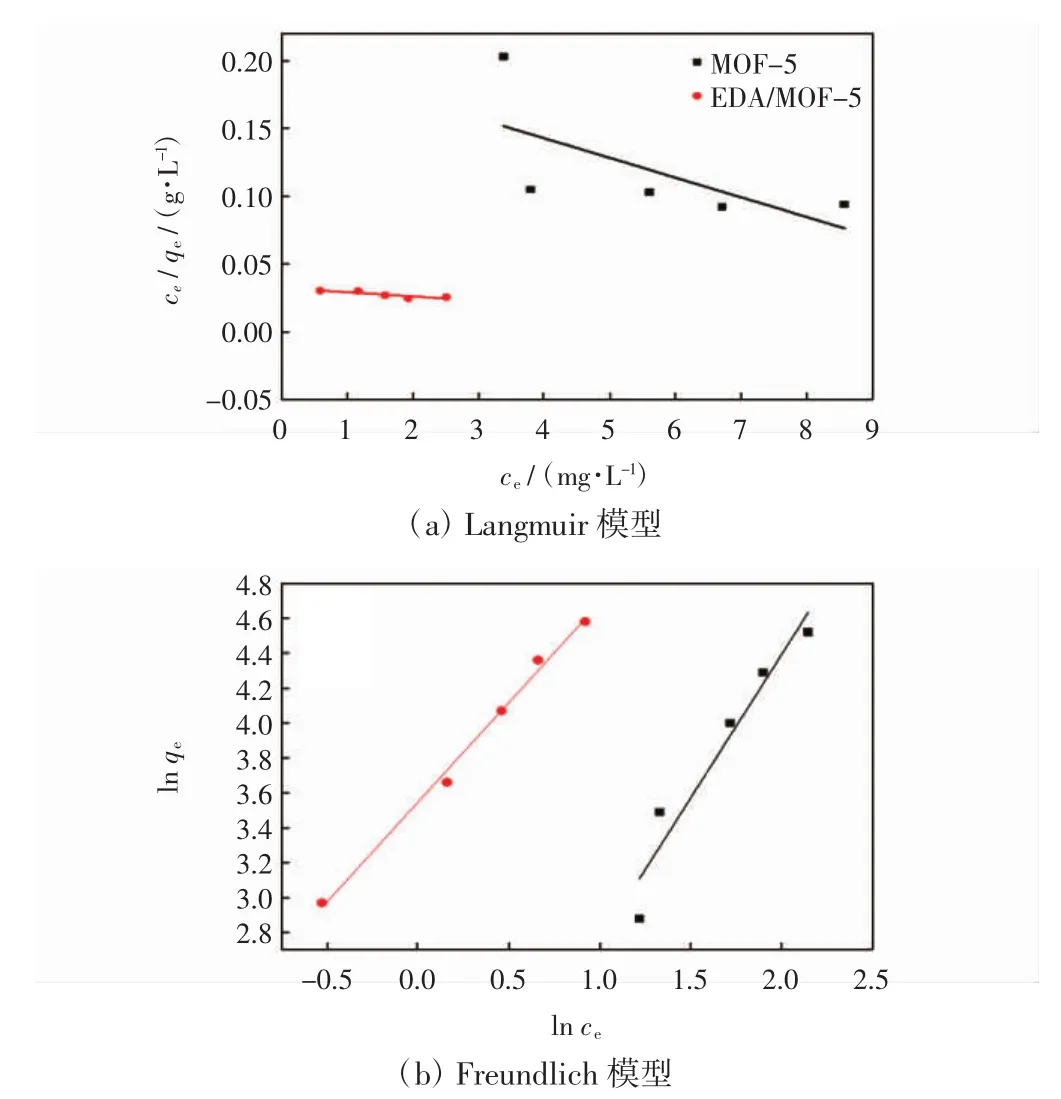
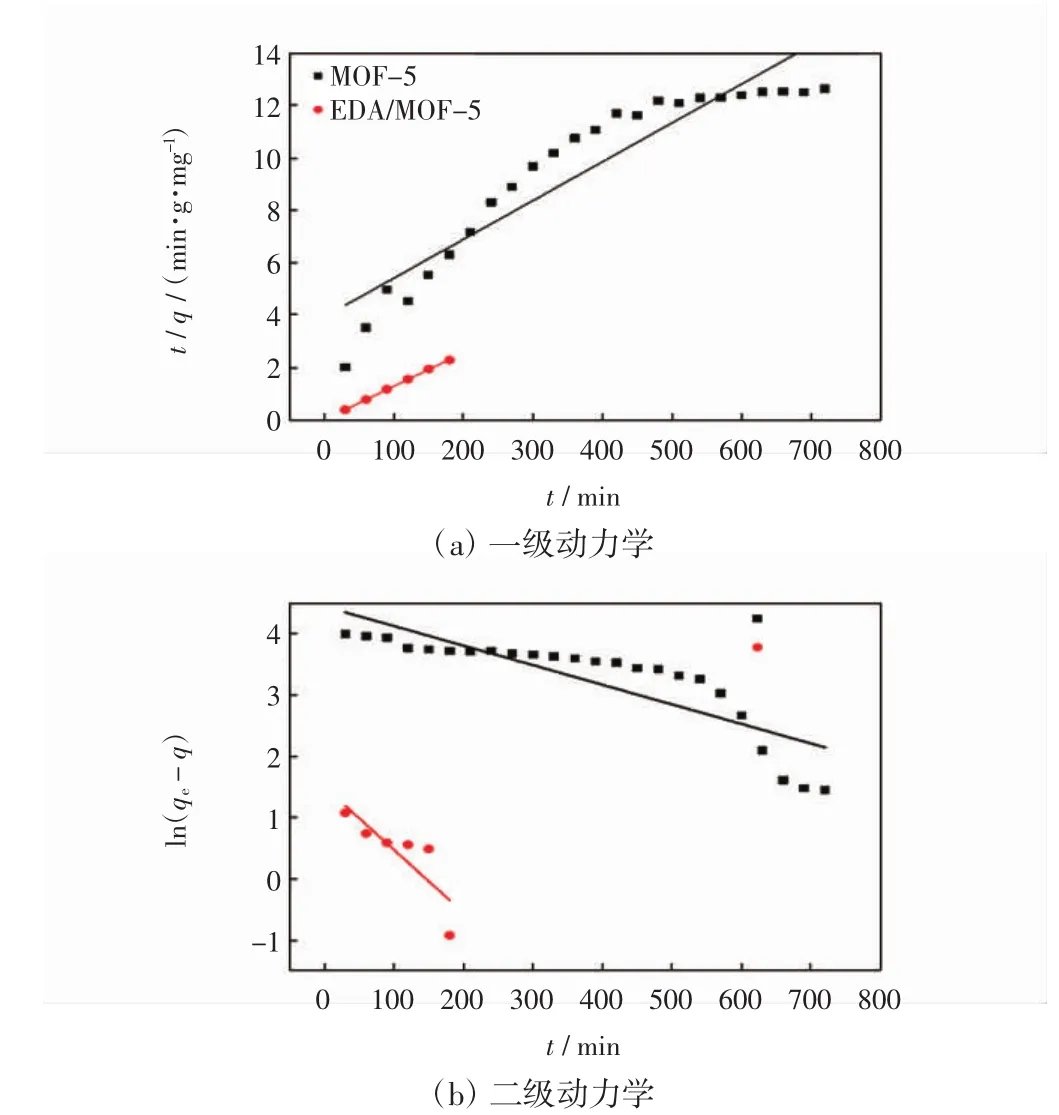
MOF-5的pHpzc为2.8,当溶液pH值高于2.8时,MOF-5表面带负电荷.因此当pH<5.2时,由于静电力的作用,其对刚果红的吸附量逐渐增加.当溶液5.2 图5为吸附时间对吸附性能的影响. 图5 吸附时间对吸附性能的影响Fig.5 Influence of adsorption time on adsorption performance 由图5可见,吸附6 h时,MOF-5对刚果红的吸附量达到最大吸附量的50%,随着时间的延长,吸附量逐渐增大,吸附时间12 h左右,吸附基本达到平衡;EDA/MOF-5在吸附3 h左右对刚果红的吸附已基本达到平衡.由于EDA/MOF-5的物理吸附和化学吸附的同时作用,使其对刚果红的吸附速率得到大幅度的提升,吸附达到平衡所用的时间大大缩短. 图6和图7分别为离子强度对MOF-5和EDA/MOF-5吸附性能的影响图. 图6 离子强度对MOF-5吸附性能的影响Fig.6 Effect of ion strength on MOF-5 adsorption performance 图7 离子强度对EDA/MOF-5吸附性能的影响Fig.7 Effect of ion strength on EDA/MOF-5 adsorption performance 如图6和图7所示,加入的离子对于刚果红吸附有一定的抑制作用,且对于未改性的MOF-5的影响明显高于改性后的EDA/MOF-5.由于离子强度的增加导致刚果红的移动系数减小,与刚果红分子在一定程度上构成了竞争吸附位点的关系,从而阻碍其被吸附剂的吸附,离子强度越大,抑制作用越大.此外离子强度对于低浓度的刚果红的影响较小,刚果红浓度越大,影响越明显. 吸附等温线是衡量吸附剂与吸附质之间的相互关系.为评价MOF-5和EDA/MOF-5对刚果红的吸附行为,研究中采用Langmuir模型(式(3))和Freundlich模型(式(4))对实验数据进行拟合分析. 式中:ce为吸附平衡时染料溶液的质量浓度(mg/L);qe为吸附平衡时吸附剂上染料的含量(mg/g);qm为单分子层吸附时的最大吸附量(mg/g);b为吸附过程与热力学有关的Langmuir常数;K和n分别是与吸附能力和吸附强度有关的Freundlich常数. 图8为MOF-5和EDA/MOF-5对刚果红的吸附等温线,表1为吸附等温线参数图.由图8和表1可知,MOF-5和EDA/MOF-5对刚果红的吸附体系中Freundlich的恒温吸附相关系数均高于Langmuir的恒温吸附相关系数,因此,MOF-5和EDA/MOF-5对刚果红的吸附更适合于Freundlich模型. 为了探究MOF-5和EDA/MOF-5对刚果红染料的吸附机理,本文采用准一级动力学模型(式(5))和准二级动力学模型(式(6))对实验数据进行拟合分析. 图8 MOF-5和EDA/MOF-5对刚果红的吸附等温线Fig.8 MOF-5 and EDA/MOF-5 adsorption isotherm of Congo red 式中:qe为平衡吸附量(mg/g);qt为时间为t时的吸附量(mg/g);k1为准一级动力学速率常数(min-1);k2为准二级动力学速率常数(g·g-1·min-1). 图9为MOF-5和EDA/MOF-5对刚果红的吸附动力学模型,表2为吸附动力学参数图. 图9 MOF-5和EDA/MOF-5对刚果红的吸附动力学模型Fig.9 Adsorption kinetics model of MOF-5 and EDA/MOF-5 on Congo red 表1 吸附等温线参数Tab.1 Parameters of adsorption isotherm Langmuir Freundlich 表2 吸附动力学参数Tab.2 Parameters of adsorption dynamic 由图9和表2可知,MOF-5和EDA/MOF-5对刚果红的准二级动力学的相关系数高于准一级动力学的相关系数,并且由准二级动力学计算的平衡吸附量与实验值非常接近,因此MOF-5和EDA/MOF-5对刚果红的吸附可以由准二级动力学描述. (1)EDA/MOF-5较于MOF-5对刚果红的吸附量和脱色率分别提升了13.19 mg/g和14%. (2)在试验范围内,随着刚果红初始浓度和温度的升高,EDA/MOF-5对刚果红的吸附量随之增大,当刚果红浓度为80 mg/L时,EDA/MOF-5对其吸附量和脱色率分别达到78.36 mg/g和98%. (3)MOF-5在弱碱性的条件下更容易吸附水中的刚果红染料,EDA/MOF-5受pH和离子强度的影响较小. (4)离子强度的增加对刚果红的移动系数减少,对于刚果红的吸附具有一定的抑制作用,且对于未改性的MOF-5的影响明显高于改性后的EDA/MOF-5. (5)MOF-5和EDA/MOF-5对刚果红的吸附更适合Freundlich模型和拟二级动力学方程. [1]ZHANG L J,HU P,WANG J,et al.Adsorption of methyl Orange(MO)by Zr(IV)-immobilized cross-linked chitosan/bentonite composite[J].Int J Biol Macromol,2015,81:818-827. [2]GUSMAO K A G,GURGEL L V A,MELO T M S,et al.Adsorption studies of methylene blue and gentian violet on sugar-cane bagasse modified with EDTA dianhydride(EDTAD)in aqueous solutions:Kinetic and equilibrium aspects[J].Journal of Environmental Management,2013,118:135-143. [3]GOMEZ J M,GALAN J,RODRIGUEZ A,et al.Dye adsorption onto mesoporous materials:pH influence,kinetics and equilibrium in buffered and saline media[J].Journal of Environmental Management,2014,146:355-361. [4]HAMEED B H,DIN A T M,AHMAD A L.Adsorption of methylene blue onto bamboo-based activated carbon:Kinetics and equilibrium studies[J].Journal of Hazardous Materials,2007,141:819-825. [5]AL-DEGS Y S,KHRAISHEH M A M,ALLEN S J,et al.Adsorption characteristics of reactive dyes in columns of activated carbon[J].Journal of Hazardous Materials,2009,165:944-949. [6]WANG L,LI J,WANG Y,et al.Adsorption capability for Congo red on nanocrystalline MFe2O4(M=Mn,Fe Co,Ni)spinel ferrites[J].Chem Eng J,2012(181/182):72-79. [7]QADRI S,GANOE A,HAIK Y.Removal and recovery of acridine orange from solutions by use of magnetic nanoparticles[J].Journal of Hazardous Materials,2009,169:318-323. [8]GURSES A,DOGAR C,YALCIN M,et al.The adsorption kinetics of the cationic dye,methylene blue,onto clay[J].Journal of Hazardous Materials,2006,131:217-228. [9]KHENIFI A,BOUBERKA Z,SEKRANE F,et al.Adsorption studyofanindustrialdyebyanorganicclay[J].Adsorption,2007,13:149-158. [10]DIZGE N,AYDINER C,DEMIRBAS E,et al.Adsorption of reactive dyes from aqueous solutions by fly ash:Kinetic and equilibrium studies[J].Hazard Mater,2008,150:737-746. [11]DEMIRBAS E,NAS M Z.Batch kinetic and equilibrium studies of adsorption of reactive blue 21 by fly ash and sepiolite[J].Desalination,2009,243:8-21. [12]VIJAYAKUMA G R,TAMILARASAN R,HARMENDIRAKUMAR M D.Adsorption,kinetic,equilibrium and thermodynamic studies on the removal of basic dye rhodamine-B from aqueous solution by the use of natural adsorbent perlite[J].Mater Environ Sci,2012,3:157-170. [13]DOGAN M,ALKAN M,ONGANER Y.Adsorption of methylene blue from aqueous solution onto perlite[J].Water Air Soil Poll,2000,120:229-248. [14]YAO Y,HE B,XU F,et al.Equilibrium and kinetic studies of methyl orange adsorption on multiwalled carbon nanotubes[J].Chem Eng J,2011,170:82-89. [15]KUO C Y,WU C H,WU J Y.Adsorption of direct dyes from aqueous solutions by carbon nanotubes:Determination of equilibrium,kinetics and thermodynamics parameters[J].Colloid Interf Sci,2008,327:308-315. [16]张杰,刘霖,代昭,等.新型聚合物P(DVB-co-AA)//PDVB多孔微球的制备[J].天津工业大学学报,2013,32(2):49-53.ZHANG J,LIU L,DAI Z,et al.The preparation of new polymer P(DVB-co-AA)//PDVB porous microspheres[J].Journal of Tianjin Polytechnic University,2013,32(2):49-53(in Chinese). [17]LI H,EDDAOUDI M,O'KEEFE M,et al.Design and synthesis of an exceptionally stable and highly porous metal-organic framework[J].Nature,1999,402(6759):276-279. [18]代伟,庄海堂,卢信清,等.金属有机骨架材料MOF-5上噻吩硫化物的吸附分离[J].燃料化学学报,2010(5):626-630.DAI W,ZHUANG H T,LU X Q,et al.The adsorption and separation of thiophene sulfide on the metal organic skeleton material MOF-5[J].Journal of Fuel Chemistry,2010(5):626-630(in Chinese). [19]李祥鹏,张华,张雯,等.功能化锌金属有机骨架制备及表征[J].功能材料,2017,17:55-58.LI X P,ZHANG H,ZHANG W,et al.Preparation and characterization of functional zinc metal organic skeleton[J].Functional Materials,2017,17:55-58(in Chinese). [20]李丹丹,彭昌盛,张腾,等.以纤维为造孔剂的粉煤灰基材料对染料的吸附研究[J].环境科学与技术,2016,39(2):70-74.LI D D,PENG C S,ZHANG T,et al.The study on the adsorption of the fly ash based materials with fiber as foramen[J].Environmental Science and Technology,2016,39(2):70-74(in Chinese). [21]IRAM M,GUO C,GUAN Y,et al.Adsorption and magnetic removal of neutral red dye from aqueous solution using Fe3O4hollow nanospheres[J].Journal of Hazardous Materials,2010,181(1):1039-1050.2.4 吸附时间对吸附的影响
2.5 离子强度对吸附的影响
2.6 吸附等温线
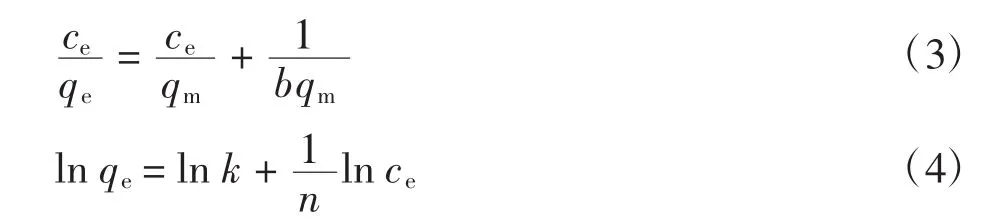
2.7 吸附动力学
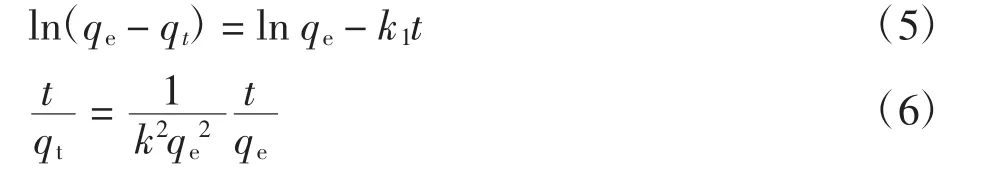


3 结论

