碱促进复合脱硫脱砷剂的制备与表征
孙蕴婕张 荣何秋平
1上海化工研究院有限公司 (上海 200062)
1聚烯烃催化技术与高性能材料国家重点实验室 (上海 200062)
2上海市聚烯烃催化技术重点实验室 (上海 200062)
3上海绿强新材料有限公司 (上海 201806)
聚丙烯是一种重要的合成树脂。粗丙烯中硫化物与砷化物的存在会严重影响聚合过程,因此各类聚丙烯工艺都对砷、硫含量(质量分数,下同)提出了严格的要求。在硫化物中羰基硫(COS)对催化剂活性的影响非常显著且难以脱除,因此丙烯原料中COS含量是一项十分重要的质量控制指标。聚合级丙烯要求 w(As)≤10 ng/g,w(COS)≤30 ng/g[1-2]。国内外有关专利报道的丙烯脱硫脱砷剂[3-10]使用氧化铜(CuO)、氧化铁(Fe2O3)、氧化锌(ZnO)及氧化铅(Pb2O3)等为主要活性组分;聚丙烯工艺中应用较多的脱硫脱砷剂以CuO-ZnO为活性组分,以共沉淀法制备。然而由于净化容量或净化深度的限制,上述脱硫脱砷剂对COS的脱除能力有限,主要用于无机硫与砷的脱除。目前丙烯精制工艺中COS净化多采用水解转化法,使用负载碱性物质的多孔载体[11-14]将COS转化为H2S,再进一步使用脱硫剂将H2S脱除,过程较为繁琐。开发一种具备高COS净化容量、适用于较高COS净化范围并能实现COS一步脱除的脱硫脱砷剂符合市场需求。
本研究采用不同配比的CuO、碱金属氢氧化物、碱金属盐及活性氧化铝制备脱硫脱砷剂并进行表征与评价。探讨了一种具有高效COS净化性能的复合脱硫脱砷剂的制备方法及其脱硫脱砷特性。本研究使用广泛易得的原料和适合工业化生产的制备工艺,具有很强的可操作性。
1 实验部分
1.1 试剂与原料
活性氧化铝粉,自制;碱式碳酸铜、氢氧化钠、氢氧化钾、碳酸氢钠、碳酸氢钾、硝酸铜、硝酸锌、硝酸铝、石墨粉,分析纯,国药集团化学试剂有限公司;去离子水,自制;1 000 μg/g COS标准气体(氮气余),上海伟创标准气体有限公司;10 μg/g砷化氢标准气体(氮气余),佛山市科的气体化工有限公司;丙烯原料(w≥99.9%),上海朗顺化工有限公司。
1.2 样品准备
将活性氧化铝粉与一定量碱式碳酸铜及造孔剂干法混碾,然后加入一定量碱金属化合物水溶液湿法混碾,物料挤出成型;在65℃下水热处理6 h,马弗炉中350℃下焙烧4 h得到成品。用相同方法制备空白活性氧化铝样品、10%CuO(不含碱)样品、5%NaOH(不含铜)样品为对照(此处及后文所述活性组分CuO及碱的含量均以其占成品的质量百分比计)。按照市售脱硫脱砷剂的制备方法,以共沉淀法制备对照样品,标记为样品b;将硝酸铜、硝酸锌及硝酸铝加入去离子水中混合溶解,调节pH至7.5~9,在70℃下反应1 h,将沉淀物洗涤干燥,加入石墨粉、活性氧化铝粉压片成型,在350℃下老化4 h。样品b中CuO含量占成品吸附剂质量的30%,氧化锌含量占20%。
1.3 测试表征
孔结构表征使用美国麦克仪器公司ASAP 2020型物理吸附仪,采用氮气吸附法测试,比表面积使用BET法计算,孔容和孔径分布采用BJH方程计算。二氧化碳程序升温脱附(CO2-TPD)测定采用浙江泛泰仪器有限公司FineSorb-3010D型全自动程序升温化学吸附仪:0.1 g净化剂在He气(30 mL/min)中升温至350℃,预处理30 min;冷却至30℃,用CO2(30 mL/min)吸附2 h;以5℃/min的速率升温至350℃进行程序脱附,热导检测器在线测定脱附的CO2含量。显微结构观察采用德国蔡司(ZEISS)公司MERLIN Compact型扫描电子显微镜(SEM)。
1.4 净化剂性能评价
1.4.1 COS净化容量评价
COS净化容量评价采用北京拓川科研设备股份有限公司定制的微反设备,反应床为内径为10 mm的经惰性化处理的不锈钢固定床反应器。量取2 mL样品(颗粒大小为0.18~0.25 mm)并称量质量(精确至0.01 g),将样品装填入反应器,上下用石英砂与石英棉填充。以1000 μg/g COS(氮气余)标准气体为原料,空速为3000 h-1,反应温度为40℃,压力为0.1 MPa,当COS含量高于20 ng/g时判定穿透,记录反应时间。通过反应时间、标准气体质量浓度及流量计算通过反应器的COS质量,将其除以样品质量即得COS净化容量。出口COS及H2S含量采用美国安捷伦仪器公司GC 7890B型气相色谱仪在线分析,色谱分析采用DB-Sulfur SCD毛细管柱及硫化学发光(SCD)355型检测器。
1.4.2 砷净化容量评价
砷净化容量评价采用内径为3 mm、经惰性化处理的不锈钢固定床反应器,样品装填量为0.1 g,使10 μg/g砷化氢标准气体(氮气余)以1 000 h-1的气相空速通过样品床层,反应温度为40℃,压力为0.1 MPa。其余评价试验条件、步骤与计算方法参考GB/T 31192—2014《常温铜系脱砷剂砷容试验方法》。
1.4.3 综合脱除性能评价
COS及AsH3的综合脱除性能评价采用含3.8 μg/g COS与0.6 μg/g AsH3的丙烯通过微反装置,在液相空速为8 h-1,温度为40℃,压力为2.5 MPa的实验条件下连续进料24 h。出口COS含量检测方法同1.4.1,出口砷含量测定采用GB/T 7686—2008《化工产品中砷含量测定的通用方法》,所用分光光度计为上海仪电科学仪器股份有限公司722s型。
2 结果与讨论
2.1 碱含量及种类对脱硫脱砷效果的影响
2.1.1 孔结构及CO2-TPD表征
多孔材料表面的Lewis碱对酸性气体吸收有促进作用,研究认为COS吸附在碱改性氧化铝表面的OH-上[15],因此COS吸收与样品碱性有关[16]。本研究以CO2-TPD考察净化剂的碱性。图1(a)显示,碱种类对样品酸性气体吸附能力有一定影响,然而并不显著,相较而言,吸附性能NaOH>KOH>K2CO3>Na2CO3。
对10%CuO含量样品进行NaOH含量影响的考察。图1(b)显示,1%NaOH-10%CuO样品的CO2脱附量明显大于空白活性氧化铝样品及10%CuOAl2O3样品,说明样品表面的碱中心向CO2提供了活性吸附位。NaOH含量为2%、5%、10%时样品有更大的CO2脱附量,而当碱含量达到20%时脱附量反而下降,这可能与样品比表面积减少有关。从图2(a)中可见,样品比表面积及孔容随NaOH含量的增加而减小。当碱含量达到20%时,比表面积下降至80 m2/g。同时,图2(b)孔径分布显示,当碱含量为1%~5%时,样品孔径分布较窄、有序度相对较高。当碱量增加到10%及以上时,孔径分布严重宽化,孔径均匀性明显降低。碱含量的增加使得氧化铝的微小孔径被填充,孔径分布向大孔径偏移,这一特征符合比表面积及孔容变化特征。
综上所述,样品酸性气体吸附能力受样品碱含量、碱种类及比表面积的综合影响,使用NaOH为碱活性组分样品的酸性气体吸附性能较佳。碱组分能提高样品酸性气体吸附能力,然而当碱含量超过一定量时,样品比表面积减小,酸性气体的活性吸附位随之减少。结合CO2-TPD与比表面积表征的结果,认为2%~5%是较为适宜的NaOH含量范围。
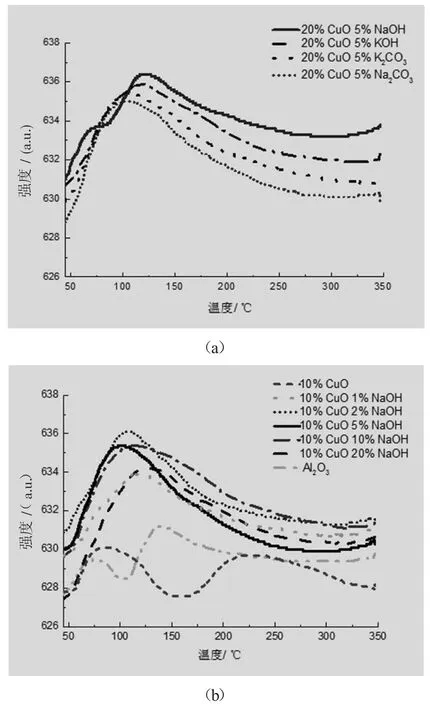
图1 不同碱种类(a)及碱含量(b)样品的CO2-TPD曲线
2.1.2 COS净化容量评价
图 3(a)显示,在 CuO 含量相同[w(CuO)=10%]时,不含碱样品的COS净化容量为14.7 mg/g,而含1%NaOH样品的COS净化容量提高至25 mg/g。随着碱含量的增加,样品的COS净化容量逐渐提高,当NaOH含量达到10%时,由于样品比表面积的下降及有效孔道的减少导致反应活性点位减少,COS净化容量呈下降趋势。
2.1.3 砷净化容量评价
钠离子是很好的电子促进剂[17-18],Nishinotffu[19]使用负载CuO与碱(土)金属的活性炭来脱除气体中的AsH3,PH3,SbH3等毒物。本研究也发现碱在一定浓度下对净化剂的脱砷性能有促进作用。碱含量对样品砷净化容量的影响如图4(a)所示,在CuO含量相同[w(CuO)=10%]的情况下,当NaOH含量为1%~5%时,砷净化容量随碱含量的增加而升高,当NaOH含量达10%及以上时,由于比表面积的减小和空间位阻效应,砷吸附容量减小。
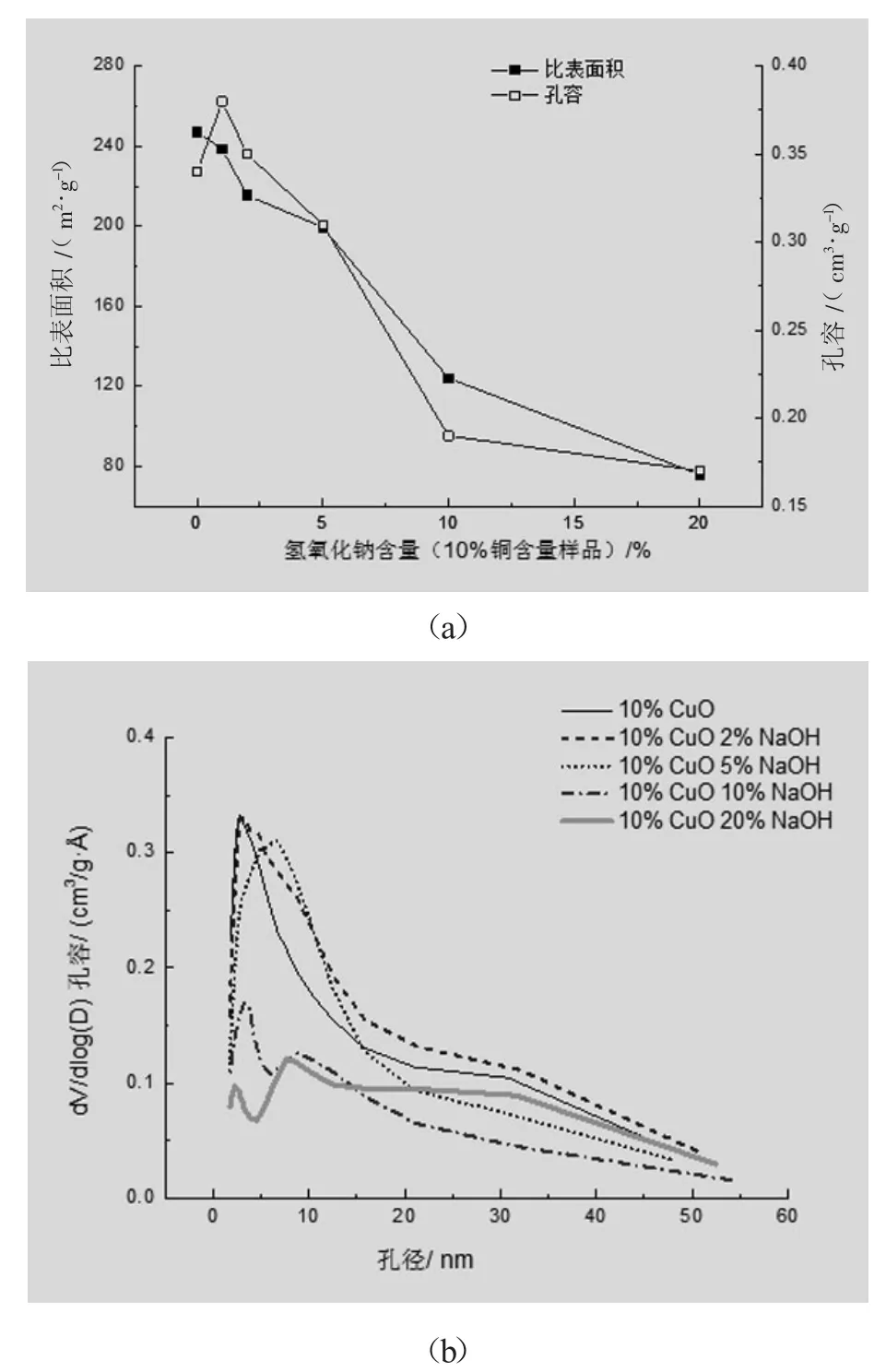
图2 碱含量对10%CuO含量样品比表面积、孔容(a)及孔径分布(b)的影响
综上所述,认为当NaOH含量为5%时,样品有较佳的脱硫及脱砷效果。
2.2 CuO含量对脱硫脱砷效果的影响
研究[20-21]认为碱改性氧化铝对COS的脱除机理为催化水解过程,在微量水的存在下,COS在碱的促进下分解为H2S与CO2,H2S进入下游会影响丙烯聚合,需使用脱硫剂进一步对H2S进行脱除。本研究将空白活性氧化铝样品、5%NaOH样品与5%NaOH-10%CuO样品做对比评价。结果显示,COS在通过空白氧化铝样品及5%NaOH样品床层后均有H2S生成,而COS在通过含10%及以上CuO活性组分的样品后出口无H2S生成。
CuO含量对COS的净化容量影响如图3(b)所示,结果显示,CuO含量在10%~30%范围内的增加可有效提高COS的净化容量,但由于比表面积和孔容的下降,当CuO含量达到40%时,COS净化容量反而略有下降。
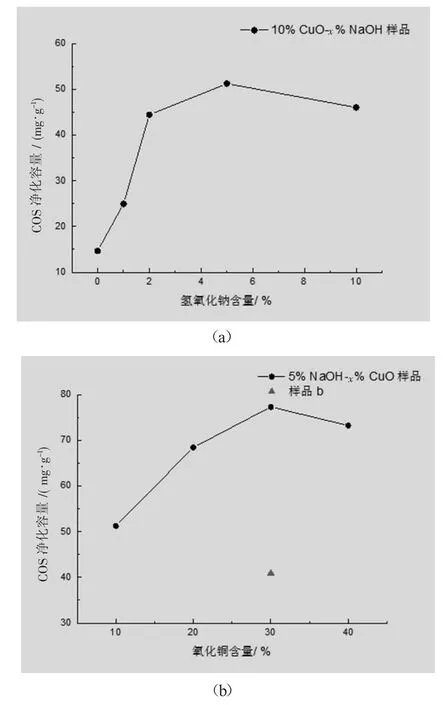
图3 不同碱含量样品(a)及不同CuO含量样品(b)的COS净化容量
图4(b)显示了CuO含量对砷容的影响,从图中可见空白活性氧化铝对砷几乎无吸附能力,5%NaOH样品有一定砷吸附量,而加入CuO后砷净化容量显著提高。当CuO含量为10%~30%时,砷容随CuO含量的增加而增加,而当CuO含量达到40%时,受样品比表面积减小的影响,砷净化容量反而略有下降。
综上所述,认为当CuO含量为30%时样品有较好的脱硫及脱砷效果。
2.4 综合脱除性能研究
结合2.2及2.3的测试效果,选用5%NaOH-30%CuO样品,模拟工况使用液相丙烯进行24 h连续评价试验。结果如图5所示,30 min后反应稳定,在方法检出限以内未有COS(检出限为20 ng/g)、H2S(检出限为20 ng/g)及AsH3(检出限为5 ng/g)检出,表明净化效果良好,反应平稳。
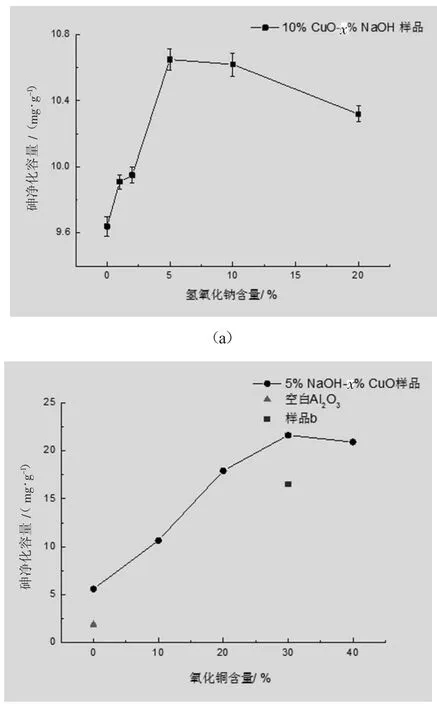
图4 不同NaOH含量样品(a)及不同CuO含量样品(b)的砷净化容量
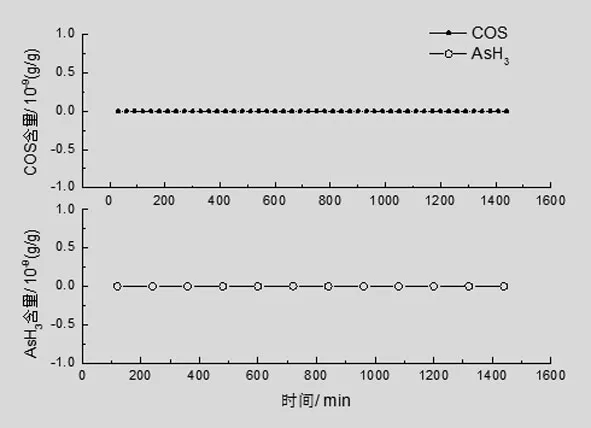
图5 5%NaOH-30%CuO样品液相丙烯连续评价结果
2.5 与CuO-ZnO脱硫脱砷剂对比
将以本文方法制备的30%CuO-5%NaOH样品标记为a,以参考市售脱硫脱砷剂制备方法制备的CuO-ZnO脱硫脱砷剂标记为b。从表1样品a与样品b表面积及孔容数据比对可以看出,在活性组分CuO含量相同的情况下,样品a的比表面积与孔容均大于样品b。图3(b)COS吸附评价结果显示,样品b的COS净化容量为40.9 mg/g,而碱促进样品a的COS净化容量可达77.4 mg/g。图4(b)中样品b砷净化容量为16.5 mg/g,而样品a的砷净化容量可达21.6 mg/g。综上可见,样品a的脱硫脱砷性能优于样品b。
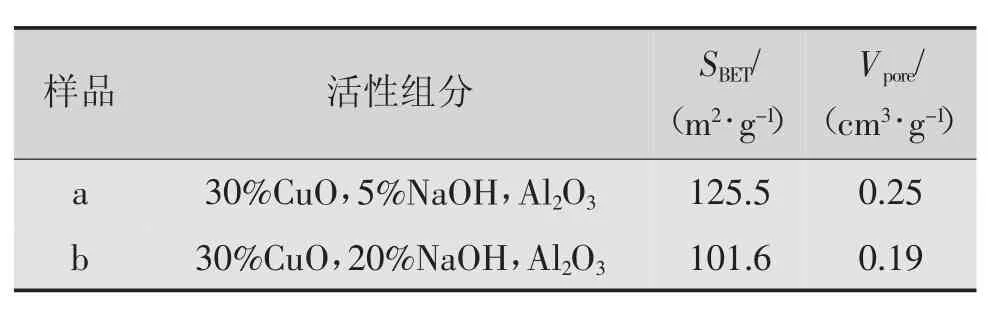
表1 样品及CuO-ZnO脱硫脱砷剂比表面积及孔容对比
从图6电镜扫描图可以看到,使用本文方法制备的样品a具有较发达的孔隙结构,而样品b表面比较光滑。从图6样品穿透后的SEM图可以看出,COS,AsH3与活性组分相结合,被吸附在净化剂的表面及内部孔道中,发达的孔隙结构提供了较多的吸附空间,因此样品a具有更大的吸附容量。
4 结论

图6 样品a与样品b的SEM形貌及其吸附COS,AsH3穿透的SEM形貌
本研究通过对不同碱含量、碱种类及CuO含量净化剂的表征,并与参考市售脱硫脱砷剂制备方法制备的CuO-ZnO样品比对评价后发现,在氧化铝体系中,碱能与CuO发挥协同作用,碱活性组分能促进COS在氧化铝表面的水解转化,碱催化水解COS后产生的H2S与CuO活性位作用得以吸附脱除,同时Na+作为电子促进剂能协同CuO提高砷净化容量。在一定范围内,碱与CuO活性组分含量的增加能提高脱硫、脱砷效果,然而过量的NaOH(≥10%)会堵塞Al2O3孔道,对净化效果有抑制作用;同时,过量的CuO(40%)也会降低样品比表面积,从而影响脱硫脱砷容量。通过对比发现:30%CuO-5%NaOH的样品具有较佳的脱硫脱砷效果,净化容量评价试验显示该净化剂可在温度为40℃、空速为3000 h-1的条件下将氮气中含量为1 000 μg/g的COS脱除至20 ng/g以下,COS净化容量可达77.5 mg/g,比相同CuO含量的CuO-ZnO样品提高近90%;砷净化容量可达21.65 mg/g,比CuO-ZnO样品提高30%。该净化剂可在液相丙烯中使用,将微量COS吸附脱除至20 ng/g以下,AsH3脱除至5 ng/g以下。
参考文献:
[1]李雪双,丁玲,姚庆,等.聚丙烯生产中原料丙烯的精制[J].广东化工,2013,12(40):47-50.
[2]冯续.聚丙烯工艺中原料丙烯的净化[J].化学工业与工程技术,2008,29(4):48-53.
[3]贾银娟,王灿,杨贺勤,等.常温脱硫脱砷剂及其制备方法:105582877A[P].2016-05-18.
[4]贾银娟,李宏旭,王灿,等.脱硫脱砷剂:104549123A[P].2015-04-29.
[5]杜文庆,刘振义.一种常温复合脱硫脱砷剂的制备方法:101591552A[P].2009-12-02.
[6]余启炎,冷冰,袁霞光,等.一种轻质烃类脱砷剂及其制备方法:1611566A[P].2005-05-04.
[7]MINORU S,SATOSHI K,OKINORI S,et al.Arsenic compound removingagent:JPS60238144[P].1985-11-27.
[8]JOHNSON MM,NOWACK G P.Process for removal of arsine impurities from gases containing arsine and hydrogen sulfide:US4593148[P].1986-06-03.
[9]LEONDARIDEI P,VENDEL A S,AKTHAR T,et al.Catalyst to remove gaseous hydride and method for removing gaseous hydride from gas vapor:JPH05317715[P].1993-12-03.
[10]BLANKENSHIP S A,VOIGHT R W.Adsorbent for the removal of trace quantities from a hydrocarbon stream and process for its use:US5990372[P].1999-11-23.
[11]FREVEL L K,KRESSLEY L J.Catalytic hydrolysis of carbonyl sulfide:US3265757[P].1966-08-09.
[12]COLLINS J J.Purification of liquid hydrocarbons containing carbonyl sulfide:US3654144[P].1972-04-04.
[13]LIU P K T.Process for removal of carbonyl sulfide from organic liquid by adsorption using alumina adsorbent capable ofregeneration:US4835338[P].1989-05-30.
[14]TRUCKO J E,TERTEL J A,LARICCHIA L,et al.Process for removing carbonyl sulfide from a hydrocarbon stream:US2015225653[P].2015-08-13.
[15]FIEDOROW R,LEAUTE R,LANA I G D.A study of the kinetics and mechanism of COS hydrolysis over alumina[J].Journal ofCatalysis,1984,85(2):339-348.
[16]李春虎,郭汉贤,谈世韶.碱改性γ-Al2O3催化剂表面碱强度分布与COS水解活性的研究 [J].分子催化,1994(4):305-312.
[17]GAO F,WANG Y L,WASHTON N M,et al.Effects of alkali and alkaline earth cocations on the activity and hydrothermal stability of Cu/SSZ-13 NH3-SCR catalysts[J].ACSCatalysis,2015,5(11):6780-6791.
[18]MORENO J LV,AREVALO R L,ESCANO MC S,et al.A theoretical study on the adsorption of CO2on CuO(110)surface[J].Journal ofthe Physical SocietyofJapan,2015,84(1).
[19]HIROSHI N,TOSHIO A.Method for removal of poisonous gases:US4532115[P].1985-07-30.
[20]RHODES C,RIDDELB S A,WESTA J,et al.The low-temperature hydrolysis ofcarbonyl sulfide and carbon disulfide:a review[J].Catalysis Today,2000,59(3):443-464.
[21]梁丽彤,上官炬,李春虎.国内外COS水解技术研究状况[J].天然气化工,2005,30(1):54-57.

