控制性低中心静脉压在腹腔镜肝切除中的应用:前瞻性随机对照研究
陈 熙 胡朝辉 彭永海 罗 华 杨 培
(四川省绵阳市中心医院肝胆外科,绵阳 621000)
肝切除是肝细胞肝癌(hepatectomy carcinoma,HCC)首选的治疗方式[1]。肝切除术中失血量与术后并发症以及远期预后有关[2,3]。控制性低中心静脉压(controlled low central venous pressure,CLCVP)技术作为减少术中失血的有效手段,广泛应用于肝切除手术中[4,5]。腹腔肝切除具有创伤小、全身反应轻、术后恢复快等优势,近几年取得了飞速的发展以及突破。腹腔镜肝切除中由于受气腹压力的影响,术中失血量往往低于传统开放手术[6~8]。CLCVP技术在腹腔镜肝切除中的有效性及安全性尚未得到证实。我们设计前瞻性随机对照研究,探讨CLCVP技术对腹腔镜肝切除术中、术后失血量及相关指标的影响,以期为其在腹腔镜肝切除中的临床应用提供参考。
1 临床资料与方法
1.1 一般资料
本研究经我院伦理委员会审批(S2016098)。
纳入标准:HCC临床诊断标准符合2011版《原发性肝癌诊疗规范》[9];CT或MRI判断能够完整切除肿瘤,切缘无残留;吲哚菁绿15 min潴留率(indocyanine green retention rate at 15 min,ICG-R15)<20%;肝功能Child-Pugh分级A~B级。
排除标准:患者拒绝行腹腔镜肝切除;心肺功能无法耐受手术;肺、骨等远处转移。
2017年1~7月,我科因HCC行肝切除60例。由SPSS24.0软件包生成随机序列,将随机序列依次放入编号且密闭封口的不透光信封保存。研究者依编号打开信封,将研究对象按随机分配顺序进行分组,低中心静脉压组30例(低压组)和正常中心静脉压组30例(对照组)。低压组3例,对照组5例拒绝行腹腔镜手术,故最终52例纳入本研究,年龄33~78岁,平均56.5岁。2组年龄、性别、肿瘤直径、肝切除范围、肝癌分期、Child分级、总胆红素升高(>20.5 μmol/L)、ICG-R15、肝硬度值差异均无统计学意义(P>0.05),具有可比性,见表1。其中ICG-R15及肝硬度值测定均在术前1~3天完成。ICG-R15测定使用日本光电工业株式会社DDG-3300K分析仪,测定方法同参考文献[10]。肝硬度值测定使用法国爱科森公司Fibroscan502,测定方法同参考文献[11],为避免人为误差,由超声科医师专人负责。肝癌分期按照巴塞罗那肝癌分期(Barcelona Clinic Liver Cancer,BCLC)[9]。
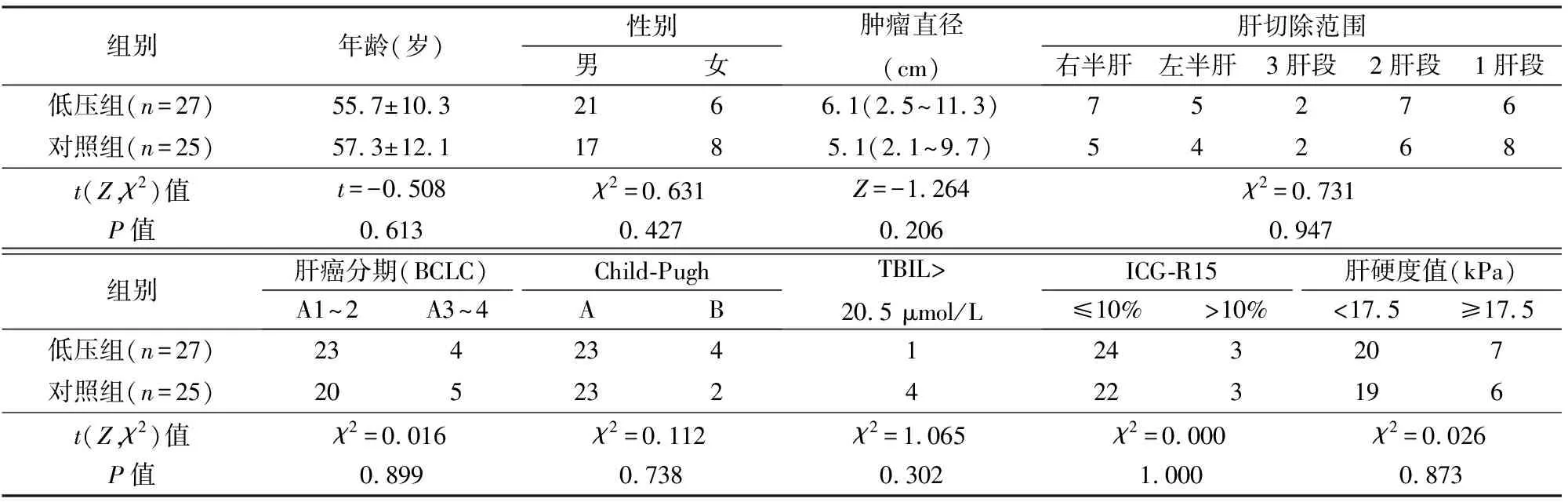
表1 2组术前资料比较
TBIL:总胆红素,正常值0~20.5 μmol/L;ICG-R15:吲哚菁绿15 min潴留率,正常值≤10%;肝硬度值正常值<17.5 kPa
1.2 术中中心静脉压控制
静脉吸入复合全身麻醉,左侧桡动脉穿刺测量动脉血压,右侧颈内静脉置管测量CVP,置尿管监测术中尿量。低压组:麻醉诱导前至肝实质离断前输液速度控制在<75 ml/h;肝实质离断过程中,中心静脉压控制在2~4 cm H2O(1 cm H2O=0.098 kPa),必要时缓慢静脉推注硝酸甘油(0.5~2.0 mg/次),维持动脉收缩压(systolic blood pressure,SBP)>90 mm Hg,若低于该标准,则减少麻醉药物用量,加快补液速度,同时应用多巴胺扩张肾血管,维持尿量25 ml/h以上;离断肝实质后,通过快速补液将CVP提高至5 cm H2O以上。对照组:按晶胶2∶1进行补液,晶体主要为乳酸钠林格注射液,胶体为羟乙基淀粉,术中通过控制麻醉药物用量以及补液速度将CVP维持在5~10 cm H2O,SBP>90 mm Hg,尿量≥1 ml/(kg·h)。2组若失血量超过全身容量25%或血气分析提示血红蛋白低于80 g/L时输入浓缩红细胞。
1.3 手术方法
术前行增强CT或MRI明确肿物部位、大小及与周围血管关系。全麻,平卧位,下肢分开60°,头高脚低位,根据术中需要调整手术台角度。采用四孔或五孔法,肝脏边缘较小病灶采取三孔法。气腹压力14~15 mm Hg(1 mm Hg=0.133 kPa)。主操作孔尽可能接近病变部位,且不与断面平行。离断肝圆韧带及镰状韧带。左半肝切除时位置比较表浅,先游离左三角韧带及左冠状韧带;右半肝切除时由于游离操作不便,大部分情况下不先游离右肝周围韧带,待肝实质离断后再做游离。肝切除范围取决于术前影像学检查、术中探查及术中超声定位,了解肿瘤范围及其与血管关系。肝门预置阻断带,不做常规性阻断,当出血量较多影响手术视野时采用间断Pringle法阻断肝血流,每次阻断15 min,开放5 min。使用超声刀、LigaSure、腔镜下CUSA联合钛夹、Hem-o-lok、切割闭合器离断肝实质。肝断面使用百克钳止血,生理盐水反复冲洗,确认无出血和胆汁漏,常规覆盖止血纱布。肝断面常规放置1~2根引流管。
1.4 术后管理
术后治疗包括抗感染、保肝、维持内环境稳定、营养支持等。术后第2天拔出胃管开始饮水,有肠鸣音后可进流质食物。术后2、5、7 d常规复查血常规、肝功能、肾功能等指标。拔腹腔引流管前常规复查腹部超声。肝功能基本恢复,无残留感染,可顺利进食、排便、适当活动,即可出院。
1.5 观察指标
肝切除范围≤2个肝段定义为小范围肝切除,>2个肝段定义为大范围肝切除[12],分别统计以下指标。
手术时间、术中失血量、肝门阻断时间由麻醉医师负责统计,术中失血量为吸引瓶中液体总量减去冲洗用水。
术后肝功能不全采用Balzan等[13]提出的术后第5天血清总胆红素仍然高于50 μmol/L和(或)凝血酶原活度低于50%,且排除胆道损伤。术后胆漏诊断标准按照国际肝脏外科学组的诊断标准[14]:术后第3天腹腔引流管中总胆红素水平大于血清总胆红素水平3倍。断面积液定义为术后需要超声穿刺处理的肝断面积液。
1.6 统计学方法
2 结果
2.1 2组手术及术后情况
2组手术时间、术中出血量、术中输血率、肝门阻断时间、中转开腹率、术后并发症发生率、术后住院时间差异均无统计学意义,见表2。肝功能不全均通过保肝、纠正凝血、维持内环境稳定等治疗治愈。胆漏及断面积液均经保守治疗或超声引导下穿刺引流治愈。无死亡。
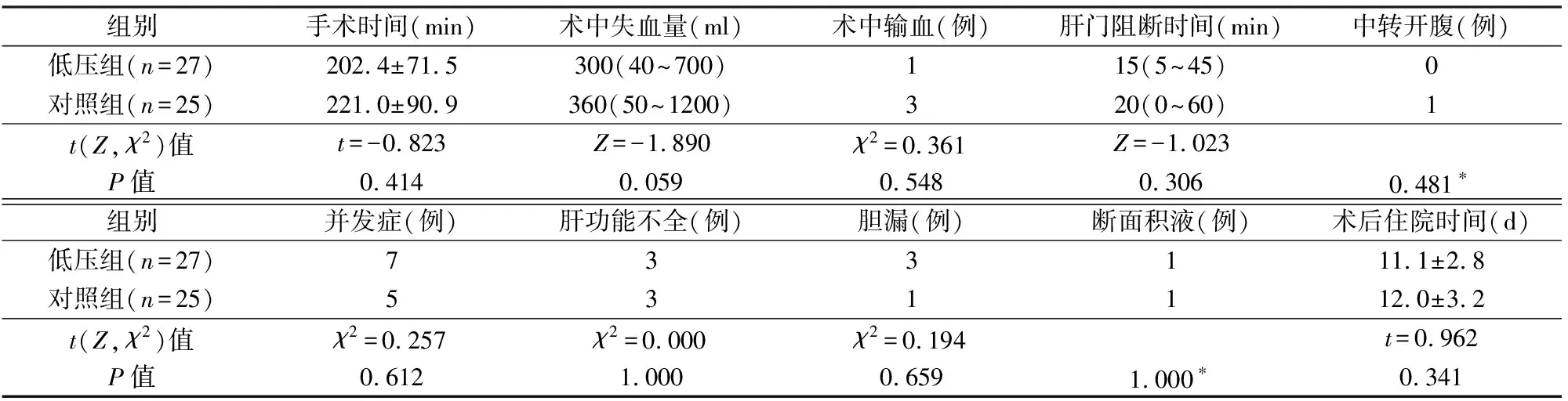
表2 2组观察指标比较
*Fisher确切概率法
2.2 小范围及大范围肝切除时2组观察指标比较
小范围肝切除时,低压组与对照组在手术时间、术中失血量、肝门阻断时间、术后并发症、术后住院时间方面差异均无统计学意义(P>0.05),见表3,2组均无术中输血。但在大范围肝切除时,低压组手术时间短,术中出血少,肝门阻断时间及术后住院时间短(P<0.05),见表4。
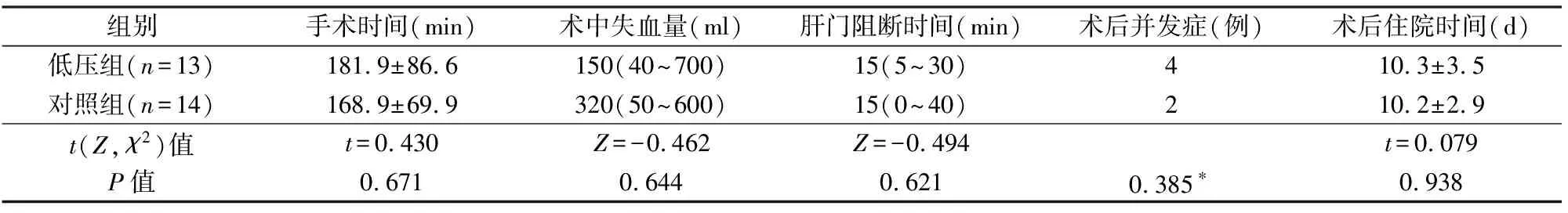
表3 小范围肝切除时2组观察指标比较
*Fisher确切概率法
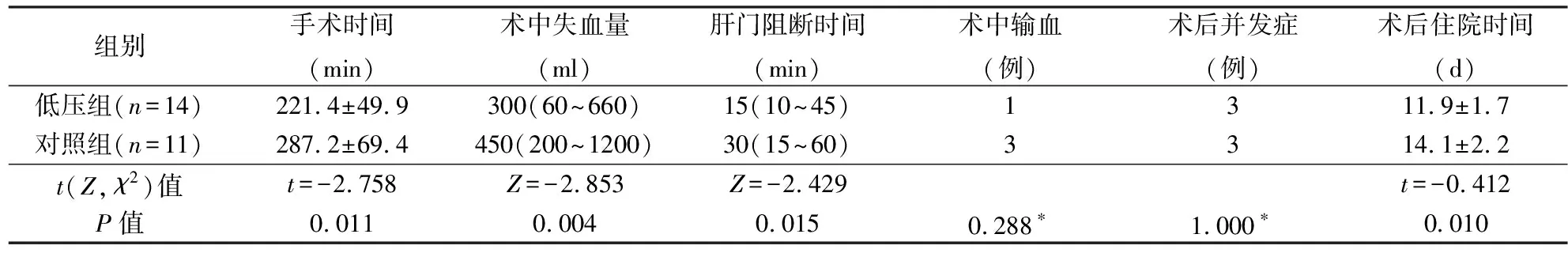
表4 大范围肝切除时2组观察指标比较
*Fisher确切概率法
3 讨论
Pringle阻断技术应用后,肝静脉出血成为肝切除过程中出血的主要来源。由于肝静脉无静脉瓣膜,其压力与中心静脉压力相关,降低中心静脉压即可降低肝静脉压,达到减少术中出血的目的。多项研究证实,CLCVP可显著减少开腹肝切除术中出血,缩短肝门阻断时间,同时降低术后并发症[15~18]。然而CLCVP技术在腹腔镜肝切除中的有效性及安全性尚未得到证实。
3.1 CLCVP与术中出血
Takagi等[19]报道当气腹压力>10 mm Hg时,门静脉血流开始减少,当压力达到16 mm Hg时,门静脉血流量可降低至基线的1/10。McLaughlin等[20]对腹腔镜胆囊切除患者的血流动力学研究显示,当气腹压力达到15 mm Hg时,心输出量(CO)以及每搏输出量(SV)降低30%。Trendelenburg体位也会导致平均动脉压以及心指数明显降低[21]。上述血流动力学的改变,加上腹腔镜下良好的手术操作视野,使腹腔镜肝切除术中出血量往往较开腹肝切除明显减少。这一推论在多个临床研究中得到印证[6,22]。那么腹腔镜肝切除过程中,是否仍有必要使用CLCVP减少中出血?
本研究结果显示,小范围肝切除时,CLCVP并未减少术中出血,其原因可能与术中出血量本身不多有关。当大范围肝切除时,低压组与对照组比较出血量明显减少,表明腹腔镜肝切除过程中CLCVP仍然有助于减少术中出血。CLCVP导致肝血窦压力降低后,断面显露更加清晰,超声刀、LigaSure等能量设备止血效果更好,肝门阻断时间随之下降,减少术后发生肝功能不全的风险。同时,由于断面处理更加确切,避免术中对断面反复烧灼、缝扎止血所耗费的时间,缩短了整个手术进程,降低手术对患者的打击,缩短住院日。
3.2 CLCVP与空气栓塞
Bryant等[23]报道腹腔镜肝切除术中空气栓塞发生率为1.72%,Dagher等[24]报道210例腹腔镜肝切除术发生空气栓塞3例(1.43%)。Jayaraman等[25]动物实验表明,空气栓塞发生率与气腹压及中心静脉压的比值有关,当比值升高时,空气栓塞发生率明显增加。因此,在腹腔镜肝切除时,使用CLCVP的确可能增加CO2栓塞风险。但由于CO2在血浆中溶解率高,腹腔镜下绝大部分CO2栓塞均不会对身体机体产生显著影响。本研究未观察到有临床意义的空气栓塞发生。但Jayaraman等[25]的研究指出,当涉及较大肝静脉周围操作时,应当适当降低气腹压力,升高中心静脉压,缩小气腹压力与中心静脉压比值,避免严重的CO2栓塞。
3.3 CLCVP与急性肾损伤
CLCVP时常会使用小剂量硝酸甘油同时限制液体输入,上述操作在降低中心静脉压的同时,常会带来动脉压力降低,为了维持足够的动脉压,目前的方案是使用小剂量多巴胺,维持SBP>90 mm Hg或MAP>60 mm Hg,从而保证肾及其他重要脏器灌注。目前大部分学者认为,肝切除中CLCVP的应用并不会增加急性肾损伤发生的风险[6,20,22]。Correa-Gallego等[26]总结2116例CLCVP辅助下肝切除资料,术后急性肾损伤发生率<1%。张日新等[27]对51例腹腔镜肝切除的研究同样未能观察到明显肾功能损害。本研究低压组术后亦未发生显著的肾功能损害,验证了腹腔镜肝切除时使用CLCVP技术的安全性。
本研究结果显示,腹腔镜肝切除术中应用CLCVP技术是安全、有效的。小范围肝切除时是否采用CLCVP对手术及术后指标影响不大;当大范围肝切除时,使用CLCVP技术可明显减少术中出血量、缩短肝门阻断时间、缩短手术时间,同时缩短住院时间,值得临床推广应用。

