小叶三点金醇提物对尖吻蝮蛇毒的抑制作用*
和七一,余晓东,李博,熊艳,肖静
(重庆师范大学生命科学学院∥教育部活性物质生物技术工程研究中心∥重庆市生物活性物质工程研究中心, 重庆401331 )
毒蛇咬伤是一个严重的公众健康问题,尤其在热带和亚热带地区。据不完全统计,全球每年有超过500万蛇伤事件发生,造成约2.5万~12.5万人丧生[1-2]。为此,2009年,世界卫生组织首次将毒蛇咬伤认定为一种长期被忽视的人类健康问题[3]。在中国,每年有近10万人被毒蛇咬伤,蛇伤致死率高达5%~10%[4]。尖吻蝮蛇Deinagkistrodonacutus是中国特有蛇种,蛇毒中富含金属蛋白酶、丝氨酸蛋白酶、磷脂酶A2和去整合素家族,蛇伤后易造成组织水肿、坏死、出血、血液不凝等症状,并引发全身多器官功能衰竭,致死致残率极高[5]。抗蛇毒血清作为一种有效的蛇伤治疗药物,在实际应用中,也暴露出一些不足,如保存不便、价格昂贵、适用范围狭窄、可能引起过敏反应等等[6]。近年来,国内外学者发现大量中草药提取物或其组分具有抑制蛇毒的作用[7-10],为蛇伤药物的研究开发提供了新的思路。小叶三点金Desmodiummicrophyllum为豆科三蚂蝗属植物,具有清热解毒、利湿通络、消炎止血、活血化瘀的功效,用于治疗尿路感染、糖尿病、泌尿系结石、慢性胃炎、慢性气管炎等症[11]。在民间,小叶三点金常被用于治疗毒蛇咬伤,但其对蛇毒的抑制效果及其作用机制国内外尚无研究报道。本研究以尖吻蝮蛇毒为研究对象,重点研究小叶三点金醇提物在体外对蛇毒中蛋白质水解酶、磷脂酶A2、透明质酸酶、纤维蛋白水解酶活性的抑制作用;通过体内动物实验,研究小叶三点金醇提物对蛇毒引起的小鼠出血、水肿、组织坏死以及致死作用的中和能力。探究小叶三点金对尖吻蝮蛇毒体外、体内活性的抑制作用,为其治疗蛇伤作用提供科学依据。
1 材料与方法
1.1 材料
小叶三点金采于重庆市北碚区,经鉴定为小叶三点金,阴干后保存备用。成年五步蛇采用咬皿法取毒,冷冻干燥后低温保存备用。
1.2 试剂与仪器设备
CK试剂盒,南京建成生物工程研究所;琼脂糖,酪蛋白,纤维蛋白原,Biosharp公司;透明质酸钠,XiyaReagent公司;溴代十六烷基三甲胺,Amresco公司;丙烯酰胺,甲叉双丙烯酰胺,考马斯亮蓝R250,鼎国生物;SDS-PAGE蛋白上样缓冲液(5×),上海碧云天生物技术有限公司。
主要仪器与设备:四川蜀科TGL-20高速冷冻离心机,Christ RVC2-18真空离心浓缩仪,北京博医康FD-1A-50冻干机,东莞大华DH-HP80A恒温恒湿培养箱,北京君意东方JY-SCZ2+电泳仪,巩义宇翔RE-52A旋转蒸发器。
1.3 实验方法
1.3.1 小叶三点金醇提物制备 称取小叶三点金500 g,切碎后浸泡于1 000 mLφ=75%乙醇中,加热回流萃取1 h,过滤得提取液,重复提取3次。将3次提取液10 000 r/min转速离心10 min,所得上清液低压旋转浓缩回收乙醇,剩余浸膏冷冻干燥后,-20 ℃保存备用。
1.3.2 对蛋白水解酶活力的抑制作用 蛋白水解酶活力检测参照Okoroma等[12]的方法进行。称取琼脂糖和酪蛋白各1 g,加入100 mL PBS缓冲液(50 mmol/L pH 7.5),溶解后倒板,待平板冷却后打孔。取10 μL尖吻蝮蛇毒(2 μg/μL)加入点样孔内,37 ℃孵育过夜。平板经考马斯亮蓝R-250染色,脱色液脱色后测量透明圈直径。抑制作用检测:不同质量比的蛇毒与小叶三点金醇提物[m(蛇毒)∶m(提取物):1∶5、1∶25、1∶50、1∶100]预先在37 ℃孵育30 min,再按照上述方法进行活性检测,重复3次。以单独蛇毒组作为阳性对照,蛋白水解酶活力定义为100%。
1.3.3 对磷脂酶A2活力的抑制作用 磷脂酶A2活力检测参照Habermann和Hardt[13]的方法进行。称取1 g琼脂糖,加入100 mL醋酸钠缓冲液(50 mmol/L pH 6.5),溶解后冷却至50 ℃,加入φ=4%蛋黄液(蛋黄与w=0.85% NaCl溶液按1∶3的比例混合,然后于3 000 r/min离心5 min,取上清)以及c=2% 10 mmol/L CaCl2溶液,混合后倒板,待板凝固后,打孔。取10 μL尖吻蝮蛇毒(1 μg/μL)加入上样孔内,37 ℃孵育9 h后测量透明圈直径。抑制作用检测:不同质量比的蛇毒与小叶三点金醇提物[m(蛇毒)∶m(提取物):1∶5、1∶10、1∶25、1∶50]预先在37 ℃孵育30 min,再按照上述方法进行活性检测,重复3次。以蛇毒组作为阳性对照,磷脂酶A2活力定义为100%。
1.3.4 对透明质酸酶活力的抑制作用 透明质酸酶活力参照Singer等[14]的方法进行。称取2 g琼脂糖,加入100 mL醋酸钠缓冲液(50 mmol/L pH 5.0),溶解后50 ℃孵育备用;称取0.2 g透明质酸钠,加入100 mL相同缓冲液溶解,与琼脂糖溶液混匀后倒板,待板凝固后,打孔。取10 μL蛇毒(5 μg/μL)加入孔内,37 ℃孵育15 h后,加入w=0.75%溴代十六烷基三甲胺溶液,放置2 h后观察透明圈大小。抑制作用检测:不同质量比的蛇毒与小叶三点金醇提物[m(蛇毒)∶m(提取物):1∶5、1∶10、1∶25、1∶50]预先在37 ℃孵育30 min,再按照上述方法进行活性检测,重复3次。以蛇毒组作为阳性对照,透明质酸酶活力定义为100%。
1.3.5 对纤维蛋白原水解酶活力的抑制作用 纤维蛋白原水解酶活力参照Edgar和Prentice[15]的方法进行检测。取20 μL尖吻蝮蛇毒(1 μg/μL)与等体积牛纤维蛋白原(20 μg/μL)37 ℃孵育1 h,加入10 μL 5×蛋白质变性电泳上样缓冲液,混匀后沸水加热5 min,于w=12% SDS-PAGE凝胶电泳检测。抑制作用检测:不同质量比的蛇毒与小叶三点金醇提物[m(蛇毒)∶m(提取物):1∶5、1∶10、1∶25、1∶50、1∶100]预先在37 ℃孵育30 min,再按照上述方法进行活性检测,重复3次。以纤维蛋白原组和蛇毒组作为对照,对抑制结果进行判定。
1.3.6 对蛇毒出血活性的中和作用 蛇毒出血活性的测定参考Roodt等[16]的方法进行。取昆明小鼠(20±2)g 30只,随机分为5组,蛇毒组每只小鼠皮下注射100 μL尖吻蝮蛇毒(0.2 μg/μL);对照组每只小鼠注射100 μL生理盐水,注射后3 h,动物经乙醚深度麻醉致死,解剖观察皮下出血情况;抑制作用检测:不同质量比的蛇毒与小叶三点金醇提物[m(蛇毒)∶m(提取物):1∶25、1∶50、1∶100]预先在37 ℃孵育30 min,再按照上述方法进行活性检测。以蛇毒组引起的出血活性定义为100%。
1.3.7 对蛇毒水肿活性的中和作用 蛇毒水肿活性的测定参考Maiorano等[17]的方法进行。取昆明小鼠(20±2 g)30只,随机分为5组,蛇毒组每只小鼠足趾注射20 μL尖吻蝮蛇毒(0.15 μg/μL),对照组每只小鼠注射20 μL生理盐水,每隔1 h用游标卡尺测量小鼠脚掌厚度。抑制作用检测:不同质量比的蛇毒与小叶三点金醇提物[m(蛇毒)∶m(提取物):1∶25、1∶50、1∶100]预先在37 ℃孵育30 min,再按照上述方法进行活性检测。小鼠脚掌的肿胀率=(注射后某时刻脚掌厚度-注射前脚掌厚度)/注射前脚掌厚度。
1.3.8 对蛇毒组织坏死活性的中和作用 蛇毒组织坏死活性的测定参考Mebs等[18]的方法进行。取昆明小鼠(20±2)g 30只,随机分为5组,蛇毒组每只小鼠肌肉注射50 μL尖吻蝮蛇毒(1 μg/μL);对照组每只小鼠注射50 μL生理盐水,注射后3 h,小鼠眼球取血制备血清,对肌酸激酶活性进行检测。抑制作用检测:不同质量比的蛇毒与小叶三点金醇提物[m(蛇毒)∶m(提取物):1∶25、1∶50、1∶100]预先在37 ℃孵育30 min,再按照上述方法进行活性检测。以蛇毒组引起的肌酸激酶活性定义为100%。
1.3.9 蛇毒致死及中和作用研究 尖吻蝮蛇毒半致死剂量(The median lethal dose,LD50)的测定根据Meier和Theakston[19]的方法进行。选取40只昆明雄性小鼠(20±2)g,随机分为5组,分别于腹腔注射200 μL不同质量分数的尖吻蝮蛇毒(1.0、2.0、3.0、4.0、5.0 mg/kg),观察24 h内小鼠死亡数。结果采用SPSS软件Pbobit模块进行统计分析。中和蛇毒致死作用的研究,选取48只昆明雄性小鼠(20±2)g,随机分为6组。2LD50尖吻蝮蛇毒分别与不同质量比的小叶三点金醇提物[m(蛇毒)∶m(提取物):1∶25、1∶50、1∶100]在37 ℃孵育30 min,按照上述方法进行注射,以尖吻蝮蛇毒、生理盐水以及高剂量提取物作为对照,记录小鼠24 h内的生存状况。
1.3.10 数据分析与处理 采用SPSS 18.0 软件one-way ANOVA对数据进行分析,P< 0.05为差异具有统计学意义。
2 结果与分析
2.1 小叶三点金醇提物对尖吻蝮蛇毒酶活力的抑制作用
2.1.1 对蛋白水解酶活力的抑制 尖吻蝮蛇毒中含有丰富的蛋白水解酶,如金属蛋白酶,丝氨酸蛋白酶,这些酶类能破坏动物组织、导致血液系统紊乱,引起水肿、出血以及组织坏死等症状[20]。以酪蛋白为底物检测蛇毒中蛋白水解酶的活力,结果显示,小叶三点金醇提物对尖吻蝮蛇毒中蛋白水解酶具有抑制作用,且呈显著的剂量效应关系(图1)。当蛇毒与提取物质量比为1∶25时,蛇毒蛋白水解酶活力降低35.22%;当蛇毒与提取物质量比为1∶50时,蛇毒蛋白水解酶活力降低55.15%;蛇毒与提取物质量比为1∶100时,提取物能够完全抑制蛇毒蛋白水解酶活性。
2.1.2 对磷脂酶A2活性的抑制 磷脂酶A2是一类广泛存在于蛇毒中的酶类,表现出多种生理药理功能,如出血毒性、肌肉毒性、神经毒性,心脏毒性,以及溶血活性,水肿活性和抗血小板聚集等活性[21]。卵黄琼脂糖平板结果显示(图2),当蛇毒与提取物质量比在1∶5时,可使蛇毒磷脂酶A2活力减低21.98%。而当两者比例达到1∶25时,可以完全抑制磷脂酶A2活性,提示小叶三点金对蛇毒磷脂酶A2具有显著的抑制作用。
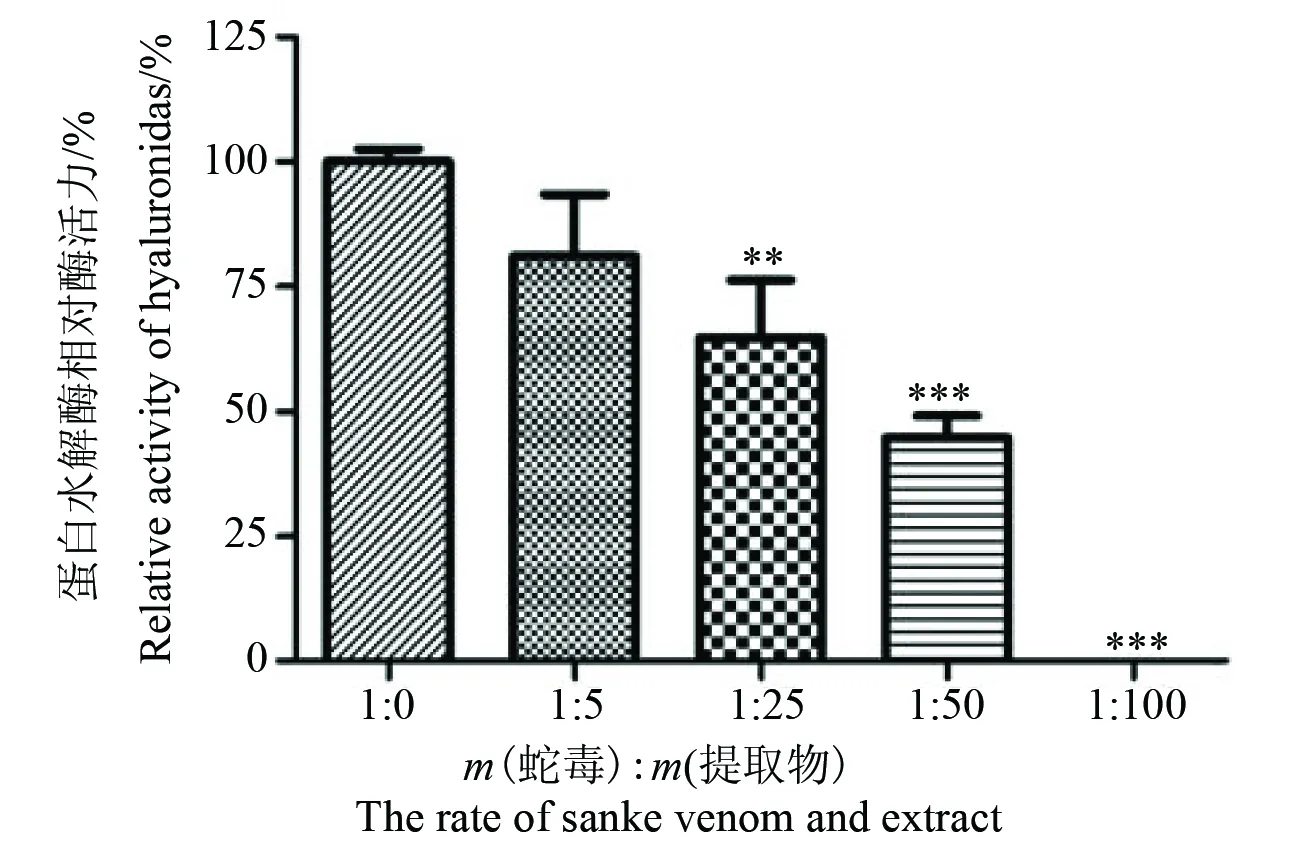
图1 小叶三点金醇提物对尖吻蝮蛇毒蛋白水解酶的抑制作用 (与蛇毒处理组比较,**∶ P < 0.05; ***: P<0.001)Fig.1 Inhibitory effect of ethanol extract of D. microphyllum on proteolytic enzyme activity from D. acutus venom
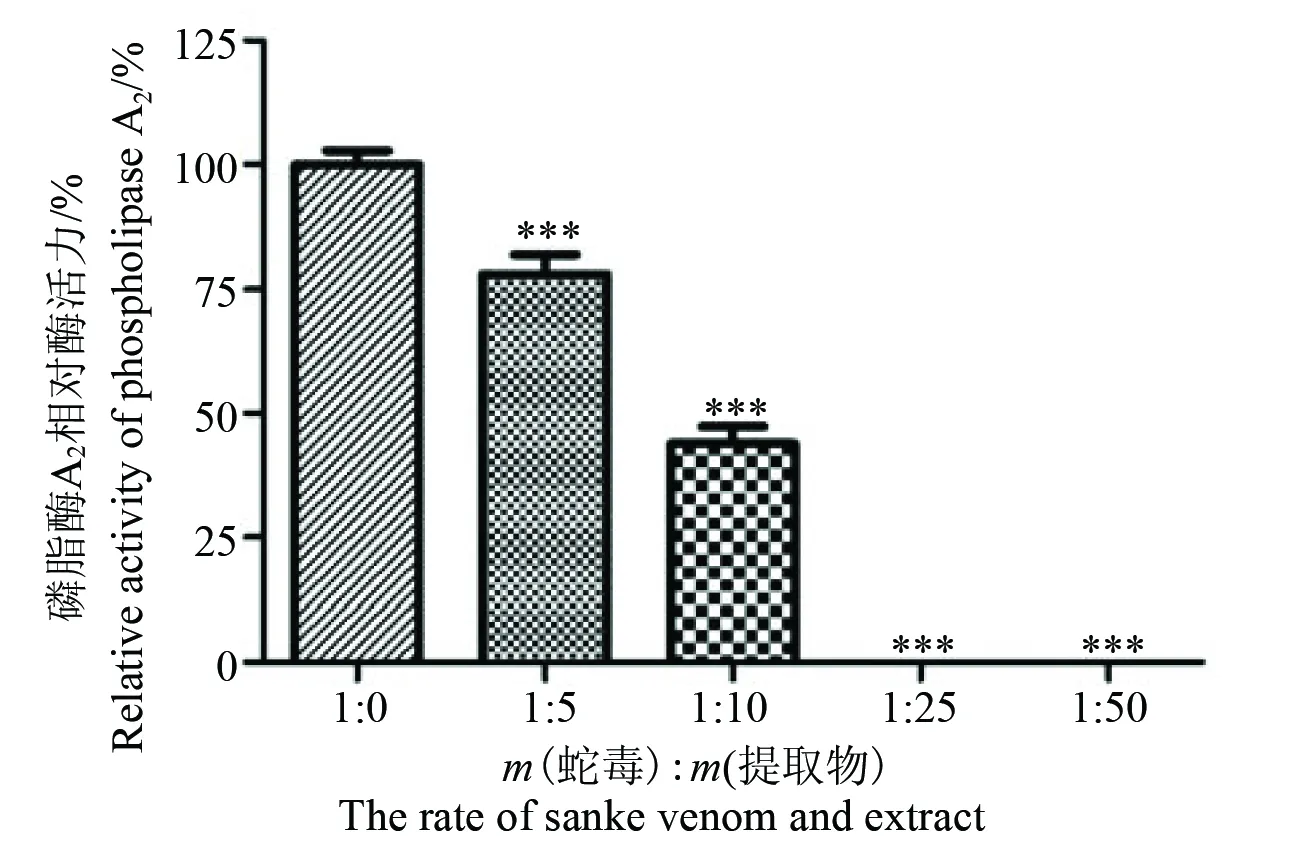
图2 小叶三点金醇提物对尖吻蝮蛇毒磷脂酶A2的抑制作用(与蛇毒处理组比较, ***: P<0.001)Fig.2 Inhibitory effect of ethanol extract of D. microphyllum on phospholipase A2 activity from D. acutus venom
2.1.3 对透明质酸酶活力的抑制 透明质酸酶存在于多种蛇毒中,尤其在蝰科蛇毒中含量较高。该酶能溶解细胞与纤维间质间的透明质酸,破坏结缔组织的完整性,促使蛇毒从局部向周围组织扩散,扩大局部毒性;同时,该酶能促使蛇毒经淋巴管和毛细血管吸收进入血液循环,加速蛇毒引发的系统性毒性,因而也被称为“扩散因子”[22]。透明质酸平板检测显示(图3),小叶三点金提取物具有显著的抑制透明质酸酶活性。当蛇毒与小叶三点金提取物质量比为1∶5时,可使蛇毒透明质酸酶活力降低51.83%;而当两者比例达到1∶25时,可以完全抑制透明质酸酶活性。
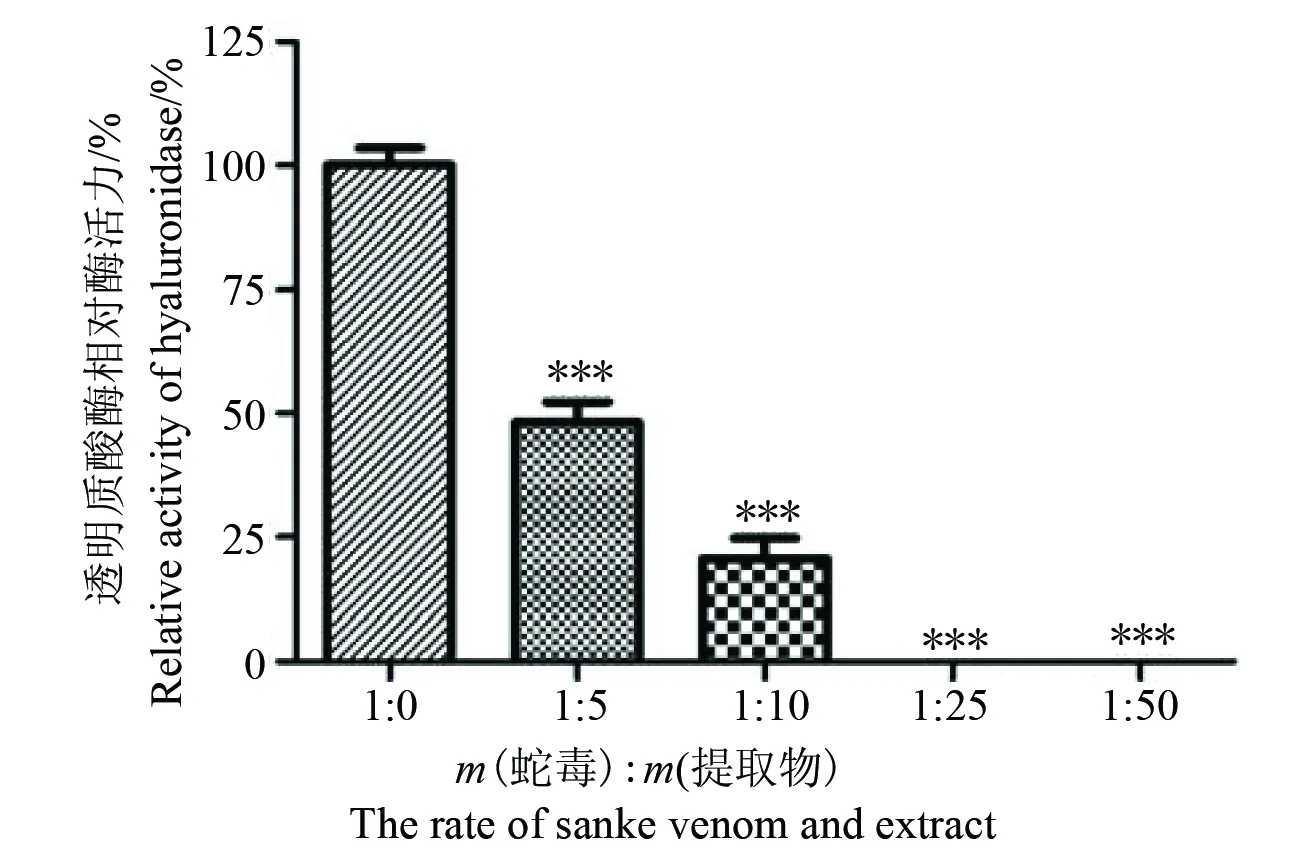
图3 小叶三点金醇提物对尖吻蝮蛇毒透明质酸酶的抑制作用(与蛇毒处理组比较, ***: P<0.001)Fig.3 Inhibitory effect of ethanol extract of D. microphyllum on hyaluronidase activity from D. acutus venom
2.1.4 小叶三点金提取物抑制蛇毒水解纤维蛋白原活性 SDS-PAGE结果显示(图4),牛纤维蛋白原呈现3条蛋白质条带,分别为Aα、Bβ、γ。在尖吻蝮蛇毒的作用下,纤维蛋白原Aα、Bβ链被降解,产生多条水解片段。当小叶三点金醇提物与蛇毒孵育后,可以有效抑制蛇毒对纤维蛋白原的降解,随着提取物浓度的增加,纤维蛋白原依次恢复正常的3条蛋白质条带,且水解片段逐渐消失。当蛇毒与小叶三点金提取物质量比为1∶5时,可以保护部分Bβ链被降解;当两者比例达到1∶10时,可以完全抑制尖吻蝮蛇毒对纤维蛋白原Bβ链的降解,保护部分Aα被降解。

图4 小叶三点金醇提物对尖吻蝮蛇毒纤维蛋白原水解酶的抑制作用Fig.4 Inhibitory effect of ethanol extract of D. microphyllum on fibrinogenolytic activity from D. acutus venom
2.2 小叶三点金醇提物对尖吻蝮蛇毒体内毒性的中和作用
2.2.1 对出血活性的中和作用 金属蛋白酶是尖吻蝮蛇毒中含量最高的一类蛋白水解酶,能够降解微血管基底膜,引发微血管壁损伤造成局部出血症状[20]。小鼠皮下出血结果显示(图5),当蛇毒与小叶三点金提取物质量比为1∶25时,可以抑制尖吻蝮蛇毒64.53%的出血活性;当两者质量比为1∶100时,可以抑制尖吻蝮蛇毒91.73%的出血活性。结合蛋白水解酶抑制实验结果,我们推测小叶三点金中存在能够与蛇毒金属蛋白酶相互作用的功效组分。

图5 小叶三点金醇提物对尖吻蝮蛇毒出血活性的中和作用Fig.5 Neutralization of ethanol extract of D. microphyllum on hemorrhagic activity from D. acutus venomA∶ 各处理组引起小鼠皮下相对出血活性. ***: 与蛇毒处理组比较, P<0.001; B∶ 各处理组小鼠皮下出血代表图谱. a:蛇毒组; b-d:分别为不同m(蛇毒) ∶ m(提取物)(1∶25, 1∶50, 1∶100)孵育30 min后处理组; e:PBS处理组
2.2.2 对水肿活性的中和作用 水肿是尖吻蝮蛇伤诱发的另一显著症状,主要涉及金属蛋白酶和磷脂酶A2的参与,引起内源性炎症因子释放从而导致水肿发生[23-24]。小鼠脚趾水肿实验结果显示(图6),小叶三点金提取物可以有效抑制尖吻蝮蛇毒引起的水肿症状,且呈剂量效应关系。在单独注射蛇毒后3 h,小鼠脚掌肿胀度达到75.17%;当蛇毒与小叶三点金提取物质量比为1∶25时,可以使肿胀度降低14.02%;当蛇毒与提取物质量比为1∶50时,可以使肿胀度降低22.30%;当两者质量比为1∶100时,可以使肿胀度降低28.82%。基于蛋白水解酶抑制实验和磷脂酶A2抑制实验,我们推测小叶三点金可能通过作用于蛇毒中这两类酶起到抑制水肿作用。
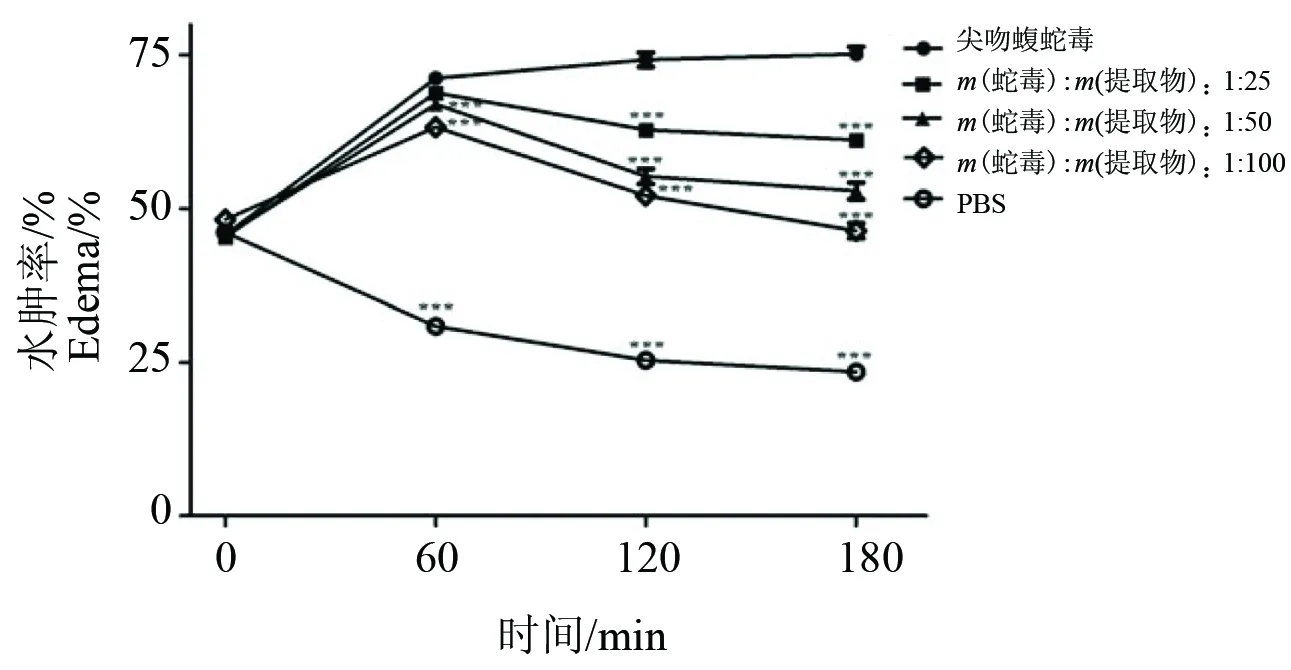
图6 小叶三点金醇提物对尖吻蝮蛇毒水肿活性的中和作用(与蛇毒处理组比较, ***:P<0.001)Fig.6 Neutralization of ethanol extract of D. microphyllum on edema activity from D. acutus venom
2.2.3 对组织坏死活性的中和作用 肌酸激酶主要存在于细胞质和线粒体中,在组织细胞内能量代谢与转运、肌肉收缩、ATP再生等方面起着重要作用。蛇伤后引起动物肌肉组织损伤,引起细胞膜破裂,肌酸激酶释放到胞外,通过检测血清中肌酸激酶含量可用来评价蛇毒导致组织损伤情况[25]。结果显示(图7),小叶三点金提取物各浓度组均能够显著的抑制尖吻蝮蛇毒诱导的肌肉毒性,且呈剂量效应关系。当蛇毒与提取物质量比为1∶100时,其肌肉毒性可以完全被抑制。
2.2.4 致死保护性实验 经小鼠腹腔注射测得,尖吻蝮蛇毒LD50为2.88 mg/kg。以2LD50尖吻蝮蛇毒作为致死剂量,分别与不同质量比的提取物孵育后注射动物,结果显示(图8),小叶三点金提取物能够显著增加小鼠存活时间,且呈量效关系。单独注射蛇毒对照组,小鼠在5 h内全部死亡;当蛇毒与提取物质量比为1∶25时,24 h内小鼠存活率达到57.14%;当蛇毒与提取物质量比为1∶50时,24 h内小鼠存活率达到85.71%;当蛇毒与提取物质量比为1∶100时,小鼠在24 h内全部存活。在生理盐水或高剂量提取物对照组中,小鼠均未表现出中毒或者致死情况(结果未显示),提示小叶三点金可以作为一种安全的蛇伤治疗制剂。
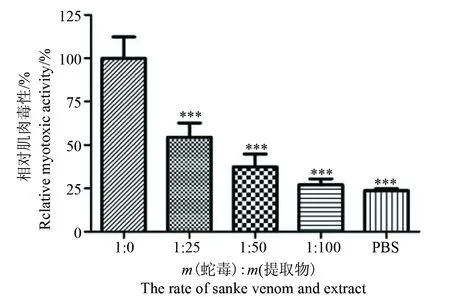
图7 小叶三点金醇提物对尖吻蝮蛇毒肌肉毒性的中和作用(与蛇毒处理组比较, ***:P<0.001)Fig.7 Neutralization of ethanol extract of D. microphyllum on myotoxic activity from D. acutus venom

图8 小叶三点金醇提物对尖吻蝮蛇毒致死活性的中和作用Fig.8 Neutralization of ethanol extract of D. microphyllum on lethal potency from D. acutus venom
3 讨 论
在中国,蛇伤是一种危害较严重的疾病,频发于农村和偏远山区,而这些地区抗蛇毒血清供应往往较为匮乏。因此,中草药常被作为蛇伤救治的首选药物。在民间,虽然大量的中草药被用于蛇伤治疗[27],然而其治疗效果缺乏科学的实验证据,治疗机制尚不清楚,难以得到大范围的推广应用。
本研究中,我们选取常用于蛇伤治疗的中草药小叶三点金为研究对象,体外酶活结果显示,小叶三点金醇提物能够有效抑制尖吻蝮蛇毒中蛋白水解酶、磷脂酶A2、透明质酸酶以及纤维蛋白原水解酶活性。体内动物实验中,尖吻蝮蛇毒引起的小鼠皮下出血、水肿、组织坏死症状可以被小叶三点金醇提物显著抑制。大量研究发现,小叶三点金中除含有蛋白质、糖类外,还含有黄酮类、酚类、生物碱类、苯丙素类以及苷类物质[27-28]。目前,研究人员已从小叶三点金中分离鉴定出9个黄酮类化合物[27]。研究证实,来源于不同植物中的黄酮类化合物能够抑制蛇伤引起的炎症和出血症状;同时,类黄酮物质,如Quercetin、kaempferol、luteolin等,还具有显著的抑制透明质酸酶活性[29]。酚类化合物是植物中一类重要的代谢产物,已经被发现具有抑制蛇毒中乙酰胆碱酯酶、蛋白水解酶、磷脂酶A2、透明质酸酶、L-氨基酸氧化酶的活性,能够抑制蛇毒引起的出血、皮肤坏死症状[7, 8, 10, 30]。生物碱是小叶三点金中含量较高的一种组分[11],该类物质也被证实具有抑制蛇毒磷脂酶A2的活性。部分植物来源的苯丙素类、苷类以及蛋白质也被发现能够通过与蛇毒中酶类或毒素相互作用发挥抗蛇毒功效[7, 8, 31]。蛇伤后引起的动物致死是由蛇毒中多种组分(蛋白酶类和毒素)共同作用的结果,保护性实验显示,小叶三点金能够显著延长实验小鼠存活时间,提示其可能通过多组分多途径发挥协同效应,从而达到抑制蛇毒活性的作用。
本研究首次证实了小叶三点金具有抑制尖吻蝮蛇毒的功效,为该中草药在蛇伤救治中的应用提供了科学依据。然而,小叶三点金中抗蛇毒功效组分的筛选、鉴定及其作用机制尚需进一步研究。

