复合酶处理废弃烟末制备烟用美拉德香精
游 霞, 刘彩红, 崔步云, 李雅琪, 韦凤杰, 吴鸣建*
(1.郑州大学 化工与能源学院,河南 郑州 450001;2.河南烟草公司,河南 郑州 450002)
关键字:烟草废弃物;淀粉酶;美拉德反应;GC-MS分析
中国烟草的种植面积和产量均居世界前列,但其中20%~30%烟叶是不能用作卷烟原料的,这不仅浪费资源,还污染环境,因此合理综合利用烟草废弃物变得尤为重要[1]。
美拉德反应又称为非酶棕色化反应,主要是氨基化合物与羰基化合物之间的复杂反应,美拉德反应会产生很多致香物质,其中大部分也是烟草中重要的香味成分。目前对烟草废弃物的综合利用主要是从中提取茄尼醇、烟碱、蛋白质、果胶、烟酰胺和黄酮类等物质,但附加值较低。烟草中水溶性糖中还原糖的质量分数可达25%,非还原糖可达5%;不溶性的多糖中淀粉和果胶的质量分数可达8%,在酶的作用下水解为单糖,即能为美拉德反应提供足够的碳源[2-10]。
利用美拉德反应制备的烟用香精,因其具有天然、健康和安全的特性而倍受青睐[11],大部分研究主要集中在以单糖和氨基酸为原料来来研究美拉德反应[12],而以烟草废弃物为原料的研究较少。作者是以烟草废弃物为原料来制备美拉德烟用香精,作者以α-淀粉酶和β-淀粉酶的复合酶处理烟草废弃物,以复合酶解液为主要碳源,外加氨基酸为氮源,通过美拉德反应制备烟用香精;采用GC-MS分析美拉德反应产物的化学成分,并评价其感官效果,以期为烟用香精的制备和烟草废弃物的利用化提供技术指导。
1 材料与方法
1.1 材料与设备
烟草废弃物:由河南省平顶山烟叶示范田提供,50℃烘干,粉碎,过80目筛;α-淀粉酶和β-淀粉酶:南宁庞博生物工程有限公司提供;其他试剂均为分析纯。
FW-400A倾斜式高速万能粉碎机:北京中兴伟业仪器有限公司产品;98-3数显磁力搅拌器:郑州凯鹏实验仪器有限公司产品;752N紫外可见分光光度计:上海精密科学仪器有限公司产品;Agilent7890A/5975C气相色谱质谱联用仪:美国安捷伦科技有限公司产品。
1.2 实验方法
1.2.1 美拉德反应基液的制备 将废弃烟末置于圆底烧瓶中,按照一定料液质量体积比加入柠檬酸-柠檬酸钠缓冲溶液,加入α-淀粉酶和β-淀粉酶,调节pH,在适当的温度下电动搅拌反应一段时间。在5000r/min下离心30min,取上清液,旋蒸浓缩。
1.2.2 美拉德反应 在装有温度计、回流冷凝管的烧瓶中依次加入美拉德反应基液、丙二醇与水的混合溶剂60 mL,用质量分数10%NaOH或6 mol/LHCl调节pH,在115℃下,反应5 h,反应结束后,在冰水浴中冷却。
1.2.3 还原糖和水溶性总糖的测定 还原糖:参考文献[5]提供的方法;水溶性总糖:DNS比色法。
1.2.4 美拉德反应产物质量评定
1)褐变程度的测定 取1 mL美拉德反应产物使其溶于10 mL的蒸馏水中,参比为蒸馏水,在752N型紫外分光光度计下测定420 nm下的吸光值,吸光值越大,其颜色强度就越大,说明美拉德反应越充分,得到的反应物色泽越好[6]。
2)风味评价 把制备的Maillard反应产物样品装入喷雾器中,喷雾器喷洒到低档次的烟丝上,其中确保喷物量为烟丝质量的1.5‰,把喷洒过的烟丝经过相应处理后,由评吸小组进行感官评吸[8],对其香气、光泽、协调性、刺激性、余味、杂气6项指标进行评吸打分,评分标准如表1。
1.2.5 GC-MS分析条件
1)美拉德反应产物醚溶性成分的分离 取30 mL美拉德反应的产物,加15 g NaCl使其饱和,再分别加入40、40、20 mL乙醚,依次萃取,然后用无水硫酸钠干燥,过滤,在旋转蒸发仪中浓缩至1mL,进行气质联用仪器分析[7]。
2)色谱检测条件 色谱柱:DB-5MS(30 m×0.25 mm×0.25 μm); 程序升温:60 ℃保持 3 min,以5℃/min的速度升至250℃,并保持20 min;进样温度:250 ℃;载气:纯 He,载气流量:1 mL/min;分流比 10∶1;进样量为 1 μL。

表1 各单项指标评分标准Table 1 Score standard about each single index
3)质谱检测条件 离子源温度:230℃;质量扫描范围为35~500;离子源电子能量:60 eV。MS谱图:NIST质谱数据图进行检索。
2 结果与讨论
2.1 单一酶酶解对还原糖质量体积浓度的影响
由图1可看出,酶解液上清液中还原糖的质量浓度随着酶用量的增加而增加,最后趋于平衡。α-淀粉酶质量分数在0~0.1%之间时,还原糖的质量浓度随着α-淀粉酶质量分数的增加而快速增加,在0.1%~0.2%之间时,α-淀粉酶质量分数增加速率明显没有在0~0.1%的快,当α-淀粉酶质量分数为0.2%时,还原糖质量浓度达到最大值,再继续增加α-淀粉酶用量对还原糖质量浓度几乎没有变化,因此α-淀粉酶用量的最适区间为0.1%~0.2%。

图1 α-淀粉酶和β-淀粉酶质量分数对还原糖质量浓度的影响Fig.1 Influence of α-Amylase and β-Amylase content on the quality volume concentration of reducing sugar
β-淀粉酶质量分数在0~2.0%时,还原糖的质量浓度随着β-淀粉酶质量分数的增加而剧烈增加,当β-淀粉酶质量分数在2.0%~3.5%时,还原糖质量浓度虽随着β-淀粉酶质量分数增加而增加,但增加幅度明显没有在0~2%之间变化的大,仍有增长的趋势。因此,选择β-淀粉酶的最适质量分数变化范围为2%~3%。
2.2 复合酶配比组合的筛选
由图2可看出,当双酶复配时,会表现出不同于两种酶的活性,可促进反应,也可抑制反应。整体还原糖的质量体积浓度先随着复合酶用量的增加而增加,增加到最大值,接着还原糖的质量体积浓度随复合酶用量增加又降低。当α-淀粉酶用量变化时,总体变化趋势是一致的,当β-淀粉酶质量分数在2%~3%时,会发现两条曲线几乎是重合的,还原糖的质量浓度成上升趋势,说明在这区间,α-淀粉酶的用量对还原糖的质量浓度影响很小;当β-淀粉酶质量分数在3%~4%时,两条曲线完全分开,此时还原糖的质量浓度呈下降趋势,α-淀粉酶质量分数为在0.2%时,还原糖的质量浓度相对高点。综合可得双酶复配组合最佳为:质量分数0.2%α-淀粉酶+3%β-淀粉酶。
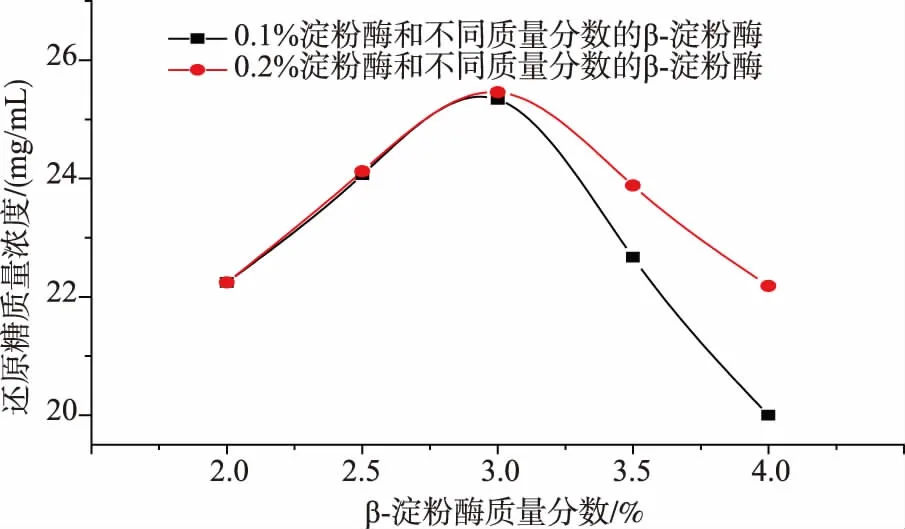
图2 复合酶质量分数对还原糖质量浓度的影响Fig.2 Influence of compound enzyme content on the quality volume concentration of reducing sugar
2.3 复合酶酶解单因素实验分析
将质量分数0.2%α-淀粉酶和3%β-淀粉酶对废弃烟末进行酶解,分别考察酶解时间、酶解温度和酶解pH对酶解的影响。
2.3.1 酶解温度对复合酶酶解废弃烟末效果的影响 由图3可见,酶解液上清液中还原糖质量浓度是先增加至最大值后降低的趋势。在温度由30℃开始升高时,热运动加快,使酶的反应速度加快,温度至50℃时,这时还原糖的质量浓度达到最大值,继续增加温度,酶的反应速度会快速降低,此时温度过高会使酶蛋白的结构发生变化,导致蛋白酶部分失活,因此复合酶的最适温度为50℃。

图3 温度对还原糖质量浓度的影响Fig.3 Influence of compound enzyme content on the quality volume concentration of reducing sugar
2.3.2 酶解时间对复合酶酶解废弃烟末的影响由图4可以看出,还原糖的质量浓度总体变化趋势是:先增加最后趋于平衡的。在1~7 h内,说明溶液中有足够的多糖与酶结合,使还原糖质量浓度增加,速度也比较快,随着反应的进行,多糖逐渐消耗,与酶结合量减少,当反应进行到7 h时,还原糖的质量浓度到达最大值,之后缓慢变化,趋于平衡。因此,时间的最佳选择为7 h。
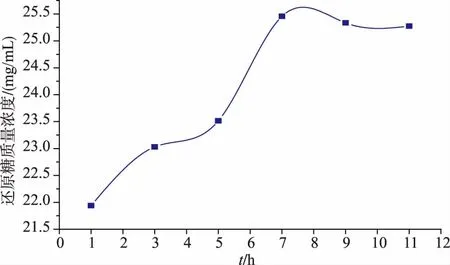
图4 时间对还原糖质量体积浓度的影响Fig.4 Influence of reaction time on the quality volume concentration of reducing sugar
2.3.3 酶解pH对复合酶酶解废弃烟末效果的影响由图5可看出,还原糖的质量浓度变化的整体趋势是:随着pH值的增加先增加后降低的。随着pH的增加,酶活性随pH的增加而变大,当pH值增加到5.4时,还原糖的质量浓度达到最大值25.46 mg/mL,此时酶的反应速率也是最快的,随着pH的继续增加,酶催化活性受到抑制,反应速率降低,还原糖的质量体积浓度也有所降低。因此,复合酶的最适pH值为5.4。
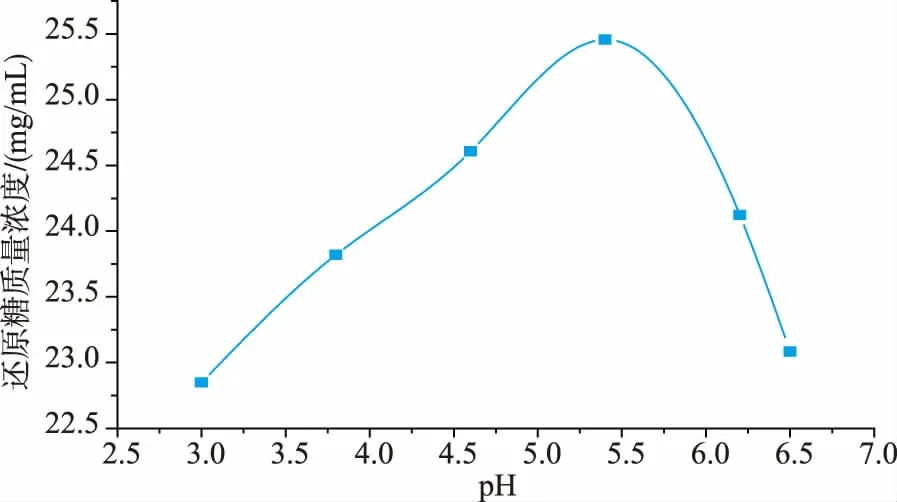
图5 pH对还原糖质量浓度的影响Fig.5 Influence of pH on the quality volume concentration of reducing sugar
2.4 美拉德反应工艺的优化
2.4.1 氨基酸种类的确定 根据酶解液中还原糖的质量体积浓度计算出浓缩液中还原糖的质量,采用氨基酸与糖类的摩尔比为1∶1进行美拉德反应。各取3 g的L-丙氨酸、L-谷氨酸、L-半胱氨酸、L-胱氨酸、L-苯丙氨酸分别与 6.06、3.67、4.46、2.25、3.25 g的复合酶酶解的浓缩液加入圆底烧瓶中,再加入51 mL的1,2-丙二醇与9 mL的蒸馏水,用质量分数10%NaOH或6 mol/L HCl调节pH 7,反应温度为100℃,在磁力搅拌器中回流5 h。经过相应的处理,测定美拉德反应产物的颜色强度和评吸得分,结果见图6。
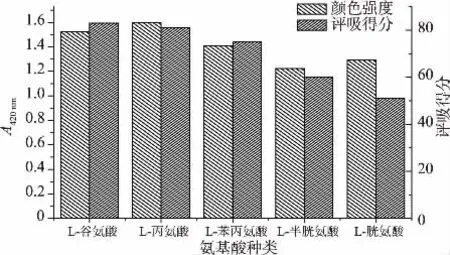
图6 氨基酸的种类对美拉德反应的影响Fig.6 Effect of the kind of amino acid on Maillard reaction
氨基酸种类的不同,会使美拉德反应速率不同,其美拉德反应产物的组成与香气特征也不同,由图6可知,L-谷氨酸、L-丙氨酸、L-苯丙氨酸、L-半胱氨酸、L-胱氨酸的颜色强度分别为:1.521、1.6、1.41、1.223、1.295,L-丙氨酸数值最高, 说明其反应比其他氨基酸反应充分。评吸得分分别为83、81、75、60、51,虽然 L-谷氨酸评吸得分最高,但其反应程度没有L-丙氨酸大,因此选择氨基酸为L-丙氨酸。
2.4.2 正交试验优化美拉德反应的工艺 试验中,根据含水量、反应时间、反应温度和pH值等因素的影响,设计正交试验(如表2)在不同条件下合成了一系列新型香料。通过感官评吸和褐变程度,确定试验的最佳条件。
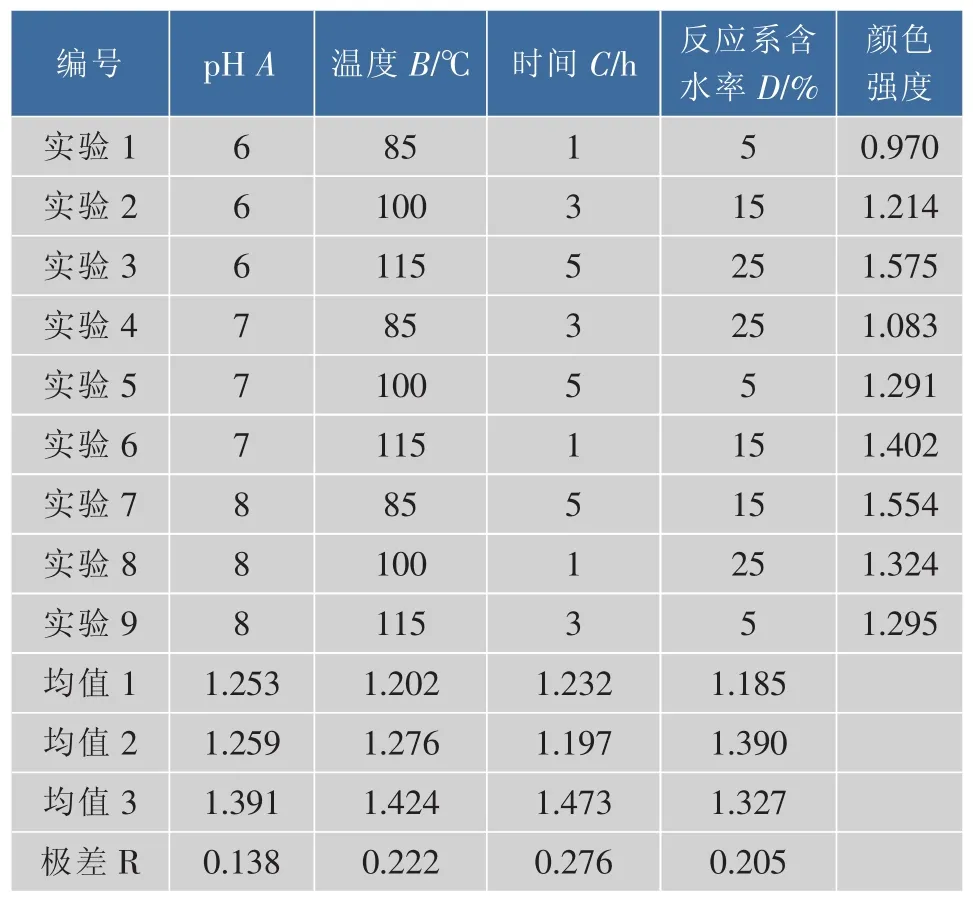
表 2 3 水平 4 因素 L9(34)正交表Table 2 Orthogonal table for L9(34)
由表2的数据可知:pH值、温度、时间、反应系含水率对颜色强度的影响大小。极差的值表现出因素对颜色强度的影响情况,极差值越大,说明对颜色强度的影响越深。右表2可知,4个因素的极差值由大到小分别为:R时间>R温度>R反应系含水率>RpH值。 可知时间对美拉德反应影响最深,其次,温度,影响最小的则为pH值。
按均值选取最佳水平。通过比较每个因素的3个均值大小,选择均值最大的为最佳水平,最佳水平为A3B3C3D2。也就是,美拉德反应的最佳条件为:pH值为8、温度115℃、反应时间5 h、水质量分数为15%。在此条件下重复进行3次试验,得到颜色强度的平均值为1.617,根据卷烟评吸程序得到的评吸得分的平均值为79。总体上来说,美拉德反应产物的香气比较纯正、干净,刺激性小。
2.4.3 美拉德反应产物的GC-MS分析 酶解烟草废弃物进行美拉德反应得到的产物,共检测出100种物质,其中与烟草香味有关的化合物有57种,所占的相对百分含量为71.277%,如图7各种致香成分所占百分比。主要包括吡嗪类、吡咯类、吡啶类、吲哚类、醇类、酸类、呋喃类、酮类、酯类、醛类、酚类、羰基类、芳香族类、烷烃类等,这些物质大多数由美拉德反应产生的,作为烟用香精能产生较好的陈烟香,略带甜香,烟气细顺。
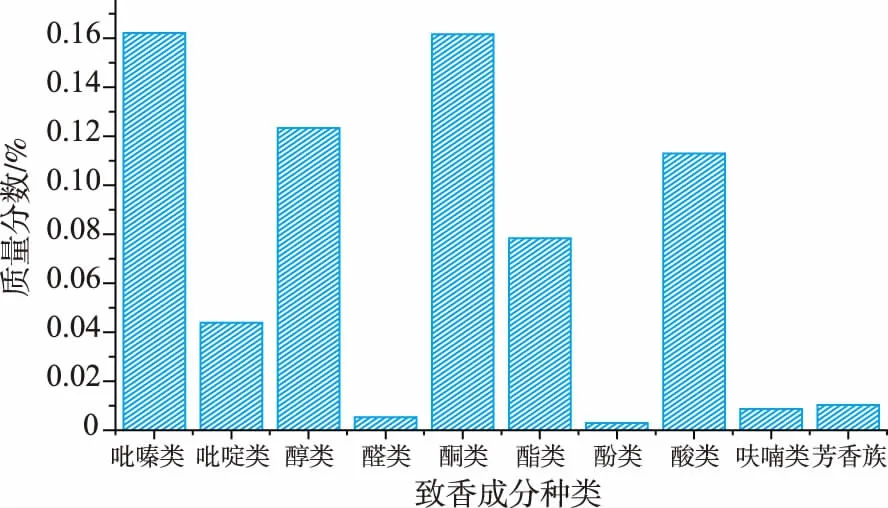
图7 致香成分质量分数Fig.7 Percentage of aroma components
3 结语
作者以烟草废弃物为原料,以还原糖得率为指标,通过单因素试验,确定酶法制备美拉德反应基液的工艺为:质量分数0.2%α-淀粉酶与3%β-淀粉酶,温度为50℃,缓冲溶液pH值为5.4,反应时间为7 h,该条件下还原糖的质量浓度为25.46 mg/mL。该试验为美拉德反应提供了天然又充足的还原糖,节省了原料,使烟草废弃物得到了资源化利用。另外,利用复合酶酶促水解液和外加氨基酸进行美拉德反应,通过正交试验确定最佳反应工艺:外加氨基酸为丙氨酸,pH值为8、温度115℃、反应时间5 h、反应系含水率为15%。在最佳条件下进行的美拉德反应,通过GC-MS可检测出共检测出100种物质,其中与烟草香味有关的化合物有57种,这些物质具有沁鼻的烘烤味和甜香,能改善烟草吸食品质,促进其风味,对卷烟加香能够起到很好的修饰作用。

