兽用加米霉素研究与应用现状
李先强
(塔里木大学动物科学学院,新疆生产建设兵团塔里木畜禽科技重点实验室,新疆阿拉尔 843300)
大环内酯类抗生素(macrolides,MALs)是一类均具有14~16元大环内脂基本结构的抗生素,主要与敏感菌的核蛋白体50S亚单位的L27及L22蛋白质结合,通过对转肽作用和/或mRNA位移的阻断作用,而抑制肽链的合成与延长,影响病原菌蛋白质的合成[1]。MALs主要用作需氧革兰阳性菌和革兰阴性菌以及厌氧球菌等感染的首先药,以及对β-内酰胺类抗生素过敏或耐药情况下的替代用药。近年来,伴随着MALs在临床上的广泛与不合理应用,陆续有许多耐MALs细菌的出现,如弯曲杆菌属(Campylobacter)[2]。为此,1995年芬兰和欧盟相继禁止了泰乐菌素(tylosin)和螺旋霉素(spiramycin)用于动物促生长用饲料添加剂,以防止耐MALs的弯曲杆菌属传播给人[3]。然而,现阶段集约化与规模化养殖正处于快速发展阶段,一些如呼吸道、消化道、乳腺炎等病原菌感染引发的畜禽死淘汰率不容乐观,因此研制新型广谱高效的大环内酯类抗生素迫在眉睫。
加米霉素(gamithromycin)是法国梅里亚(Merial)动物保健公司研发的一种新型的半合成MALs兽用抗生素,通过抑制敏感菌RNA依赖性蛋白合成而起到杀菌作用。该药分别于2007年、2010年和2011年被欧洲药品局(EMA)、加拿大保健产品与食品管理局(HPFB)和美国食品与药品管理局(FDA)批准用于防治因巴氏杆菌、支原体、睡眠嗜组织菌、溶血性曼氏杆菌等引起的牛呼吸道疾病(BRD)。加米霉素作为新一代大环类脂类抗菌药,具有给药吸收快、肺部药物浓度高、抗菌活性强、毒性低以及动物可食性组织残留少等优点,具有广阔的临床应用前景。本文从加米霉素的理化性质、抗菌机理、抗菌活性、药动学、毒性与残留、临床应用等方面进行综述,为其能在我国兽医临床上的合理应用、制剂研制与新药开发等方面提供参考。
1 理化性质
加米霉素的结构式如图1所示,化学名称为13-[(2,6-二脱氧-3-C-甲基-3-O-甲基-a-L-吡喃核糖基)氧]-2-乙基-3,4,10-三脱氧3,5,8,10,12,14-六甲基-7-丙基-11[[3,4,6-三脱氧-3-(二甲氨基)-b-D-吡喃木糖基]氧]-,(2R,3S,4R,5S,8R,10R,11R,12S,13S,14R)-1-氧杂-7-氮杂环-15-单环,分子式为C40H76N2O12, 分子量为777.04。本品为白色至米黄色粉末,不易溶于水,具有吸湿性,在高温条件下稳定,对光不敏感,重结晶后只有1 种构型。加米霉素在7 a位上由单一丙基取代,该特殊结构有利于其在生理pH条件下被快速吸收,且能在肺组织中维持较长作用时间。
2 合成工艺
目前加米霉素的合成工艺主要有以下三种:①9-脱氧-8a-氮杂-8a-红霉素A为原料,在乙酸为反应溶剂,四(三苯基膦)钯为催化剂,油浴80℃的条件下与乙酸烯丙酯反应7 h后,常压加氢3 h后以10%的钯碳为催化剂,经层析技术得终产物加米霉素,收率为12%[4]。②9-脱氧-8a-氮杂-8a-红霉素A为原料与乙醛反应,在乙醇/水为反应溶剂的条件下常压氢化48 h,得终产物加米霉素,收率为62.3%。③以红霉素9,12-亚胺醚为原料,在Pt/C 5%为催化剂,温度为15~25℃和压力为50 bar的条件下与乙酸反应,再分别加入丙醛和乙酸,控制温度在40~45℃和压力为20 bar的条件下反应数小时后,得终产物加米霉素,收率为79.0%[4]。

图1 加米霉素结构式
3 抗菌机理
加米霉素作为新一代半合成氮杂内酯类抗菌药,与MALs具有相似的抗菌机理,主要通过对转肽作用和/或mRNA位移的阻断作用,抑制肽链的合成与延长而影响病原菌蛋白质的合成。加米霉素的结构与其他MALs不同,由15元半合成物组成得内酯环,且在7a位置上有着独特的烷基化氮原子,使得加米霉素不仅具有抑菌作用,还具有较强的杀菌作用[5]。目前还未见有病原菌对加米霉素的耐药现象报道。
4 药效学
加米霉素分别于2007、2010和2011年被欧洲药品局(EMA)、加拿大保健产品与食品管理局(HPFB)和美国食品与药品管理局(FDA)批准用于防治因巴氏杆菌、支原体、溶血性曼氏杆菌等引起的牛呼吸道疾病(BRD)。加米霉素皮下注射剂量按6 mg/kg可有效治疗BRD,给药组未出现BRD症状(86%)显著高于生理盐水对照组(61%),BRD发病率可降低64%[6]。另外,加米霉素推荐剂量在防治羊腐蹄病上也有很好的效果,且优于土霉素[7-8]。2016年2月,加米霉素经欧盟批准用于治疗多杀性巴氏杆菌、胸膜肺炎放线杆菌和副猪嗜血杆菌引起的猪呼吸道疾病[9],推荐剂量仍为6 mg/kg,其抗菌活性见表1。
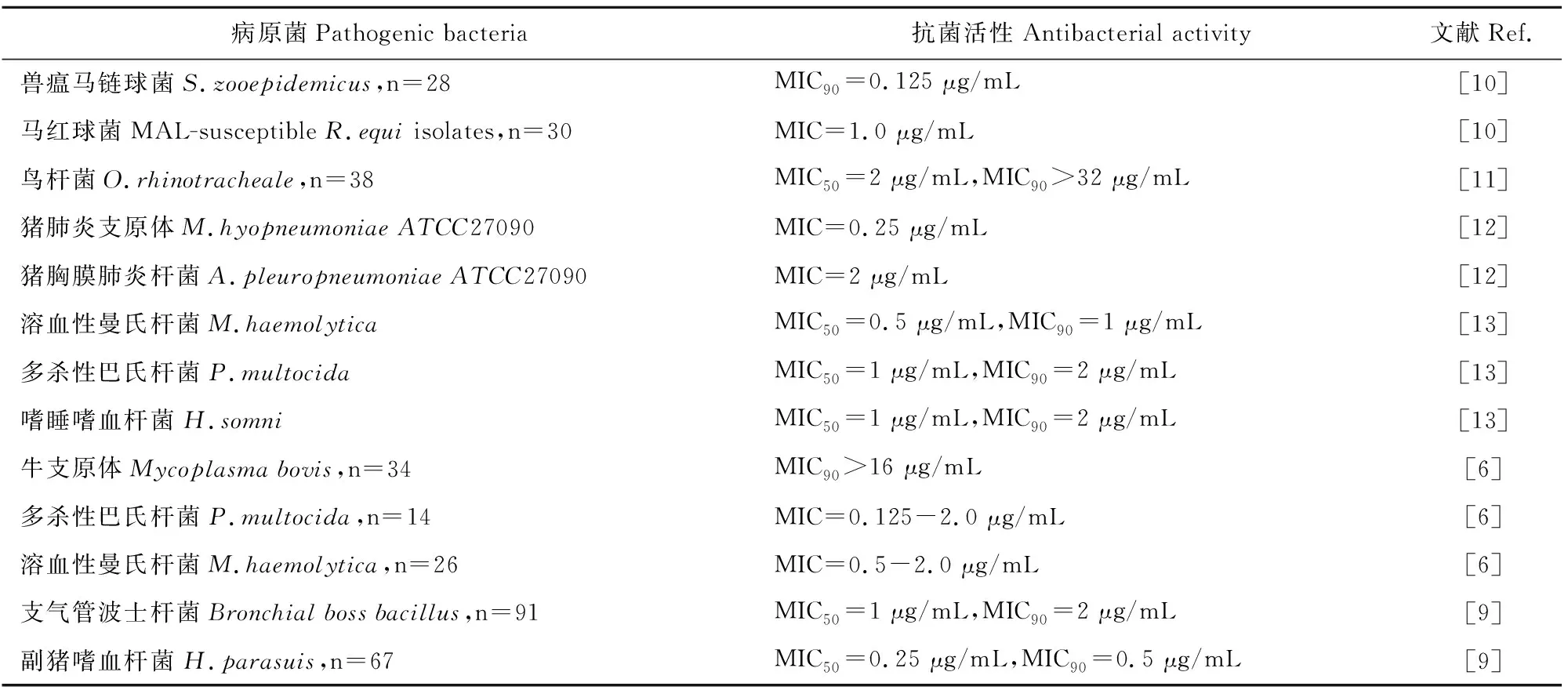
表1 加米霉素的抗菌活性
5 药动学
虽然加米霉素只被批准用于牛、猪呼吸道感染性疾病,但其在其他种属动物体内的药动学研究也有大量报道。从现有的药动学研究中可以看出,加米霉素具有皮下给药后吸收迅速、体内分布广泛、半衰期长、肺部药物浓度高优点。动物种类及给药方式的不同,药动学过程略有差异,这可能与肝微粒体酶系的差异有关,相关药动学参数如表2所示。加米霉素对敏感菌的MIC值一般在0.5 μg/mL~2 μg/mL,而其推荐剂量(6 mg/kg)在大多种属动物体内的药物浓度均高于2 μg/mL,且平均滞留时间(MRT)可达数天。从防耐药给药方案角度看,加米霉素用于牛、猪呼吸道感染性疾病的治疗剂量不应高于6 mg/kg。

表2 加米霉素在不同动物体内的主要药动学参数
注:AUC.药时曲线下面积;MRT.平均滞留时间;Cmax.峰浓度;Tmax.达峰时间;T1/2ke.消除半衰期;Plasma.血浆;PELF.肺上皮细胞衬液;BAL.支气管肺泡灌洗液。表中数据为平均值,均来源于文献中的原始值,未作任何处理。
Note:AUC.The area under the curve of the drug; MRT.Average stay time; Cmax.peak concentration; Tmax.peak time; T1/2ke:Elimination of half-lives; Plasma.Plasma; PELF.Pulmonary epithelial cell liner; BAL.Bronchial alveolar lavage solution.The data in the table is an average,all derived from the original values in the literature,without any processing.
6 毒理学
FDA报道了加米霉素在CD-1品系大鼠的毒理学,以0、50、100、500 mg/kg 剂量持续饲喂13周后,进行组织病理学检查和血液学检查,结果显示所有实验大鼠的临床症状、日增重、摄食量等均未出现异常,且血液学参数与对照组无显著性差异。FDA又在SD品系大鼠上以0、30、60、100 mg/kg 持续饲喂13周后,得出加米霉素在雄性大鼠上的未观察到作用剂量(NOEL)为26.7 mg/kg,磁性大鼠上的NOEL为35.6 mg/kg。EMA报道了加米霉素高剂量(300 mg/kg)对实验动物的心脏、肾脏、神经系统等主要组织器官无明显毒副作用。Zactran进行了加米霉素的致癌性研究,雄性小鼠和雌性小鼠分别以30、110、325 mg/kg 和40、150、440 mg/kg 剂量饲喂18个月,大鼠以0、10、30、100 mg/kg 饲喂24月,结果显示小鼠和大鼠的发病率和微观损伤发生率均维持在正常水平或无剂量反应关系,进行得出加米霉素无致癌性。EMA报道了加米霉素在200 kg牛的安全性,以正常剂量的1、3、5倍(0、6、18、30 mg/kg )皮下注射给药后,未观察到明显的毒理学症状和不良反应,结果表明加米霉素低于5倍推荐剂量皮下给药安全可行。
7 残留与休药期
兽药在动物源性食品以及畜禽可食性组织中的残留问题已引起社会广泛关注,尤其是食品安全方面。EMA报道了加米霉素按推荐剂量给予牛皮下注射给药后,分别在第10、21、35、49、70 d处死,以加米霉素原型为残留标示物,检测到肝脏组织、肾脏组织、脂肪组织和注射位点第10天加米霉素浓度依次为2.79、2.47、0.03、25.563 mg/kg。肝脏组织第35天为0.175 mg/kg,肾脏组织第49天为0.017 mg/kg,注射位点第49天仍可达0.372 mg/kg[9,13]。另外,EMA报道了加米霉素按推荐剂量给予猪肌肉注射给药后,分别在第1、2、3、5、7、10、15天处死,以6-3H标记加米霉素为残留标示物,检测到给药后第7、10、15天肾脏加米霉素浓度为0.33 mg/kg、0.57 mg/kg和0.04 mg/kg,肝脏为0.27 mg/kg、0.05 mg/kg和小于0.01 mg/kg,肌肉为0.06 mg/kg、0.03 mg/kg和0.02 mg/kg,注射部位为0.98 mg/kg、0.52 mg/kg和0.23 mg/kg[9,13]。根据EMA、FDA以及CVMP(欧盟兽药委员会)公布的加米霉素最大残留限量(MRL)以及休药期(表3)。
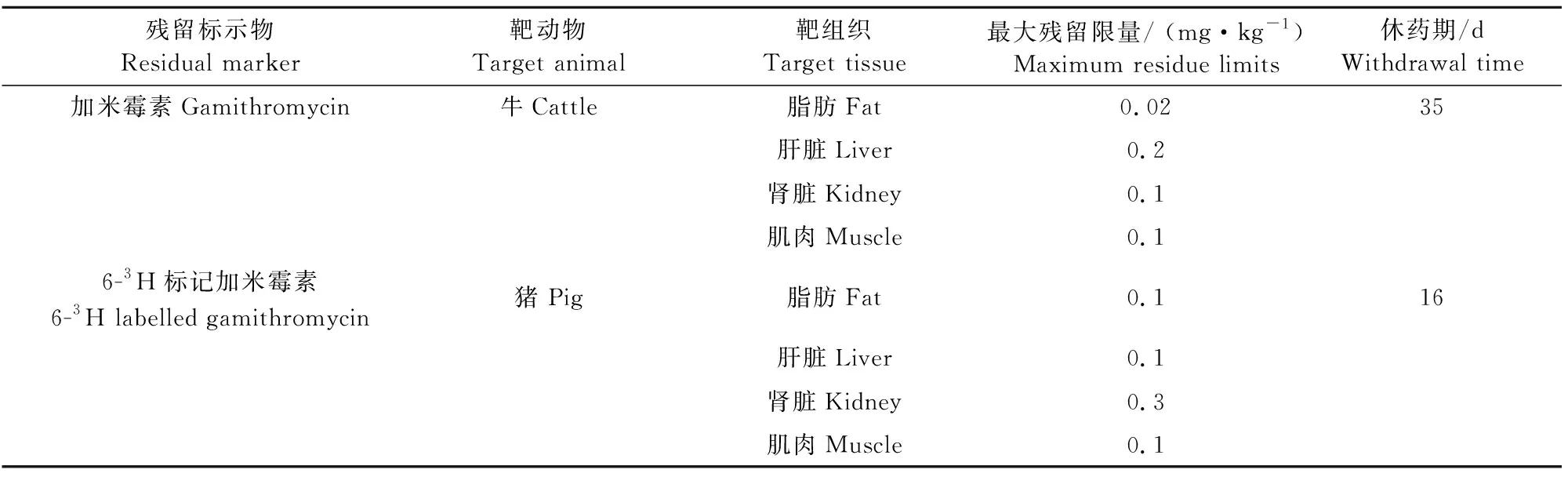
表3 加米霉素在牛和猪的组织最大残留限量和休药期
8 结语
加米霉素作为新一代半合成氮杂内酯类抗菌药,具有给药吸收快、组织浓度高、消除半衰期长等优点,且比同类大环类脂类抗菌药有着明显优势,理应在兽医临床上应对牛和猪巴氏杆菌、胸膜肺炎杆菌等细菌感染性疾病的预防及治疗有着广阔的应用前景。然而加米霉素的水溶性较差且未有渗透性相关研究,从制剂学角度看,这将在一定程度上限制其扩大应用,同类药物如阿奇霉素、替米考星等已有很多制剂研制报道,如脂质体、纳米粒、注射剂、混悬剂[18-19]等。为此,今后应加大加米霉素相关制剂学研究,已扩大其临床给药途径以及临床疗效。另外,近年来虽有加米霉素在不同种属动物的药动学研究以及药效学研究,但未见其对敏感菌如巴氏杆菌、胸膜肺炎杆菌、溶血性曼氏杆菌等的药动学-药效学(PK-PD)以及群体PK-PD同步模型研究,未有其科学合理的临床给药方案制定研究,从药物耐药性角度看,这将很容易滋生加米霉素的耐药菌[20-21]。另外,与单方制剂相比,复方制剂有着如改善药品的依从性、提高药物疗效、降低不良反应与毒性作用、减少耐药性产生和降低用药费用等优点[22-24],未来可考虑开展加米霉素联合用药以及复方制剂的相关研究。

