当归胶囊中三种有效成分含量测定的方法学验证
(美霖佳生物医学科技(苏州)有限公司,江苏苏州 215000)
当归为伞形科植物当归(Angelicasinensis(Oliv.)Diels)的干燥根,性甘、辛、温,具有补血活血、调经止血、润肠通便等保健功效[1]。当归中分离鉴定到的化合物主要包括挥发油、有机酸、多糖和黄酮等成分[2],苏氨酸、亮氨酸、异亮氨酸等多种氨基酸,以及铜、铁、锰、锌等多种微量元素[3],此外,还含有尿嘧啶、腺嘌呤、维生素E、青霉菌属的代谢产物,以及香豆素类等物质[4]。这些有效成分对机体血液、免疫、神经、循环、呼吸等系统均有较强的药理作用,同时具有一定的抗肿瘤、抗氧化、抗炎等作用[5]。当归增强免疫力的功效成分研究主要集中在当归多糖、阿魏酸和以当归内酯。杨轶虹等[6]研究表明,当归多糖能增强正常及免疫抑制小鼠的非特异性免疫功能,而对正常小鼠的体液免疫功能有抑制作用;高向东等[7]的研究表明当归中的阿魏酸对非特异性免疫、体液免疫和细胞免疫功能均有较强的促进作用;龙锐[8]的研究表明当归内酯具有免疫调解作用和抗肿瘤活性。
当归产品能否有效增强免疫力与其多糖、阿魏酸和以及当归内酯三个功效成分的含量有密切关系。自制当归胶囊是当归经过优化后的提取工艺提取,得到当归醇提物、当归水提物并配以麦芽糊精制粒填充胶囊而组成。当归醇提物中,主要含有当归内酯、有机酸;当归水提物中,主要为多糖。当归内酯主要包括藁本内酯、洋川芎内酯、丁烯基酞内酯、以及苯酞类二聚体,其中以藁本内酯含量最高[9];有机酸有多种,代表为阿魏酸,还有丁二酸、烟酸、十六烷羧酸、香荚兰酸、邻二苯酸、茴香酸、壬二酸、棕榈酸、亚油酸、硬脂酸等酸性成分[10];当归水提物中,当归多糖主含量为15%。所以,藁本内酯、阿魏酸、粗多糖可选做为自制当归胶囊的质量控制指标。藁本内酯和阿魏酸的检测方法有多种,且多用于当归和当归浸膏的检测,少见用于制剂成品;粗多糖的检测方法有苯酚-硫酸分光光度法、蒽酮-硫酸分光光度法、碱性酒石酸铜滴定法,且不同方法间的检测结果具有一定的差异。故建立适合的藁本内酯、阿魏酸、粗多糖含量的测定方法,确保含量检测的准确性,对严控自制当归胶囊的质量标准具有意义。
本文主要建立当归胶囊中三种有效成分藁本内酯、阿魏酸、粗多糖含量测定的方法,并通过对三项指标的检测方法进行系统适应性、专属性、线性、检出限、准确度、精密度、重复性、稳定性的方法学验证,以确定三个成分检测方法的可行性,为当归胶囊制定质量标准提供依据。
1 材料与方法
1.1 材料与仪器
当归(171103) 甘肃岷归中药材科技有限公司;麦芽糊精 山东保龄宝公司;藁本内酯标准品 纯度≥99.8%,上海安谱公司;阿魏酸标准品 中国食品药品检定研究院,纯度≥99.6%;D-无水葡萄糖标准品 纯度≥99.9%,中国食品药品检定研究院;甲醇、乙腈 美国Fisher公司,色谱纯;磷酸 分析纯,阿拉丁公司;乙醇、硫酸、苯酚 上海凌峰化学,分析纯;糖化酶 阿拉丁公司;超纯水 自制。
WBT-5半自动胶囊填充机 广州嘉成制药设备;JA2003电子天平 上海舜宇恒平仪器;HH-S6恒温水浴锅 常州国宇仪器;KQ-300DE超声波清洗器 昆山超声仪器公司;QL-861漩涡混合器 海门其林贝尔仪器;ST-16R离心机 Thermo公司;Cary 50紫外分光光度计 Vivian;Lambda 25紫外分光光度计 Perkin Elmer;LC-20AT高效液相色谱仪、LC-20AD高效液相色谱仪 岛津;Hypersil GOLD C18色谱柱(150 mm×4.6 mm,5 μm) Thermo。
1.2 实验方法
1.2.1 当归胶囊的制备 经过前期的工艺研究,当归胶囊制备工艺为:当归粉碎,过筛,得当归粗粉,加入80%乙醇,最佳醇提工艺(提取次数2次,醇浓度为80%,提取温度85 ℃,料液比为8∶1,每次提取时间为2 h)下提取得醇提液,醇提液浓缩、真空干燥得到当归醇提物;醇提后的药渣再用水(提取次数3次,提取温度100 ℃,料液比为9∶1,每次提取时间为1 h)加热提取得水提液,水提液浓缩、真空干燥得到当归水提物。将上述当归醇提物、当归水提物辅以麦芽糊精按照4∶1∶6比例混匀,加入90%的乙醇制粒,干燥,得到干燥颗粒,将干燥颗粒放入胶囊填充机中,填充为0.3 g/粒胶囊,即得当归胶囊。
1.2.2 成分检测方法
1.2.2.1 藁本内酯的测定 方法参考《WM/T 4-2004 当归提取物》[11]而制定。
a.供试品溶液的制备:称取当归胶囊内容物0.5 g,置于50 mL棕色容量瓶中,加入5 mL超纯水,摇匀,使固形物全部溶解呈乳白色溶液,然后加入约40 mL甲醇溶液,超声处理10 min后取出,放置至室温,加入甲醇溶液至刻度,摇匀,用0.45 μm微孔滤膜过滤于棕色试样瓶中,即得。
b.对照品溶液的制备:取藁本内酯对照品,精密称定20 mg,置50 mL棕色量瓶中,加甲醇定容,制成每1 mL含400 μg对照品储备液(即:400 μg/mL),摇匀,精密量取上述对照品储备液2.5 mL置25 mL量瓶中,加甲醇稀释至刻度,摇匀,即得40 μg/mL藁本内酯对照品溶液,备用。
c.样品测定:分别精密吸取对照品溶液与供试品溶液各10 μL,注入液相色谱仪,测定,即得。
d.色谱条件:流动相:A相:甲醇,B相:超纯水;检测波长:320 nm;柱温:30 ℃;流速:0.8 mL/min;洗脱方式:梯度洗脱,20 min内A相由40%线性变化为100%;进样量:10 μL;稀释剂:甲醇。
1.2.2.2 阿魏酸的测定 方法参考《中华人民共和国药典(2015版一部)》[1]“当归 含量测定 阿魏酸”而制定。
a.供试品溶液的制备:称取当归胶囊内容物0.4 g,置于25 mL棕色容量瓶中,加入70%甲醇20 mL,超声处理10 min后取出,放置至室温,加入70%甲醇至刻度,摇匀,用0.45 μm微孔滤膜过滤于棕色试样瓶中,即得。
b.对照品溶液的制备:取阿魏酸对照品,精密称定10 mg,置25 mL棕色量瓶中,加70%甲醇定容,制成每1 mL含400 μg对照品母储备液(即:400 μg/mL),摇匀,精密量取上述对照品储备液2.5 mL置25 mL量瓶中,加70%甲醇稀释至刻度,摇匀,即得40 μg/mL阿魏酸对照品溶液,备用。
c.样品测定:分别精密吸取对照品溶液与供试品溶液各10 μL,注入液相色谱仪,测定,即得。
d.色谱条件:流动相:乙腈-0.085%磷酸溶液(17∶83);检测波长:316 nm;柱温:35 ℃;流速:0.8 mL/min;洗脱方式:等度洗脱;样量:10 μL;稀释剂:70%甲醇。
1.2.2.3 粗多糖的测定 方法参考白鸿主编的《保健食品功效成分检测方法》[12]中“粗多糖的苯酚-硫酸分光光度测定法”而制定。
a.供试品溶液的制备:称取当归胶囊内容物2.0 g,置于容量瓶中,加入纯化水,于沸水浴中加热15 min,冷却至60 ℃以下,加入1 mL糖化酶,于55 ℃,酶解60 min,完成后于电炉上加热至沸(灭酶),冷却,定容,混匀后过滤,弃初滤液,收集余下滤液。吸取部分滤液于具塞离心管中,加入无水乙醇,混匀,醇沉,静置过夜,离心弃去上清液,残渣用80%乙醇溶液数毫升洗涤,离心后弃去上清液,反复操作3次。残渣用纯化水溶解并定容,即可。
b.标准曲线的绘制:准确吸取葡萄糖使用液0、0.25、0.375、0.50、0.625、0.75、1.0 mL(相当于葡萄糖0、0.05、0.075、0.10、0.125、0.15、0.20 mg)置于25 mL比色管中,补加水至2.0 mL,加1.0 mL的5%苯酚溶液混匀。小心加入浓硫酸10 mL,小心混匀,置沸水浴中20 min,冷却至室温,用分光光度计在480 nm波长处试剂空白为参比,1 cm比色皿测定吸光度值。以葡萄糖质量为横坐标,吸光度值为纵坐标,绘制标准曲线。
c.对照品溶液的制备:准确称取干燥恒重的D-无水葡萄糖标准品500 mg加水溶解,并定容至50 mL,此溶液1 mL含10 mg葡萄糖(10 mg/mL),用前稀释50倍为葡萄糖使用液(0.2 mg/mL),备用。
d.样品测定:准确吸取上液适量置于25 mL比色管中,补加水至2.0 mL,然后按上述法测定吸光度值。从标准曲线上查出葡萄糖含量,计算样品中粗多糖含量。
1.2.3 方法学验证 对当归胶囊中有效成分藁本内酯、阿魏酸、粗多糖含量测定的方法,进行方法学验证。藁本内酯[13]、阿魏酸[14-15]采用高效液相色谱法含量测定,并进行方法学考察,包括系统适应性、专属性、线性、检出限、准确度、精密度、重复性、稳定性等[16-17];粗多糖采用紫外分光光度法[18],并进行方法学考察,包括专属性、线性、检出限、准确度、精密度、重复性、稳定性等[19-20]。具体方法学考察项目见表1[21-22]。
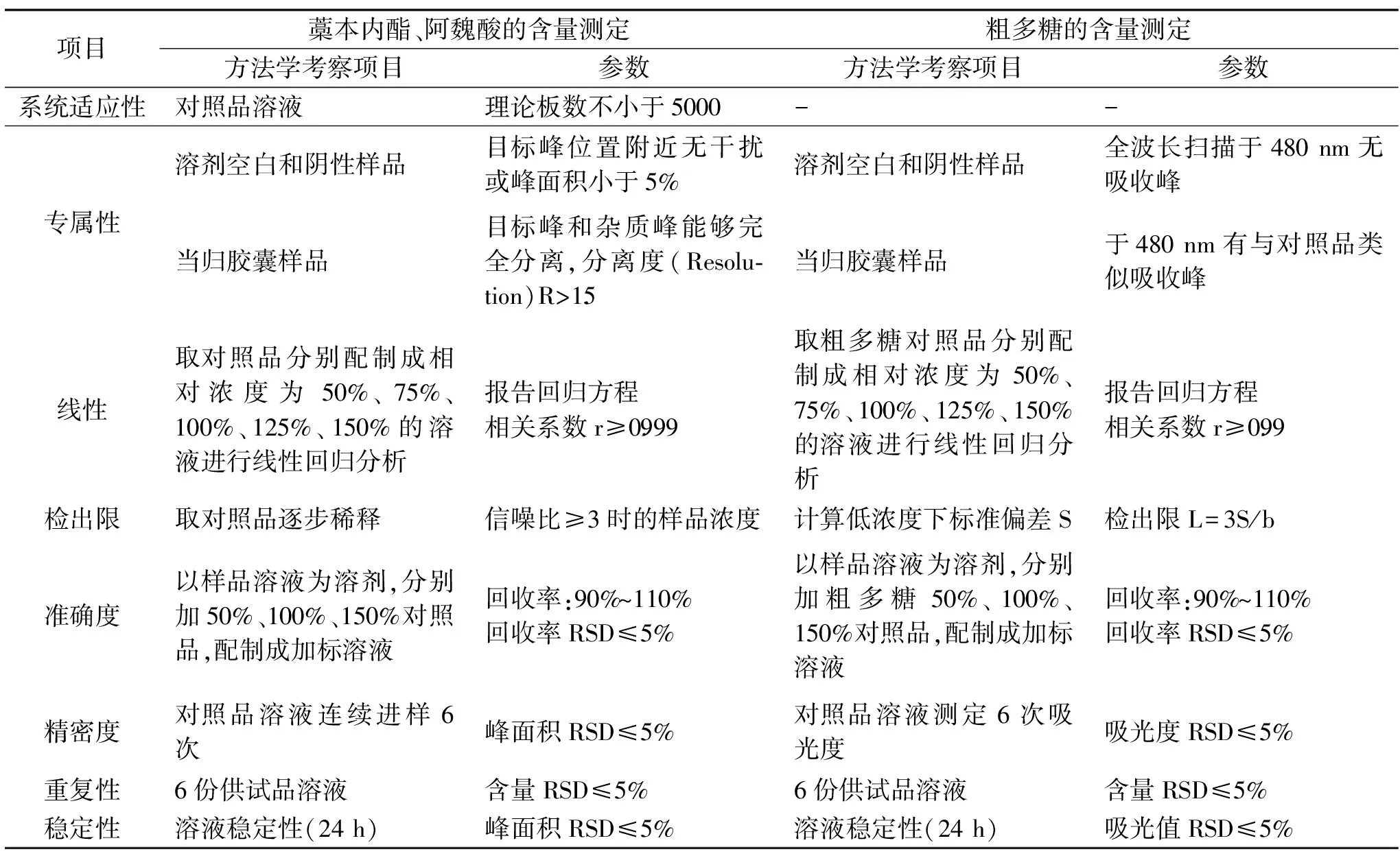
表1 藁本内酯、阿魏酸、粗多糖含量测定的方法学考察项目安排Table 1 Project arrangement of method validation on the determination of ligustilide,ferulic acid and polysaccharide
2 结果与分析
2.1 系统适应性
分别按照1.2.2.1、1.2.2.2对照品溶液制备方法制备对照品溶液,各自连续进样6次,记录色谱图,查看理论塔板数,见表2,结果表明:理论板数均远大于5000,藁本内酯、阿魏酸含量测定的系统适应性良好。

表2 藁本内酯、阿魏酸含量测定系统适应性结果Table 2 System adaptability results of the determination of ligustilide and ferulic acid
2.2 专属性
藁本内酯专属性:将空白溶液(甲醇)、阴性样品(麦芽糊精)、对照品溶液、供试品溶液,分别进样,记录色谱图,见图1。结果表明:供试品与对照品的藁本内酯色谱峰位置一致,阴性和试剂空白在相应保留时间处不显示色谱峰,供试品目标峰与杂质峰能够完全分离,分离度(Resolution)R>1.5,表明该方法专属性良好。
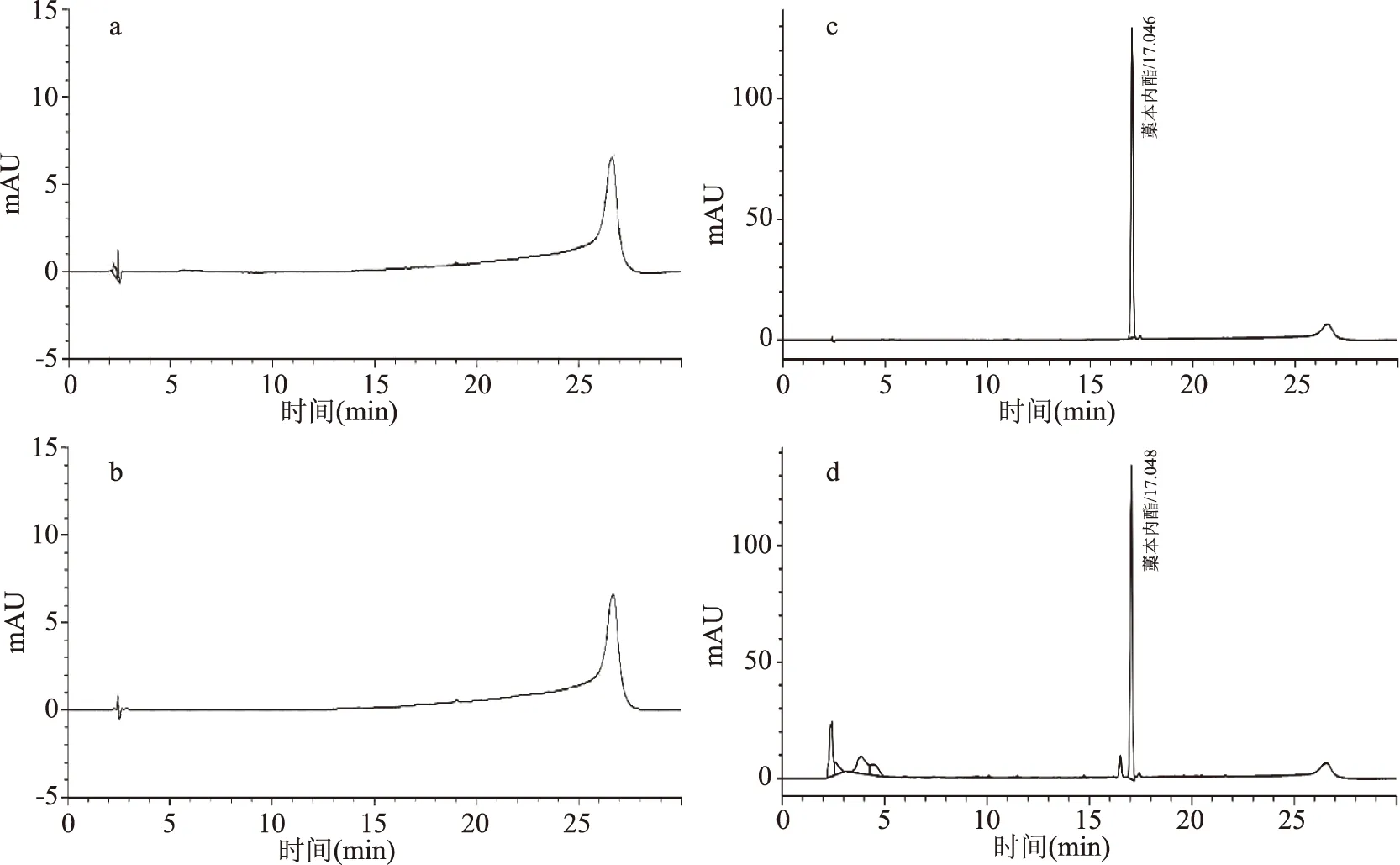
图1 藁本内酯含量测定专属性结果Fig.1 Exclusivity results of the determination of ligustilide注:a:空白;b:阴性样品;c:对照品;d:供试品。
阿魏酸专属性:将空白溶液(70%甲醇)、阴性样品(麦芽糊精)、对照品溶液、供试品溶液,分别进样,记录色谱图,见图2。结果表明:供试品与对照品的阿魏酸色谱峰位置一致,阴性和试剂空白在相应保留时间处不显示色谱峰,目标峰与杂质峰能够完全分离,R>1.5,表明该方法专属性良好。
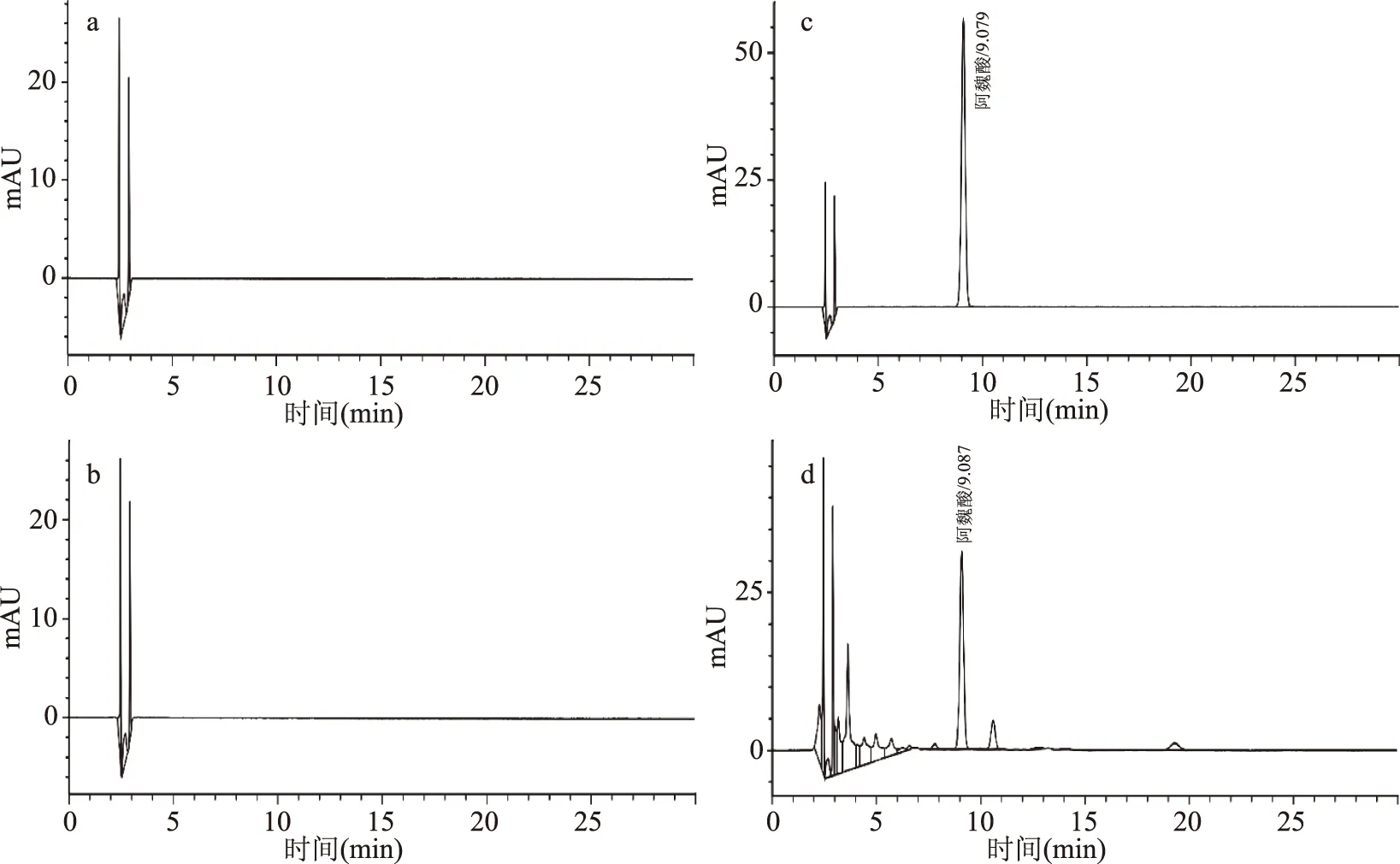
图2 阿魏酸含量测定专属性结果Fig.2 Exclusivity results of the determination of ferulic acid注:a:空白;b:阴性样品;c:对照品;d:供试品。
粗多糖专属性:将试剂空白、阴性样品(麦芽糊精)、对照品溶液、供试品溶液,分别进样,记录400~600 nm扫描图,见图3。结果表明:阴性样品和试剂空白,在480 nm处无吸收峰;供试品溶液和对照品溶液在480 nm,均有吸收峰,表明该方法专属性良好。
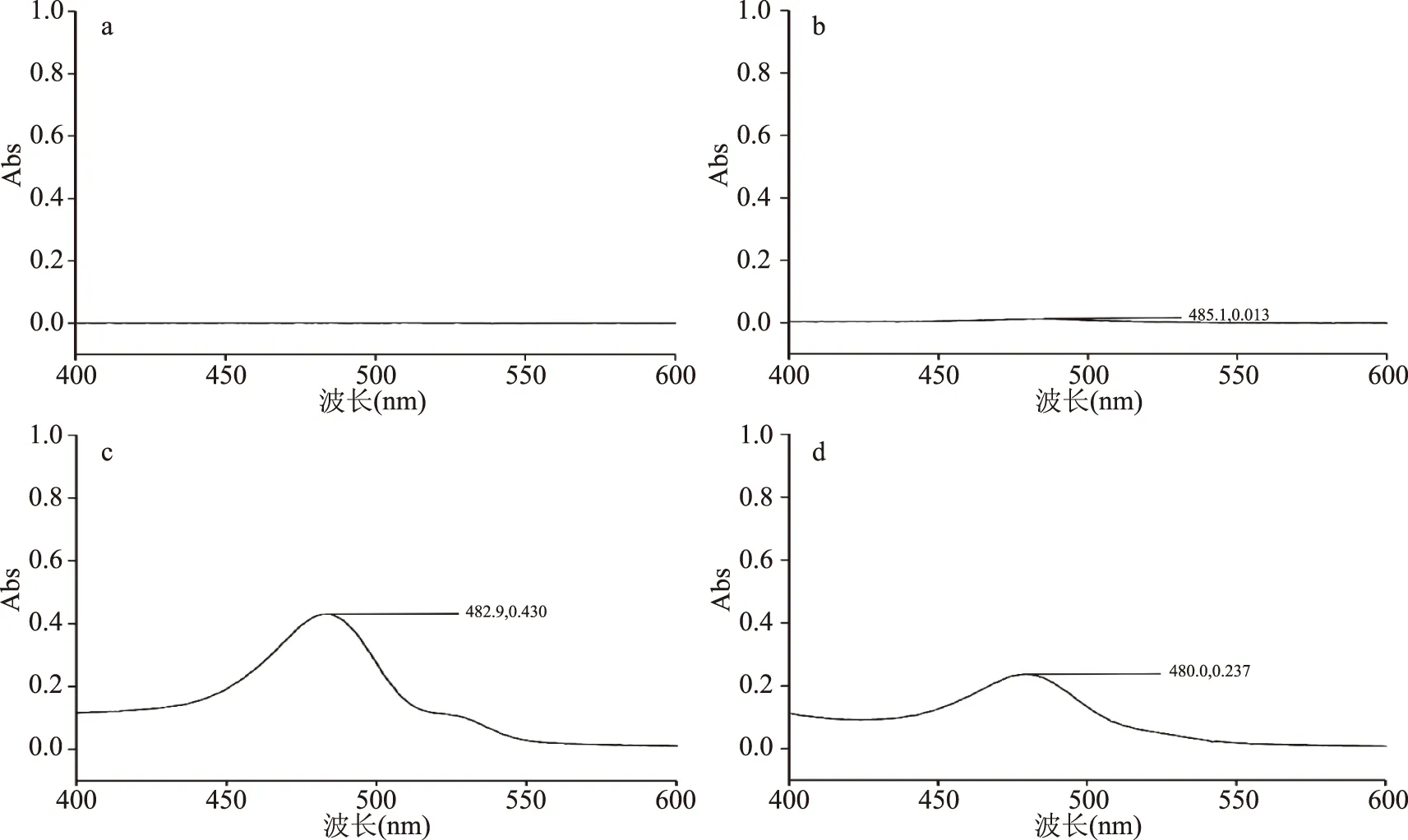
图3 粗多糖含量测定专属性结果Fig.3 Exclusivity results of the determination of polysaccharide注:a:空白;b:阴性样品;c:对照品;d:供试品。
2.3 线性考察
藁本内酯:精密量取400 μg/mL藁本内酯对照品溶液0.5、0.75、1.0、1.25、1.5 mL,并稀释至10 mL,配制成相对浓度为50%、75%、100%、125%、150%的对照品溶液。取上述对照品溶液,分别进样,记录色谱图,以测得的色谱峰峰面积对浓度作图,计算线性回归方程及相关系数,结果见表3。
阿魏酸:精密量取40 μg/mL阿魏酸对照品溶液1.5、2.25、3.0、3.75、4.5 mL,并稀释至10 mL,配制成相对浓度为50%、75%、100%、125%、150%的对照品溶液。取上述对照品溶液,分别进样,记录色谱图,以测得的色谱峰峰面积对浓度作图,计算线性回归方程及相关系数,结果见表3。
粗多糖:按照1.2.2.3步骤,绘制标准曲线,计算线性回归方程及相关系数,结果见表3。
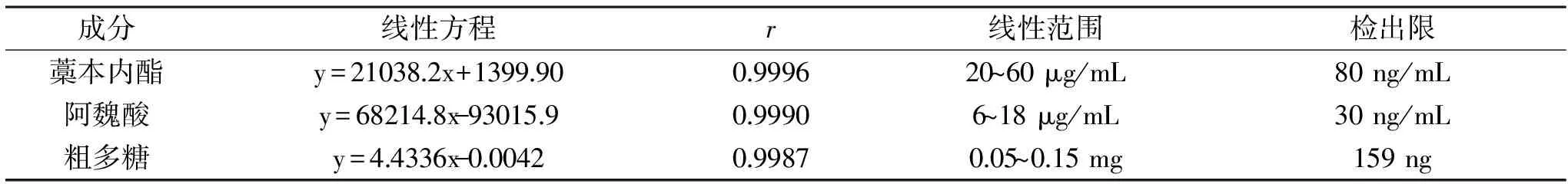
表3 藁本内酯、阿魏酸、粗多糖含量测定线性关系和检出限考察结果Table 3 Linearity and detection limit results of the determination of ligustilide,ferulic acid and polysaccharide
从线性考察可知,藁本内酯、阿魏酸的线性回归方程相关系数分别为0.9996和0.9990,符合表1中藁本内酯、阿魏酸相关系数≥0.999的要求,粗多糖的线性回归方程相关系数为0.9987,符合表1中粗多糖参数R≥0.99的要求。由此可见,三种检测方法在范围内均成良好的线性关系。
2.4 检出限
藁本内酯:取藁本内酯对照品溶液适量,用稀释剂逐步稀释。按照检测方法进样测定,计算各色谱峰信噪比(S/N),以S/N≥3时质量浓度为检出限,结果见表3。
阿魏酸:同藁本内酯检出限方法,结果见表3。
粗多糖:取20份空白溶液,进样,计算20次测定结果的标准偏差S,按照公式:L=3S/b,计算,结果见表3。
2.5 准确度
取供试品溶液各9份,分别加50%、100%、150%对照品,配制成加标溶液,计算回收率和RSD,结果见表4。藁本内酯、阿魏酸、粗多糖含量测定方法的回收率均在90%~110%,RSD≤5%,说明三个含量测定方法的准确度均良好。
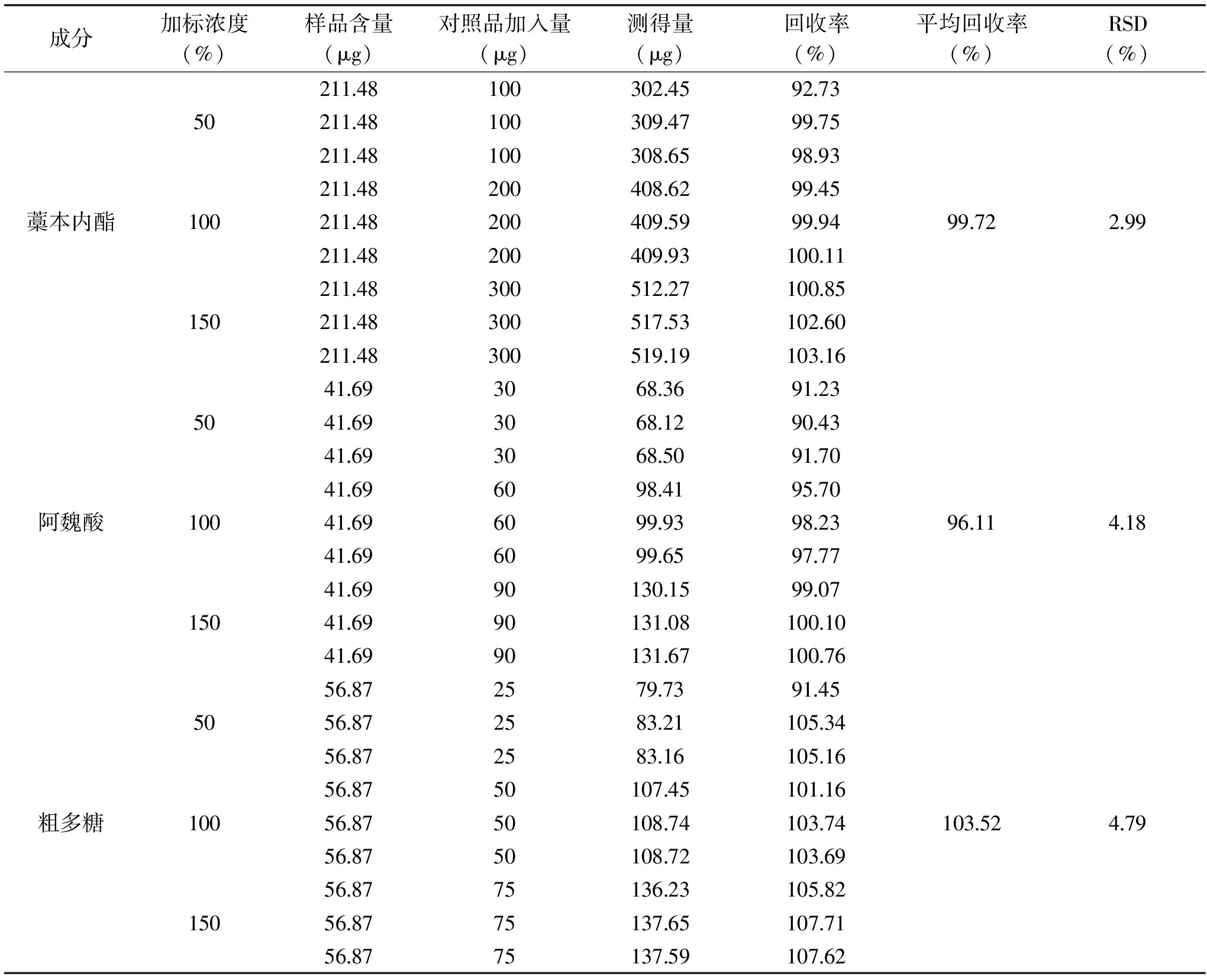
表4 藁本内酯、阿魏酸、粗多糖含量测定准确度考察结果Table 4 Accuracy results of the determination of ligustilide,ferulic acid and polysaccharide
2.6 精密度
藁本内酯:同一对照品溶液,连续进样6 次,测定峰面积,计算RSD,结果见表5。
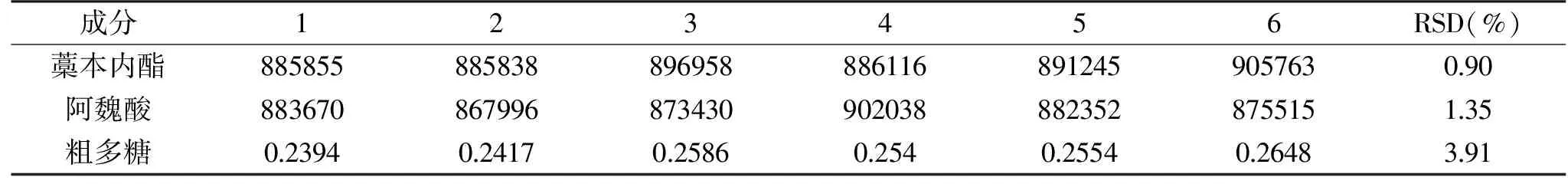
表5 藁本内酯、阿魏酸、粗多糖含量测定精密度考察结果Table 5 Precision results of the determination of ligustilide,ferulic acid and polysaccharide
阿魏酸:同藁本内酯精密度考察方法,结果见表5。
粗多糖:同一对照品溶液,测定6次吸光度,计算RSD,结果见表5。
藁本内酯、阿魏酸、粗多糖含量测定方法的精密度RSD≤5%,说明三个含量测定方法的精密度均良好。
2.7 重复性
藁本内酯:取当归胶囊样品(20180711)6份,制成供试品溶液,进样,测定,计算藁本内酯含量,计算RSD,结果见表6。
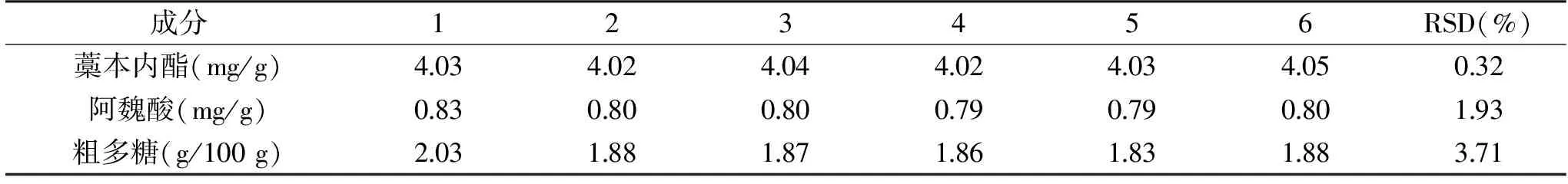
表6 藁本内酯、阿魏酸、粗多糖含量测定重复性考察结果Table 6 Repeatability results of the determination of ligustilide,ferulic acid and polysaccharide
阿魏酸:同藁本内酯重复性考察方法,结果见表6。
粗多糖:同藁本内酯重复性考察方法,结果见表6。
藁本内酯、阿魏酸、粗多糖含量测定方法的重复性RSD≤5%,说明三个含量测定方法的重复性均良好。
2.8 稳定性
藁本内酯:取供试品溶液,于0、2、4、6、8、12、24 h进样,观察峰面积变化,并计算峰面积的RSD,结果见表7。
阿魏酸:同藁本内酯稳定性考察方法,结果见表7。
粗多糖:同藁本内酯稳定性方法,观察吸光值变化,计算吸光值的RSD,结果见表7。

表7 藁本内酯、阿魏酸、粗多糖含量测定稳定性考察结果Table 7 Stability results of the determination of ligustilide,ferulic acid and polysaccharide
结果可见,三个方法的稳定性RSD≤5%,说明三个含量测定方法的稳定性均良好。
3 结论
本研究依据当归胶囊的组方特性,选择藁本内酯、阿魏酸、粗多糖为标志性成分,建立了当归胶囊三个组分含量测定的方法。藁本内酯、阿魏酸采用液相色谱法,粗多糖采用紫外分光光度法,通过对系统适用性、专属性、线性、检出限、准确度、精密度、重复性和稳定性等指标的考察,证明当归胶囊中藁本内酯、阿魏酸、粗多糖含量测定的方法准确、稳定、可靠。

