混凝-超滤工艺去除水中复合污染物试验研究
赵纯,金凡,安叶,孙志华,郑怀礼
(1.重庆大学 城市建设与环境工程学院;三峡库区生态环境教育部重点实验室;低碳绿色建筑国际联合研究中心,重庆 400045;2.石河子大学 水利建筑工程学院,新疆 石河子 832003)
近年来,随着居民生活质量的提高,饮用水安全问题备受关注,研究日趋深入。纳米材料作为一种广泛应用于化工制造、个人护理及食品工业等的新材料,进入天然水体后,天然有机物质(NOM,如腐植酸、富里酸等)与纳米粒子间的相互作用可能改变其毒性和稳定性,对其在环境中的迁移和转化有重要影响,给饮用水安全带来威胁[1-3]。学者们考察了纳米材料本身的性质,以及环境溶液的化学性质和物理因素对纳米材料在水体中的沉积、聚集及其潜在危害的影响,而关于纳米材料与NOM在水溶液中形成的复合污染物的研究却很少[4-5]。因此,研究NOM与纳米颗粒在水中的相互作用具有实际价值。
传统的水处理工艺对纳米颗粒的去除并不理想,而超滤因能有效截留水中胶体、悬浮物、细菌等,在纳米颗粒去除方面展现出优势,但却面临膜污染等问题[6]。不过,将超滤与其他技术(混凝[7-8]、吸附[9-10]、预氧化[11-12]等)相结合,能有效减轻膜污染,其中,混凝-超滤因具有成本低、操作简单、处理效果好等优点而得到广泛应用。纳米颗粒经过混凝后凝聚,用膜过滤有很好的去除效果,且与传统的过滤方法相比,膜滤对水中的纳米颗粒表现出更好的去除效果[13-14]。
选取腐殖酸(HA)和纳米二氧化钛(纳米TiO2)作为研究对象,对纳米TiO2与腐殖酸之间的相互作用进行简单分析,探究混凝剂投加量、溶液pH值及钙离子浓度对混凝-超滤工艺(C-UF)去除HA-纳米TiO2复合污染物(HA-T)的影响。
1 实验材料与方法
1.1 实验材料
实验所涉及的材料及药品信息见表1。

表1 实验所用材料及药品一览表Tabel 1 List of materials and drugs used in the experiment
续表1
注:实验中原水用蒸馏水配制,其他所有试剂溶液均采用超纯水(18.20 MΩ·cm)配制。
1.2 实验方法
1.2.1 聚合硫酸铁配制 混凝剂聚合硫酸铁(PFS)为实验室所制备[15],PFS母液配制浓度为2.857 mol/L,有效浓度为80%,稀释20倍,制得的混凝剂PFS浓度C0=0.114 mol/L。
投药后水样中PFS浓度C(mmol/L)按式(1)计算。
C=C0×V1/V2
(1)
式中:V1为PFS体积,mL;V2为实验水样体积,L。
1.2.2 原水配制 配制1.0 g/L HA储备液:将1.0 g HA和0.40 g NaOH溶解于1 000 mL超纯水中,室温(25 ℃)下搅拌24 h,用0.45 μm滤膜过滤后,于4 ℃环境中保存备用。
配制1.0 g/L 纳米TiO2储备液:将0.10 g TiO2固体粉末溶解于100 mL超纯水中,并在超声机内(40 kHz)超声0.5 h以上,使其均匀分散,然后于4 ℃环境中保存备用。
配置10 mg/L HA-T复合污染物:将纳米TiO2储备液超声处理20 min,分别取4 mL 1.0 g/L HA储备液和4 mL纳米TiO2储备液,用蒸馏水稀释至400 mL,待用。
1.3 实验装置及流程
C-UF工艺去除HA-T污染物的实验装置如图1所示。取400 mL水样置于烧杯中,调节pH值为8.0,并加入1.6 mL PFS溶液进行烧杯实验,按照以下程序运行:快搅2 min(240 r/min),慢搅20 min(40 r/min)。烧杯实验后,水样转移至超滤装置(MSC300),以0.15 MPa的恒定压力过滤,与电子天平(JJ523BC)相连接的电脑PC端实时记录滤液质量。
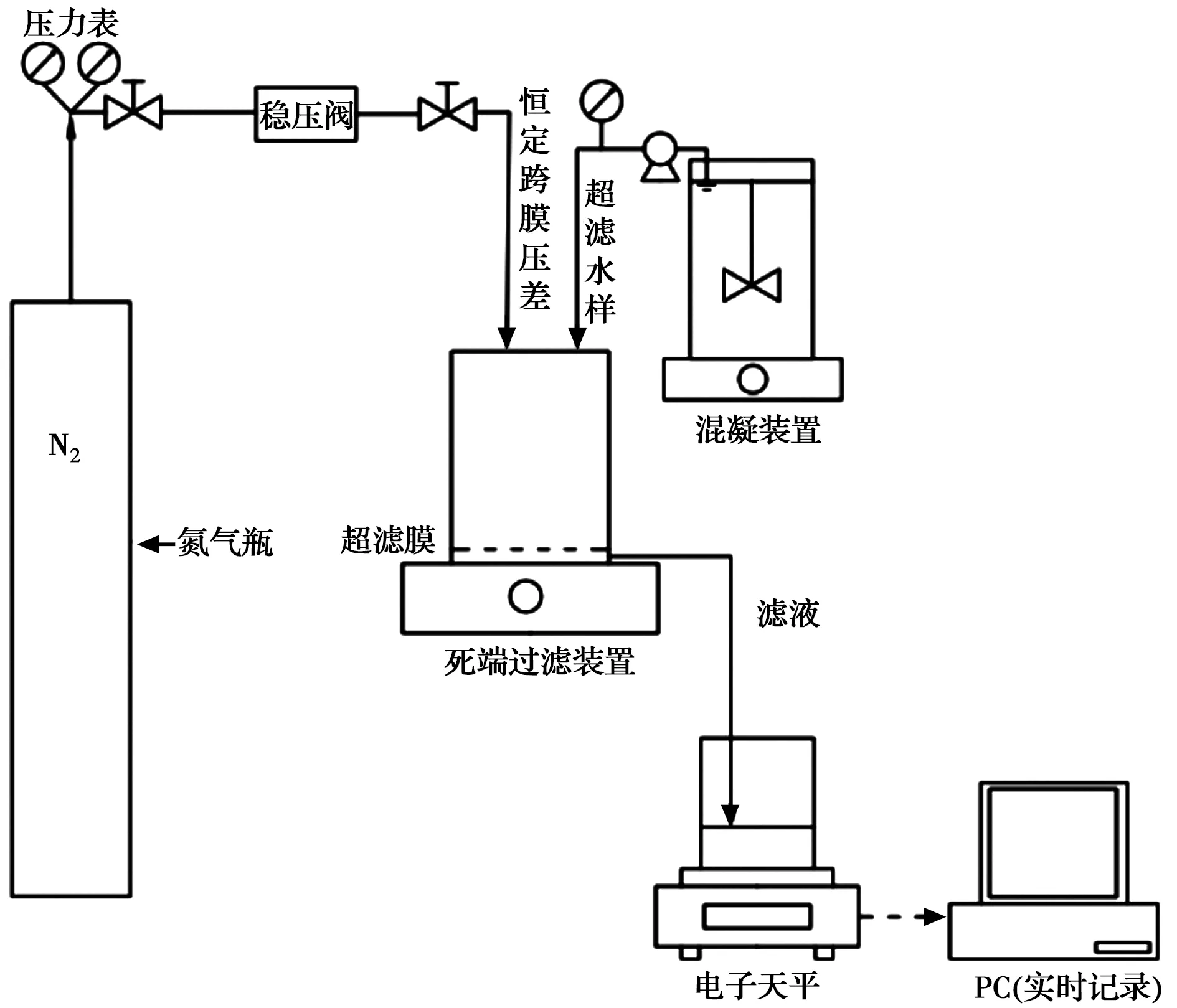
图1 实验装置Fig.1 Scheme of the experimental
1.4 检测与分析
实验过程所涉及的分析检测项目见表2。
1.5 膜通量测定
膜通量是指在一定压力下,单位时间内单位面积膜材料所通过的流体量。它是反映膜性能的一个重要参数,同时,膜污染状况也可以通过膜通量的变化来体现。由于每个膜初始通量不同,实验采用比通量Jt/J0来反映膜污染程度,Jt为过滤t时刻的膜通量,J0为初始时刻膜通量。膜通量采用式(2)进行计算。
Jt=V/At
(2)
式中:Jt为过滤t时刻的膜通量,L/(m2·h);V为t过滤时间内的滤液体积,L;A为膜的有效面积,m2。

表2 分析检测项目汇总Table 2 Summary of analysis and test items
2 结果与讨论
2.1 纳米TiO2与HA的相互作用
2.1.1 Zeta电位变化分析 水中悬浮的纳米TiO2颗粒表面基团不饱和会与水配位,水发生离解吸附而生成羟基化表面[18]。表面羟基可以在水溶液中发生质子迁移,通过质子化呈现出酸性,也可以通过去质子化表现出碱性。即

为考察纳米TiO2与HA在水环境中的相互作用,分别测定了10 mg/L纳米TiO2颗粒悬浮液与10 mg/L HA的Zeta电位。当pH值在3~11范围内变化时,分别测定纳米TiO2颗粒及HA的表面电位,结果如图2所示。由图2可知,当pH<5.5时,纳米TiO2表面羟基通过质子化,带正电;在pH=5.5 时,纳米TiO2表面存在等电位点;纳米TiO2表面羟基在pH>5.5时,因失质子而带负电,在pH值为7、9、11时,所对应的Zeta电位分别为-9.5、-15.6、-19.6 mV,这说明pH的增大会导致纳米TiO2表面负电性增强。
当pH值在4~5.5范围内,由于静电吸引(Zeta(HA)<0,Zeta(TiO2)>0),纳米TiO2易吸附在HA表面,且纳米TiO2随着有机物的迁移而迁移;在pH>5.5时,Zeta(TiO2)、Zeta(HA)皆小于0,纳米TiO2主要通过配位交换方式富集在HA表面,使其本身Zeta电位进一步降低,静电斥力加强,从而在水溶液中更稳定,易于迁移,这与已有研究相符[19-20]。
2.1.2 同步光谱扫描分析 为进一步考察两者之间的关系,在10 mL 10 mg/L的HA溶液中,分别加入10 mL浓度为1、2、5、10、20 mg/L的纳米TiO2溶液,在240~600 nm的波长下进行同步光谱扫描,结果如图3所示。由图3可知,荧光淬灭程度随纳米TiO2浓度的增加而加大,这归因于HA复杂的结构,其含有羧酸、酚羟基等官能团以及共轭芳香结构,纳米TiO2与其作用生成配位化合物,造成荧光强度的降低[17, 21]。因此,纳米TiO2浓度越高,与HA发生的配位反应越多,荧光淬灭度越高,引起空间位阻增大,分散性变好,迁移增强。
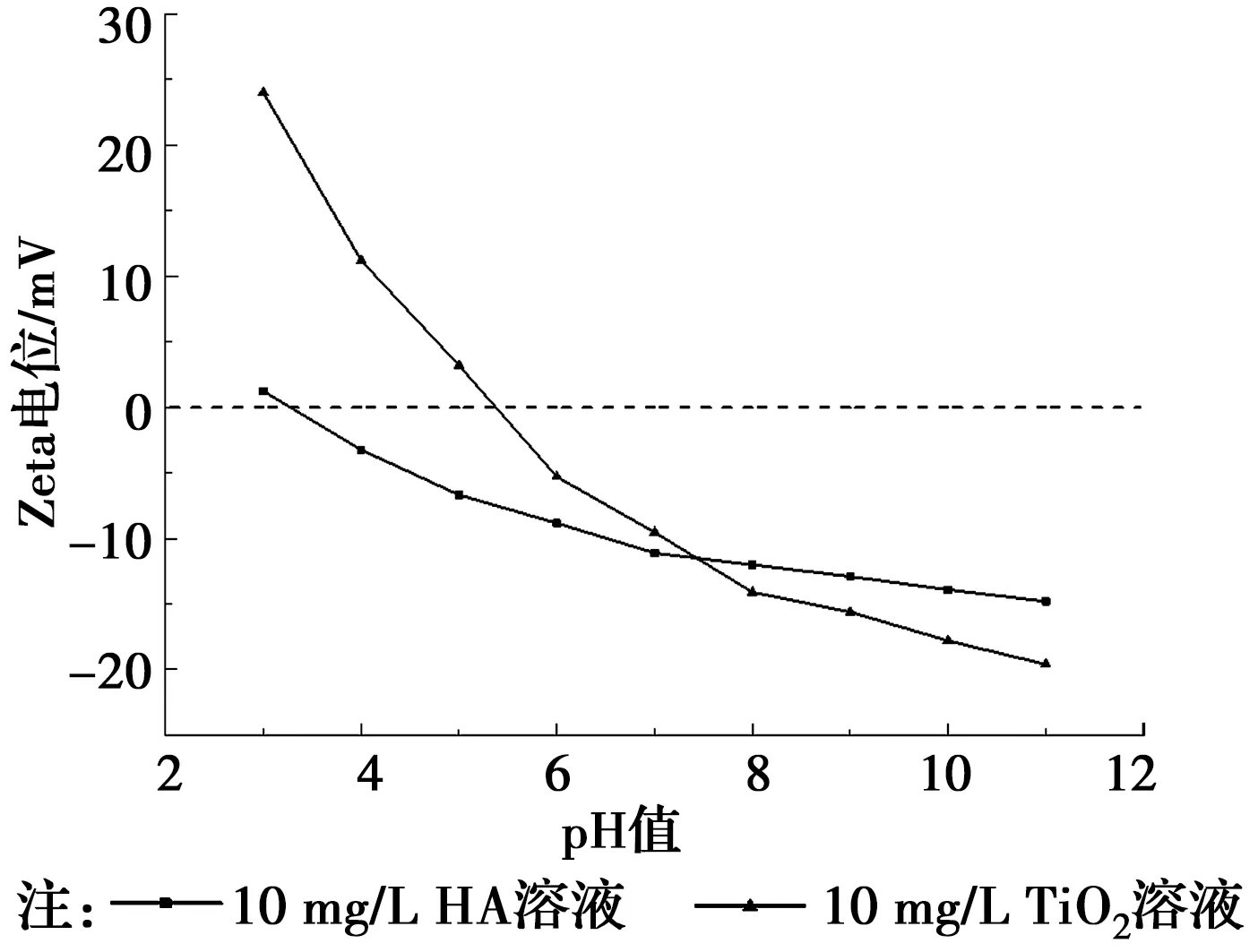
图2 Zeta 电位变化图Fig.2 The change of Zeta
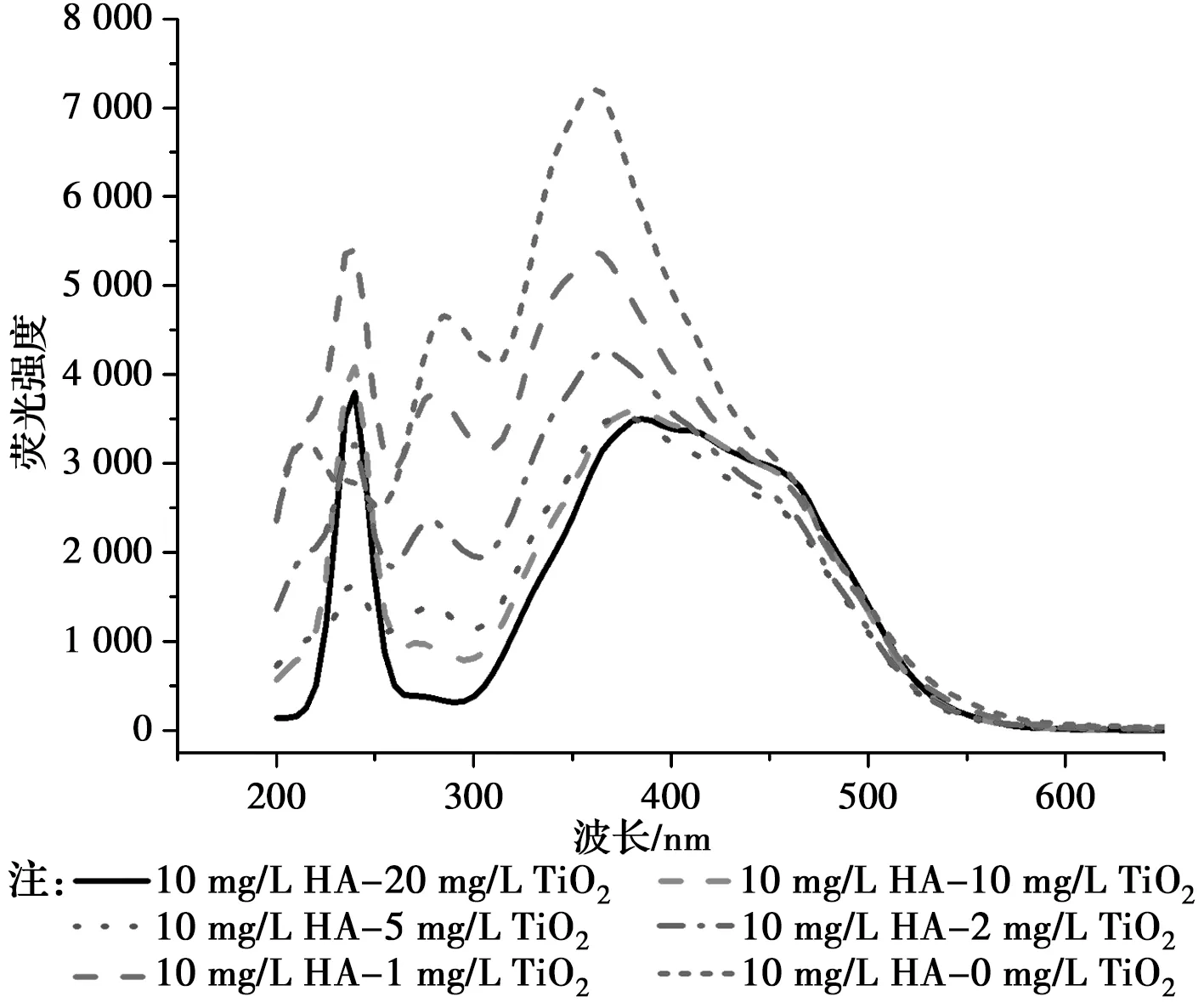
图3 不同纳米TiO2浓度下HA-T溶液的同步扫描光谱Fig.3 The SSF spectrum of HA-T under different TiO2-nano
2.2 不同因素对C-UF工艺处理效果的影响
2.2.1 混凝剂投加量对C-UF工艺处理效果的影响 控制其他实验条件不变,改变混凝剂用量,通过测定出水中TOC和纳米TiO2的含量来反映C-UF工艺的处理效果。由图4(a)可以看出,当水样中混凝剂浓度分别为0.17、0.23、0.29、0.34、0.40、0.46、0.51、0.57 mmol/L时,TOC和纳米TiO2的去除率先上升后下降,当混凝剂浓度为0.46 mmol/L,TOC和纳米TiO2去除率分别为92.32%、90.56%,说明出水中HA及纳米TiO2含量很低,且出水余浊经检测均低于0.50 NTU,处理效果较好,出水水质最优。图4(b)表明,当混凝剂浓度分别为0.23、0.46、0.57 mmol/L时,膜过滤通量衰减幅度分别为35.83%、20.75%和35.17%,说明当PFS浓度为0.46 mmol/L时,膜污染速率相对较低。这主要是因为膜通量的大小与水样中的絮体尺寸直接相关,而絮体尺寸又与混凝剂投加量密切相关。当PFS投加量较低时,混凝主要通过电性中和作用形成较小的絮体,从而造成膜孔堵塞;随着PFS的投加量增大,混凝主要通过吸附架桥或网捕卷扫作用形成较大的絮体,这些较大尺寸的絮体不易堵塞膜孔,从而减缓膜污染。但是,当PFS过量使用时,絮体所带电荷反转而相互排斥,再加上搅拌所形成的水力剪切作用,较大尺寸的絮体会解体,从而又加剧了膜污染。
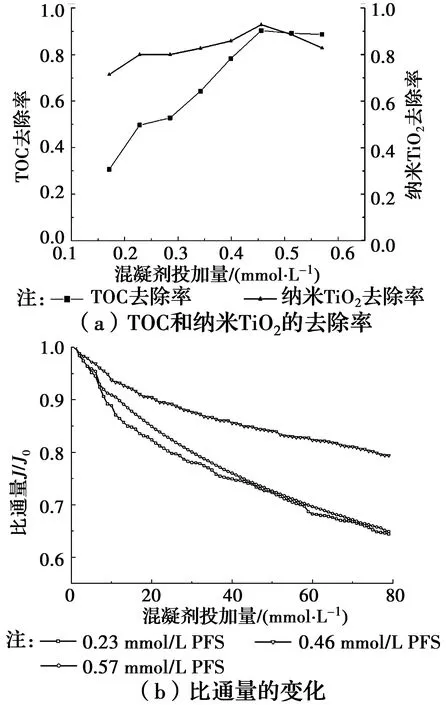
图4 不同混凝剂投加量对C-UF工艺处理效果及膜通量的影响Fig.4 Effect of different coagulant dosage on C-UF process
2.2.2 pH对C-UF工艺处理效果的影响 pH值是给水处理中重要的水质参数,它的变化会影响水处理的效果。实验通过固定其他反应条件,改变进水初始pH值来进行。
从图5(a)可观察到,随pH值增大,TOC、纳米TiO2去除率均先升高后降低。出水余浊经检测皆低于0.30 NTU。图5(b)显示,随pH值升高,膜通量的衰减幅度先减小后增加,在pH值为8时最高。这可能是因为pH对纳米颗粒和HA之间的相互作用有一定的影响,HA主要通过静电吸附和配位交换的方式吸附于纳米颗粒表面,酸性条件下,HA表面官能团难以离解,分子链趋于卷曲成团;强碱性条件下,絮体因带负电而相互排斥,难以聚集,且PFS水解加速易生成Fe(OH)3沉淀,容易引起膜孔窄化而堵塞膜孔,所以,pH值在7~8时,更有利于控制膜污染。
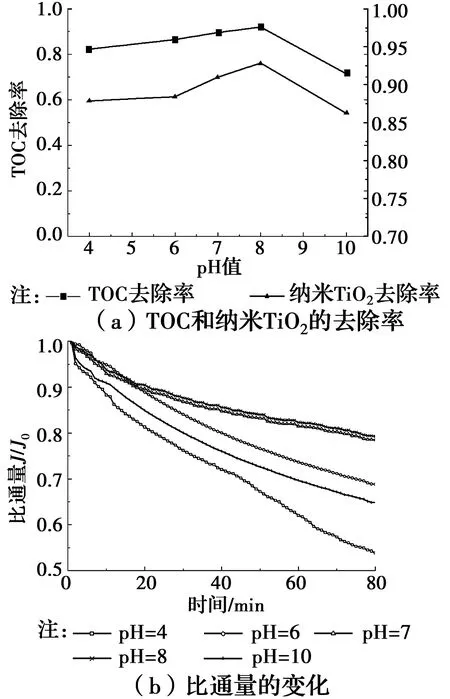
图5 pH对C-UF工艺处理效果及膜通量的影响Fig.5 Effect of pH level on C-UF process and membrane
2.2.3 钙离子浓度对C-UF工艺的影响 图6(a)、(b)分别显示了钙离子浓度对C-UF工艺去除率和膜通量的影响。由图6(a)可知,随着Ca2+浓度增加,TOC去除率降低,纳米TiO2去除率先增加后减小。经检测,出水余浊也由99.00%降至94.21%,这表明,添加Ca2+不利于反应的进行。图6(b)显示出膜通量的衰减幅度也随Ca2+浓度的增加而增大,这是由于Ca2+进一步降低了膜表面的电荷,絮体带正电荷发生胶体保护现象,从而使水处理效果变差。
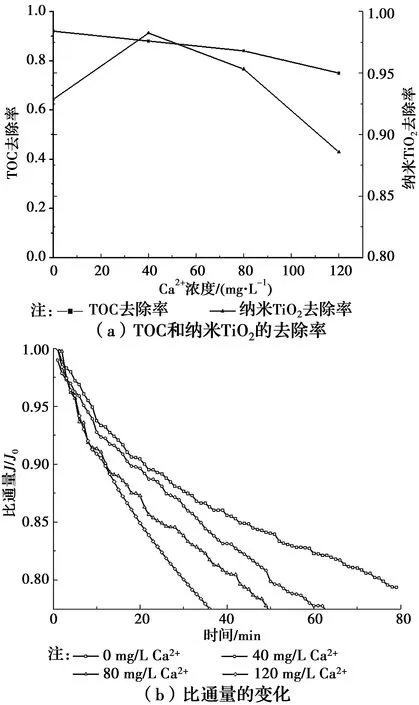
图6 Ca2+浓度对C-UF工艺处理效果及膜通量影响Fig.6 Effect of Ca2+ concentration on C-UF process

图7 不同条件下滤膜的扫描电镜图Fig.7 SEM of ultrafiltration membrane under different
2.3 膜表面滤饼层形态分析
对实验后的滤膜进行SEM扫描,可以更加直观地观察膜表面滤饼层微观形态。图7(a)为原始滤膜表面,干净光滑;图7(b)为最优条件下(pH=8,混凝剂投加量为0.46 mmol/L,不添加Ca2+)滤膜表面滤饼层,可观察到其交连的大分子骨架结构,孔隙率高,膜堵塞情况较轻;图7(c)为将pH值调整为4时滤膜表面滤饼层,表面絮体密实,骨架结构分布不均匀,孔隙率低;图7(d)为80 mg/L Ca2+时滤膜表面滤饼层,其他条件同图7(b),与图7(b)的大分子骨架结构明显不同,絮体结构致密,孔隙小,说明Ca2+的存在会加重膜污染。根据XDLVO理论,pH值、PFS浓度、Ca2+浓度对膜表面的污染程度主要取决于污染物与膜材料、离子等相互作用的自由能,调低pH值、投加阳离子等措施都将导致自由能减少,膜污染加重[22-23]。
3 结论
1)水溶液中纳米TiO2与HA会发生静电吸附以及配位反应,使纳米TiO2水溶液体系的有效粒径减小,静电斥力变大,纳米TiO2稳定性增强,胶体分散更均匀,易于迁移。
2)混凝剂投加量、pH值、Ca2+浓度都是影响C-UF工艺处理效果的重要因素。PFS浓度为0.46 mmol/L,弱碱性(pH值7~8)时,不添加钙离子,处理效果较好;其中,混凝剂投加量过低或过高,原水pH过低或过高,都会对C-UF工艺处理HA-T复合污染物产生不利影响,使超滤膜过滤通量减小,加重膜污染。
3)当混凝机理为以网捕卷扫、吸附架桥为主,以电性中和为辅时,膜污染较轻,膜通量较高。

