高分辨率CT在特发性肺纤维化诊断中的研究进展
赵大伟, 房学梅, 付维林
特发性肺间质纤维化(idiopathic pulmonary fibrosis,IPF)是原因不明的、慢性、进展性纤维化疾病,是特发性间质性肺炎最主要、最严重的类型。IPF发病率逐年升高,预后差,病死率高,平均生存时间为3~5年[1],大多数患者死于呼吸衰竭和并发症[2]。诊断IPF需除外已知病因的间质纤维化疾病、环境因素致病的纤维化、无胶原血管病[3]。新抗纤维化药物可提高疗效、改善预后[4],要求早期、精确诊断IPF[5,6]。2018年美国胸科协会会议更新IPF诊断指南,对IPF及表现为普通型间质性肺炎(usual interstitial pneumonia,UIP)的高分辨率CT(high resolution CT,HRCT)诊断标准分类为:UIP、可能UIP、不确定、不符合[7]。HRCT也是监测疾病和疗效预测的主要手段[8]。IPF和UIP的概念不可随意互换,UIP不是IPF的同义词。IPF是临床诊断,UIP是IPF的放射、病理学表现形式。本文归纳总结IPF的HRCT表现,解读IPF的影像学诊断标准,并与相关疾病进行鉴别诊断,同时强调HRCT在IPF预后评估方面的重要作用。
IPF的临床特点
IPF主要见于60岁以上老年人,与吸烟明显相关,约2/3的患者有吸烟史[9]。临床表现无特异性,常有原因不明的劳力性呼吸困难、慢性干咳、Velcro啰音等。杵状指常见,几乎所有IPF患者均出现爆裂音,听诊爆裂音可提示IPF[10]。劳力性呼吸困难一般在发病数月至数年后出现。IPF患者常伴胃食管返流,食管裂孔疝可能与IPF发病有关[11]。
IPF的HRCT表现
分布:90%的IPF患者HRCT表现为胸膜下分布[12]。分布的不均匀性:HRCT肺外周部位和胸膜下区不均匀分布,正常肺组织和病变区(网格、牵拉性支气管扩张或蜂窝)交替。病变常呈双侧不对称分布,不同于非特异性间质性肺炎(non-specific interstitial pneumonia,NSIP)(均匀、对称分布)[13]。
网格:Fleischner学会将网格影定义为小叶间、小叶内多余的线影,或由蜂窝壁整体上形成的网状形状[14]。网格影不等同于小叶间隔增厚[15]。网格影一般分布于两肺基底部、胸膜下,常伴结构扭曲。Gruden等[16]认为上叶的网格影对UIP型诊断至关重要。
蜂窝:呈镞状囊性低密度影,囊壁光整,厚度1~3 mm,直径常为3~10 mm,偶尔可达2.5 cm[14]。蜂窝是HRCT的UIP型最具特征性的表现,蜂窝影预测UIP的灵敏度和特异度较高。蜂窝的组成目前尚不清楚,推测为扩张的小气道,是纤维化进展的标志,提示预后差。依据诊断标准,HRCT诊断UIP型需要蜂窝影的存在[17]。但Gruden等[13]发现即便缺乏蜂窝影,如果严格依据特定的CT标准,诊断UIP的精确性依旧很高。蜂窝的诊断主观性较强,放射学医师间存在显著的观察者间差异[18]。因为蜂窝影与牵拉性气管扩张有时难以鉴别,特别是牵拉性支气管扩张和肺气肿共存的情况[19,20],最大密度投影图像有助于鉴别诊断。
磨玻璃密度影:网格内磨玻璃密度影(ground-glass opacification,GGO)代表低于HRCT分辨率的肺纤维化病变,一般不超过网格范围。而网格、蜂窝及牵拉性支气管扩张、细支气管扩张范围外的GGO则提示感染或其他疾病。
肺结构扭曲:影像学上将肺结构扭曲定义为肺小叶结构的改变(从多边形到变小的三角形)、非节段分布(跨越叶间裂胸膜)[16];还可表现为胸膜表面和支气管血管束不规则[21],该征像有助于鉴别过敏性肺炎(肺小叶、叶间裂不受累,节段分布)。
尖-基底分布:UIP典型分布于基底部,但也可分布于上肺。当肺基底部以上肺区内出现网格影,同时伴肺下叶蜂窝影,可诊断UIP。
淋巴结肿大:HRCT上70%~86%的UIP型患者存在纵隔和肺门的淋巴结肿大,25%为非对称分布[16]。
IPF的HRCT诊断标准分类及其发展更新
2011年美国胸科协会(American Thoracic Society,ATS)、欧洲呼吸协会(European Respiratory Society,ERS)、日本呼吸协会(Japanese Respiratory Society,JRS)和拉丁美洲胸科协会(Latin American Thoracic AssociationALTS)联合发布IPF诊疗指南,将HRCT表现分为3类[17]:UIP、可能UIP、不符合UIP(表1)。
UIP:病理学上UIP具有位置异质性和时间异质性[12]。位置异质性指肺纤维化区与正常肺组织相间、分界清晰,仅以菲薄的肺泡壁相隔。时间异质性是指老瘢痕(密集成熟的胶原瘢痕,常伴脂肪、平滑肌化生)和新瘢痕(成纤维细胞灶)共存。相对应的HRCT表现为病变区与正常肺组织相间;病变区内密度不均、分布不均(图1)。HRCT表现为“UIP”,无需外科肺活检可直接诊断为UIP型[7,19],且不同的观察者应用HRCT诊断UIP的一致性高[22]。然而仅约1/3的IPF患者表现为UIP。很多疑诊IPF患者,由于正处于进展期或为了避免可能出现的并发症而不便行肺活检,从而错失只授权于明确诊断IPF患者的治疗。对此,许多研究试图拓展足以精确诊断UIP的HRCT表现范围以避免肺活检[16,23,24]。相关研究认为主要分布于基底部的粗网状影,尽管无蜂窝,对病理学UIP型仍有预测意义[23]。
可能UIP:HRCT表现为可能UIP型的患者需肺活检明确诊断,但实际上很少实行。IPF患者肺活检后并发IPF急性加重,在UIP基础上发生弥漫性肺泡损伤的发病率及病死率不容忽视。Chung等[23]发现可能UIP组与诊断不明确组(不能被诊断为UIP型,可能为UIP型和不符合UIP型的患者)最终病理学诊断为UIP的比例两组差异有统计学意义。Yagihashi等[25]研究证实,HRCT上为“可能UIP”的大部分病例最终病理学诊断为“很可能”和“明确UIP”(图2)。
不符合UIP:HRCT表现复杂多样,如弥漫性空气潴留、弥漫性纵向分布、弥漫性轴位分布、中上叶或广泛分布的GGO等[25]。“不符合UIP”型病例一般较少,出现GGO、空气潴留、实变提示“非UIP”病理诊断,但与病变的分布关系不大。Soo等[15]研究发现,HRCT上“不符合UIP”的病例中94.7%病理学诊断为“UIP”或“很可能UIP” ,认为“不符合UIP”分类使IPF诊断不够明确。Chung等[26]研究认为“不符合UIP”命名存在误导意义,需重新命名。
对此,有研究讨论增加“很可能UIP”的必要性[15,16]。2018年5月ATS会议上,ATS/ERS/JRS/ALTS联合发布更新IPF诊疗指南,将HRCT表现分为4类[7]:UIP、很可能UIP、不确定和不符合(表2)。

表2 2018年修订版IPF放射学诊断标准
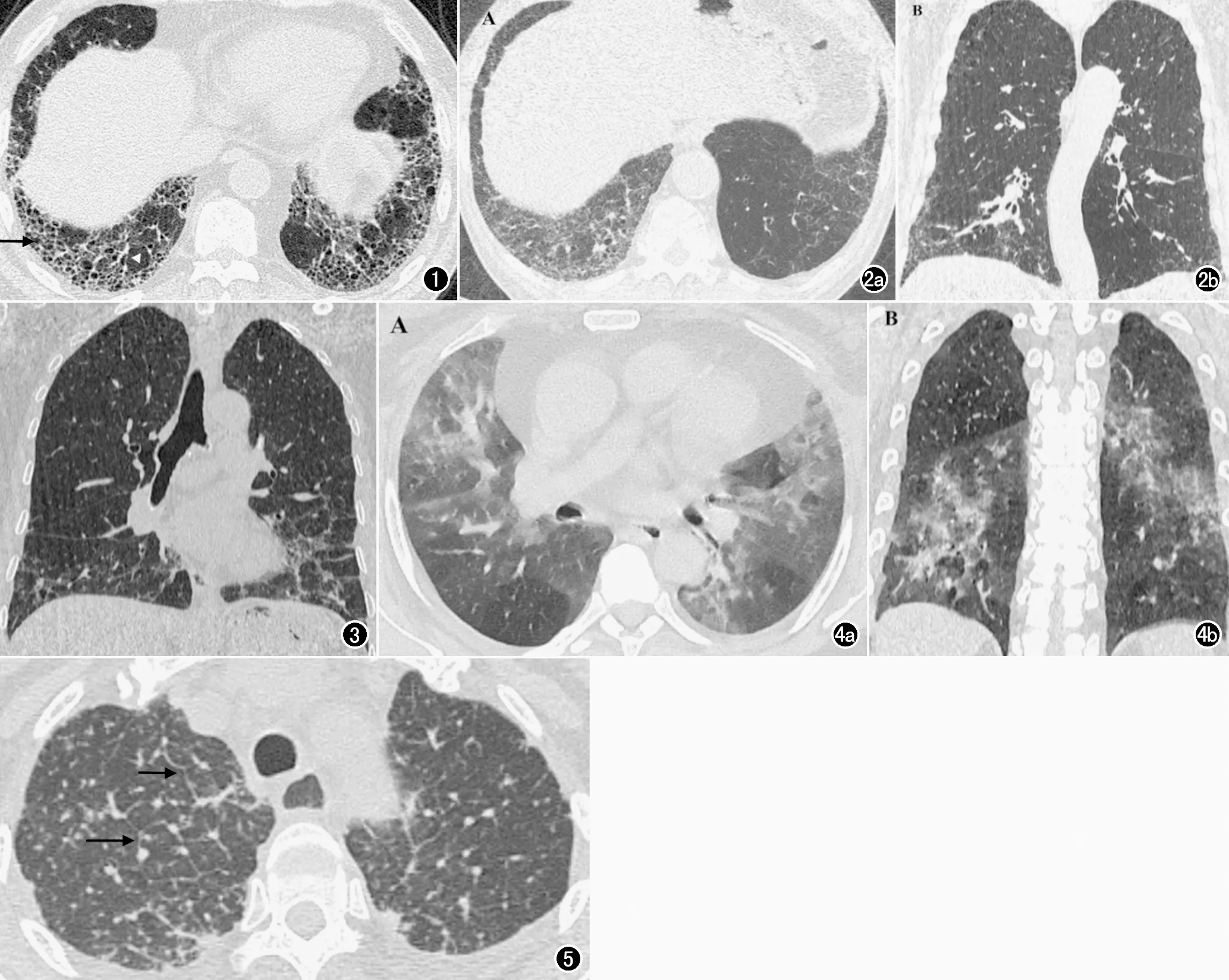
图1 IPF患者,男,61岁。HRCT轴面显示明确UIP型表现:两肺内网状影、蜂窝影(黑箭),伴牵拉性支气管扩张,主要分布于胸膜下及肺基底部。病变具有位置和时间上的不均匀性:病变与正常肺组织(白三角形)相间,病变区内密度不均。 图2 UIP患者,男,73岁。CT诊断为可能型UIP型,但如果考虑患者年龄,可诊断为UIP。CT示以基底部分布为主的网格影,无蜂窝,可见小的牵拉性支气管扩张。a)轴面CT图像;b)冠状面CT图像。 图3 患者,女,55岁,肺活检病理诊断为NSIP,冠状面CT显示“直缘征”存在。 图4 患者,女,46岁,临床诊断为CrHP。a)轴面CT示两肺多发磨玻璃密度影,并可见马赛克征,无小叶中心结节;b)冠状面CT示病变未累及膈面以下肺组织。 图5 慢性肺结节病患者,女,53岁。轴面CT示两肺中上部沿支气管血管束淋巴管分布走形的间质结节影,并可见小叶间隔增厚,网状影(箭)。
对于HRCT表现为UIP型患者,不建议行外科肺活检、支气管肺活检和冷冻肺活检,有选择性地反对支气管肺泡灌洗(Bronchoalveolar lavage,BAL)。建议多学科联合讨论,强烈反对仅将血清标志物作为唯一区分IPF和其他间质性肺炎的方法。对于HRCT表现为很可能UIP、不确定和不符合者,有选择性地建议行BAL和肺活检,但由于缺乏证据,经支气管镜肺活检和冷冻肺活检,推荐与否不明确[7]。
鉴别诊断
非特异性间质性肺炎:非特异性间质性肺炎(non-specific interstitial pneumonia,NSIP)最初指一过性的纤维化过程,病理学表现为肺泡壁和小叶间隔的均匀增厚,在纤维化区域内正常肺组织不可见,可有或无炎性细胞浸润。纤维化型NSIP较细胞型NSIP更加常见。位置异质性、时间异质性和蜂窝一般不可见。大多数NSIP患者HRCT表现为以两肺下叶分布为主的均匀磨玻璃阴影和牵拉性支气管扩张[27]。UIP和NSIP都以两肺下叶分布为主,但是与UIP相比,NSIP一般不累及胸膜下。NSIP也可表现为界线清楚的网格和牵拉性支气管扩张,Salvatore等[12]指出早期UIP分布更不均匀,可位于基底部、胸膜下和间隔旁,而NSIP分布则更加均匀,胸膜下不累及。早期UIP与NSIP鉴别诊断困难,特别是纤维化型NSIP。NSIP病理学与影像学表现变异很大,一些HRCT表现为NSIP的患者最终病理学诊断为UIP。Zhan等[28]发现HRCT未见“直缘征”有助于鉴别NSIP与UIP(图3)。直缘征的定义为孤立于肺基底部的、头向尾方向边缘锋利的、无沿两肺外侧扩张的网格影。Zhan等[28]研究表明双侧肺无直缘征的存在,对于外科肺活检(surgical lung biopsy,SLB)的UIP的诊断敏感度、特异度、阳性预测值、阴性预测值分别为56.9%、93.3%、96.7%和38.9%。
慢性过敏性肺炎:慢性过敏性肺炎(chronic hypersensitivity pneumonitis,CrHP)的病理特征复杂[29],可有多种病理改变重叠组成:UIP型、NSIP型、机化性肺炎(organizing pneumonia,OP)和伴或不伴肉芽肿的小叶中心性纤维化。CrHP的HRCT表现为小叶内间质增厚、小叶间隔不规则增厚、牵拉性支气管扩张、小叶中心结节、马赛克征、网格影、磨玻璃密度影,在疾病的亚急性期可见蜂窝。CrHP的HRCT表现以纤维化为特征。纤维化典型征像包括网格、牵拉性支气管扩张和蜂窝,与病理学纤维化相关性强。纤维化是预测CrHP患者病死率的独立影响因子[30]。CrHP的CT表现可与UIP、纤维化性NSIP类似(图4),最主要的鉴别点为小叶中心性磨玻璃结节、小叶性马赛克征和肺下部不累及[29],小叶中心结节代表细支气管中心的感染[31]。CrHP患者伴发肺气肿不常见。
肺结节病:病理学特点为非干酪样肉芽肿和间质纤维化。纤维化改变常从外周肉芽肿开始,向中心进展,导致彻底的纤维化和透明样变。肉芽肿性炎症特征性分布于支气管血管周围间质间隙、胸膜下间质间隙和小叶间隔内的淋巴管。肺结节病典型的HRCT表现为淋巴管分布的圆形小结节影,直径2~4 cm,呈双侧、对称性分布(图5)。大部分结节随疾病进展逐渐消失,20%患者晚期出现纤维化,以中上叶分布为主[29]。Ⅳ期肺结节病其他HRCT表现包括线状影、牵拉性支气管扩张、肺结构扭曲、纤维化囊肿、肺大泡、间隔旁型肺气肿。蜂窝样的囊肿偶尔可见,分布于肺中上叶胸膜下区,但肺底部不累及。纤维化密度不均,沿支气管血管束分布是鉴别诊断的关键[12]。
HRCT与IPF预后
IPF预后差,在HRCT表现为“UIP”或“可能UIP”的IPF患者,较“不符合UIP”者生存期更短。Kondoh等[32]发现HRCT同样表现为"可能UIP"的IPF患者的预后,较非IPF患者(如NSIP、CrHP和未分类IIPs)差。HRCT表现为NSIP、病理学表现为UIP(不一致的UIP)的患者,存活率高于那些表现一致的UIP患者。Arcadu等[33]研究IPF患者不同HRCT表现型与肺功能之间的关系,发现肺功能检查结果与不同的UIP型无明显相关性,而与疾病的范围相关性非常好。纤维化的进展速度也是重要的预后影响因素。
HRCT对于IPF的诊断至关重要,熟悉IPF的HRCT表现及其分类标准是正确诊断的前提。尽管IPF与NSIP、CrHP、Ⅳ期结节病的HRCT表现有重叠,但一些特征性表现有助于鉴别诊断。同时HRCT在IPF的预后评估方面也有着重要作用。

