门氏芪元颗粒的制备工艺研究
靳贝贝 郭鹏飞 梅桂馨 裴香萍 梁惠珍 门九章

【摘 要】 目的:建立门氏芪元颗粒的制备工艺方法。方法:以出膏率和颗粒中黄芪甲苷提出量为评价指标,影响因素分别为加水量、提取次数和提取时间,采用L9(34)正交设计试验法优选门氏芪元颗粒的最佳提取工艺。以颗粒的成型性、溶化性、吸湿性、堆密度和休止角的综合评分为评价指标筛选辅料糊精、淀粉的比例确定最佳制备工艺。结果:10倍量水、每次0.5h、提取3次为最佳提取工艺;润湿剂95%乙醇,药粉:糊精:淀粉的比例为4∶1∶3为最佳制备工艺。结论:门氏芪元颗粒的提取工艺和制备工艺稳定、可行,评价指标合理、可靠。
【关键词】 门氏芪元颗粒;提取工艺;制备工艺;正交试验法;黄芪甲苷
【中图分类号】R283.3 【文献标志码】 A【文章编号】1007-8517(2019)12-0034-05
Study on Preparation Process of Mens Qiyuan Granules
JIN Beibei1 GUO Pengfei1 MEI Guixin1 PEI Xiangping1* LIANG Huizhen1 MEN Jiuzhang2
1.College of Traditional Chinese Medicine, Shanxi University of Traditional Chinese Medicine, Jinzhong 030619, China;
2.Integrated Traditional Chinese and Western Medicine, Shanxi University of Traditional Chinese Medicine, Jinzhong 030619, China
Abstract:Objective To establish the extraction and preparation process of Mens Qiyuan granules.Methods The extraction rate and the amount of astragaloside IV in the granules were used as the evaluation indexes. The water addition, extraction times and extraction time were the influencing factors. The best extraction process of Mens Qiyuan granules was optimized by L9(34) orthogonal design test method.The optimum preparation process was determined by screening the ratios of excipient dextrin and starch by using the comprehensive scores of the formability, solubility, hygroscopicity, bulk density and angle of repose of the particles as the evaluation index.Results The optimal extraction process was: 10 times the amount of water, each time 0.5h,extraction 3 times; the best preparation process was wetting agent 95% ethanol, powder: dextrin: the ratio of starch was 4∶1∶3.Conclusion The extraction process and preparation process of Mens Qiyuan granules are stable and feasible, and the evaluation indexes are reasonable and reliable.
Key words:Mens Qiyuan Granules;Extraction Process; Preparation Process; Orthogonal Test Method; Astragaloside IV
門氏芪元颗粒来源于山西名医门九章教授的经验方门氏芪元汤,由黄芪、当归、玄参、金银花等中药组成。门氏芪元汤临床使用多年,具有益气养阴,化瘀解毒的功效,用于气阴两虚证。方中的金银花具有抗内毒素、解热、抗炎作用[1],玄参、当归含有多糖[2]、黄酮类化合物[3]、挥发油[4]等多种化学成分,具有抗肿瘤、抗氧化等生理活性[5-7],黄芪主要有效成分为黄芪甲苷,具有免疫调节、降糖、抗病毒等药理作用[8]。本方在临床上疗效明确,为满足临床用药需求,将其由传统汤剂研发成为医院颗粒制剂。门氏芪元颗粒欲申报医院制剂,中试生产已经完成,质量标准也已经确定,本研究通过L9(34)正交设计试验法优选门氏芪元颗粒的最佳提取工艺,然后通过考察不同辅料配比、润湿剂用量,以颗粒成型性、溶化性、吸湿率、堆密度及休止角为指标,筛选处方中加入辅料配比及最佳成型工艺,为门氏芪元颗粒的制备工艺研究提供科学依据。
1 仪器与试药
1.1 仪器 Waters-e2695高效液相色谱仪及Waters-2424蒸发光散射检测器(美国Waters公司);BGZ-76型烘箱(上海博讯实业有限公司医疗设备厂);TDZ5-WS型离心机(湖南湘立科学仪器有限公司);DiamonsilC18色谱柱(4.6mm×200mm,5μm);微量进样器(批号:113048;上海高鸽工贸有限公司);SB-5200DTDN超声清洗器(新芝生物科技股份有限公司);AB-135型十万分之一电子天平(瑞士METTLER公司);FA2014型万分之一天平(上海科技有限公司);FW100型万能粉碎机(北京市永光明医疗仪器有限公司);定性滤纸(杭州富阳北木浆纸有限公司),蒸锅,烧杯,量筒,砝码,培养皿,蒸发皿,玻璃棒,漏斗,纱布,塑料布,药匙,筛网,5mL离心管,分液漏斗,玻璃干燥器,称量瓶。
1.2 试药 黄芪药材(太谷县广源堂药业有限公司,市售,1.0kg/袋,批号:1607001);玄参药材(河北全泰药业有限公司,市售,1.0kg/袋,批号1608003);当归药材(郑州瑞龙制药股份有限公司,市售,1.0kg/袋,16120102);金银花药材(河北全泰药业有限公司,市售,1.0kg/袋,批号:1608201);糊精(天津市科密欧化学试剂有限公司,500g/瓶);可溶性淀粉;氯化钠。
2 方法与结果
2.1 门氏芪元颗粒提取工艺
2.1.1 单因素考察 分别对溶剂倍量、提取时间、提取次数进行了考察,结果表明溶剂倍量为14倍、提取次数为3次,每次1.0h时,综合评分达到最大;提取次数不断增加,综合评分也随之增加。
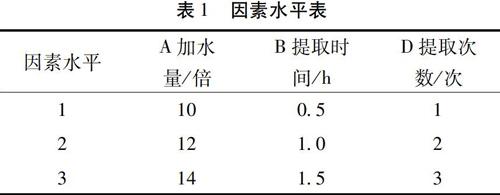
2.1.2 正交试验设计 以出膏率、黄芪甲苷的提出量作为考察指标,以水为提取溶剂,进行L9(34)正交试验[9]选择三个影响因素分别为加水量(A),提取时间(B)和提取次数(D),确定提取的最佳条件。
2.1.3 按照处方称取各药材,共9份,按表1正交试验设计方案进行提取,计算出膏率。
2.2 黄芪甲苷含量测定
2.2.1 色谱条件 Diamonsil C18色谱柱(200mm×4.6mm,5.0μm);以乙腈-水(32∶68)为流动相,流速为1.00mL/min;柱温:30℃;蒸发光散射检测器参数;载气流速2.1L/min,漂移管温度为100℃。
2.2.2 对照品溶液的制备[10] 精密称取黄芪甲苷对照品加甲醇制备0.314mg/mL的对照品溶液。
2.2.3 供试品溶液的制备[11] 精密称取样品干膏2.0g,置锥形瓶中并精密加入甲醇100mL,加热回流1h,冷却,过滤。用甲醇少量多次洗涤药渣,合并滤液,蒸干,残渣加水20mL使其溶解。加水饱和正丁醇液40mL,振摇提取3次,合并正丁醇液,加氨水40mL,洗涤3次。弃去氨液,蒸干正丁醇液,残渣用甲醇溶解,作为供试品溶液。
2.2.4 标准曲线的绘制 分别精密吸取黄芪甲苷对照品储备溶液4、8、10、12、16、20μL,注入高效液相色谱仪,以黄芪甲苷进样质量的对数为横坐标,峰面积的对数为纵坐标,绘制标准曲线,回归方程为Y=1.6442X+5.3244,r=0.9999,在1.256~9.420μg范围内线性关系良好。结果见表2和图1。
2.2.5 测定法 采用高效液相色谱法,精密吸取供试品溶液20μL,记录峰面积,计算黄芪甲苷的提出量。
2.2.6 测定结果 见表3。
通过表3极差r可知,三个影响因素的影响大小是:D>A>B,即提取次数影响最大,而提取时间影响最小。直观分析可得,较佳提取工艺条件为:A3B2D3,即14倍量水,提取3次,每次1.0 h。从表4方差分析可知,B和A因素没有显著性影响,D因素有显著性影响。综合考虑经济效益等因素,得出门氏芪元颗粒的最佳提取工艺为:A1B1D3,即10倍量水,提取3次,每次0.5h。
2.2.7 工艺验证 按处方比例称取药材3份,按最佳提取工艺进行提取,按照供试品溶液的制备方法进行制备,记录峰面积,计算出膏率和黄芪甲苷的提出量,结果见表5。
2.3 制剂成型工艺研究
2.3.1 制粒方法选择 湿法制粒[12]是当前最为广泛应用的制粒方法,在制粒之前将粘合剂或者湿润剂等添加到药粉中,将药粉制成湿润颗粒,其制粒效果较高。通过湿法制粒增强了颗粒的粘合性且颗粒容易成型。采用稠浸膏干燥,粉碎后以相应比例的辅料补足至处方量,混匀,制成颗粒。本制剂采用药粉∶辅料=1∶1。
2.3.2 润湿剂的选择 本复方在经过水煎煮浓缩后发现稠膏黏性较强,而且含糖量高。颗粒制剂过程中以一定浓度的乙醇为润湿剂,降低粘性和吸湿性便于颗粒成型。以手捏成团,轻压则散为原则筛选乙醇的浓度。结果见表6和图2~4。
因此,选择95%的乙醇做为润湿剂进行制粒。
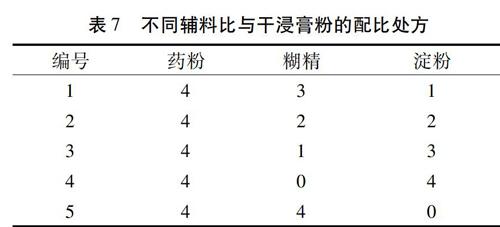
2.3.3 吸收剂淀粉、糊精用量的选择 选择糊精和可溶性淀粉作为辅料进行处方筛选。结果见表7。
2.3.4 颗粒成型性比较 将干浸膏粉按表表六中方法与相应辅料混匀,95%乙醇制粒。以筛分法[13]对颗粒进行测定,取平均值。结果见表8。
成型率=(过筛后颗粒的质量/过筛前颗粒的质量)×100% 。
2.3.5 颗粒溶化性比较 精密称定的颗粒0.2g,加入干燥恒重的5mL离心管中,精密加入沸水5mL,振荡5min,3000r/min离心15min,弃去上清液,80℃进行干燥,精密称定重量,计算溶化率。结果见表9。
溶化率=溶化颗粒质量/颗粒质量×100%。
2.3.6 颗粒吸湿率的比较 在玻璃干燥器装入过饱和室温氯化钠溶液,置于25℃的恒温培养箱24h,干燥器内部相对湿度为75%,在已恒重的称量瓶底部放入各处方颗粒,准确称重后置于装有过饱和氯化钠溶液的玻璃干燥器内(称量瓶盖打开),放于25℃恒温培养箱,72h后称定重量,计算颗粒吸湿百分率[14]。结果见表10。
吸湿百分率(%)=(吸湿后颗粒质量-吸湿前颗粒质量)/吸湿前颗粒质量×100%。
2.3.7 堆密度的测定 将过筛后的质量作为M(g)并装入干燥的量筒中,轻轻振动,记录体积(V),两者的比值即为堆密度。结果见表11。
堆密度=M/V。
2.3.8 休止角的测定 采用固定漏斗法,计算休止角tga=H/R.重复做5次,计算平均值。结果见表12。
2.3.9 綜合评分 根据表中综合评分可知,处方3号92.23分为最高分,故筛选最优原辅料配比为浸膏粉∶糊精∶淀粉=4∶1∶3,95%的乙醇进行制粒。见表13。
2.4 门氏芪元颗粒样品 见图5。
3 讨论
提取工艺的确定 采用正交试验和高效液相色谱法,以出膏率和黄芪甲苷在复方中的提出量为评价指标进行评价。最后确定的提取工艺为:10倍量水,提取3次,每次0.5h。
颗粒成型工艺的确定 按最优原辅料配比,即处方浸膏粉∶糊精∶可溶性淀粉=4∶1∶3,以95%乙醇为润湿剂制粒。
门氏芪元颗粒来源于名老中医门九章经验方门氏芪元汤,临床效果良好,中药汤剂作为中医临床用药的主要剂型,可以随证加减、灵活组方,但攜带、煎煮不便,汤液味苦量大,不易被接受。中药配方颗粒与传统汤剂相比不需要煎煮,服用时温开水配成冲剂即可,便于携带、保存方便;解决了传统中药保质期短、中药饮片易潮易虫蛀的缺点。
本方为复方,所含成分较多,若使用紫外检测波长检测杂质对色谱峰的干扰较大。而ELSD检测器作为一种通用型的的检测器,可检测挥发性低于流动相的任何样品,不需要样品含有发色基团。基线稳定仅对不挥发性物质颗粒进行检测,不存在紫外末端吸收的问题,流动相低温雾化和蒸发,对热不稳定和挥发性化合物亦有较高灵敏度,对温度变化不敏感,即使在梯度洗脱时基线也很平稳,所以本文最终确定了用 HPLC-ELSD方法对门氏芪元颗粒中的黄芪甲苷进行含量测定。
中药颗粒剂是以中药汤剂为原料,经过提取、分离、制粒、干燥、制粒过程完成,且成分较为复杂,为充分发挥中药的各种成分,提高中药颗粒的疗效,在中药颗粒剂提取、纯化分离、制粒过程中需认真仔细,中药颗粒剂发展迅速,可取代传统中药汤剂,满足人们用药治病的需求。
参考文献
[1]雷玲,李兴平,白筱璐,等.金银花抗内毒素、解热、抗炎作用研究[J].中药药理与临床,2012,28(1):115-117.
[2]曹蔚,李小强,侯颖,等.当归酸性多糖的分析[J]. 药物分析杂志,2007,27(12):1898-1902.
[3]张新国,王强林,李春雷,等.当归多糖的酶法提取新工艺研究[J].中医药学报,2012,40(3):96-100.
[4]谢小艳,夏春森.中药玄参的化学成分及药理研究进展[J].亚太传统医药,2010,6(5):121.
[5]吴素珍,李加林,陈水亲,等.硫酸酯化当归多糖抗肿瘤实验研究[J].时珍国医国药,2012,23(2):319-320.
[6]Gao M,Zhang JH,Zhou FX,et al.Angelica sinensis suppresses human lung adenocarcinoma A549 cell metastasis by regulating MMPs/TIMPs and TGF-β1[J].Oncology Reports,2011,7(2):585-593.
[7]Hung JY,Yang CJ,Tsai YM,et al.Antiproliferative activity of aucubin is through cell cycle arrest and apoptossis in human non-small cell lung cancer A549 cells[J].Clin Exp pharmacol physiol,2008,35(9):995.
[8]W J Zhang,P Hufnagl,B R Binder,et al.Antiinflammatory activity of astragaloside IV is mediated by inhibition of NF-kappaB activation and adhesion molecule expression[J].Thromb Haemostasis,2003,90(5): 904.
[9]陈阿丽,崔永霞,周立艳,等.正交试验法优选人参水提工艺[J].中国现代药物应用,2009,3(9):21-22.
[10]国家药典委员会.中华人民共和国药典[M].一部.北京:中国医药科技出版社,2015:338-339.
[11]王俊香.张华.黄芪醇提工艺研究[J].辽宁中医药大学学报,2012(2):179-180.
[12]王弘,郭代红,刘皈阳.湿法制粒工序参数的应用进展[J].中国新药杂志,2007,16(5):361-365.
[13]国家药典委员会.中华人民共和国药典[M].四部.北京:中国医药科技出版社,2015:132-134.
[14]谢冬梅.顽痹康颗粒制备工艺、质量标准及车间工艺初步设计[D].济南:山东大学,2007.

