咪唑啉固体缓蚀剂的溶解性能及缓蚀性能
(长江大学 化学与环境工程学院,荆州 434023)
缓蚀剂可抑制金属材料腐蚀,因而广泛应用于石油工业中[1],其主要形态为液体缓蚀剂和固体缓蚀剂[2-9]。液体缓蚀剂优点突出,但在特殊情况下具有显著的缺陷。液体缓蚀剂在油气井中的有效含量维持时间短,必须采取连续加药措施,这会导致成本升高、投加难度增大,且不能有效保护油管尾部以下套管的腐蚀。在苛刻条件下,由于产出液流速快,井内产生的压力大,液体缓蚀剂无法加入,即使加入因停留时间短而达不到理想的缓蚀效果,导致液体缓蚀剂无法正常使用[10-15]。与液体缓蚀剂相比较,固体缓蚀剂具有投加工艺简单,有效含量维持时间长等优点,广泛适用于上述特殊工况条件下[16-18]。
针对油气田用液态缓蚀剂使用的缺陷,本工作采用胶结黏合法制备了一种咪唑啉固体缓蚀剂,并通过设计五因素四水平的正交试验,确定了固体缓蚀剂的最佳配方;采用静态玻管法、失重法、动电位极化曲线、电化学阻抗谱、扫描电镜等方法对固体缓蚀剂的溶解特性及缓蚀行为进行了研究。
1 试验
1.1 试验材料、试剂和仪器
试验材料为N80钢,主要化学成分(质量分数)为0.35% C,0.33% Si,1.65% Mn,0.02% P,0.015% S,余量为Fe。将N80钢加工成用于浸泡试验的片状试样(40 mm×13 mm×2 mm)和用于电化学测试的圆柱状电极试样(留出1 cm2工作面积,其余的部分用环氧树脂涂封)。所有试样用400号,800号,1 200号金相砂纸逐级打磨光滑,使其表面各处的表面粗糙度一致。
1.2 固体缓蚀剂的合成
1.2.1 咪唑啉季铵盐主剂的合成
在一个装有温度计、搅拌器、冷凝管、分水器的三口烧瓶中按一定的比例依次加入油酸、二乙烯三胺、二甲苯混合均匀,其中二甲苯为携水剂。逐渐升温至160 ℃酰化反应4 h,再逐渐升温至220 ℃进行环化反应4 h,然后冷却到140 ℃减压蒸馏出多余的二甲苯和二乙烯三胺,再冷却到110 ℃左右按比例逐滴加入氯化苄,保温反应4 h得到油酸咪唑啉季铵盐主剂。
采用Nicolet 6700智能型傅立叶变换红外光谱仪对合成产物的成分进行表征。
1.2.2 固体缓蚀剂的合成
将增效剂、助剂、致孔剂按比例混合均匀加入到主剂中,最后加入黏合剂搅拌均匀,加热到一定的温度,使所有试剂熔融成液态倒入模具中,冷却至常温,脱模成型后即可得到固体缓蚀剂。
1.3 正交试验设计
在固体缓蚀剂的合成时,根据固体缓蚀剂的组成和各组分的加量设计5因素4水平的正交试验,如表1所示,并以失重法计算的缓蚀率ηw为判断缓蚀性能优劣的指标,确定固体缓蚀剂的最佳合成配方。
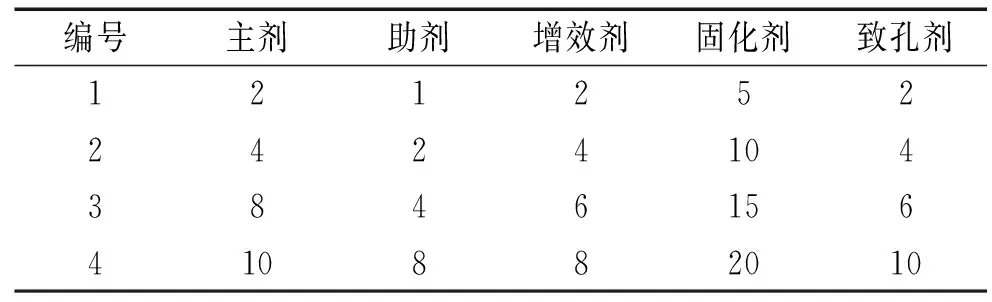
表1 正交试验5因素4水平表Tab. 1 Orthogonal table of five factors and four levels g
1.4 性能评价
1.4.1 浸泡试验
对N80钢进行浸泡试验,并参照SY/T 5273-2014《油田采出水用缓蚀剂性能评价方法》采用静态失重法评价缓蚀剂的缓蚀性能。用丙酮清洗去除试样(上述片状试样)表面的油,再用无水乙醇脱水、脱脂,将清洗干净后的试片置于干净滤纸上,冷风吹干,在干燥器中干燥4 h后称取质量。在试验瓶中加入5%(质量分数)HCl溶液及不同量固体缓蚀剂,浸泡时间为24 h后,将处理好的试样悬挂于试验瓶中,保证试样与容器壁不能接触,相同条件下取2个平行样,将密封的试验瓶放入恒温水浴中,静置一个试验周期。到达腐蚀时间后,取出试片并记录试片表面状态及腐蚀产物分布,用水清洗、并清除其表面腐蚀产物,干燥至恒重,精确称取试片质量。根据式(1)计算腐蚀速率,根据式(2)计算缓蚀率。
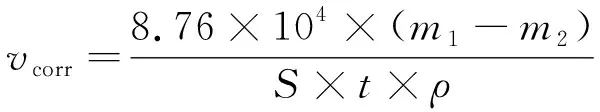
(1)

(2)
式中:vcorr为均匀腐蚀速率,mm/a;m1为试验前试片质量,g;m2为试验后试片质量,g;S为试片的总面积,cm2;t为试验时间,h;ρ为试片材料的密度,g/cm3;ηw为缓蚀率,%;v0为未加缓蚀剂的腐蚀速率,mm/a;v为加入缓蚀后的腐蚀速率,mm/a。
1.4.2 电化学试验
电化学测试在CHI660电化学工作站上进行。工作电极为N80钢,辅助电极为铂电极,参比电极为饱和甘汞电极(SCE)。极化曲线测量时电位扫描由阴极向阳极进行,扫描速率为 0.5 mV/s,扫描范围为-200~200 mV(相对开路电位),试验溶液为5%(质量分数)HCl溶液,温度20~80 ℃,在试验溶液中加入不同量的固体缓蚀剂(在最优合成条件下合成)。根据Tafel曲线外推得到的腐蚀电流密度评价缓蚀剂的缓蚀率ηP,如式(3)所示。
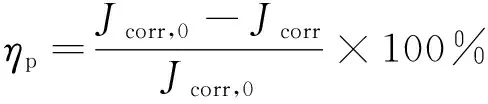
(3)
式中:Jcorr为加入缓蚀剂后的腐蚀电流密度,Jcorr,0为未加缓蚀剂时的腐蚀电流密度。
电化学阻抗施加的交流信号幅值为10 mV,从高频向低频扫描,扫描频率范围为1~105Hz,试验溶液为15%(质量分数)HCl溶液,温度60 ℃,在试验溶液中加入不同量的固体缓蚀剂。采用 Zview软件对电化学阻抗谱进行解析,得到极化电阻Rp,并按式(4)计算缓蚀率ηR。
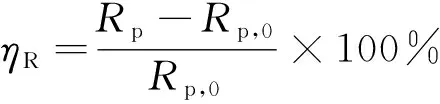
(4)
式中:Rp,0和Rp分别为未添加缓蚀剂和添加缓蚀剂时的极化电阻。
1.4.3 固体缓蚀剂的溶解性评价
采用静态玻管法对30 g棒状的固体缓蚀剂(在最优合成条件下合成)进行塑模封闭处理,并加固,使其一端裸露,静止浸入到60 ℃水中使其溶解,定期更换介质,计算其在水中的溶出率和溶出速率。溶出率和溶出速率的计算公式为
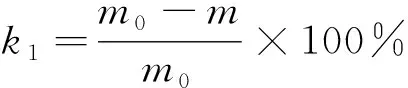
(5)

(6)
式中:k1为溶出率;k2为溶出速率,g/h;m0为溶解前质量,g;m为溶解后质量,g;t为溶解时间,h。
1.4.4 表面形貌观察
将N80钢在未添加固体缓蚀剂的5% HCl溶液和加入150 mg/L固体缓蚀剂的5% HCl溶液中腐蚀4 h,温度为60 ℃,然后用S-250型扫描电镜(SEM)观察其表面腐蚀形貌,并与未腐蚀的N80钢进行比较。
2 结果与讨论
2.1 合成产物的红外光谱
图1为合成的咪唑啉季铵盐的红外光谱。由图1可知,在1 605.62 cm-1处有C═N双键吸收峰,2 853.96 cm-1和2 925.77 cm-1处有C-H的伸缩振动峰,1 455 cm-1处是-CH2-剪式弯曲振动的吸收峰,合成的咪唑啉季铵盐除了有咪唑啉环的特征吸收峰外,还有咪唑啉季铵盐的特征吸收峰,在700~800 cm-1处有单取代苯的特征吸收峰。因此,可以确定合成的产物为咪唑啉季铵盐。
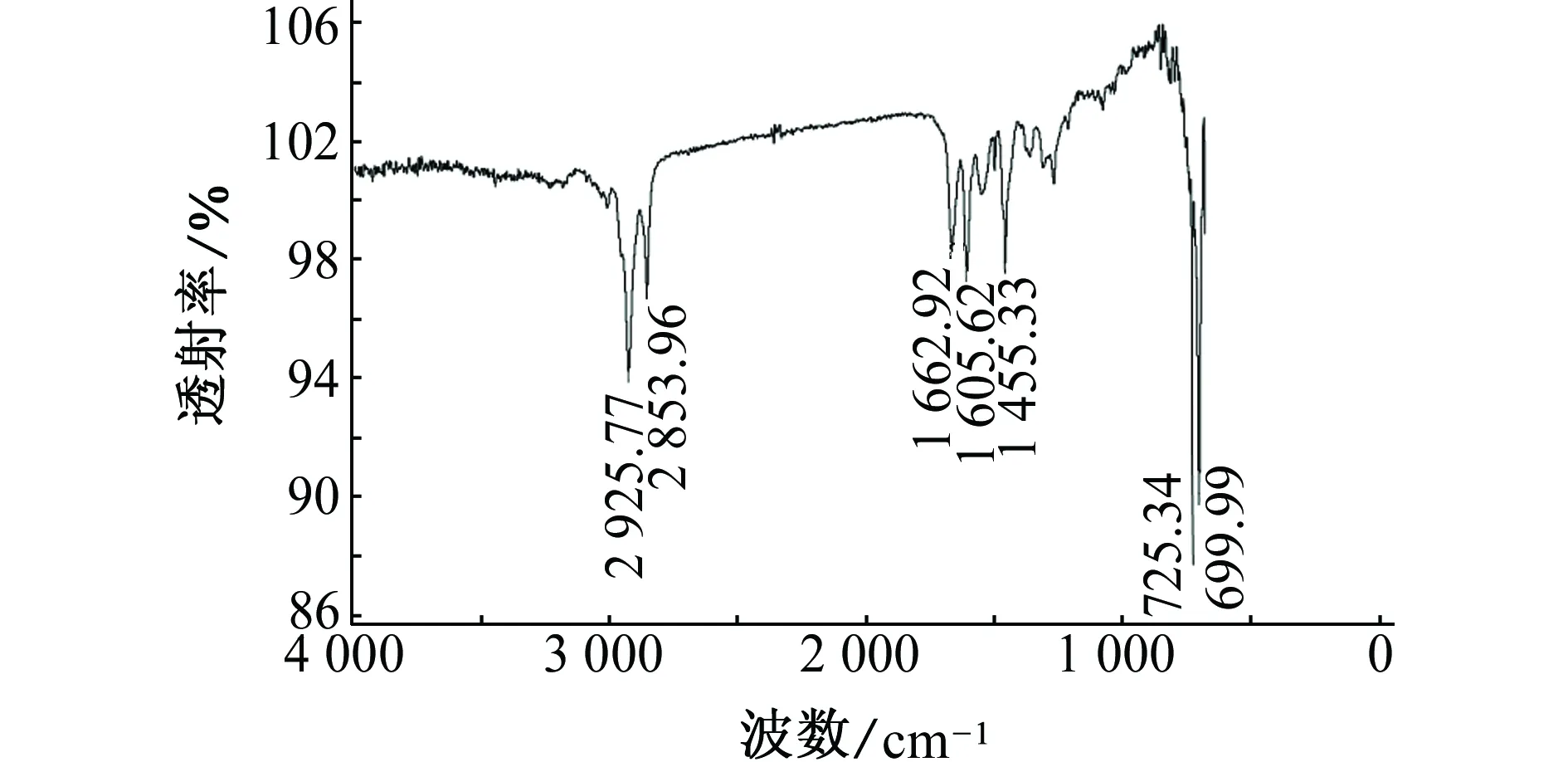
图1 合成的咪唑啉季铵盐的红外光谱Fig. 1 Infrared spectrum of synthesized imidazoline quaternary ammonium salt
2.2 固体缓蚀剂的合成优化
对正交试验结果进行分析,见表2。由表2可知,各因素对缓蚀率的影响顺序为:主剂>固化剂>增效剂>助剂>致孔剂。根据极差分析得最优合成条件为:主剂10 g,固化剂20 g,增效剂2 g,助剂4g,致孔剂2g。以下试验均是在最优合成条件基础上进行的。
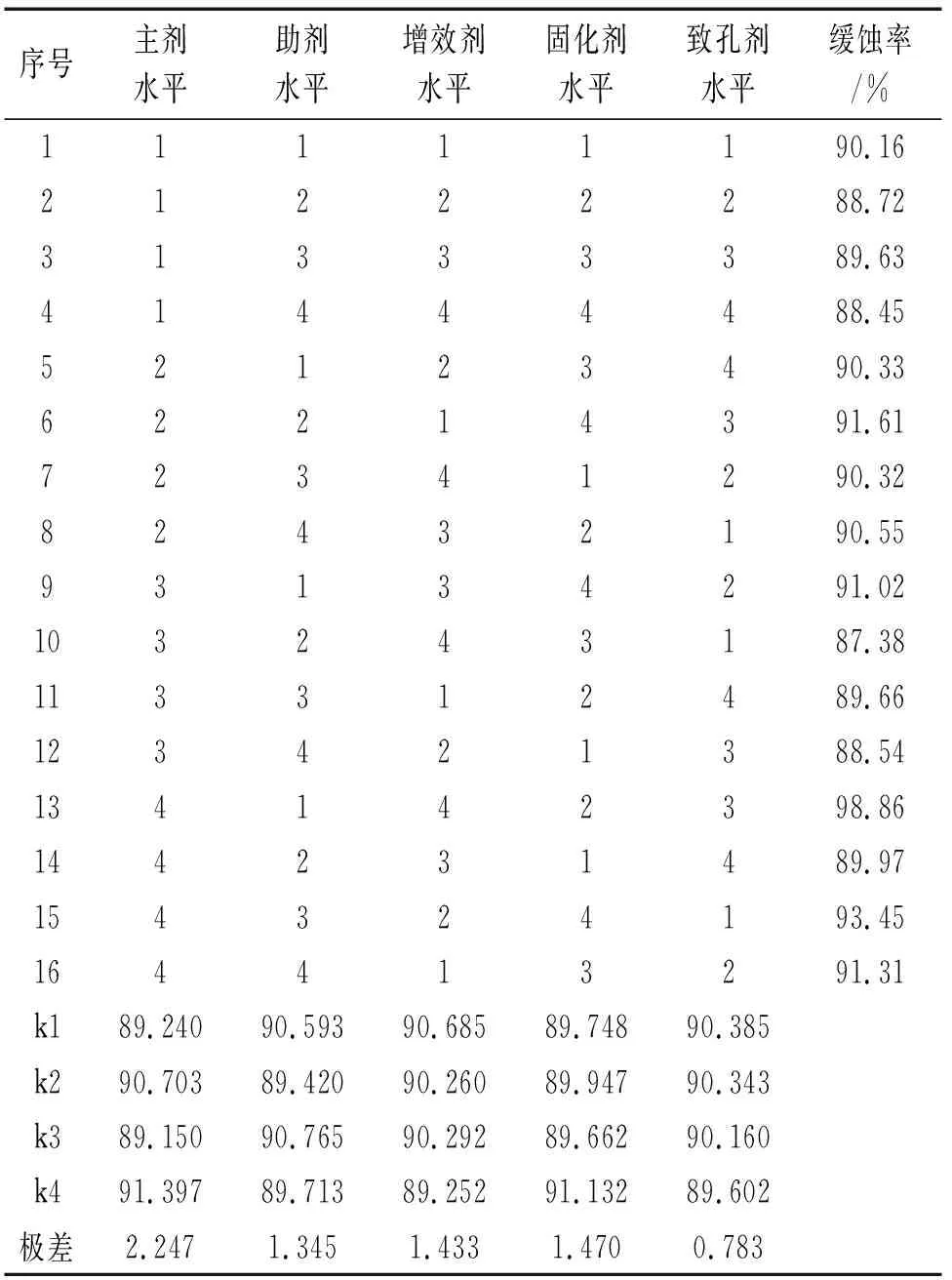
表2 正交试验结果及分析Tab. 2 Results and analysis of orthogonal experiment
2.3 固体缓蚀剂的溶解性
按照静态玻管法计算固体缓蚀剂的溶解结果如图2所示。由图2可知:随着放置时间的延长,固体缓蚀剂的溶出率逐渐增大,溶出速率逐渐减小,72 h后溶出速率为0.403 g/h,是一种缓释型缓蚀剂。固体缓蚀剂的长效缓蚀机理由骨架材料的溶解和缓蚀剂的扩散来实现。固体缓蚀剂的溶解分为两个阶段。第一阶段为表层骨架材料和缓蚀剂的溶解,当固体缓蚀剂加入到腐蚀介质中,表层骨架材料首先与介质直接接触,缓慢溶解到介质中,接着处于表层的致孔剂也随之溶解到介质中,致孔剂溶解后使骨架材料中形成许多孔道,缓蚀剂的主要成分沿着这些孔道扩散。随着溶解时间的延长,致孔剂的溶解限制了缓蚀剂在孔道中的扩散,从而导致溶出速率降低。第二阶段是缓蚀剂从内部骨架材料向外扩散。随着时间的延长,外层骨架材料溶解达到稳定的状态,由于扩散路径的延长,致孔剂的溶出速率越来越慢,因此缓蚀剂从内部向外的扩散速率减缓,固体缓蚀剂的溶解进入缓慢释放阶段,使缓蚀剂的有效成分可以维持更长的时间,从而达到长效缓蚀的目的。
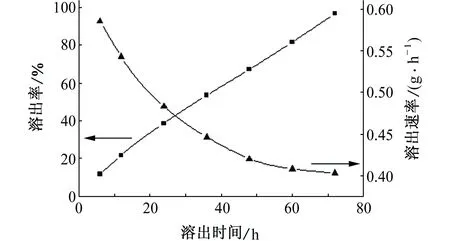
图2 静态玻管法测定结果Fig. 2 The results of static glass tube method
2.4 极化曲线
在不同温度、不同固体缓蚀剂加量的5% HCl溶液中进行动电位极化曲线测试,结果见图3,对极化曲线进行拟合,得到的电化学参数见表3。
由图3可知:添加了固体缓蚀剂后,自腐蚀电位正移,表明制备的固体缓蚀剂是一种阳极型缓蚀剂,随着固体缓蚀剂加量的增大,阴阳极极化曲线均向低电流方向移动,表明加入固体缓蚀剂后能同时抑制阳极的溶解和阴极析氢过程,缓蚀剂浓度越大缓蚀效果越好。由表3可见:加入固体缓蚀剂后,腐蚀电流密度明显减小,表明固体缓蚀剂的加入抑制了N80钢的腐蚀,且随着缓蚀剂加量的不断增大,腐蚀电流密度越来越小,这是因为固体缓蚀剂在介质中溶解后在N80钢表面形成的吸附膜越来越致密,阻止了腐蚀介质与金属基体的接触,从而抑制了金属的腐蚀;同时,在相同的缓蚀剂加量下,随着温度的升高,缓蚀率逐渐降低,因为主剂咪唑啉季铵盐是一种吸附型缓蚀剂,随着温度的升高,咪唑啉季铵盐可能会发生分解和脱附,导致钢材基体与腐蚀介质重新接触,而且温度的升高会增加H+的活性,使金属的腐蚀速率增大,缓蚀率降低。
2.5 电化学阻抗谱
在60 ℃下,测定了N80钢在添加不同量固体缓蚀剂的15% HCl溶液中的电化学阻抗谱,如图4所示,其电化学参数如表4所示。其中,Rs是溶液电阻,Rp是极化电阻。

(a) 20 ℃ (b) 40 ℃
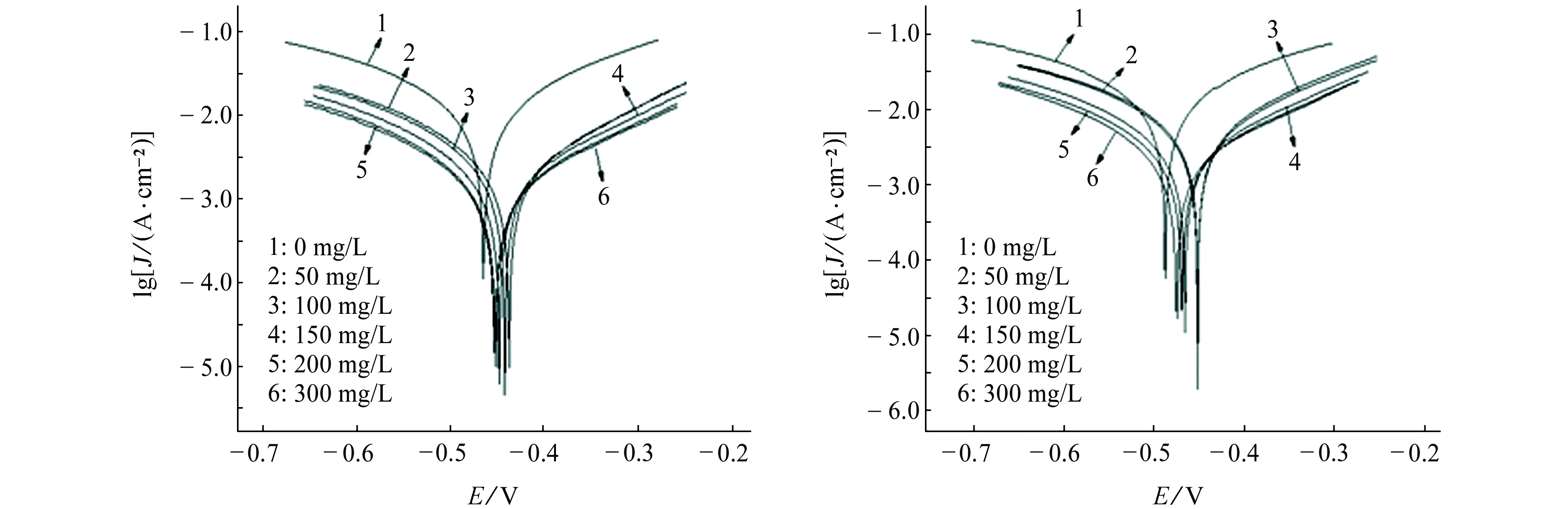
(c) 60 ℃ (d) 80 ℃图3 N80钢在不同温度及固体缓蚀剂加量的HCl溶液中的极化曲线Fig. 3 Polarization curves of N80 steel in HCl solutions added with different dosages of solid corrosion inhibitor at different temperatures
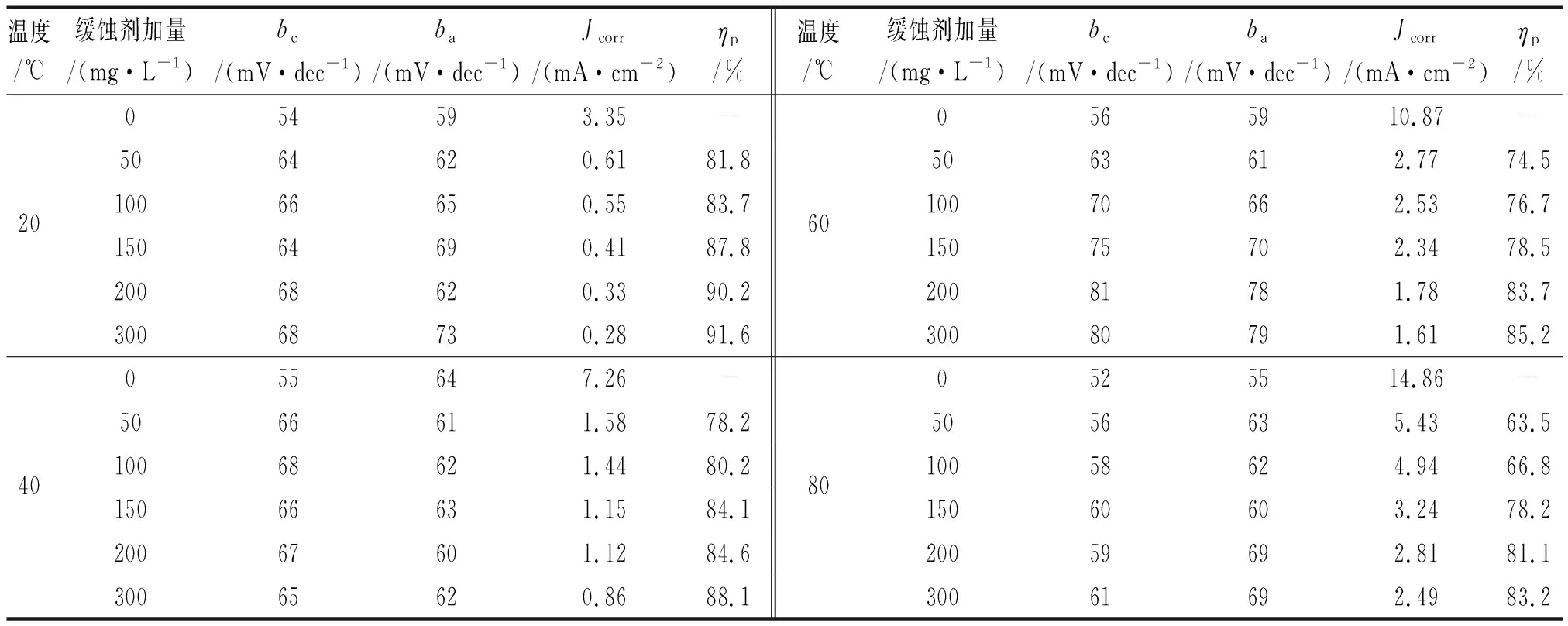
温度/℃缓蚀剂加量/(mg·L-1)bc/(mV·dec-1)ba/(mV·dec-1)Jcorr/(mA·cm-2)ηp/%温度/℃缓蚀剂加量/(mg·L-1)bc/(mV·dec-1)ba/(mV·dec-1)Jcorr/(mA·cm-2)ηp/%054593.35-0565910.87-5064620.6181.85063612.7774.52010066650.5583.76010070662.5376.715064690.4187.815075702.3478.520068620.3390.220081781.7883.730068730.2891.630080791.6185.2055647.26-0525514.86-5066611.5878.25056635.4363.54010068621.4480.28010058624.9466.815066631.1584.115060603.2478.220067601.1284.620059692.8181.130065620.8688.130061692.4983.2
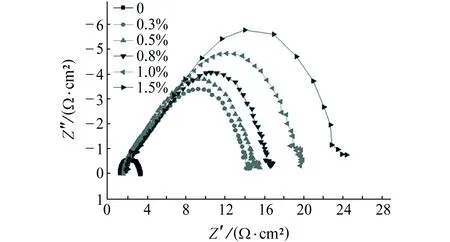
图4 N80钢在不同固体缓蚀剂加量15% HCl溶液中的Nyquist曲线Fig. 4 Nyquist curvs of N80 steel in 15% HCl solution added with different dosages of solid corrosion inhibitor
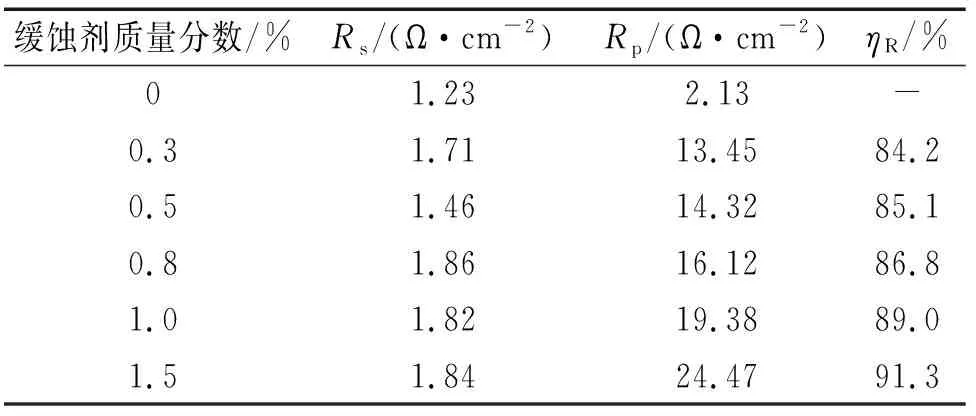
表4 图4中电化学阻抗谱的电化学参数及其相应的缓蚀率Tab. 4 Electrochemical parameters of EIS in figure 4 and relative inhibition efficiency
从图4和表4可以看出:与空白HCl溶液相比,在添加了固体缓蚀剂的HCl溶液中容抗弧明显增大,容抗弧的直径对应的是极化电阻(Rp),Rp越大,缓蚀率越高;随着缓蚀剂加量的增加,容抗弧的直径越来越大,即Rp越来越大,缓蚀率随之增大,腐蚀抑制效果越来越好。
2.6 吸附机理
腐蚀过程可以认为是一种Arrhenius反应过程,根据Arrhenius公式,N80钢发生腐蚀的表观活化能可由式(7)给出。
lnJcorr=-Ea/RT+A
(7)
式中:Jcorr为腐蚀电流密度,mA/cm2;Ea为反应活化能,kJ/mol;R为摩尔气体常数;T为热力学温度;A为指前因子。
根据极化曲线所得腐蚀电流密度作lgJcorr与1/T的线性拟合线段,所得结果如图5所示。通过斜率求得缓蚀剂加量为0 mg/L和200 mg/L时腐蚀反应活化能Ea分别为21.170 kJ/mol和30.056 kJ/mol。这说明在未添加固体缓蚀剂HCl溶液中N80钢的腐蚀更容易进行,加入固体缓蚀剂后,缓蚀剂分子在钢表面吸附成膜,覆盖了金属表面的活性点,腐蚀反应需要克服更大的能垒才能继续进行。
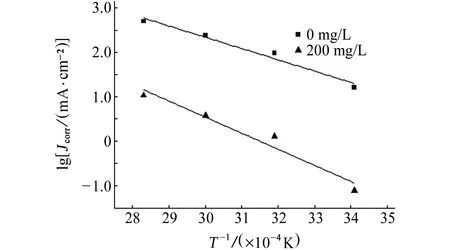
图5 N80钢在不同固体缓蚀剂加量HCl溶液中的Arrhenius曲线Fig. 5 Arrhenius curves of N80 steel in HCl solution added with different dosages of solid corrosion inhibitor
固体缓蚀剂溶解后在金属表面的吸附符合Langmuir吸附等温式,见式(8)。缓蚀剂在N80钢表面的吸附是单分子层吸附,表面覆盖度近似等于由Tafel极化曲线拟合得到缓蚀率,不同温度下缓蚀剂在金属表面的覆盖度列于表5。
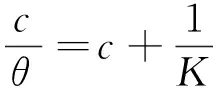
(8)
式中:c是缓蚀剂的质量浓度,g/L;θ是缓蚀剂的表面覆盖度;K是Langmuir吸附平衡常数。
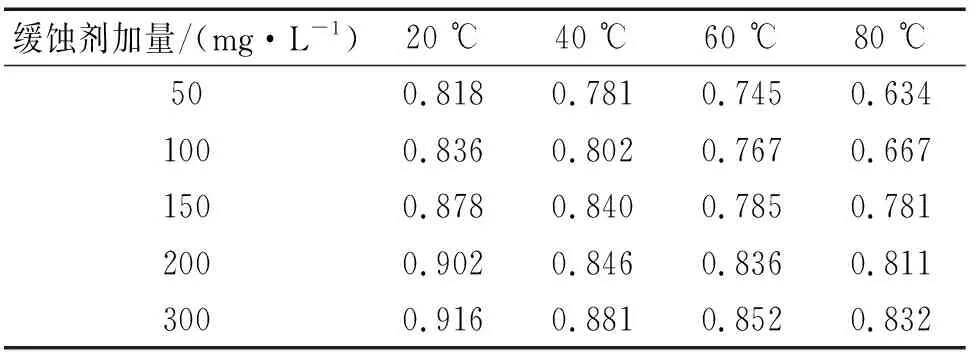
表5 不同温度下缓蚀剂在金属表面的覆盖度Tab. 5 Corrosion inhibitor coverage on metal surface at different temperatures
缓蚀剂的缓蚀效果主要通过缓蚀剂在金属表面的特性吸附过程实现,为了研究其吸附行为,对不同温度下的吸附等温线进行了拟合,结果见图6,其线性拟合参数见表6。结果表明,c/θ与c的线性回归性良好,斜率近似等于1,表明固体缓蚀剂在N80钢的表面吸附符合Langmuir吸附等温式。
理论上Langmuir吸附平衡常数K的大小反映吸附能力的强弱。由表6可知,随着温度的升高,K值逐渐减小,表明缓蚀剂的吸附能力逐渐减弱。Langmuir吸附平衡常数K与吸附标准Gibbs自由能ΔG的关系如式(9)所示。
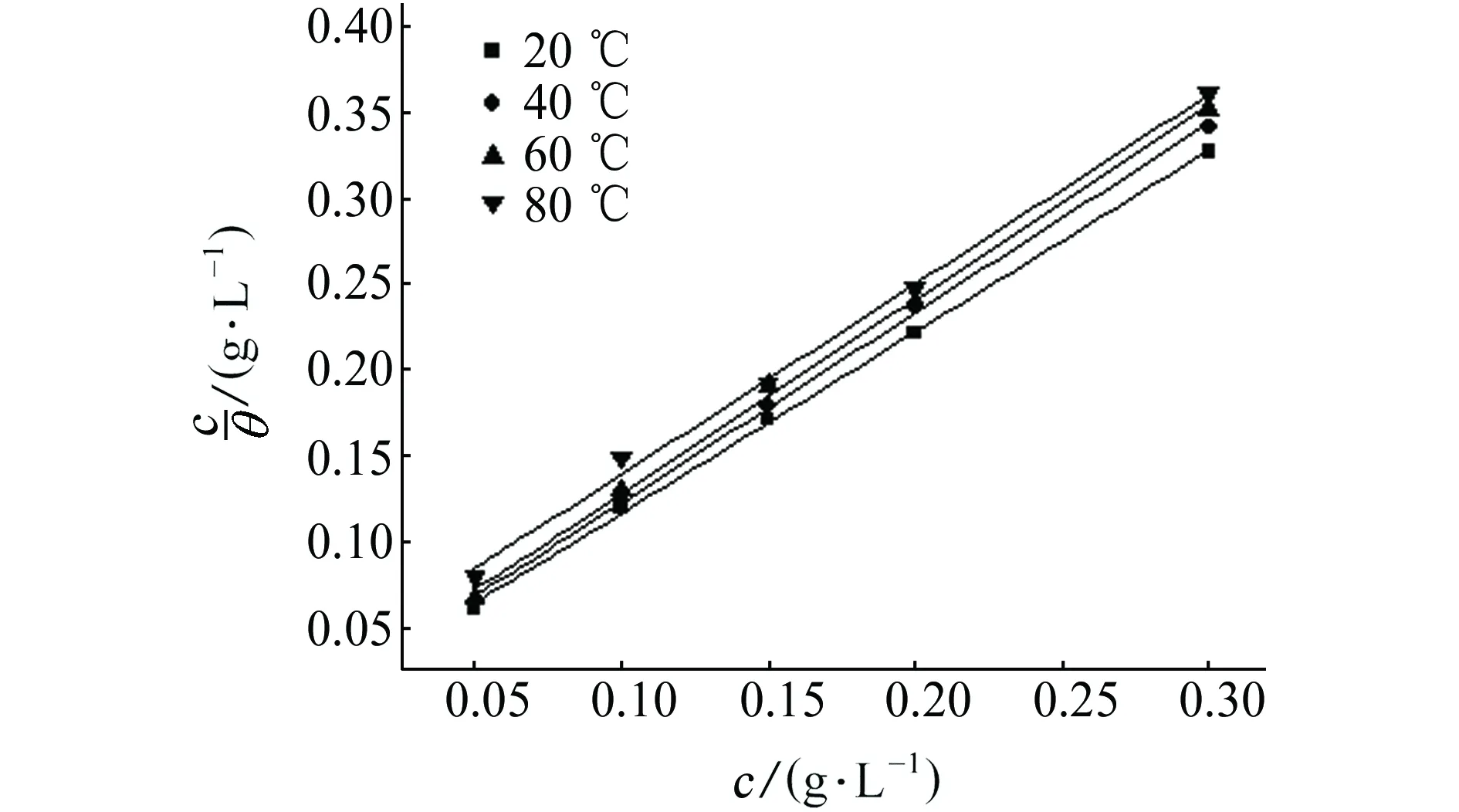
图6 不同温度下缓蚀剂在N80钢表面的吸附拟合曲线Fig. 6 Adsorption fitting curves of corrosion inhibitor on N80 steel surface at different temperatures

温度/℃K斜率R2201001.0550.999 44081.31.1040.999 06065.791.1280.997 98034.121.1030.995 4
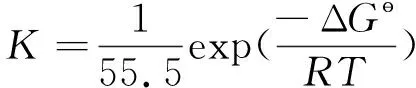
(9)
式中:55.5 mol/L是溶剂水的浓度。
根据式(9)求出吸附标准Gibbs自由能ΔG为-22.71 kJ/mol。ΔG<0表明缓蚀剂在N80钢表面的吸附是自发的,|ΔG|>20 kJ/mol,说明缓蚀剂在钢表面的吸附为化学吸附和物理吸附的混合吸附过程[19]。
2.7 表面形貌
由图7中可以看出:腐蚀前N80钢表面十分平整;在不添加缓蚀剂的溶液中,试样发生了严重的腐蚀,整个表面被腐蚀成多孔疏松状,如图7(b)所示;而添加缓蚀剂后,试样表面较为平整,可以清晰看到打磨痕迹,腐蚀程度较轻。这说明固体缓蚀剂吸附在N80钢表面形成一层致密的保护膜,覆盖了反应活性中心,有效阻止了腐蚀性介质与金属基体的接触,从而抑制了N80钢的腐蚀。

(a) 腐蚀前 (b) 未添加缓蚀剂(c) 添加固体缓蚀剂图7 N80钢在未添加和添加150 mg/L缓蚀剂5% HCl溶液中腐蚀前后的表面形貌Fig. 7 Surface morphology of N80 steel before (a) and after corrosion in 5% HCl solution added with 0 mg/L (b) and 150 mg/L (c) inhibitor
3 结论
(1) 制备了一种咪唑啉类固体缓蚀剂,通过正交试验确定了最佳的合成条件。随着放置时间的延长,固体缓蚀剂的溶出速率逐渐降低,72 h后溶出速率为0.403 g/h,是一种缓释型缓蚀剂,可以达到长效缓蚀的目的。
(2) 固体缓蚀剂属于阳极型缓蚀剂,在N80钢表面的吸附符合Langmuir吸附等温式,吸附方式为化学吸附和物理吸附共存的混合吸附,随着缓蚀剂加量的增加,腐蚀反应的活化能增加,从而有效地抑制了腐蚀反应的发生。
(3) 缓蚀剂能够在金属基体表面形成一层致密的保护膜而起到减缓腐蚀的作用。

