利用固体电解质在CaCl2熔盐中电解固态SiO2制备Si
黄振彪,高运明,秦庆伟,李光强
(1.武汉科技大学钢铁冶金及资源利用省部共建教育部重点实验室,湖北 武汉,430081;2.武汉科技大学钢铁冶金新工艺湖北省重点实验室,湖北 武汉,430081)
硅材料广泛应用于半导体、光纤通信、航空航天等领域。源自FFC剑桥工艺[1]、采用固态SiO2阴极制备硅材料的熔盐电解法因具有流程短、成本低、不受SiO2在熔盐中溶解度限制等优点而受到冶金工作者的广泛关注[2-7],但先前研究多以石墨为辅助电极或阳极[4-5],或在两电极体系条件下采用外加高电压的方式于石墨坩埚内对SiO2进行电解[6],存在电解效率低、易发生副反应、产品易受杂质污染且生成了温室气体CO或CO2等问题[4-6]。此外,即便采用三电极体系电解SiO2,当温度较高时,所用Pt等金属电极一般只能作为准参比电极,无法精确控制电解过程中的电极电位[7]。有鉴于此,本文分别在惰性阳极和炭阳极条件下对固态SiO2的理论分解电压进行计算,比较分析SiO2电化学还原的特点,并结合理论计算结果,利用Y2O3稳定的ZrO2固体电解质(YSZ)管构建集成有参比电极的新型电解池[8],探讨了无炭即不使用石墨电极及石墨坩埚条件下,在CaCl2熔盐介质中绿色电解固态SiO2阴极制备硅材料的可行性。
1 实验
1.1 原料及样品制备
实验用CaCl2、SiO2粉末均为分析纯。利用真空干燥箱将CaCl2粉末在473 K下干燥8 h,充分脱水后备用。在无添加黏结剂条件下,借助FW-4A型压样机以2 MPa的压强将SiO2粉末压制成直径为5 mm、高度为10 mm的圆柱样,再将SiO2圆柱样置于硅钼棒炉中,在空气气氛下经1673 K烧结4 h后随炉冷却制得SiO2圆柱状电解样品。
1.2 电解池及电极
电解池由一端封闭的8% mol Y2O3稳定的ZrO2固体电解质(YSZ)管及工作、辅助、参比等3个电极组成。YSZ管内径为18 mm、外径为20 mm、长为100 mm,YSZ管外封闭端附近两个相邻环形区域分别涂覆铂浆,在空气气氛下于1173 K烧结后制得辅助电极(面积为6.28 cm2)和参比电极(面积为1.88 cm2)。将钼丝穿过SiO2圆柱状电解样品中心并和样品外包钼网缠绕构成工作电极。
1.3 实验方法
实验装置如图1所示,由图1可见,SiC管式高温炉主体为可密封不锈钢套管结构,利用高温水泥将YSZ管与刚玉管(内径22 mm、长度45 cm)密封连接。
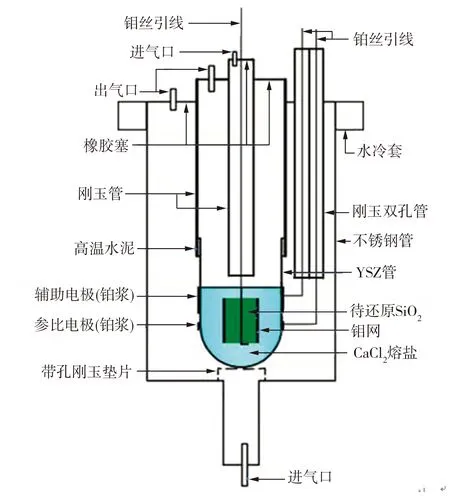
图1 实验装置示意图
通过与计算机连接的Ivium电化学工作站(荷兰制造)测试并记录实验数据。首先,称取12 g经干燥处理后的CaCl2粉末装入YSZ管,并将YSZ管置于SiC管式高温炉的恒温区,同时在炉内及YSZ管内通入高纯氩气,流量分别为300、40 mL/min。以5 K/min的升温速率将高温炉升温至973 K并保温2 h,进一步去除CaCl2的水分。然后,继续升温至1273 K,将SiO2工作电极缓慢降至熔盐液面以下,使熔盐与工作电极充分接触并保温30 min。因炉内充满流动的高纯氩气,故可以借助其中微量的氧,在YSZ管外侧铂浆烧结处构建氧分压稳定的Pt,O2(Ar)|ZrO2参比电极。基于理论计算所得SiO2圆柱样的初始还原电压,利用电化学工作站外加一定电压对SiO2圆柱样进行恒电位电解。电解结束后,将工作电极升至熔盐液面以上,继续通入氩气冷却至室温,取出电解产物,经蒸馏水结合超声波清洗3 min后置于真空干燥箱中在333 K条件下干燥。使用数码相机对电解前后的SiO2工作电极拍照并进行宏观观察,利用Nova 400 Nano型场发射扫描电镜(SEM)并结合INCA IE 350PentaFET X-3型能谱仪(EDS)对相关样品显微组织及成分进行分析与表征,采用X’Pert PRO MPD型 X射线衍射仪(XRD)对SiO2原料、烧结后及电解后的SiO2圆柱样进行物相分析。
2 理论分解电压的计算
由于本研究采用YSZ管(氧离子导体)作为阴、阳极的隔离膜,在足够高外加电压条件下,除SiO2外,熔盐中的杂质CaO以及YSZ管中的Y2O3与ZrO2也有可能被还原,从而对SiO2还原研究产生干扰。因此,需对本研究中涉及的氧化物组元如SiO2、CaO、Y2O3、ZrO2等在不同条件下的分解电压进行理论计算,并结合所选参比电极确定对应的分解电压,为分析SiO2电还原机理提供理论依据。
2.1 标准态下SiO2理论分解电压
(1) 惰性阳极
由于SiO2的熔点约为1973 K,Si的熔点约为1687 K,因此在本研究实验温度下,Si、SiO2均以纯固态形式存在,故有

(1)
在标准态(标准氧分压Pθ为100 kPa)时,有
(2)
(2) 活性炭阳极
采用活性炭阳极时,SiO2电解析出的氧气会与阳极反应,生成CO或CO2气体,相应理论分解电压分别计算如下:
①气体产物为CO
(3)
结合式(1)和式(3),有

(4)
联立式(4)和式(2),可计算出气体产物为CO时,标准态下SiO2理论分解电压Eθ为0.61 V。
②气体产物为CO2

(5)
结合式(1)和式(5),有

(6)
联立式(6)和式(2),可计算出气体产物为CO2时,标准态下SiO2的理论分解电压Eθ为0.74 V。在反应过程中,炭阳极上可能会同时排放CO与CO2气体,此时,标准态下SiO2(s)的理论分解电压应介于上述两种产物条件下计算所得相应值之间。
理论计算结果表明,相比惰性阳极,采用炭阳极后,标准态下SiO2(s)的理论分解电压大幅降低,使得SiO2(s)的电化学还原更易发生,这也是已有研究多采用炭阳极或石墨坩埚的重要原因。
2.2 非标准态、惰性阳极条件下的理论分解电压
(1)SiO2理论分解电压
由于实验中SiO2以固态参与电化学还原,一般可忽略SiO2在熔盐中的溶解度,即使SiO2在熔盐中发生溶解,熔盐中SiO2的浓度在本实验条件下也会达到饱和。假设析出的Si在阴极上以纯固态形式存在,则在非标准态下,当反应中氧气处于高纯氩气环境时,有

(7)
(8)
式(8)中:ΔrGm为非标准态下反应的吉布斯自由能变化;R为气体常数,R=8.314 J·mol-1·K-1;aSiO2与aSi分别为固态SiO2和固态Si均以相应纯物质为标准态时的活度,aSiO2=aSi=1;PO2为高纯氩气中的氧分压,根据氩的国家标准(GB/T 4842-2006),可估算本研究条件下PO2=0.15 Pa;E为非标准态下固态SiO2的理论分解电压。联立式(7)和式(8),可求得非标准态下固态SiO2的理论分解电压E为1.40 V。
对比标准态、惰性阳极条件下的计算结果可知,随着氧分压的下降,SiO2的分解电压明显减小,这表明采用低氧分压环境时,外加较小电压更有利于SiO2的电解。
(2)其它相关组元的理论分解电压
基于相关热力学数据[9],按上述方法,可以计算出在惰性电极、高纯氩气条件下, CaO、Y2O3、ZrO2的理论分解电压分别为2.43、2.60、1.86 V。
Pt,O2|ZrO2(Y2O3)参比电极实质为O2-/O2参比电极,其稳定性、灵敏性、可靠性较好,在高温科学研究中应用较为广泛[8,10],本研究采用Pt,O2(Ar)|ZrO2(Y2O3)作为参比电极,在高纯氩气、稳定的氧分压条件下,SiO2、CaO、ZrO2、Y2O3的理论分解电压可以转换为各自相对于参比电极的初始还原电位,只要准确控制还原电位,就可保证上述氧化物中仅有SiO2被电解还原,从而避免其它副反应的发生。结合理论计算结果,并考虑实际电解过程中极化、压降损耗以及电解还原速率等因素,本研究设定对SiO2圆柱样进行恒电位电解的外加电压为-1.80 V。
3 实验结果与讨论
3.1 产物表征
图2所示为SiO2样品在外加电压为-1.80 V时的恒电位电解曲线,其电解前后的实物照片如图3所示。由图3可见,白色的SiO2圆柱状烧结样(图3(a))经16 000 s电解后基本保持了其电解前的原始形状,但颜色变成红褐色,且产物容易破碎(图3(b)),可研磨成粉末。根据文献[3,5-7]相关描述,可初步认定本研究中SiO2圆柱样还原较完全且红褐色的电解产物为硅。
SiO2工作电极电解前后的SEM 照片见图4。由图4(a)可以看出,电解前的SiO2圆柱样微观结构为致密的不规则片状,尺寸介于1~4 μm;而电解后的产物结构疏松多孔,呈现出长棒状(图4(b))、短棒状(图4(c))、不规则六边形状(图4(d))等多种形貌,其中,棒状产物直径介于1~3 μm,不规则六边形产物尺寸稍大,达到3~5 μm。由此可见,SiO2电解产物形貌与其原始形貌相似度较小。
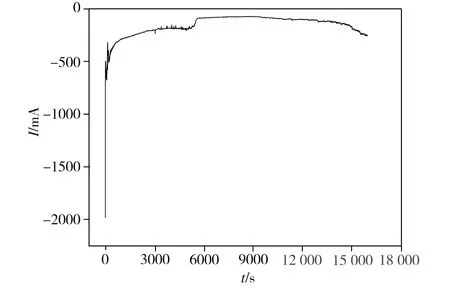
图2 SiO2的电解曲线

(a) 电解前 (b)电解后
图3 工作电极SiO2电解前后的照片
Fig.3 Photograph of working electrode SiO2before and after electrolysis

(a) 电解前的片状SiO2(b) 电解后长棒状产物 (c) 电解后短棒状产物 (d) 电解后不规则状产物
图4 SiO2电解前后的SEM照片
Fig.4 SEM images of SiO2before and after electrolysis
图5所示为图4中各测试点的EDS检测分析结果。图5(a)测试结果确认了电解前的样品成分为SiO2。由图5(b)~5(g)可知,SiO2电解后所得不同形状产物中的测试点都存在Si,且Si含量相比电解前SiO2样品中的相应值大幅增加,这表明使用该法电解SiO2制备单质Si是可行的。此外,结合图4(d)及相应EDS测试结果表明, SiO2样品电解所得不规则六边形产物测试点O含量不高,尤其产物表面平坦处O含量极低(图5(g)),同时也检测到少量的Cl、Ca元素。对图4(d)中方形选定区域进行面扫描检测的结果如图6所示。从图6中可以看出,检测区域除大量的Si元素外,还存在一定量的O、Cl、Ca等元素,其中O可能来源于电解还原的Si在冷却时与高纯氩气中微量氧反应所生成的SiO2,也可能来源于CaCl2熔盐中存在的少量CaO,而同时存在的Cl、Ca元素表明产物中有CaCl2相,这是因为样品经超声波清洗时,清洗时间较短(3 min),造成CaCl2熔盐残留所致。图7为SiO2原料(未烧结)、SiO2烧结样及其电解产物的XRD图谱。从图7中可见,SiO2烧结前后的XRD谱线变化不大,SiO2主要以晶态结构存在,但SiO2烧结后的衍射主峰强度略低于其烧结前的相应值,且基线出现少许漫散峰,表明SiO2原料在1673 K条件下烧结4 h后存在极少量SiO2由晶态转化为非晶态的可能。而SiO2电解产物中只存在Si和CaCl2两晶相,其中Si相衍射峰较强,表明电解产物中存在大量的Si和少量残留的CaCl2熔盐,XRD检测与能谱分析结果吻合,证实SiO2已被电解还原为Si。此外,在电解产物中没有检测到SiO2、CaO的衍射峰,表明二者含量甚小,其XRD图谱基线也存在一些小的漫散峰,结合能谱分析,推测其中少量存在的SiO2可能以非晶态形式存在。
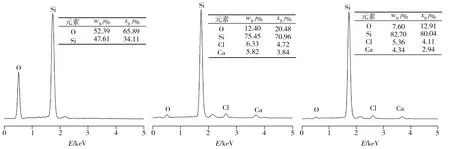
(a)图4(a)中点1 (b) 图4(b)中点1 (c) 图4(b)中点2
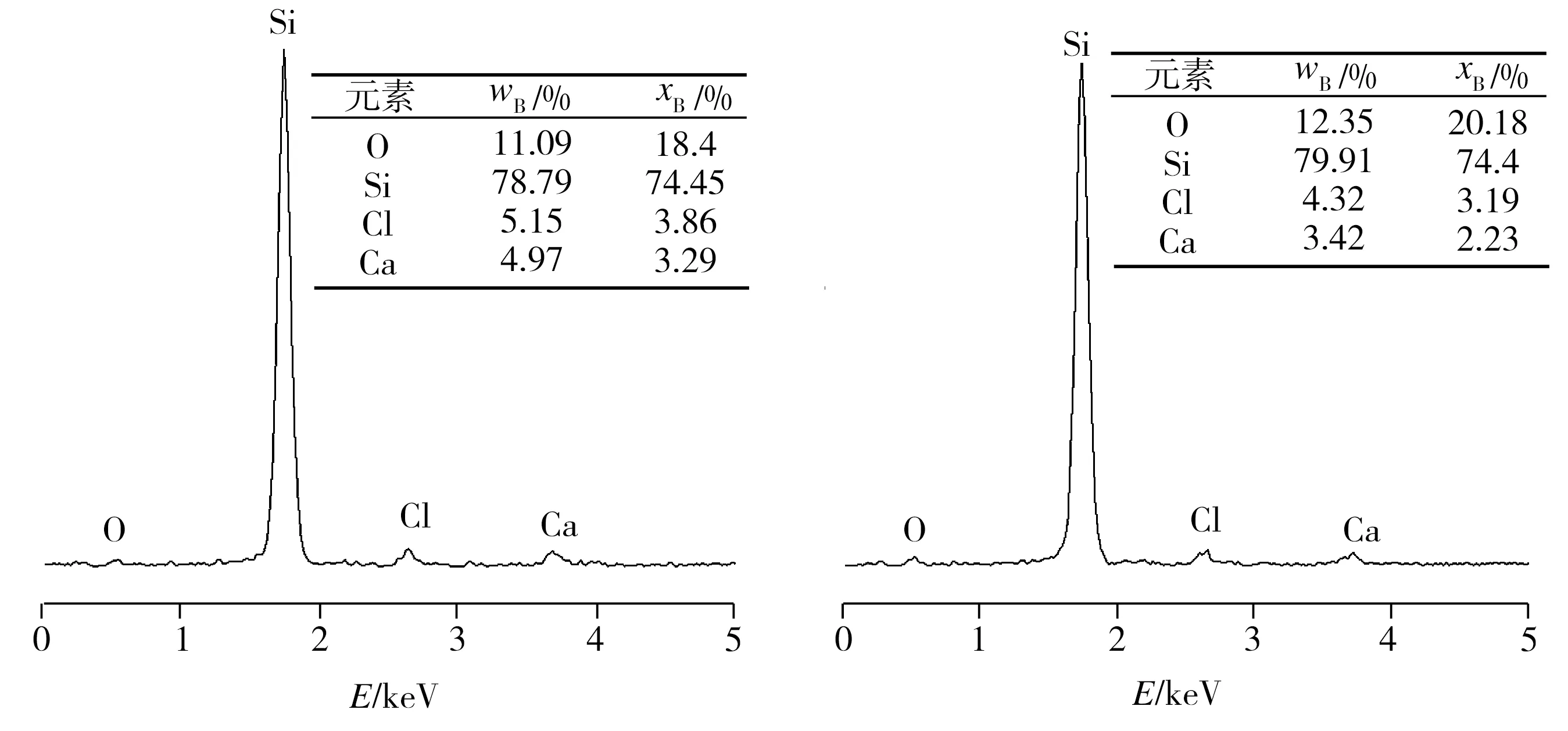
(d) 图4(c)中点1 (e) 图4(c)中点2
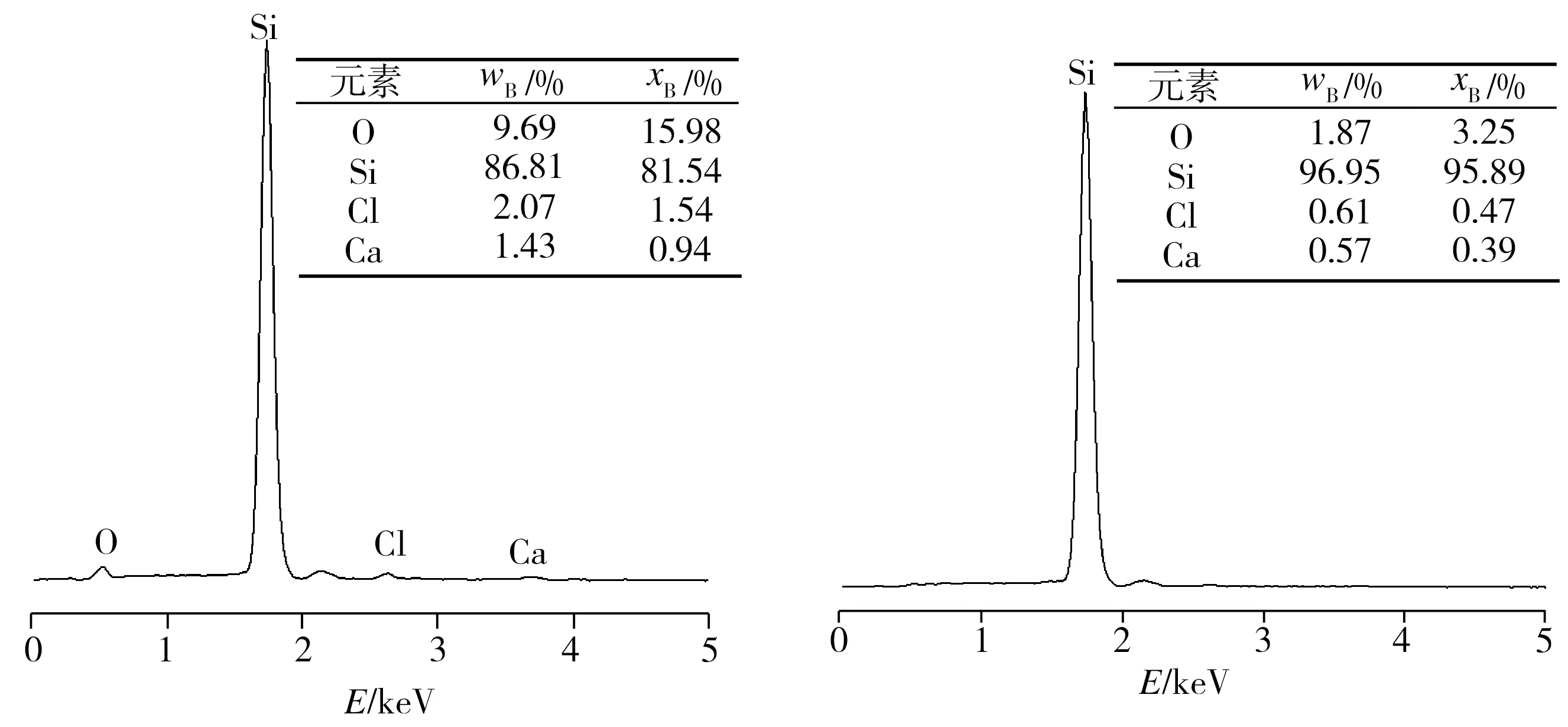
(f) 图4(d)中点1 (g) 图4(d)中点2
图5 EDS图谱
Fig.5 EDS patterns

(a)Si (b)O (c)Cl (d)Ca
图6 元素分布
Fig.6 Element distribution
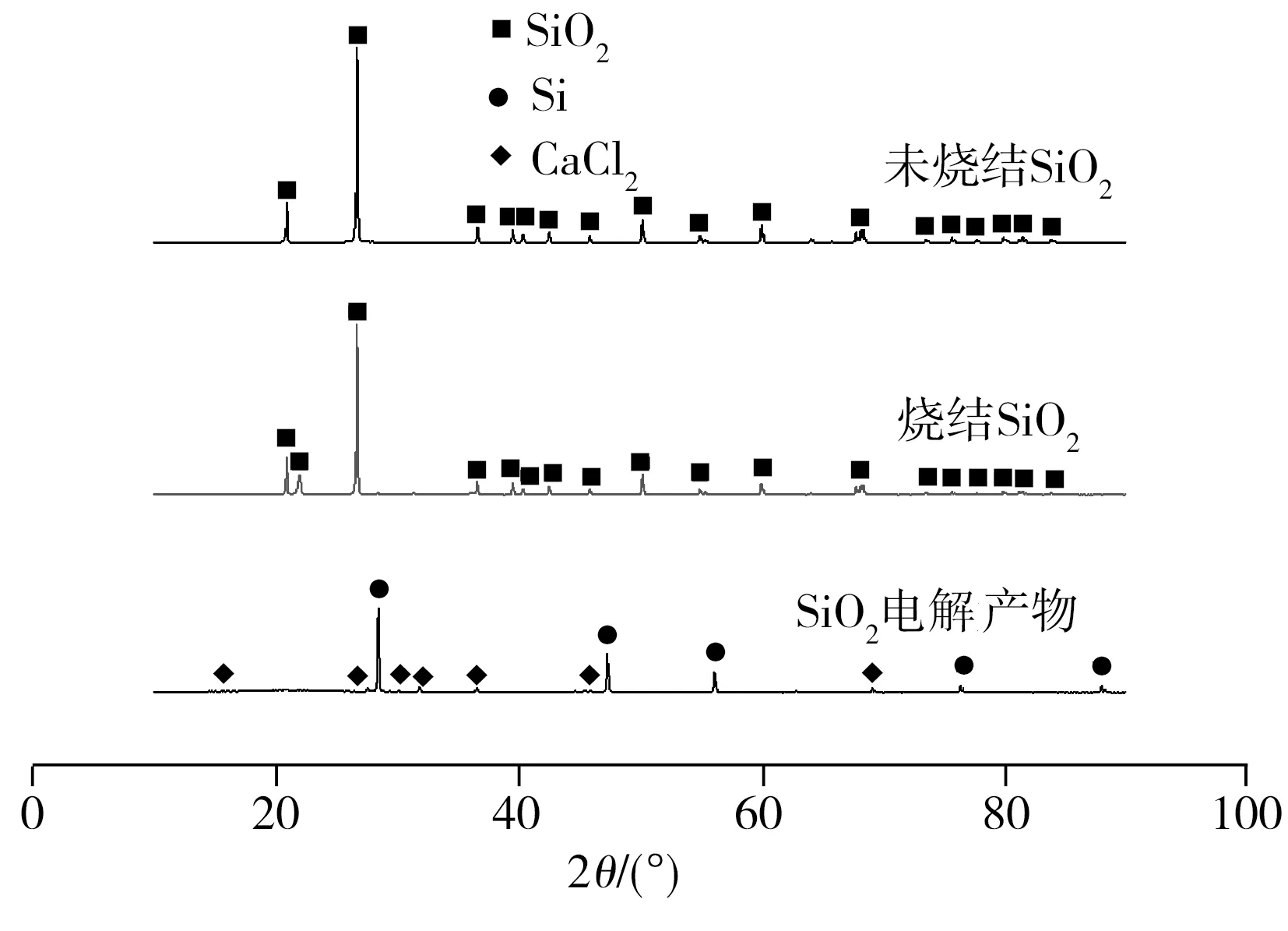
图7 样品的XRD图谱
3.2 电解过程分析
由于固态SiO2不导电,SiO2的还原只能在导电集流体(引线)-固态SiO2阴极-熔盐的三相界线(3PIs)处进行[2,5,11]。基于前述产物特征,结合如图2对SiO2电解过程分析如下:在实验开始瞬间,负向起始电流绝对值较大,与双电层的充电电流有关,随后负向电流绝对值急剧减小,表明SiO2的电化学还原已经在3PIs处开始。还原产物Si在高温下具有良好导电性,可在后续的电解过程中充当新的电子导体并扩展形成新的3PIs,由于3PIs的表面横向长度扩展较易进行[11],其横向尺度的增加将导致负向电流绝对值小幅增加,随后负向电流绝对值减小则表明三相界线纵向扩展受限,一方面熔盐向SiO2圆柱体内部渗透减慢,另一方面,SiO2阴极还原释放的O2-从其内部出发,在穿过多孔Si产物层进入熔盐本体时,其迁移速度因受到阻力而减慢,导致扩散极化,电流绝对值减小,3PIs表面横向长度扩展与纵向扩展受限过程交替进行,直至SiO2完全还原后电流达到较稳定的数值。在还原过程中,绝缘的SiO2藉由不断扩展的3PIs完成由SiO2到Si的转变,其还原的具体速控环节以及产物Si微观结构的构建机理还有待后续进一步研究。
4 结论
(1)理论计算表明,惰性阳极条件下SiO2的电解还原比炭阳极条件下困难,1273 K标准态下前者的理论分解电压明显高于后者。降低气相中的氧分压,有利于SiO2的电解还原。
(2)借助集成有Pt,O2(高纯Ar)|ZrO2(Y2O3)参比电极的三电极电解池,在惰性阳极条件下,当外加电压为-1.8 V(相对参比电极)时,在1273 K 的CaCl2熔盐介质中电解固态SiO2可制得外观红褐色、内部疏松多孔的Si,且电解前的SiO2样品与其电解产物Si的微观形貌相似度较小,SiO2的还原过程可以用三相界线反应机制进行解释。

