二丁颗粒HPLC 指纹图谱建立及5种成分测定
梁梓敏,覃洁萍,郭海姣
(广西中医药大学药学院,广西 南宁530001)
二丁颗粒为2015年版《中国药典》 收载的中药成方制剂,由紫花地丁、半边莲、蒲公英、板蓝根4味药材组成,功效清热解毒,用于火热毒盛所致的热疖痈毒、咽喉肿痛、风热火眼[1],可治疗痤疮、慢性支气管炎、急性咽炎等[2-7]。目前,药典中二丁颗粒质量控制指标仅为秦皮乙素[1];近来有学者报道了其中单咖啡酰基酒石酸、秦皮乙素、菊苣酸3种成分含有量的测定方法[8],但仍未能对制剂整体质量进行有效评价,如表告依春为板蓝根主要有效成分,具有很强的抗病毒活性[9-10],但目前并无相关报道。
单咖啡酰基酒石酸、咖啡酸、菊苣酸等酚酸类成分具有抑病毒、抑菌、抗炎、抗氧化等药理作用[11-12],秦皮乙素具有抗炎、抗肿瘤作 用[13-15],为二丁颗粒药效成分。因此,本实验建立二丁颗粒HPLC 指纹图谱,并测定表告依春、单咖啡酰基酒石酸、秦皮乙素、咖啡酸、菊苣酸含有量,以期为该制剂质量控制提供参考。
1 材料
1.1 仪器 Agilent 1260高效液相色谱仪,配置UV 型紫外检测器、安捷伦工作站(美国安捷伦公司);密思博超纯水器;SQP 电子分析天平[十万分之一,赛多利斯科学仪器(北京)有限公司];TGL-16G 离心机(上海安亭科学仪器厂);KQ5200B 超声波清洗器(昆山市超声仪器有限公司);HWS-26电热恒温水浴锅(上海一恒科学仪器有限公司)。
1.2 试药 紫花地丁(批号20180501)、板蓝根(批号20180101)、蒲公英(批号20180201)、半边莲(批号20180201)均由南宁市景昌中药饮片有限公司提供,经广西中医药大学鉴定教研室蔡毅教授鉴定为正品。表告依春(批号171206)、单咖啡酰 基酒 石(批号171130)、菊苣酸(批号171130)对照品(上海融禾医药科技有限公司);秦皮乙素(批号110741-200102)、咖啡酸(批号110885-201708)对照品(中国食品药品检定研究院),含有量均大于98%。二丁颗粒共10批,批号171193(20 g/袋),购自四川古蔺肝苏药业有限公司;批 号 180120(20 g/袋)、180401(20 g/袋)、181410D(20 g/袋)、180604D(无糖,4 g/袋)、180317(20 g/袋),购自修正药业集团长春高新制药有限公司;批 号180911(无 糖,4 g/袋)、180918(无 糖,4 g/袋)、180903(20 g/袋)、180926(20 g/袋),由广西中医药大学药学中心实验室制备。
甲醇、乙腈为色谱纯;乙醇等其他试剂均为分析纯;水为超纯水。
2 方法与结果
2.1 色谱条件 Agilent Poroshell 120 EC-C18色谱柱(250 mm×4.6 mm,4.0 μm);流动相乙腈(A)-0.1% 磷酸(B),梯度洗脱(0~12 min,5%~10% A;12~20 min,10% A;20~30 min,10%~17%A;30~50 min,17%~24% A);体积流量1.0 mL/min;检测波长242 nm(0~12 min)、330 nm(12~50 min);柱温30 ℃;进样量5 μL。
2.2 溶液制备
2.2.1 对照品溶液 精密称取各对照品适量,置于5个10 mL 量瓶中,甲醇溶解并定容,制得贮备液,取适量置于同一量瓶中,甲醇稀释,制成分别含表告依春、单咖啡酰基酒石酸、秦皮乙素、咖啡酸、菊苣酸10.8、60.4、111、11.1、28.0 μg/mL,即得。
2.2.2 供试品溶液 精密称取相当于原药材2~5 g的颗粒适量,置于100 mL 具塞锥形瓶中,加入40 mL 60%乙醇回流45 min,滤过,滤液挥干,残渣用60%乙醇溶解并定容至10 mL,13 000 r/min离心,取上清液过微孔滤膜,即得。
2.2.3 阴性样品溶液 按处方工艺制备缺紫花地丁、板蓝根、蒲公英、半边莲的其他药材各1份,按“2.2.2”项下方法制备,即得。
2.3 HPLC 指纹图谱
2.3.1 稳定性试验 取颗粒(批号180926)2.5 g,按“2.2.2”项下方法制备供试品溶液,于0、2、4、8、12、24 h 在“2.1”项色谱条件下各进样5 μL 测定。以4号峰(秦皮乙素)保留时间和色谱峰面积为参照,测得其余10个色谱峰相对保留时间RSD 在0.03%~0.17%之间,相对峰面积RSD在0.27%~2.8%之间,表明溶液在24 h 内稳定性良好,符合指纹图谱测定要求。
2.3.2 精密度试验 取供试品溶液(批号180926),在“2.1”项色谱条件下进样测定6次。以4号峰(秦皮乙素)保留时间和色谱峰面积为参照,测得其余10个色谱峰相对保留时间RSD 在0.05%~0.29%之间,相对峰面积RSD 在0.37%~2.0%之间,表明仪器精密度良好,符合指纹图谱测定要求。
2.3.3 重复性试验 取同一批颗粒(批号180926)2.5 g,共6份,按“2.2.2”项下方法制备6份供试品溶液,在“2.1”项色谱条件下各进样5 μL 测定。以4号峰(秦皮乙素)保留时间和色谱峰面积为参照,测得其余10个峰相对保留时间RSD 在0.02%~0.13% 之间,相对峰面积RSD在0.30%~1.6% 之间,表明该方法重复性良好,符合指纹图谱测定要求。
2.3.4 建立方法 取10批颗粒适量,按“2.2.2”项下方法制备供试品溶液,在“2.1”项色谱条件下进样测定,结果见图1,再采用《中药色谱指纹图谱相似度评价系统》(2012.130723版)对指纹图谱进行分析,发现11个共有峰(图2),其中4号峰为秦皮乙素,是君药紫花地丁主要活性成分,该色谱峰分离度较好,响应值较高,保留时间适宜,故选择其为参照峰。相似度见表1,可知各批样品相似度均在0.90以上,表明指标成分一致性较好。
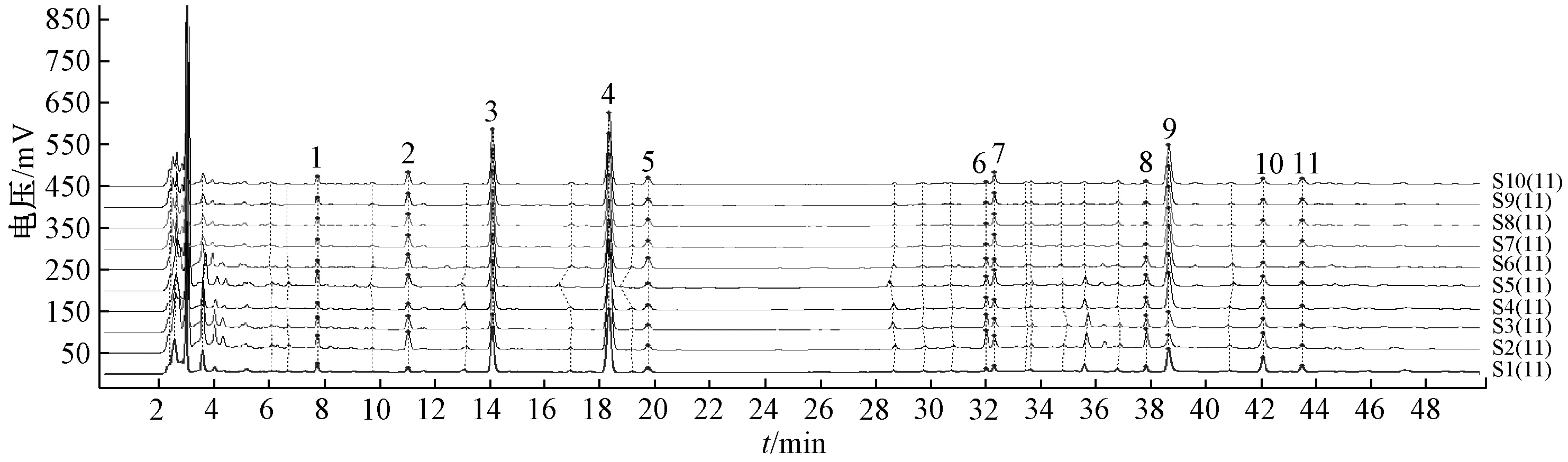
图1 10批样品HPLC 指纹图谱Fig.1 HPLC fingerprints of ten batches of samples
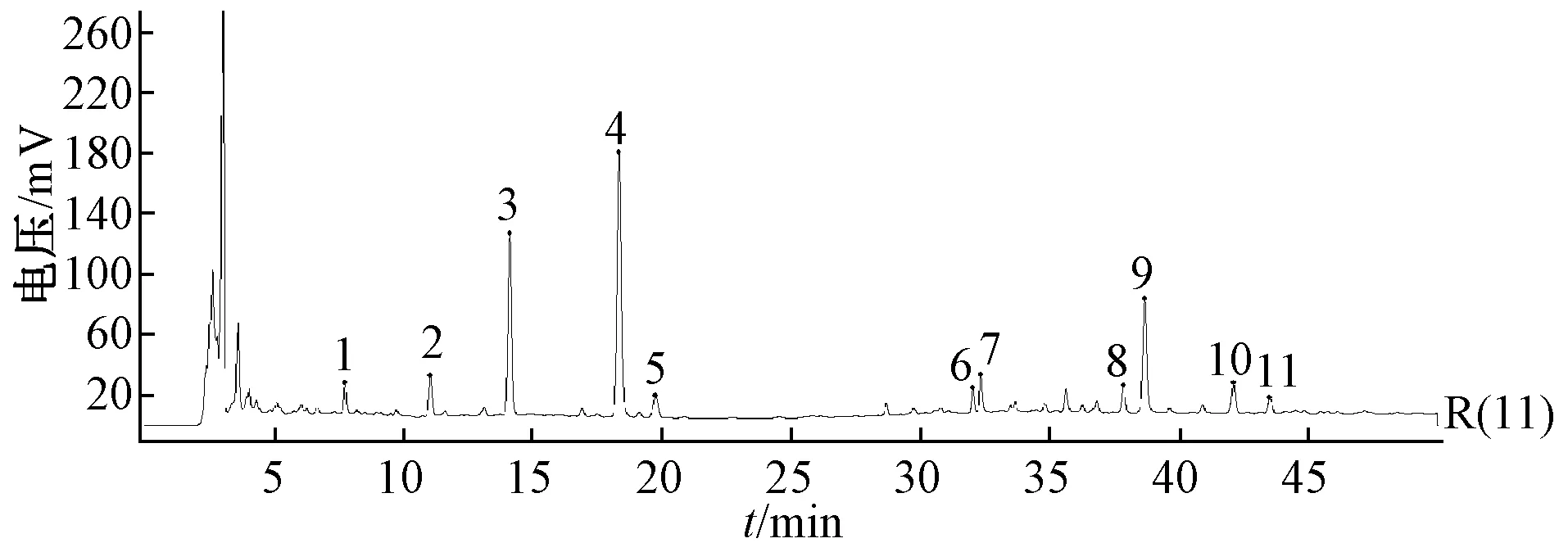
图2 HPLC 指纹图谱共有峰Fig.2 Common peaks of HPLC fingerprints
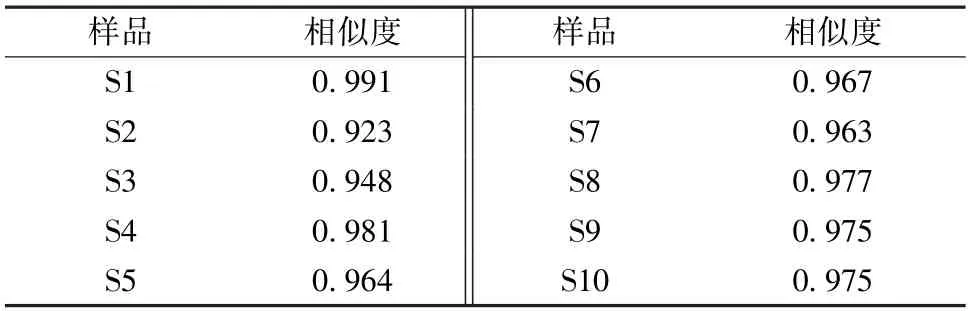
表1 10批样品相似度Tab.2 Similarities of ten batches of samples
2.3.5 特征峰归属 精密吸取表告依春、单咖啡酰基酒石酸、秦皮乙素、咖啡酸、菊苣酸对照品溶液,在“2.1”项色谱条件下进样测定,二极管阵列检测器同时记录色谱图和各色谱峰紫外吸收光谱,并与指纹图谱共有模式中共有特征峰进行对比,发现共有模式中2~5、9号特征峰的保留时间及其紫外光谱分别与表告依春、单咖啡酰基酒石酸、秦皮乙素、咖啡酸、菊苣酸对照品一致,故确认为相应成分。然后,精密吸取缺紫花地丁、蒲公英、半边莲、板蓝根阴性样品溶液,在“2.1”项色谱条件下进样测定,并与颗粒指纹图谱共有模式中共有特征峰进行比对,结果见图3,可知1、8号峰为4种药材共有特征峰,2号峰(表告依春)归属为板蓝根,4号峰(秦皮乙素)、7号峰归属为紫花地丁,3号峰(单咖啡酰基酒石酸)、5号峰(咖啡酸)、9号峰(菊苣酸)归属为蒲公英,6、10~11号峰归属为半边莲。
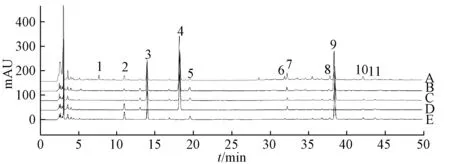
图3 二丁颗粒及阴性样品HPLC 色谱图Fig.3 HPLC chromatograms of Erding Granules and negative samples
2.4 含有量测定
2.4.1 专属性试验 取供试品、对照品、阴性样品溶液,在“2.1”项色谱条件下进样测定,结果见图4。由图可知,对照品、供试品色谱图相应位置具有相同保留时间色谱峰,阴性无干扰,理论塔板数以秦皮乙素(3号峰)计应不少于6 000。
2.4.2 线性关系考察 取对照品贮备液适量,逐级稀释制成分别含表告依春、单咖啡酰基酒石酸、秦皮乙素、咖啡酸、菊苣酸2.16~86.2、12.1~133、22.1~244、2.22~24.4、5.60~61.6 μg/mL 的溶液,各精密吸取5 μL,在“2.1”项色谱条件下进样测定。以峰面积为纵坐标(Y),溶液质量浓度为横坐标(X)进行回归,结果见表2,可知各成分在各自范围内线性关系良好。
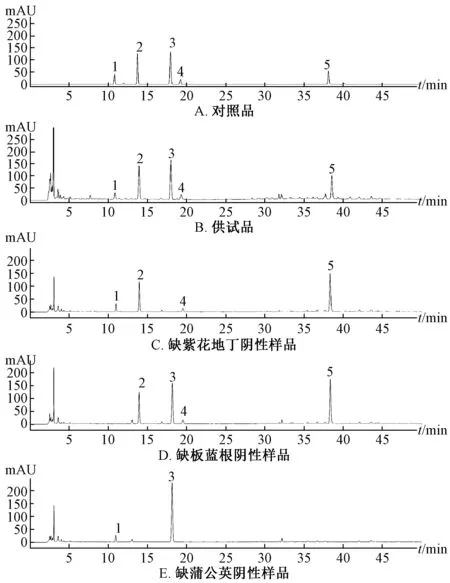
图4 各成分HPLC 色谱图Fig.4 HPLC chromatograms of various constituents
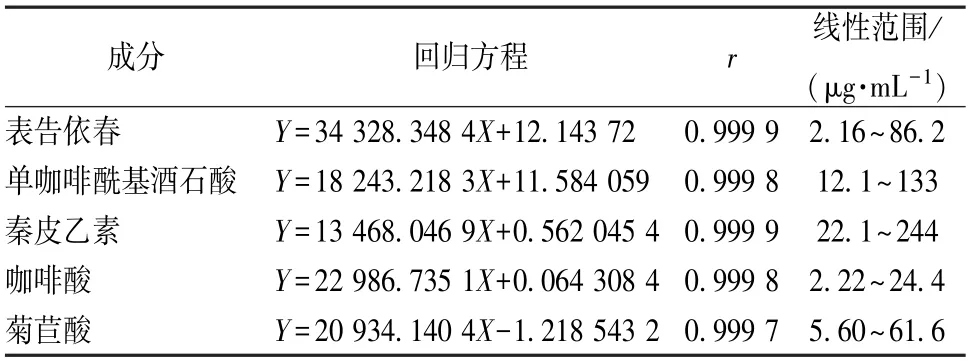
表2 各成分线性关系Tab.1 Linear relationships of various constituents
2.4.3 精密度试验 精密吸取对照品溶液5 μL,在“2.1”项色谱条件下进样6次,测得表告依春、单咖啡酰基酒石酸、秦皮乙素、咖啡酸、菊苣酸峰面积RSD 分别为0.77%、1.0%、0.97%、1.1%、0.20%,表明仪器精密度良好。
2.4.4 稳定性试验 取同一供试品溶液(批号180926),于0、2、4、8、12、24 h 在“2.1”项色谱条件下各进样5 μL,测得表告依春、单咖啡酰基酒石酸、秦皮乙素、咖啡酸、菊苣酸峰面积RSD 分别为 0.39%、0.44%、0.34%、0.60%、0.82%,表明供试品溶液在24 h 内稳定性良好。
2.4.5 重复性试验 精密称取同一批样品(批号180926)6份,每份2.5 g,按“2.2.2”项下方法制备供试品溶液,在“2.1”项色谱条件下各进样5 μL,测得表告依春、单咖啡酰基酒石酸、秦皮乙素、咖啡酸、菊苣酸含有量RSD 分别为1.2%、1.6%、1.2%、1.5%、1.4%,表明该方法重复性良好。
2.4.6 加样回收率试验 精密称取各成分含有量已知的样品(批号180926)1.25 g,共6份,精密加入含表告依春(0.040 4 mg/mL)、单咖啡酰基酒石酸(0.401 mg/mL)、秦皮乙素(0.686 mg/mL)、咖啡酸(0.066 6 mg/mL)、菊苣酸(0.269 mg/mL)对照品溶液各1.00 mL,按“2.2.2”项下方法制备供试品溶液,在“2.1”项色谱条件下进样5 μL测定,结果见表3。
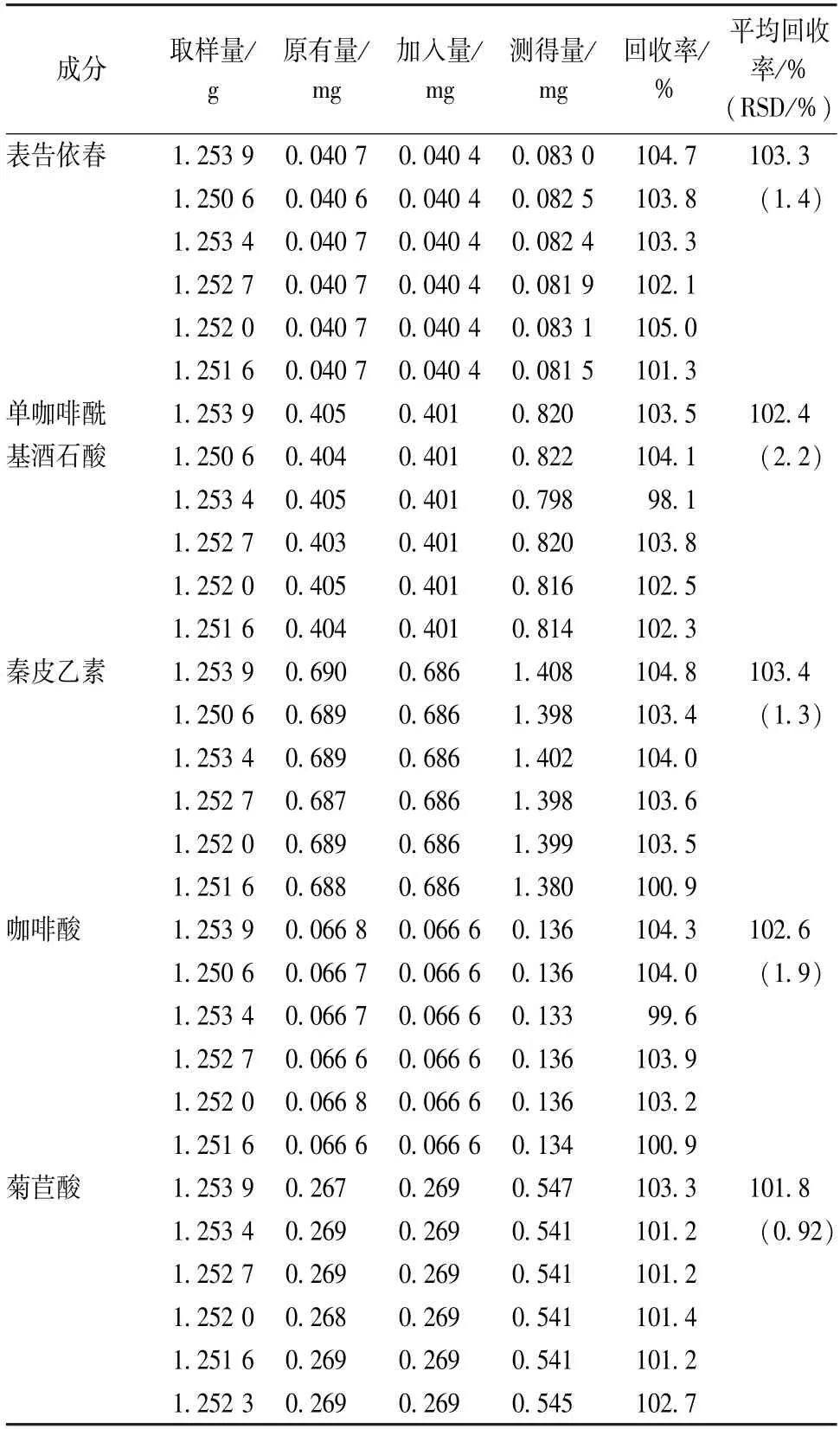
表3 各成分加样回收率试验结果(n=6)Tab.3 Results of recovery tests for various constituents(n=6)
2.4.7 样品含有量测定 精密称取相当于原药材2~5 g 的不同批号颗粒粉末,按“2.2.2”项下方法制备供试品溶液,在“2.1”项色谱条件下各进样5 μL 测定,计算含有量,结果见表4。
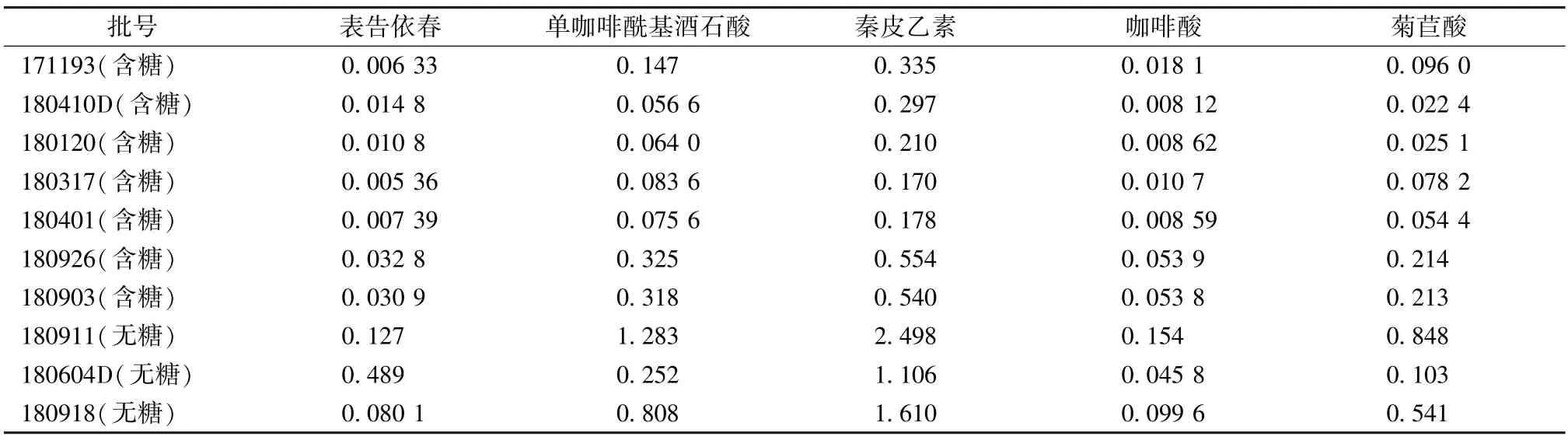
表4 各成分含有量测定结果(mg/g, n=2)Tab.4 Results of content determination of various constituents(mg/g, n=2)
3 讨论
3.1 色谱条件选择 本实验考察了甲醇-水、乙腈-水、甲醇-0.1% 磷酸、乙腈-0.1% 甲酸、乙腈-0.1%冰乙酸、乙腈-0.1%磷酸、乙腈-0.08%磷酸、乙腈-0.12%磷酸流动相,发现乙腈-0.1%磷酸洗脱时各成分色谱峰分离度较好,而且出峰时间适中;考察 了Agilent Poroshell 120 EC-C18(250 mm ×4.6 mm,4.0 μm)、Agilent ZORBAX Eclipse XDBC18(4.6 mm × 250 mm,5.0 μm)、Phenomenex Gemini-C18(250 mm×4.6 mm,5 μm)色谱柱,发现Agilent Poroshell 120 EC-C18色谱柱分离度、峰形、柱效较好;考察了柱温25、30、35 ℃,发现30 ℃时分离度、峰形较好;考察了体积流量0.8、1.0、1.2 mL/min,发现1.0 mL/min 时洗脱效果较好;采用DAD 检测器在190~400 nm 波长处进行扫描,发现表告依春、单咖啡酰基酒石酸、秦皮乙素、咖啡酸、菊苣酸最佳吸收波长分别为242、330、344、322、330 nm,为了使各成分均能获得尽可能高的测量灵敏度,本实验采用双波长切换时间序列采样方式进行检测,即0~12 min 242 nm,12~50 min 330 nm,发现在此条件下各成分吸收及峰型较理想,并可达到良好的分离效果。综上所述,最优色谱条件为Agilent Poroshell 120 EC-C18色谱柱(250 mm×4.6 mm,4.0 μm);流动相乙腈-0.1%磷酸,梯度洗脱;体积流量1.0 mL/min;检测波长242、330 nm;柱温30 ℃。
3.2 提取条件选择 本实验考察了甲醇、30%甲醇、60% 甲醇、水、乙醇、30% 乙醇、60% 乙醇、40%甲醇(含1% 乙酸)[12]、70% 甲醇(含5% 甲酸)[16],发现以60%乙醇为提取溶剂时各成分综合提取率最高;考察了冷浸、超声、回流提取,发现回流提取效率明显优于超声提取与冷浸提取;考察了25、40、55 mL 提取溶剂体积及15、30、45、60、90 min 提取时间,发现40 mL、45 min 时各成分基本提取完全。综上所述,最优提取条件为40 mL 60%乙醇回流提取45 min。
4 结论
本实验建立二丁颗粒HPLC 指纹图谱,并测定表告依春、单咖啡酰基酒石酸、秦皮乙素、咖啡酸、菊苣酸含有量,发现指纹图谱专属性较强,测定方法简便准确,重复性较好,对提高该制剂质量标准有着积极的参考意义。

