W105脱汞剂制备以其在污酸中脱除Hg和As的应用
胡晓佳 化前珍

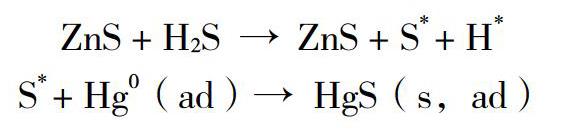
摘 要:制备一种高效的脱汞剂—W105,实现了高效去除污酸中胶体态汞的效果,研究脱汞参数对污酸中Hg和As脱除效果的影响。研究结果表明:制备的脱汞剂碳表面上生长出了晶体,表明制备得到的脱汞剂具备较强活性。为了保持脱汞剂内的汞稳定性,依次对经过使用的脱汞剂实施常温、60 ℃加热以及将其放入水中浸泡的方式进行处理。当W105添加量增大后,溶液中含有的Hg与其它各类重金属离子浓度发生了持续减小的现象,脱除效果最优的是Hg,最差的是锌。脱汞剂产生脱汞作用的机理是先吸附硫化氢反应得到活性硫组分,之后再跟单质汞生成稳定的硫化汞。新鲜脱汞剂比再生脱汞剂的活性更低,同时当再生次数增大后,脱汞剂可以获得更优的脱汞性能。
关 键 词:胶体聚结;污酸;汞;脱除
中图分类号:X703 文献标识码: A 文章编号: 1671-0460(2019)09-2002-04
Abstract: A kind of high-efficiency mercury removal agent W105 was prepared to achieve the high-efficiency removal effect of colloidal mercury from contaminated acid, and the influence of mercury removal parameters on the removal effect of Hg and As in contaminated acid was studied. The results showed that crystals were grown on the carbon surface of the prepared mercury remover, indicating that the prepared mercury remover had strong activity. In order to maintain the stability of mercury in the mercury remover, used mercury remover was treated at normal temperature, by heating at 60 ℃ and soaking in the water. When the addition amount of W105 increased, the concentration of Hg in the solution and other heavy metal ions continued to decrease, and the removal effect of Hg was best, and the removal effect of zinc was worst. The mechanism of mercury removal is to adsorb hydrogen sulfide to obtain active sulfur components to form stable mercury sulfide with elemental mercury. The activity of fresh mercury removal agent is lower than that of regenerated mercury removal agent, and the mercury removal agent can obtain better mercury removal performance when the regeneration times increase.
Key words: colloidal coalesence; waste acid; mercury; removal
汞是一種重金属污染物,其在污酸中的存在形式包括胶体、颗粒、离子。在高温状态下,汞以气态形式与烟气一起被污酸吸收,其中的离子态汞将会和污酸中的化学成分反应得到处于不同化合价状态的汞化合物,如HgCl2,并以颗粒形态悬浮在污酸液体中[1-3]。同时,还有一些原子态汞和污酸接触后不会反应,但会与污酸溶液里的某些离子产生吸附作用而变为胶体态,从而溶解到污酸中。剩余的汞则会和污酸里的氯离子相互结合得到配合离子,并以HgCl2、HgCl3-与HgCl42-的多种形式存在,此部分汞形成了水溶性离子的状态,占到所有汞总量的20%~30%[4-6]。
现阶段,对含汞污酸的处理方法基本以硫化沉淀与混凝沉淀形式为主[7,8]。其中,混凝沉淀的过程把石灰、氯化铝等混凝试剂加入到污酸里,此时将原来酸性状态的污酸转变为弱碱性状态,实际pH介于8~10,从而得到氢氧化物絮凝体,形成架桥结构来实现汞的絮凝效果,之后汞将会和絮凝体一起发生沉淀析出的现象[9,10]。当汞在污酸中的含量为0.3~0.6 mg/L时,采用石灰与FeCl3对其实施混凝沉淀处理后,可以使处理后的汞浓度减小到0.05~0.1 mg/L之间。Hg+/Hg2+和硫化剂的S2-可以形成很强的结合力,从而生成硫化汞沉淀,实现汞从污酸中分离的目的[11,12]。但在实际工业应用期间发现,采用硫化法通常无法把汞与其它各类重金属从污酸中有效去除到标准值以下。根据相关研究文献可知:无法达到HG排放标准的一个重要因素是在污酸中含有较多胶体态汞,因此无法将这部分Hg有效去除。因为胶体态汞具有特殊的性能,这些元素汞会与其它离子间产生吸附作用而形成“保护层”的结构,所以要想去除这类胶体态汞应先破坏其保护层才可以深度去除污酸中的汞,这对实际指导具有重要的作用[13,14]。
随着脱汞工艺的不断进步,一些学者开始使用硫化物来实现烟气脱汞的过程,并取得了良好的效果。汞是一種具备良好亲硫性能的物质,在处理飞灰吸附剂中的含汞成分时通常是利用渗硫的方式来实现脱汞的效果,并且实际脱汞效率受到表面硫覆盖率及其活性位数量的共同影响[15]。根据以上汞去除原理,并在之前工程开发经验基础上,制备得到了一种高效的脱汞剂—W105,实现了高效去除污酸中胶体态汞的效果,通过现场测试发现,采用W105去除污酸中的汞可以有效达到最终的排放标准。
1 试验部分
1.1 试验材料
本实验从某铅锌冶炼厂的排放污水池中采集污酸试样,并以W105作为液体型脱汞剂。
1.2 仪器设备
需要使用的实验仪器与设备包括:0.5~10 mL的移液管、玻璃棒、洗耳球、橡胶管、容积为1 L的烧杯、?50 mm×800 mm的气浮柱、型号为HH-6的搅拌水浴锅、ICP光谱仪、空气压缩机、冷原子吸收测汞仪。
1.3 试验方法
从生产现场采集污酸样品,并利用移液管按照设定添加量吸取W105脱汞剂并加入污酸中再对其实施搅拌与水浴处理,在设定温度下放置一段时间后再将其倒入气浮柱中,按照由下往上的方向对气浮柱进行鼓气,使胶体发生凝结,再将生成的含汞产物从气浮柱上部出口向外排出,同时从气浮柱下部将经过净化处理的水排出,之后测试溶液的汞浓度。
往烧杯中加入污酸和W105,并混合均匀;然后将混合液体倒入气浮柱,之后通过调控气体流量来进行气浮试验,最后对反应一段时间的混合液体进行测试分析
1.4 分析方法
通过冷原子吸收测汞仪测试汞在溶液中的浓度。同时,利用ICP测试了该溶液的其它重金属离子含量。最后,利用滴定法测试了溶液pH值。
2 脱汞剂的制备
制备脱汞剂可以通过下述步骤来实现:第一,烘干石油焦(PC)原料并对其实施破碎与筛分,得到粒径介于0.25~0.42 mm范围内的颗粒;第二,按照设定质量比将硝酸锌溶解于无水乙醇中再跟之前的石油焦进行混合,把上述混合物通过超声震荡器进行蒸干后再将其放入烘箱内进行干燥得到预浸料;第三,采用通入N2的管式炉对预浸料进行焙烧获得石油焦负载锌试样;第四,对试样进行活化。图1给出了制备脱汞剂的具体流程。
图2是对脱汞剂进行SEM表征得到的微观形貌图。根据图2可知,在碳表面上生长出了晶体,表明制备得到的脱汞剂具备较强活性。
采用固体脱汞剂来实现去除煤气中汞的过程,但却会因此生成新的固体废弃物,一旦出现处理不当的情况便会引起二次污染。由此可见,当脱汞剂吸附汞之后,汞能否在脱汞剂中稳定存在对于脱汞剂性能发挥着重要影响。同时,外界因素也会对脱汞剂的回收与再生过程造成一定的干扰,为了进一步分析脱汞剂内的汞稳定性,依次对经过使用的脱汞剂实施常温、60 ℃加热以及将其放入水中浸泡的方式进行处理。再对处理后的试样测定汞容值,具体结果见表1。
3 脱汞剂添加量对Hg和As脱除效果的影响分析
有色冶炼工厂排放的污酸中含有多种不同成分,并且各成分的浓度经常发生较大幅度的波动,无论是pH还是重金属离子含量都不太稳定,此外各个地区与不同季节中温度也会发生明显改变,这些都会对W105脱汞剂的处理效果产生显著影响,本实验除了分析W105添加量、通气时间、混合时间、气流量等因素对脱汞效果产生的影响外,还研究了酸度与温度的作用,由此实现对W105适用性的综合评价过程。
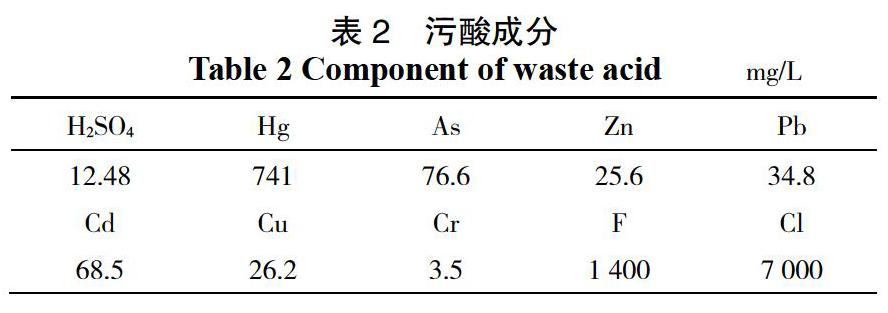
从现场采集的污酸,表2给出了对该污酸样品近元素分析所得的结果。
在脱汞剂W105中存在能够和胶体汞形成良好结合状态的官能团,需要根据污酸的汞含量来确定脱汞剂的添加量,并且在污酸中也会存在其它各类重金属离子和脱汞剂结合,表现为和汞产生竞争关系,因此本文将W105控制在不同的添加量来净化溶液中的汞与各类重金属,同时比较了不同W105添加量对应的汞与其它重金属之间的变化关系。
将混合温度设定为50 ℃,总共混合15 min,把气浮柱的通气时间也设置为15 min,控制通气流量为0.25 m3/L以及酸度等于14%,将污酸中的脱汞剂W105添加量控制在不同的比例并对比了各比例下得到的处理结果,经过以上净化处理后Hg、As在溶液中的残余浓度见图3。
根据图3可知,当W105添加量增大后,溶液中含有的Hg与其它各类重金属离子浓度发生了持续减小的现象,通过对比各金属含量的变化趋势可知,脱除效果最优的是Hg,最差的是锌,以150 mL污酸为例,在脱汞剂W105的添加量未超过4 mL的情况下,汞脱除率显著高于其它种类的重金属离子,随着W105添加量达到4 mL之后,从表3中可以看到各个重金属的实际脱除率。
将脱汞剂分子量按照200进行计算,其中,W105和污酸里含有的汞质量比等于8∶1,随着W105添加量的继续增加,经过净化处理后可以使溶液内的汞残余浓度不断减小,进一步改善脱除效果,并且还可以同步提高重金属的脱除效率。对W105添加量进行合理调控能够显著提高对污酸溶液中汞进行分离的选择性。
对图3测试数据进行分析可以发现,随着污酸中加入的W105质量与汞质量的比例达到10∶1时,可以使溶液中的汞浓度降到最低,测试得到此时的汞浓度等于0.065 mg/L,经过净化后得到的溶液中汞浓度将会逐渐增大,表明存在其它重金属离子和汞的竞争关系,当W105官能团被其它重金属结合后,将引起汞脱除效果降低的结果,同时还会导致W105用量的显著升高,但实际脱汞效果并无法获得较大改善,甚至出现变差的结果,因此按照与污酸中的汞含量等于10倍的比例关系来确定W105的最佳添加量。并且,为了克服污酸中的Hg与As分离难度大的问题,后续测试过程只分析W105脱汞剂对Hg与As的去除情况。
为进一步探讨H2S对于脱汞剂发挥的作用,通过测试得到图4所示的脱汞率曲線。可以看到,在初期1 h内,可以实现高达95%的脱汞率,当H2S供应停止后则会明显减小脱汞剂的汞去除率,当H2S停止供给达到2.5 h时脱汞率减小为30%,此时脱汞率与初期未通入H2S时一致。
4 脱汞剂中汞的稳定性
脱汞剂产生脱汞作用的机理是先吸附硫化氢反应得到活性硫组分,之后再跟单质汞生成稳定的硫化汞,反应式如下所示:
考虑到脱汞剂在脱汞阶段先以物理吸附方式和硫化氢气体结合再生成活性硫,因此随着温度的上升,这一吸附作用将下降,从而减小脱汞剂的脱汞活性。由于硫化氢浓度与单质汞之间相差非常大,基本可以忽略单质汞消耗硫化氢的量,可以忽略脱硫的影响。
可以将脱汞剂是否易于再生作为一个重要的评价指标。其中,热再生法属于脱汞剂再生的一项最广泛方法。通过热再生法来完成W105脱汞剂的再生过程。处理流程与具体操作步骤如下:先把经过脱汞处理的脱汞剂放入石英管内,再通入N2,并将N2流量控制在1 L/min ,将炉温升温至500 ℃,再保持恒温至尾气汞含量达到0.5 μg/m3 以下再停止加热,此时整个再生过程完成。之后继续对脱汞剂实施脱汞与再生,从图5中可以看到新鲜的以及经过再生处理的脱汞剂在脱汞方面的性能测试曲线。
通过对比可以发现,新鲜脱汞剂比再生脱汞剂的活性更低,同时当再生次数增大后,脱汞剂可以获得更优的脱汞性能。这主要是由于对脱汞剂进行再生时形成的HgS,会在高温下分解生成单质硫并被保留于吸附剂内,可以起到对单质汞的脱附作用,从而可以增强再次脱汞的效果。
5 结 论
(1)制备的脱汞剂碳表面上生长出了晶体,表明制备得到的脱汞剂具备较强活性。为了保持脱汞剂内的汞稳定性,依次对经过使用的脱汞剂实施常温、60 ℃加热以及将其放入水中浸泡的方式进行处理。
(2)当W105添加量增大后,溶液中含有的Hg与其它各类重金属离子浓度发生了持续减小的现象,脱除效果最优的是Hg,最差的是锌。
(3)脱汞剂产生脱汞作用的机理是先吸附硫化氢反应得到活性硫组分,之后再跟单质汞生成稳定的硫化汞。新鲜脱汞剂比再生脱汞剂的活性更低,同时当再生次数增大后,脱汞剂可以获得更优的脱汞性能。
参考文献:
[1]陈浩,黄亚继,董璐,曹健华,夏志鹏,秦文慧.磁性凹凸棒土制备及其脱汞性能研究[J/OL].燃料化学学报,2018(11):1-9.
[2]周强,段钰锋,卢平.燃煤电厂脱汞剂喷射脱汞技术的研究进展[J].化工进展,2018,37(11):4460-4467.
[3]曹朋怀.高级氧化法在烟气脱硫脱硝脱汞中的应用分析[J].民营科技,2018(10):89.
[4]喻珊,黄振山,唐美如,张再利,樊青娟,魏在山.氧含量对嗜热膜生物反应器烟气脱硝脱汞的影响[J].环境工程学报, 2018, 12 (10): 2797-2806.
[5]周成,邹康,冯远扬,潘光.煤中硫元素的热解组分与氧化组分耦合反应特性与脱汞性能研究[J].科技经济导刊,2018,26(28):4-8.
[6]娄彤,方晓东,陆明智,许仁发.燃煤烟气多污染物协同治理试验研究[J].洁净煤技术,2018,24(05):132-135+141.
[7]杨茹,刁永发.改性稻壳气化焦的烟气脱汞性能[J/OL].东华大学学报(自然科学版),2018(05):797-803.
[8]金玉群,雷静,陈智佳,刘发圣.氧化增效剂对湿法脱硫系统脱硫脱汞效率的影响[J].江西电力,2018,42(08):64-66.
[9]赵如恒,李凯,宁平,梅毅,孙鑫,王驰.生物炭干法同时脱硫脱硝脱汞研究进展[J].现代化工,2018,38(10):71-75.
[10]周洋.300MW级燃煤电站锅炉烟气低温脱硝及脱汞试验研究[J].上海电力学院学报,2018,34(04):329-332.
[11]兰吉勇,许月阳,张勇,朱懿灏,吴军辉,白勇,张艳艳.320 MW机组燃煤添加剂脱汞试验研究[J].电力科技与环保,2018,34(04):22-24.
[12]赵毅,王涵,徐梦楠,王晓慧.燃煤烟气脱硫脱硝脱汞研究文献计量分析[J].热力发电,2018,47(06):8-15.
[13]陈坤洋,郭婷婷,王海刚,胡冬.超低排放改造后燃煤烟气净化设备协同脱汞潜力分析[J].中国电力,2018,51(06):160-165.
[14]刘英波.液化天然气装置净化与液化工艺关键技术研究[J].当代化工,2016,45(11):2593-2595.
[15]王立坤. 吸附法去除电厂汞的研究进展[J]. 当代化工, 2014, 43 (02): 213-215.

