添加剂对Fe3O4/NiFe-LDHs生长的影响
方鹏飞,王忠川,于 欢,许英伟,王卫伟
(山东理工大学 材料科学与工程学院,山东 淄博 255049)
层状双金属氢氧化物(简称LDHs)是一种典型的结构可调的阴离子层状化合物,近年来在催化、离子交换、吸附以及环境治理等领域得到广泛应用[1]。LDHs具有大的比表面积和良好的离子交换性,可作为吸附剂用于工业废水的治理。但在实际使用中,存在着吸附剂不易回收,吸附性能有待提高等问题,限制了其应用。为提高LDHs的性能,常将LDHs与其他物质复合,如将LDHs与碳纳米管复合,提高LDHs的电催化性能;将LDHs与氧化石墨烯复合,提高LDHs对多巴胺的电催化性能[2];将LDHs与氧化物复合,提高其吸附性能[3]。Fe3O4因具备较好的磁性能,与LDHs复合后可以利用磁性能回收样品,解决LDHs材料不易回收的问题;且Fe3O4表面常吸附有大量的羟基,带有负电荷,而LDHs层板带正电荷,两者易于复合。目前LDHs与Fe3O4的合成方法主要为分步合成法和沉淀法[4-5]。研究发现,通过控制制备过程中的工艺条件,如表面活性剂种类、溶液pH值、Fe3O4表面吸附官能团种类和数量、反应温度等,能够控制Fe3O4/LDHs复合材料的结构、形貌、粒径,从而影响其性能。Zhang等[4]利用分步合成法制备了Fe3O4-C-NiAl-LDHs复合材料,通过改变制备条件,提高Fe3O4表面官能团总量,有利于LDHs复合材料的制备,同时提高LDHs的除铀能力。Azra等[5]利用沉淀法将Fe3O4和MgAl-LDHs复合,通过控制溶液pH值,得到MgAl-LDHs片层水平生长(包裹在Fe3O4表面)的核壳结构。赵满等[6]采用共沉淀法将Fe3O4和MgAl-LDHs复合,并包覆药物,制备具有特异选择性磁靶性的药物载体,研究发现制备条件如复合材料中两相含量影响复合材料的饱和磁靶向性。Tang等[7]通过水热法合成了磁性凹凸棒土/碳载NiFe-LDHs,研究发现NiFe-LDHs可以控制复合材料的磁响应和吸附性能,增强了复合材料对污染物的吸附能力和可回收性。LDHs的组成金属离子是多样的,如二价金属离子可以为Mg2+、Ni2+,三价金属离子可以为Al3+、Fe3+。组成离子种类不同,LDHs的性能不同。其中,NiFe-LDHs作为吸附剂具有更大的吸附容量,如利用共沉淀法制备的NiFe-LDHs对甲基橙(MO)的饱和吸附量为205.76 mg/g,比MgAl-LDHs(169.11 mg/g)大的多[8-9]。同时NiFe-LDHs可用于多种污染物的去除,如有机染料和重金属金属离子的吸附剂(如CR、PB等)[7],而NiAl-LDHs主要用作电极材料,很少用作吸附剂[10-11]。本文以Fe3O4为前驱体,通过溶剂热法合成Fe3O4/NiFe-LDHs复合材料,研究添加剂的种类和浓度对Fe3O4/NiFe-LDHs复合材料结构、形貌、结晶性等方面的影响,并探讨其生长规律。
1 实验部分
1.1 样品制备
实验药品有柠檬酸三钠、硝酸镍、无水乙醇、酒石酸钾钠、氯化铁、硝酸铁、乙二醇、乙酸钠、氢氧化钠(粒)、无水甲醇,均为分析纯。
采用溶剂热法制备前驱物Fe3O4[12]。 FeCl3·6H2O (0.125 mmol/L) 溶解于32 mL乙二醇中,再加入Na(CH3COO)·3H2O(0.656 mmol/L),充分搅拌30 min,然后转移到50 mL的反应釜中,200 ℃保温8 h,自然冷却至室温。离心水洗3次,醇洗1次,室温自然干燥,得到最终样品。
溶剂热法制备Fe3O4/NiFe-LDHs复合材料:(1)配置30 mL NaOH甲醇溶液(0.35 mol/L),并根据需要加入添加剂。将50 mg Fe3O4分散到其中,超声分散20 min。(2)配置30 mL 甲醇溶液,其中Ni(NO3)2·6H2O和Fe(NO3)3·9H2O的浓度分别为0.05 mol/L、0.025 mol/L。(3)将步骤2中配制的溶液一滴滴加入到步骤1配置的溶液中,将反应溶液转移到反应釜中,置入干燥箱,在100 ℃保温48 h。自然冷却至室温。离心水洗3次,醇洗1次,室温自然干燥,得到最终样品。5个样品中,镍铁比均为2∶1,添加剂用量见表1。
表1 添加剂种类及用量
Tab. 1 The kinds and amounts of additives

编号添加剂种类添加用量/mmol·L-1F1柠檬酸三钠0.5F2——F3柠檬酸三钠0.25F4柠檬酸三钠0.75F5酒石酸钾钠0.5
1.2 性能测试
X射线衍射分析(XRD)使用D8 ADVANCE多晶X 射线衍射仪,以Cu Kα为衍射源(λ =1.5406Å)。用FEI-Sirion 200F的场发射扫描电镜(SEM)对样品表面形貌进行表征,利用附件EDS进行成分分析;用Thermo Nicolet 5700型傅立叶红外光谱仪(FTIR)对样品的结构进行解析;利用MicroMag 3900型磁强计测试样品的磁性能。
2 结果与讨论
2.1 前驱物Fe3O4的制备与表征
图1 (a)为Fe3O4的XRD图谱,图中有多个尖锐的特征衍射峰,分别对应反尖晶石Fe3O4的(111)、(220)、(311)、(410)、(422)、(511)、(440)晶面的衍射峰,与标准卡片(JCPDS file NO.65-3107)一致,说明前驱物为Fe3O4。没有观察到其它杂质相的衍射峰。Fe3O4的衍射峰狭窄尖锐,说明其结晶性好。Fe3O4由许多形状较规整的球状颗粒构成,粒径较均匀,约为200 nm,如图2(a)所示。
2.2 添加剂的影响
2.2.1 样品结构和形貌分析
以Fe3O4为前驱物,利用溶剂热法制备Fe3O4/NiFe-LDHs,并对复合材料的结构和形貌进行分析。由图1(b)可知,当使用柠檬酸三钠作为添加剂时,样品F1中出现了LDHs(003)晶面的衍射峰(JCPDS file NO.40-0215),没有检测到明显的Fe3O4的衍射峰。LDHs常利用(003)晶面间距代表其层间距。由布拉格方程2dsinθ=λ,根据XRD衍射数据计算LDHs层间距为0.901 nm,说明层间吸附阴离子为NO3-离子,NO3-离子来源于制备复合材料时使用的硝酸盐(硝酸镍和硝酸铁)[10]。从图2(b)可以看到,样品F1粒径呈片层状,在片层附近存在粒子。由LDHs和Fe3O4的形貌特征可判断,层状结构为LDHs,小粒子为Fe3O4。利用能谱检测到其中的镍铁比约1∶2,远远小于LDHs中的镍铁比(2∶1),说明复合后由于引入Fe3O4,铁含量增加。从图2(e)可以看到,NiFe-LDHs片与Fe3O4粒子混合在一起,在片层表面生长着Fe3O4粒子。
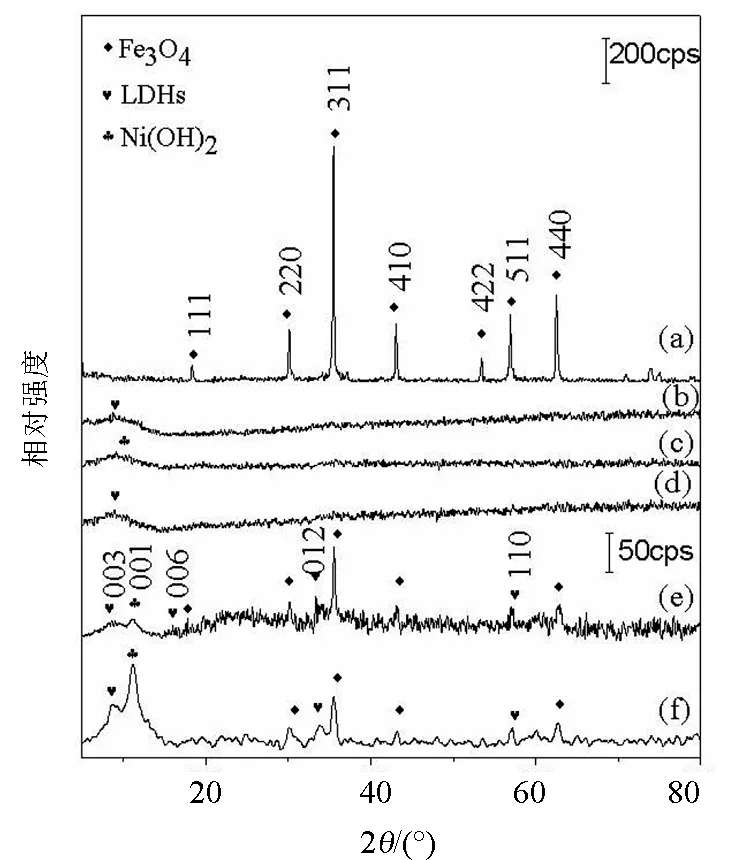
(a)Fe3O4;(b)样品F1;(c)样品F2;(d)样品F3;(e)样品F4;(f)样品F5图1 样品XRD谱图Fig.1 XRD patterns of samples

图2 样品SEM和TEM照片(插图为EDS谱图)Fig.2 SEM images of samples(insets are EDS spectra)
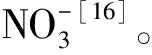

图3 样品FTIR图谱Fig.3 FTIR spectra of samples
2.2.2 添加剂用量的影响
改变柠檬酸三钠的用量,研究添加剂用量对样品生长的影响。不使用添加剂时,样品F2出现了Ni(OH)2(001)晶面的衍射峰(JCPDS file NO.22-0752),没有检测到Fe3O4和LDHs的衍射峰,如图1(c)所示。由图2(c)可以看出,样品F2为片构成的团聚状,在团聚体附近存在小粒子。利用能谱检测到其中的镍铁比约1∶2.1,说明复合后由于引入Fe3O4,铁含量增加。由图2(f)可以看出,样品团聚严重,由片层结构和球形离子构成。当添加剂用量较少时,样品F3的XRD谱图与样品F1相似,为单一物相的LDHs层状结构,仍没有检测到Fe3O4的衍射峰,如图1(d)所示。当增加添加剂用量时,样品F4中出现了LDHs的弱衍射峰和Fe3O4的衍射峰,同时检测到Ni(OH)2杂质峰,如图1(e)所示。因此柠檬酸三钠的用量影响着复合样品的生长,添加适量的柠檬酸三钠有利于样品的复合及生长。

Ni2++2OH-=Ni(OH)2
(1)
[Ni6Fe2(OH)16](CO3)·5H2O
(2)
2[Fe(C6H5O7)2]5-+6Ni2++
[Ni6Fe2OH)16](CO3)·5H2O+2C6H5O73-
(3)
2.2.3 添加剂种类的影响
改变添加剂的种类,研究添加剂种类对样品生长的影响。以酒石酸钾钠为添加剂时,样品F5出现了(003)、(012)、(110)等NiFe-LDHs的衍射峰和(220)、(311)、(410)、(440)等Fe3O4的衍射峰(JCPDS file NO.40-0215,65-3107,如图1(f)所示。同时,在2θ=11°左右出现了Ni(OH)2强的衍射峰。从图2(d)可以看出,样品F5粒径呈小球状,小球表面附着着粒子,由LDHs和Fe3O4结构和形貌判断,小球状颗粒为LDHs,粒子为Fe3O4。利用能谱检测到其中的镍铁比约1∶1.2,比LDHs中的镍铁比略低,但是与添加柠檬酸三钠制备的复合材料相比,铁含量低,结合XRD分析可知有Ni(OH)2生成,降低复合后样品中的铁含量。Fe3+与酒石酸钾钠的络合能力差,其络合能力要明显低于柠檬酸三钠[19],无法将Fe(OH)3参与的固相反应转化为较快的离子反应。所以Ni2+倾向发生沉淀反应生成Ni(OH)2。因此,添加剂的种类影响着样品的生长,以与Fe离子络合能力强的柠檬酸三钠作为添加剂时更有利于制备Fe3O4/NiFe-LDHs复合材料。
2.3 样品的磁性能分析
图4为交变梯度磁强计(VSM)在室温下测量Fe3O4/NiFe-LDHs复合材料的饱和磁滞回线。从图4可以看出,样品F1、F2、F5的磁滞回线均无明显的磁滞现象,剩余磁化强度(Mr)和矫顽力(Hc)均很小,表明3个样品均呈顺磁性。以柠檬酸三钠为添加剂,样品F1的饱和磁化强度最大,为11.8 emu/g;未添加柠檬酸三钠时,样品F2的饱和磁化强度略小(9.2 emu/g),但均比以酒石酸钾钠为添加剂制备的样品F5的饱和磁化强度大(7.0 emu/g)。因为颗粒尺寸越小,其表面效应越小,样品的矫顽力和饱和磁化强度越低。结合图2分析可知样品F1形成的聚集体尺寸最大,样品F5的最小,导致其饱和磁化强度不同。文献报道[7,20-21],样品的饱和磁化强度只需要大于5 emu/g,就可以利用外加磁场从溶液中回收吸附剂。样品的饱和磁化强度均大于5 emu/g,因此可以利用外加磁场实现吸附剂的回收。
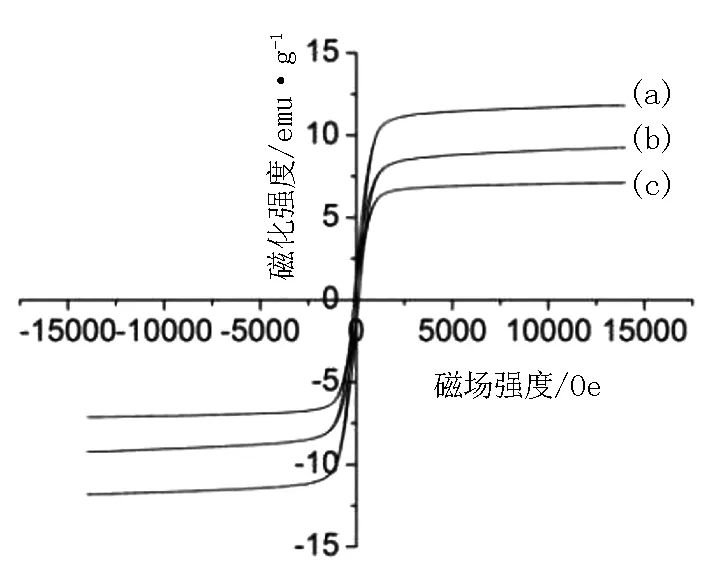
(a)样品F1;(b)样品F2;(c)样品F5图4 样品的室温磁滞回线Fig.4 Room temperature hysteresis loops of composite samples
3 结束语
利用溶剂热法合成了Fe3O4/NiFe-LDHs复合材料,并研究了添加剂用量和种类对复合材料生长的影响。与酒石酸钾钠相比,柠檬酸三钠与Fe3O4的络合作用更强。以适量的柠檬酸三钠作为添加剂可以有效防止Ni2+的沉淀,能够促进LDHs复合材料的生成。使用2种添加剂制备的Fe3O4/NiFe-LDHs复合材料磁性能相似,剩磁和矫顽力小,均为顺磁性。通过外加磁场,Fe3O4/NiFe-LDHs能与溶液快速分离。

