维药多脂大戟治疗白内障活性部位化学成分研究
廖东波 杨帆 朱智英 范淼崟 张亚梅
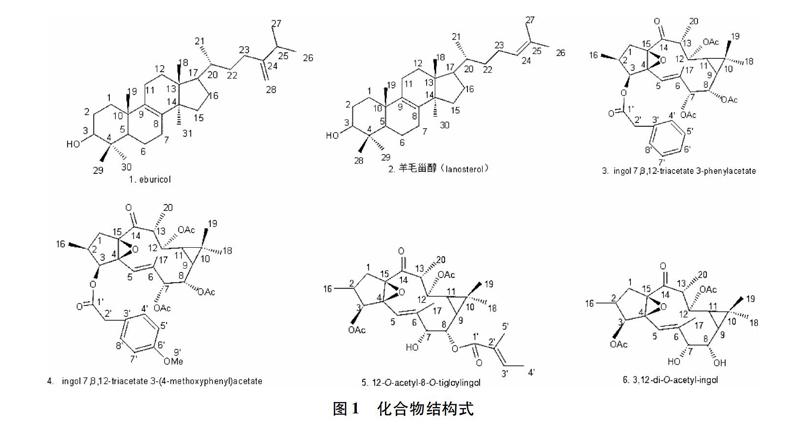
【摘 要】 目的:研究多脂大戟治疗白内障活性部位化学成分。方法:利用硅胶柱色谱、凝胶柱色谱、高效液相色谱等分离技术,对多脂大戟树脂抗白内障活性部位进行分离纯化,并通过1H-、13C-NMR等波谱技术进行结构鉴定。结果:共鉴定6个萜类化合物,分别为eburicol (1)、羊毛甾醇(2)、ingol 7,8,12-triacetate 3-phenylacetate (3)、ingol 7,8,12-triacetate 3-(4-methoxyphenyl) acetate(4)、12-O-Acetyl-8-O-tigloylingol (5)、3,12-di-O-acetylingol (6)。结论:化合物1、4、6首次从本种分离得到。
【关键词】 多脂大戟;大戟属;白内障;物质基础
【中图分类号】R282.6 【文献标志码】 A【文章编号】1007-8517(2020)23-0032-04
Study on Material Basis of Anti-cataractogesis Activity of Euphorbia resinifera
LIAO Dongbo YANG Fan ZHU Zhiying FAN Miaoyin ZHANG Yamei*
Jiangxi University of Traditional Chinese Medicine, Nanchang 330004,China
Abstract:Objective To study the material basis of anti-cataractogesis activity of Euphorbia resinifera. Methods The material basis of anti-cataractogesis activity of Euphorbia resinifera were isolated by different column chromatographic techniques. Their structures were identified by a comprehensive analysis of the spectroscopic data. Results six compounds were isolated from Euphorbia resinifera and identified as eburicol (1), lanosterol (2)、ingol 7,8,12-triacetate 3-phenylacetate (3)、ingol 7,8,12-triacetate 3-(4-methoxyphenyl)acetate (4)、3-O-acetyl-8-O-tigloylingol (5)、8-O-tigloylingol(6). Conclusion These compounds may relate to the anti-cataractogesis activity of Euphorbia resinifera.
Keywords:Euphorbia resinifera;Euphorbia;Material Basis;Anti-cataractogesis
多脂大戟Euphorbia resinifera Berg.隸属于大戟科Euphorbiaceae,其树脂状分泌物大戟脂(Euphorbium)即维药“排日非云”,具有散寒止痛、燥湿退肿、强筋健骨、消除白内障等功效,主治湿寒性或黏液质性疾病,如瘫痪、关节疼痛、腹水、白内障等疾病[1-2]。课题组前期通过硒性白内障大鼠动物模型筛选多脂大戟治疗白内障活性部位,发现大戟脂95%乙醇提取物的乙酸乙酯萃取部位具有治疗白内障活性。基于此,本实验对此部位进行化学成分研究,以探明多脂大戟治疗白内障的物质基础。
1 仪器与材料
1.1 仪器 Shimazu LC-6AD制备液相色谱仪,Buchi C605中压色谱仪,Agilent 1200液相色谱仪,Buchi R-220SE旋转蒸发仪,TripleTOF5600 质谱仪 (ESI-MS),Bruker AVANCE III 600 核磁共振波谱仪。
1.2 材料 青岛海洋硅胶G (100~200、200~300目),Sephadex LH-20凝胶,反相硅胶C18(50μ),MCI HP-20,色谱用甲醇、乙腈,其余试剂均为分析纯。多脂大戟树脂购于新疆和田药材市场,经江西中医药大学钟国跃研究员鉴定为大戟科 Euphorbiaceae 植物多脂大戟E. resinifera的树脂状分泌物。标本现存于江西中医药大学中药资源与民族药研究中心标本馆。凭证标本(20180804)存放于江西中医药大学标本馆。
2 提取分离
多脂大戟树脂活性部位(95%乙醇提取物的乙酸乙酯萃取部位)62.5g,加甲醇溶解后,通过硅胶色谱柱进行初步分离,依次用石油醚-丙酮(50∶1,Fi1),石油醚-丙酮(30∶1,Fi2)、石油醚-丙酮(15∶1,Fi3),石油醚-丙酮(5∶1,Fi4)、石油醚-丙酮(1∶1,Fi5)、乙酸乙酯(Fi6)梯度洗脱,甲醇冲柱(Fi7)。回收溶剂得到7个洗脱部分(Fi1-Fi7)。薄层色谱显色石油醚-丙酮(30∶1),即Fi2部分化合物多,且与其它组分重叠斑点较少。 故将其进一步通过MCI柱层析、凝胶柱层析、中压反相硅胶柱层析、制备反相硅胶柱层析分离,最终得到6个化合物。
3 结构鉴定
各化合物通过TLC、HPLC、香草醛浓硫酸显色、UV、以及MS、NMR等方法确定了结构。
化合物1 (246.9mg): 白色粉末。HR-ESI-MS:分子量440,分子式C31H52O。1H-NMR (600 MHz, CDCl3) δ: 4.73 (1H, brs, H-28α), 4.68 (1H, brs, H-28β), 3.23 (1H, m, H-3), 1.02 (3H, d,J= 7.1 Hz, H-26), 1.01 (3H, d, J=7.1 Hz, H-27), 0.99 (3H, s, H-29), 0.94 (3H, s, H-19), 0.96 (3H, d,J= 6.3 Hz, H-21), 0.86 (6H, s, H-30, 31), 0.74(3H, s, H-18);13C NMR (150 MHz, CDCl3) δ: 35.5 (C-1), 27.6 (C-2), 76.3 (C-3), 39.2 (C-4), 50.8 (C-5), 17.6 (C-6), 28.1 (C-7), 133.5 (C-8), 134.3 (C-9), 36.6 (C-10), 20.1 (C-11), 25.7 (C-12), 31.2 (C-13),49.6 (C-14), 30.9 (C-15), 30.7 (C-16), 50.1 (C-17), 15.6 (C-18), 18.3 (C-19), 34.9 (C-20), 18.8 (C-21), 33.9 (C-22), 31.2 (C-23), 157.1 (C-24), 31.3 (C-25), 21.6 (C-26), 22.1 (C-27), 106.1 (C-28), 27.9 (C-29), 15.4 (C-30), 24.5 (C-31)上述数据与文献报道一致[3],故鉴定为eburicol。
化合物2(611.2mg):白色粉末。HR-ESI-MS:分子量426,分子式C30H50O。1H-NMR (600 MHz, CDCl3) δ: 0.75 (3H, s, CH3-30), 0.79 (3H, s, CH3-18), 0.84 (3H, d,J =6.5Hz, CH3-21), 0.87 (3H, s,CH3-28) , 0.91 (3H, s, CH3-29) , 1.59 (3H, s, CH3-26) , 1.68 (3H, s, H-27), 3.22 (1H, dd,J= 4.5, 2.3 Hz, H-3), 5.09 (1H, m, H-24);13C NMR (150 MHz, CDCl3) δ: 35.9 (C-1), 28.2 (C-2), 79.0 (C-3), 38.9 (C-4), 50.1 (C-5), 20.1 (C-6), 28.2 (C-7), 134.0 (C-8), 133.4 (C-9), 37.4 (C-10), 28.2 (C-11), 25.8 (C-12), 44.1 (C-13),49.6 (C-14), 30.9 (C-15), 29.9 (C-16), 50.0 (C-17), 15.6 (C-18), 18.7 (C-19), 35.0 (C-20), 18.8 (C-21), 35.3 (C-22), 24.8 (C-23), 125.4 (C-24), 130.8 (C-25), 24.7 (C-26), 17.7 (C-27), 24.4 (C-28), 27.8 (C-29), 15.6 (C-30)。上述数据与文献报道一致[4],故鉴定为羊毛甾醇。
化合物3(52.2mg):白色粉末。 HR-ESI-MS:分子量610,分子式C34H42O10。1H-NMR (600 MHz, CHCl3) δ: 2.78 (1H, dd,J= 14.8、9.0 Hz, H-1α), 1.69 (1H, d, J=14.8 Hz, H-1β), 2.51 (1H, m, H-2),5.15 (1H, brs, H-3), 5.39 (1H, brs, H-5), 5.12 (1H, d,J=1.6 Hz, H-7), 4.52 (1H, dd,J= 10.4、1.6 Hz, H-8), 1.09 (1H, dd,J=10.4, 9.3Hz, H-9), 1.01 (1H, m, H-11), 4.82 (1H, dd,J= 10.7、3.8 Hz, H-12), 2.90 (1H, qd,J= 7.4、3.8 Hz, H-13), 0.92 (3H, d,J= 7.4 Hz, H-16), 2.05 (3H, 3, H-17), 1.04 (3H, s, H-18), 0.82 (3H, s, H-19), 1.04 (3H, d,J= 7.0 Hz, H-20), 3.72 (2H, br, H-2′), 7.31 (1H, m, H-4′) , 7.31 (1H, m,J= 8.6 Hz, H-5′), 7.31 (1H, m, H-7′), 7.31 (1H, d,J= 8.6 Hz, H-8′) , 2.09 (3H, s, COCH3), 2.05 (3H, s, COCH3), 1.97 (3H, s,COCH3)。13C NMR (150 MHz, CDCl3) δ: 31.4 (C-1), 29.5 (C-2), 76.3 (C-3), 73.4(C-4), 117.1 (C-5), 139.3 (C-6), 76.9 (C-7), 71.1 (C-8), 24.7 (C-9), 19.2 (C-10), 30.6 (C-11), 70.6 (C-12) , 43.0 (C-13), 207.9(C-14), 71.5 (C-15), 16.9 (C-16), 17.5 (C-17), 29.1 (C-18), 16.1 (C-19), 13.4 (C-20), 170.3 (C-1′), 41.5 (C-2′), 133.8 (C-3′), 129.3 (C-4′), 128.6 (C-5′), 127.4 (C-6′), 128.6 (C-7′), 129.3 (C-8′), 170.8 (COCH3), 170.3(COCH3),170.4(COCH3),21.0 (COCH3), 20.9 (COCH3), 20.6 (COCH3)。以上數据与文献报道一致[5],确定为ingol 7,8,12-triacetate-3-phenylacetate。
化合物4(30.4mg):白色粉末。 HR-ESI-MS:分子量 640,分子式C35H45O11。 1H-NMR (600 MHz, CHCl3) δ: 2.78 (1H, dd,J= 15.0、9.0 Hz, H-1α), 1.68 (1H, d,J=15.0Hz, H-1β), 2.51 (1H, m, H-2),5.16 (1H, d,J= 8.6 Hz, H-3), 5.40 (1H, brs, H-5), 5.14(1H, d,J=1.6 Hz, H-7), 4.54 (1H, dd,J= 10.6、1.6 Hz, H-8), 1.10 (1H, dd,J=10.6、9.1Hz, H-9), 1.04 (1H, m, H-11), 4.83 (1H, dd,J= 10.6、4.0 Hz, H-12), 2.89 (1H, qd,J= 7.3、4.0 Hz, H-13), 0.92 (3H, d,J= 7.3 Hz, H-16), 2.06 (3H, 3, H-17), 1.04 (3H, s, H-18), 0.82 (3H, s, H-19), 1.05 (3H,J=7.0Hz, H-20), 3.80 (3H, s, OCH3), 3.67 (2H, brs, H-2′), 7.20 (1H, m, H-4′) , 6.85 (1H, m, H-5′), 6.85 (1H, m, H-7′), 7.20 (1H, m, H-8′) , 2.06 (3H, s, COCH3), 2.09 (3H, s, COCH3), 1.97 (3H, s,COCH3)。13C NMR (150 MHz, CDCl3) δ: 31.5 (C-1), 29.5 (C-2), 76.9 (C-3), 73.4(C-4), 117.1 (C-5), 139.4 (C-6), 76.9 (C-7), 71.5 (C-8), 24.6 (C-9), 19.3 (C-10), 30.6 (C-11), 70.6 (C-12) , 43.0 (C-13), 207.8 (C-14), 71.1 (C-15), 16.9 (C-16), 17.4 (C-17), 29.1 (C-18), 16.0 (C-19), 13.4 (C-20), 170.4 (C-1′), 40.6 (C-2′), 113.9 (C-3′), 130.4 (C-4′), 125.7 (C-5′), 158.4 (C-6′), 125.7 (C-7′), 130.4 (C-8′), 55.4 (-OCH3), 170.6(COCH3), 20.6(COCH3), 170.5 (COCH3), 20.9 (COCH3), 170.3(COCH3), 21.0(COCH3)。以上數据与文献报道一致[6],确定为ingol 7,8,12-triacetate 3-(4-methoxyphenyl)acetate。
化合物5(21.1mg):白色粉末。 HR-ESI-MS:分子量 490,分子式C27H38O8。 1H-NMR (600 MHz, CHCl3) δ: 1.64 (1H, dd,J=14.9、1.9 Hz, H-1β), 2.76 (1H, dd,J=14.9、9.0 Hz, H-1α), 2.40 (1H, m, H-2),4.36 (1H, d,J= 8.2 Hz, H-3), 5.87 (1H, brs, H-5), 4.28 (1H, brs, H-7), 4.57 (1H, dd,J= 10.7, 1.4 Hz, H-8), 1.43 (1H, dd,J= 10.7, 9.5 Hz, H-9), 1.10 (1H, dd,J= 11.0, 9.5 Hz, H-11), 4.87 (1H, dd,J=11.0, 3.9 Hz, H-12), 2.92 (1H, dq,J=3.9, 7.3 Hz, H-13), 1.07 (3H, d,J= 7.6 Hz, H-16), 2.09 (3H, brs, H-17), 1.09 (3H, s, H-18), 0.82 (3H, s, H-19), 1.04 (3H, d,J= 7.3 Hz, H-20), 2.07(3H, s, OCH3), 6.91 (1H, qq,J=6.0, 1.2 Hz, H-3′), 1.81 (3H, dq,J=6.0, 1.6 Hz, H-4′) , 1.84 (3H, dq,J=1.6, 1.6 Hz, H-5′)。13C NMR (150 MHz, CDCl3) δ: 31.8 (C-1), 29.1 (C-2), 76.1(C-3), 74.3(C-4), 117.1 (C-5), 141.7 (C-6), 76.4 (C-7), 76.3 (C-8), 23.8 (C-9), 19.1 (C-10), 31.6 (C-11), 70.9 (C-12) , 43.2 (C-13), 207.9 (C-14), 72.8 (C-15), 16.3 (C-16), 17.5 (C-17), 29.2 (C-18), 16.3 (C-19), 13.4 (C-20), 170.7 (OCOCH3), 21.0 (COCH3),167.7 (C-1′), 138.2 (C-2′), 128.7 (C-3′), 12.0 (C-4′), 14.5 (C-5′)。以上数据与文献报道一致[7],确定为12-O-acetyl-8-O-tigloylingol 。
化合物6(47.5mg):白色固体。HR-ESI-MS:分子量450,分子式C24H34O8; 1H-NMR (600 MHz, CDCl3) δ: 2.82 (1H, dd,J= 15.0、9.3 Hz, H-1α), 1.66 (1H, d,J= 15.0, 1.9 Hz, H-1β), 2.58 (1H, m, H-2),5.21 (1H, d,J= 8.4 Hz, H-3), 5.75 (1H, s, H-5), 4.21 (1H, s, H-7), 3.46 (1H, dd,J= 10.3、1.9 Hz, H-8), 1.25 (1H, m, H-9), 1.06 (1H, m, H-11), 4.85 (1H, dd,J= 11.0、3.9 Hz, H-12), 2.93 (1H, m, H-13), 0.90 (3H, d,J= 7.4 Hz, H-16), 1.97 (3H, s, H-17), 1.09 (3H, s, H-18), 1.08 (3H, s, H-19), 1.04 (3H, d,J= 7.3 Hz, H-20), 2.10 (6H, s, C12OCOCH3, C3OCOCH3)。13C NMR (150 MHz, CDCl3) δ: 31.7 (C-1), 29.6 (C-2), 77.7(C-3), 71.3 (C-4), 116.6 (C-5), 141.7 (C-6), 78.2 (C-7), 71.5 (C-8), 27.5(C-9), 18.4 (C-10), 31.0 (C-11), 70.9 (C-12) , 43.1 (C-13), 207.7 (C-14), 73.9 (C-15), 17.0 (C-16), 17.9 (C-17), 29.4 (C-18), 16.5 (C-19), 13.4 (C-20), 20.8 (C3OCOCH3), 21.1 (C12OCOCH3), 170.9 (C3OCOCH3), 17.07 (C12OCOCH3)。以上数据与文献报道一致[8],确定为3,12-di-O-acetylingol。
4 结 论
维药“排日非云”在当地民间用于治疗白内障,但尚未见有关其清除白内障的药理和化学研究报道。本实验前期通过硒性白内障大鼠动物模型筛选出多脂大戟树脂治疗白内障的活性部位,通过进一步分离得到6个单体化合物, 其中羊毛甾醇及其类似物eburicol 为主要成分。研究表明,羊毛甾醇可以降低兔白内障晶状体白内障严重程度、提高透明度,并在体内试验中减轻了狗白内障严重程度[9]。据此,初步推断维药“排日非云”用于治疗白内障可能与所含大量的羊毛甾醇及类似物相关。
参考文献
[1]国家中医药管理局《中华本草》编委会.中华本草-维吾尔药卷[M].上海:上海科学技术出版社,2005:68.
[2]中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准-维吾爾药分册[M].乌鲁木齐:新疆科技卫生出版社,1999:149.
[3]柏玉冰,李春, 周亚敏, 等. 夏枯草的化学成分及其三萜成分的抗肿瘤活性研究[J].中草药, 2015,46(24):3623-3629.
[4]赵芬琴,朴惠善. 桦褐孔菌的抗突变活性成分研究[J]. 中草药,2006,37(12):1777-1780.
[5]王书云,李钦,李国玉. 大戟脂中二萜类成分及细胞毒活性研究[J]. 河南大学学报,2019,38(3):153-157.
[6]张艳楠,吉腾飞, 顾政一. 大戟脂化学成分的研究[J]. 新疆医科大学学报, 2019,42(5):667-672.
[7]GEWALL M B, HATTORI M,TEZUKA Y, et al. Four Ingol Type Diterpenes from Euphorbia antiquorum L.[J]. Chemical & Pharmaceutical Bulletin, 37: 1547-1549.
[8]AN L J,LIANG Y,YANG X Y, et al. anti-inflammatory agents from Euphorbia antiquorum.[J]. Bioorganic Chemistry, 2019(92) : 1370-1377.
[9]MAKLEY L N, MCMENIMEN K A, et al. Pharmacological chaperone for a-crystallin partially restores transparency in cataract models[J]. Scinece, 2015(6): 674-677.
(收稿日期:2020-06-05 编辑:刘斌)
基金项目:江西省卫生计生委中医药科研课题 (2017A300)。
作者简介:廖东波(1994-),男,汉族,硕士研究生在读,研究方向为中药质量标准研究。 E-mail:2473776179@qq.com
通信作者:张亚梅(1982-),女,汉族,博士,副教授,研究方向为中药资源与民族药开发利用研究。E-mail:yameizhang01@126.com

