手性有序无机介孔硅用作气相色谱固定相
普 青, 何宇雨, 袁黎明
(云南师范大学化学化工学院, 云南 昆明 650500)
手性是自然界的本质属性之一。手性表示一种物质的对称特点,就如同人的左手和右手,相互对称,并不会完全重叠,两者是实物和镜像的关系,这样的关系称为手性[1]。手性这一属性在大多数分子中均有体现,例如DNA、激素、药物。据统计[2],目前在约2 000种常用药物中,有接近500种药物是以外消旋体形式存在的,并且手性药物构型与其所针对的细胞中的受体相匹配是至关重要的,如果不相匹配会降低药物的效力,并且可能对身体有害。也就是说,外消旋体药物[1,3,4]中起作用的可能只是其中一种对映异构体,而另外一种异构体可能没有药效,也有可能有毒副作用[5]。例如,右旋巴比妥酸盐药理活性主要使神经兴奋,而左旋构型则抑制神经活动;(+)-甲状腺素钠具有降血脂功效,但(-)-甲状腺素钠对人体心脏有较大的毒副作用;天然的(-)-尼古丁[2]会比(+)-尼古丁具有更强的毒性。所以手性药物与细胞内受体相匹配[6,7]也就显得尤为重要。
介孔材料具有高比表面积、大孔容、可调孔径、易于将其功能化等特点[8]。Che等[9,10]采用加入助结构导向剂(co-structure-directing agent)的方法,成功合成高度有序的手性介孔硅[11]。该材料与一般的介孔材料相比,除介孔结构高度有序外,其手性来自于手性模板和结构助导剂的印迹,通过高温烧掉有机物,所得材料全部由无机成分组成,而绝大多数其他手性介孔材料是在介孔材料的孔穴中键合上有机的手性功能团。所以该材料能耐高温,分离选择性好。目前的气相色谱手性柱因为手性识别位点皆为有机基团[12,13],通常只能在230 ℃以下使用,因此手性有序无机介孔硅尤其适用于高温气相色谱手性柱的制备[14]。本文利用D-苯丙氨酸为手性源,以手性阴离子(C14-D-Phe)为表面活性剂,四乙氧基硅烷为硅源,N-三甲氧基丙基硅烷-N,N,N-三甲基氯化铵(TMAPS)为助结构剂,合成一种以氨基酸小分子为手性源的介孔硅(简称COIMS),将其作为色谱固定相制备毛细管色谱柱[15],对手性化合物进行拆分,并讨论其固定相极性、柱效。
1 实验部分
1.1 仪器、试剂与材料
GC-2014C高分辨气相色谱仪(日本岛津)。
十四烷基酰氯、D-苯丙氨酸、异丙醇、乙酰氯、三氟乙酸酐、四乙氧基硅烷(TEOS)均购自上海Adamas-beta公司;N-三甲氧基丙基硅烷-N,N,N-三甲基氯化铵(50%(体积分数)甲醇溶液)购于北京百灵威科技有限公司;外消旋体缬氨酸、苏氨酸、1,3-丁二醇、蛋氨酸、1-氨基-2-丙醇、色氨酸、乙酸二氢香芹酯和乳酸乙酯均购自美国Sigma-Aldrich公司;盐酸购自重庆川东化工化学试剂技术有限公司;氢氧化钠购买于天津风船化学试剂科技有限公司,用于毛细管柱的粗糙化;丙酮购自云南山电药业;石油醚购自成都科隆化学有限公司;用于色谱柱性能测试的正构烷烃(壬烷、癸烷、十一烷、十二烷、十三烷、十四烷、十五烷、十六烷)和正构醇类(甲醇、乙醇、丙醇、丁醇、戊醇、己醇、庚醇、辛醇)均购自北京化学试剂有限公司。以上试剂皆为分析纯或以上产品。
1.2 COIMS的制备
该手性介孔硅的合成是参照Che课题组[16]的步骤。肉豆蔻基酰氯-D-苯丙氨酸钠为模板与无机硅烷作用和自组装,形成形貌为外螺旋结构的介孔二氧化硅。该合成步骤分为两步:
(1)手性阴离子表面活性剂(C14-D-Phe)的合成。将0.1 mol D-苯丙氨酸和0.1 mol NaOH在5 ℃下搅拌溶解于纯水和丙酮的混合溶液(体积比为3∶2)中,用氢氧化钠调节pH=12左右,然后在保持碱性的情况下不断加十四烷基酰氯(0.11 mol),期间不断滴加氢氧化钠,维持pH=12。反应过夜之后再逐渐滴加浓盐酸,调节该体系的pH约为1,搅拌1 h,得到手性表面活性剂C14-D-Phe,用水洗至中性,再用石油醚洗去一些长链羧酸,在50 ℃左右挥干石油醚,将结块固体研磨,备用。
(2)手性有序无机介孔硅的合成以及模板去除。在室温下,将表面活性剂C14-D-Phe溶于纯水和NaOH的混合溶液(体积总和为25 mL)中搅拌1 h,之后在22 ℃下将1.50 g TEOS和0.26 g TMAPS混合后加入上述体系中,搅拌30 min,静置2 h,在60 ℃水浴搅拌15 h,离心水洗,在60 ℃下真空干燥,待用。
将干燥后的固体放入马弗炉中,从常温条件以2 ℃/min的速率升温至550 ℃,保持6 h去除模板。
1.3 介孔硅固定相毛细管柱的涂敷
截取15 m×250 μm i.d.的弹性石英毛细管,用1 mol/L NaOH处理毛细管内壁2.5 h,然后换成纯水洗涤,使流出的溶剂呈中性。再用0.1 mol/L盐酸处理0.5 h,用纯水再次处理至流出的溶剂呈中性。最后以氮气吹干,将上述处理过的毛细管空柱接入气相色谱仪干燥3 h,柱温设置在100~120 ℃左右。
采用动态涂敷法将手性固定相均匀涂在毛细管柱内壁[17,18]。首先取0.2 mL的聚硅氧烷OV-1701的乙醇溶液和2 mL溶解有固定相的乙醇溶液混合,超声15 min,使之分散均匀,静置30 min,若没有固体沉淀到玻璃管底部,说明该固定相能够在乙醇中较好地悬浮,可以进行毛细管的涂敷。将配制好的混合物悬浮液通过氮气吹入毛细管内,使其完全填充在毛细管柱内,再用氮气将溶剂缓慢吹干,使其在内壁均匀地涂敷,并形成一定厚度的膜,最后用程序升温的方式老化柱子,以2 ℃/min的速率从25 ℃升温至250 ℃,并保持180 min。
1.4 外消旋化合物的衍生
氨基酸通常难挥发,一些醇和胺极性较大,色谱峰容易拖尾,因此需要对氨基酸以及部分手性的醇类、胺类进行衍生化。本文测定的氨基酸都是经过衍生的。具体衍生[14,18,19]方法如下:取50~60 mg左右的氨基酸加入到反应釜内衬中,取1~2 mL的异丙醇与乙酰氯(3∶1, v/v)混合溶液将其进行溶解,并超声15 min,使其密封反应30 min,温度设置为110 ℃。待冷却后用干燥的氮气吹干溶剂,加入3 mL的四氢呋喃(THF)将产物进行溶解,并向其中缓慢滴加三氟乙酸酐并搅拌,将其密封,并在90 ℃下反应30 min,利用减压来除去溶剂,并用CH2Cl2将产物溶解待用。从而制得三氟乙酰基衍生物。
1.5 实验条件
汽化室温度:280 ℃;检测器温度:280 ℃;载气:高纯N2;燃气:H2, 65 kPa;助燃气:空气,50 kPa。
2 结果与讨论
2.1 COIMS和COIMS毛细管柱的表征
用COIMS粉末的乙醇悬浮液,测圆二色谱(CD),图1a表明该试验合成的介孔硅具有单一手性,其在240~250 nm有较强的响应值。将COIMS进行SA-XRD(小角X射线衍射)测试,图1b图谱与文献报道相似[16]。图1c为热重表征图,结果表明COIMS具有很好的热稳定性,可以用作高温气相色谱固定相。
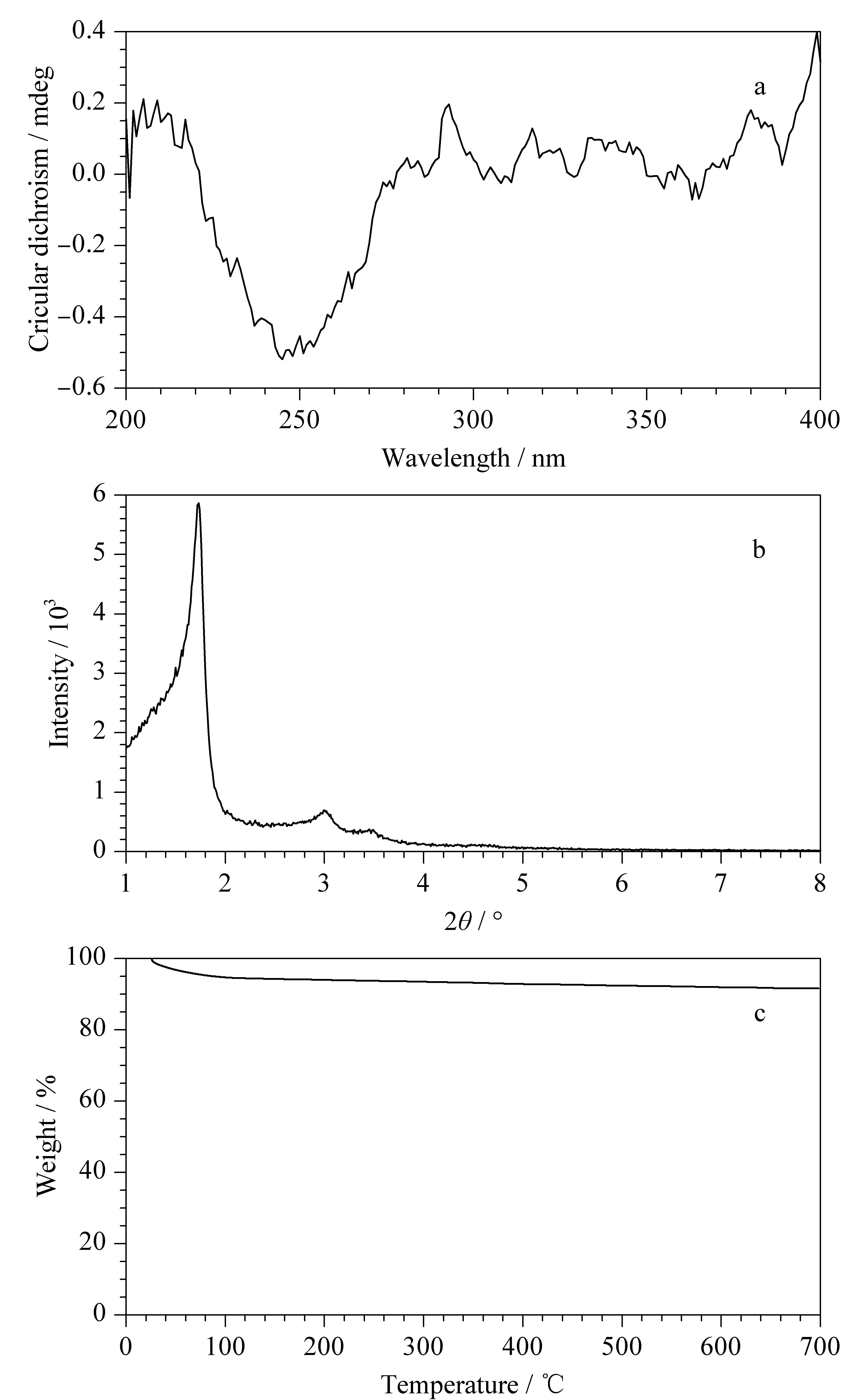
图1 COIMS的(a)CD图、(b)XRD图和(c)TGA曲线
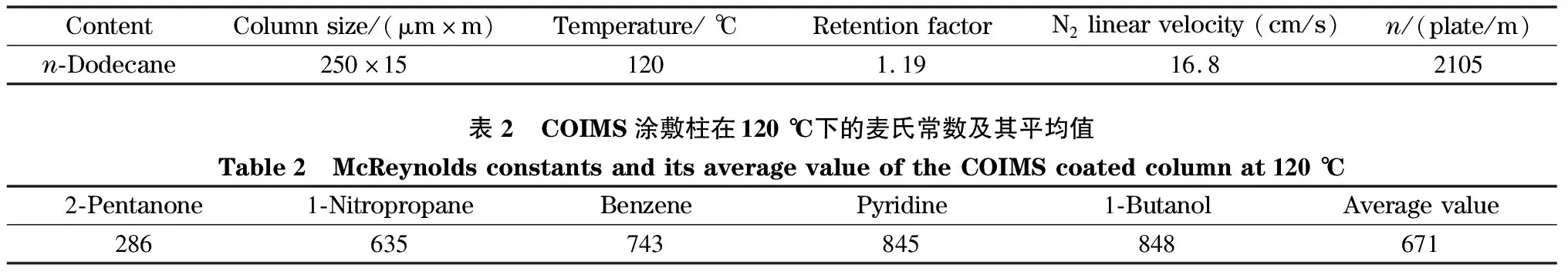
表1 COIMS涂敷柱在120 ℃下的保留因子及柱效
为了观察COIMS在毛细管柱内壁的涂敷情况,将手性柱截为长0.5 cm左右的小段,置于扫描电镜样品台上,喷金后进行SEM分析,图2a为COIMS毛细管的截面图,涂敷的毛细管厚度约为3 μm,图2b为COIMS毛细管柱内壁的形貌图,可知毛细管内壁已涂敷了一层COIMS。通过对COIMS进行SEM测试,可观察到形貌如图2c;通过透射电镜表征如图2d所示,具有有序的介孔孔道。

图2 COIMS涂敷柱截面以及COIMS的SEM图和TEM图
2.2 毛细管柱效和极性的评价
气相色谱柱的柱效通常用理论塔板数(the number of theoretical plates,n)来表示,如表1所示,表明该毛细管柱柱效较好。
一般情况下,用McReynolds常数来测试固定相的极性[20]。如表2所示,将1-硝基丙烷、2-戊酮、1-丁醇、苯和吡啶这5种物质作为测试物,在120 ℃下测试McReynolds常数。COIMS毛细管柱的McReynolds常数平均值为671,表明COIMS为强极性固定相。
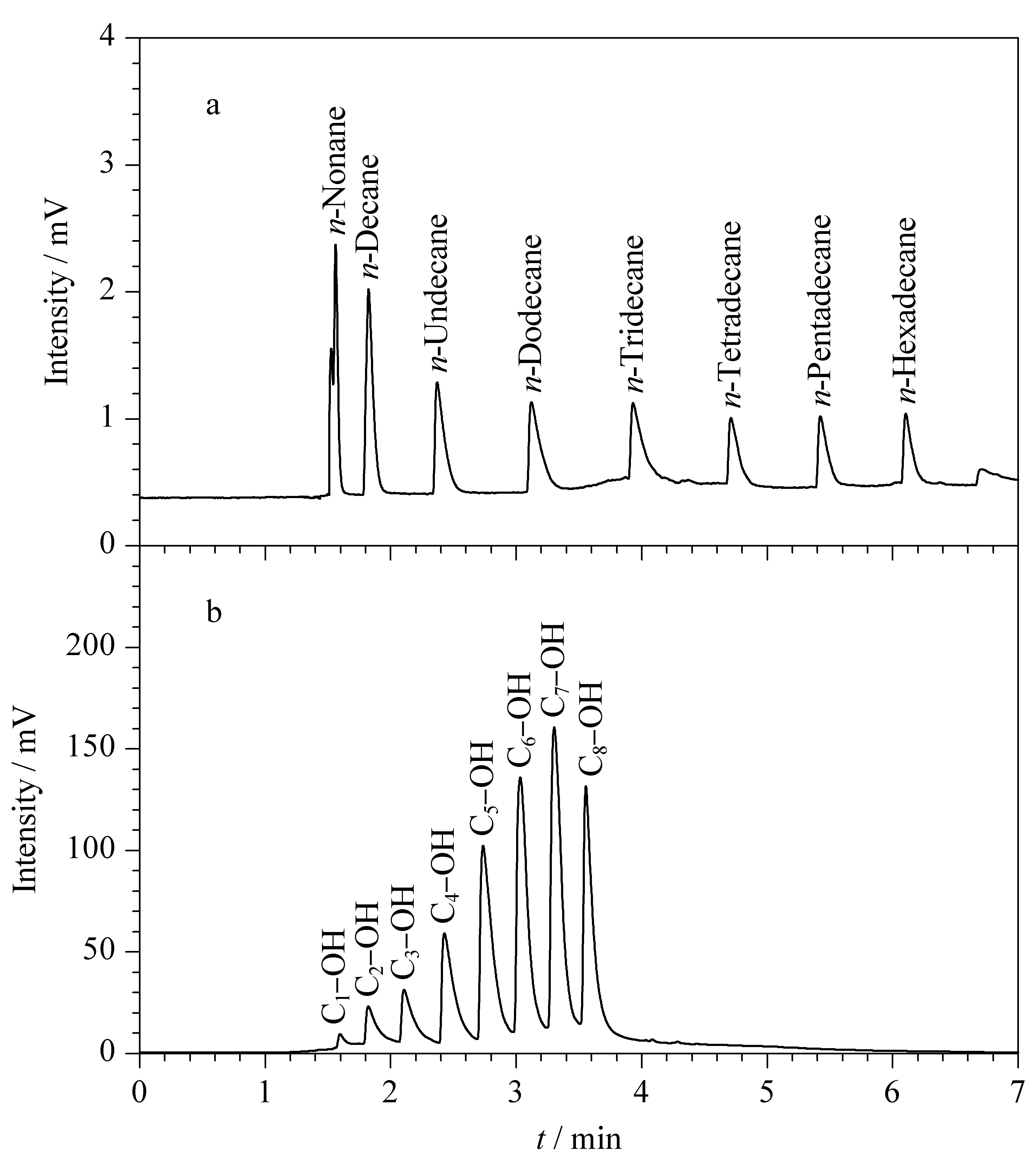
图3 在COIMS涂敷柱上进行的程序升温分离色谱图
2.3 毛细管柱对正构烷烃和正构醇的分离
如图3所示,对柱子进行了正构烷烃混合物(从壬烷到十六烷)、正构醇混合物(从甲醇到正辛醇)的分离测试,结果表明正构烷烃在该柱上已经实现基线分离,并且该毛细管柱对极性较大的醇类的分离也能基本达到基线分离。
2.4 毛细管柱对手性化合物的分离
用COIMS柱对外消旋体进行拆分,拆分数据列于表3中,拆分谱图见图4。结果表明,缬氨酸、蛋氨酸、色氨酸、苏氨酸、1,3-丁二醇、1-氨基-2-丙醇、乙酸二氢香芹酯和乳酸乙酯这8种外消旋体在该手性柱上实现了不同程度的分离。
表3 外消旋体化合物在COIMS涂敷柱上的分离
Table 3 Separation of racemates on COIMS coated column
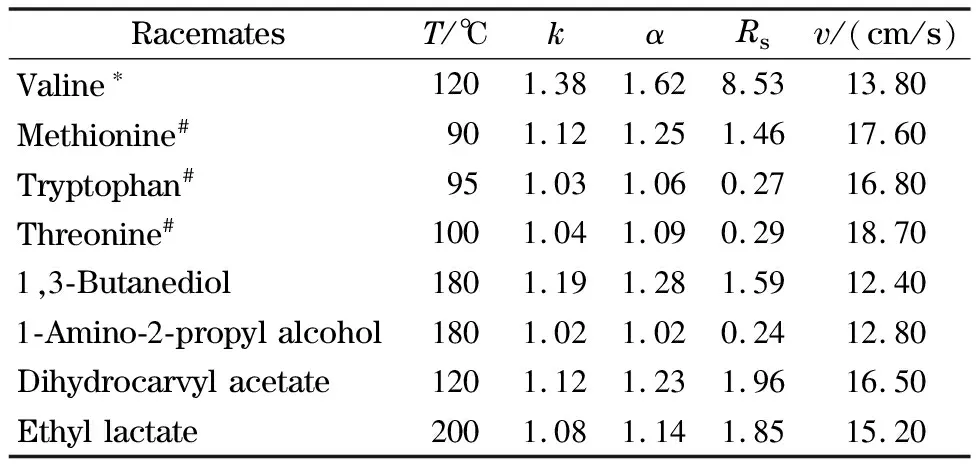
RacematesT/℃kαRsv/(cm/s)Valine∗1201.381.628.5313.80Methionine#901.121.251.4617.60Tryptophan#951.031.060.2716.80Threonine#1001.041.090.2918.701,3-Butanediol1801.191.281.5912.401-Amino-2-propylalcohol1801.021.020.2412.80Dihydrocarvylacetate1201.121.231.9616.50Ethyllactate2001.081.141.8515.20
* Trifluoroacetyl derivative; # trifluoroacetyl isopropyl ester derivative;T: temperature;k: retention factor;α: separation factor;Rs: resolution;v: the linear velocity of the N2carrier gas.
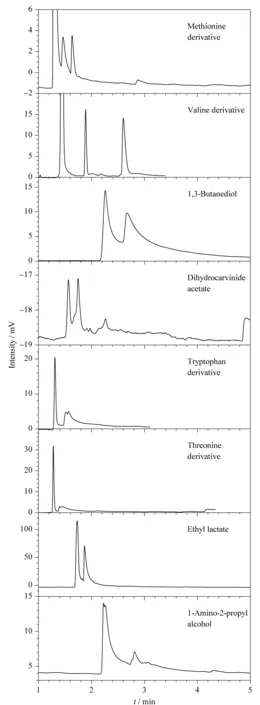
图4 手性化合物在COIMS涂敷柱上的拆分色谱图
2.5 毛细管柱的重现性及稳定性
选取1,3-丁二醇和缬氨酸衍生物作为测试物进行测试,在同一条件下,通过多次进样之后,将使用前和多次进样之后的色谱图进行对比(见图5)。用保留时间计算它们的相对标准偏差(RSD)分别为0.27和0.19,表明该柱的重现性和稳定性较好。
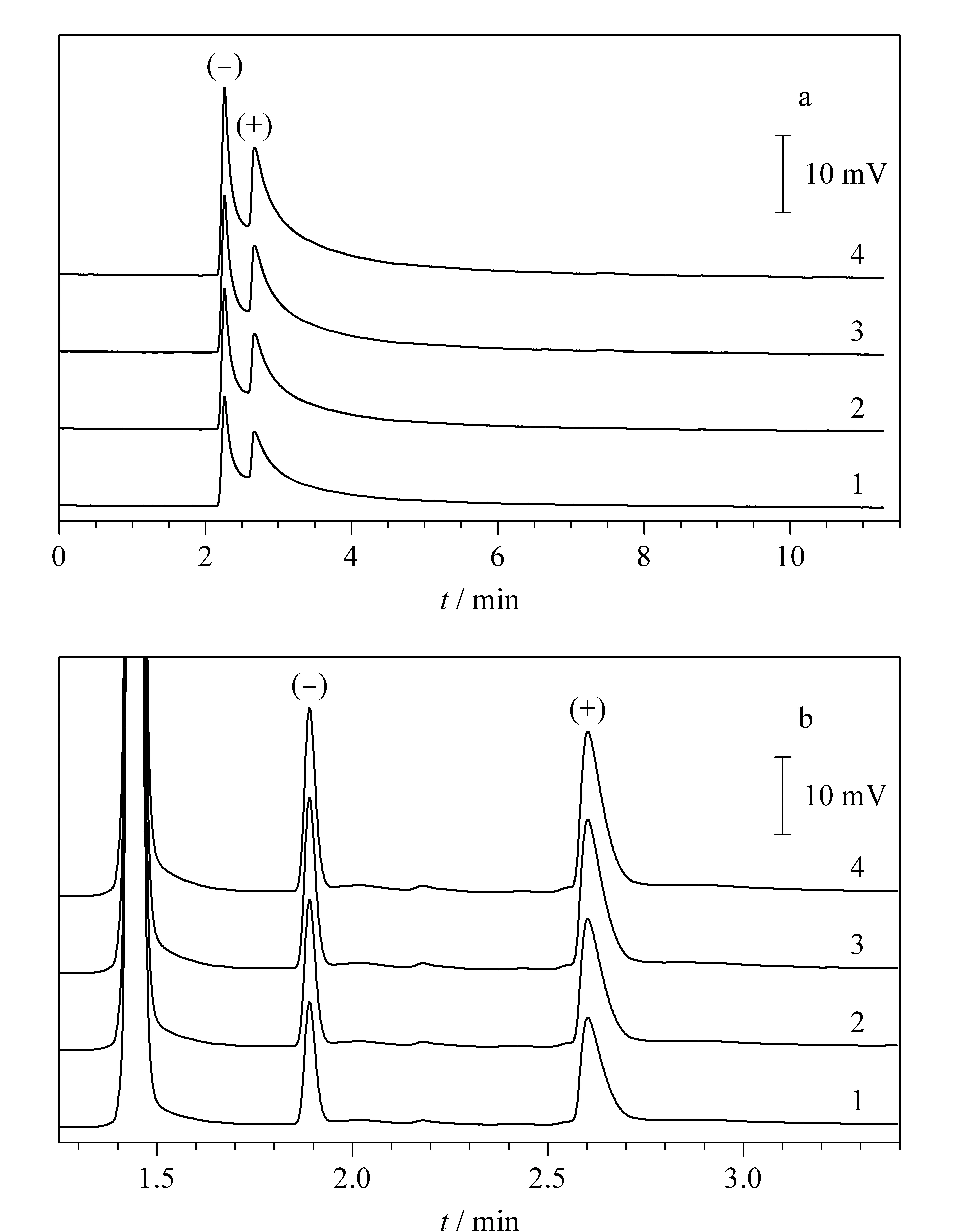
图5 COIMS涂敷柱的重现性色谱图
3 结论
本文以D-苯丙氨酸作为手性源制备一种有序介孔二氧化硅,将其用作气相色谱手性固定相,采用动态涂敷法制备毛细管柱,用其进行手性分离实验。研究结果表明:该手性柱对8种外消旋体具有手性识别能力,得到不同程度的拆分效果。该手性柱还对正构烷烃混合物、正构醇混合物都具有较好的分离能力。由于其具有耐高温的特性,因此具有作为高温手性固定相的潜力。

