曲酸衍生物的生物活性研究进展
刘褚雯,刘进兵
(邵阳学院 食品与化学工程学院,湖南 邵阳 422000)
曲酸是由葡萄糖经曲霉念珠菌在30~32℃下好氧发酵产生的具有抗菌作用的有机酸,分子结构为带取代基的γ-吡喃酮,它是合成具有生物活性曲酸衍生物的重要原料[1]。曲酸具有多种生物活性,如抑制酪氨酸酶活性、抗菌消炎活性、抗肿瘤活性等。曲酸及其衍生物可以用作防止酶促褐变的食品添加剂和皮肤美白的化妆品[2-3];在农业生产领域可作为生物杀虫剂[4]、植物生长调节剂等[5-6]。本文综述了近几年来曲酸及其衍生物的生物活性研究进展。
1 抑制酪氨酸酶活性
酪氨酸酶是黑色素形成过程中的重要酶,是食品酶促褐变的重要因素,为了提高食品品质,开发新型高效、低毒的酪氨酸酶抑制剂是一种重要途径,曲酸及其衍生物是一类重要的酪氨酸酶抑制剂。
2015年Wenlin Xie等[7]发现了一系列的对蘑菇酪氨酸酶有抑制作用的化合物,在这些化合物中,苯环上含卤素取代基的化合物对酪氨酸酶的抑制作用比含甲基、甲氧基和无取代基的化合物强,氯取代化合物的抑制活性强于溴取代化合物,结果表明吸电子基团对抑制酪氨酸酶作用是有利的。特别是化合物1(图1)的IC50值达到(4.50±0.34) μmol/L,是所有化合物中抑制酪氨酸酶活性最强的,作者推测苯环第4位的氯原子有助于提高酪氨酸酶的抑制活性。

图1 化合物1
2016年Wenlin Xie等[8]设计并合成了两个系列具有良好酪氨酸酶抑制活性的新型含曲酸结构的化合物,其IC50值在(1.35±2.15)~(17.50±2.75) μmol/L,比阳性对照曲酸的IC50(20.00±1.08 μmol/L)值小,其中含两个酚羟基的化合物2(图2)表现出最强的酪氨酸酶抑制活性,IC50值为(1.35±2.15) μmol/L。从所合成化合物的构效关系可以确定1,2,4-三唑环上带有苯环取代基类型和位置对酪氨酸酶抑制效果有明显的影响。
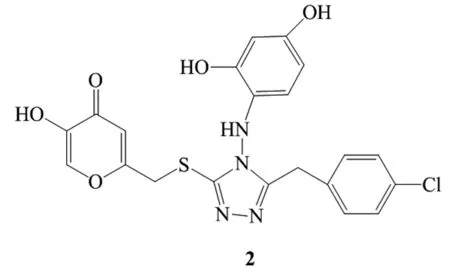
图2 化合物2
2016年Ming-Jen Chen等[9]报道的化合物3(图3)5-羟基-2-{[(1-甲基-1H-咪唑-2-基)硫]甲基}-4H-吡喃-4-酮对单酚酶活性(IC50=0.03 mmol/L)有较强的抑制作用,酚酶活性呈剂量依赖性,对双酚酶活性的抑制作用较小(IC50=1.29 mmol/L),但强于曲酸(IC50=1.80 mmol/L)。文中另一种化合物将化合物3吡喃结构上的羟基变成甲氧基后对酪氨酸酶无活性,作者推测曲酸结构上的5-位烯醇羟基结构对酪氨酸酶抑制有一定的影响。

图3 化合物3
2017年Le-Le Shao等[10]以曲酸为原料合成了一系列含肟醚羟基吡啶酮衍生物,并进行了对蘑菇酪氨酸酶单酚酶的抑制活性测试。结果表明这些化合物的酪氨酸酶抑制活性随着它们的阻断P值的增加而增加,其中4和5(图4)对蘑菇酪氨酸酶单酚酶活性的抑制作用最强,由于它们的高亲脂性,使它们很容易进入酪氨酸酶活性部位的疏水口袋。
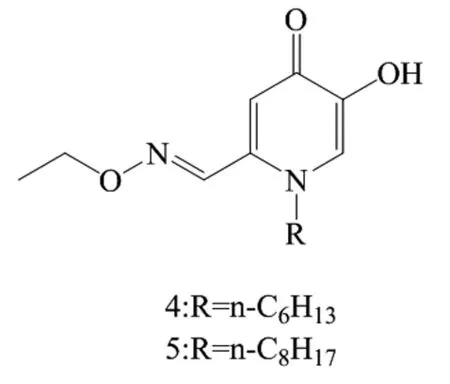
图4 化合物4和5
2019年Yan-Mei Chen等[11-12]合成了具有抑制酪氨酸酶活性的新型的曲酸衍生物,其中化合物6(图5)对二烯醇酶和单酚酶的抑制效果最好,IC50分别为7.50 μmol/L和20.51 μmol/L。通过分子模拟对接的结果得知,化合物6与酪氨酸酶形成氢键,与酶的活性部位更加紧密而且还直接与活性部位的铜离子结合,从而对酪氨酸酶活性位点附近的微环境产生影响来达到控制酪氨酸酶的活性。
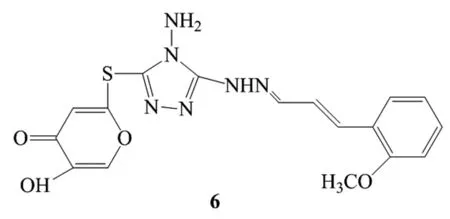
图5 化合物6
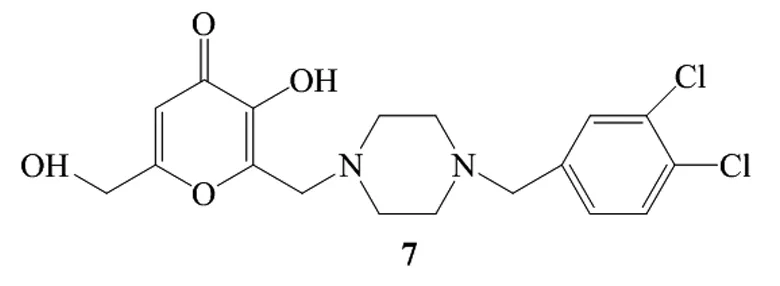
图6 化合物7
2 抗氧化活性
2016年Ming-Jen Chen等[9]化合物3的自由基清除活性(8.83%~55.23%)强于曲酸的自由基清除活性(4.63%~30.04%),且用于DPPH自由基清除活性的化合物3的IC50值为4.09 mmol/L,显著高于用于抑制酪氨酸酶活性的化合物3的IC50值(0.03 mmol/L),从中可能是抗氧化性质部分地助利于抑制酪氨酸酶活性。
2018年Liu Xiaoli等[14]合成了水溶性壳寡糖-N-曲酸聚合物(COS-N-KA),然后对其进行了抗氧化活性评价。由于COS的活性氨基酸和KA的5-羟基吡喃酮在COS-N-KA骨架中的存在,在自由基清除反应中可能充当电子供体,与自由基相结合,表现出对DPPH自由基的强烈抑制作用。
2019年Yan-Mei Chen等[12]合成的化合物6,抗氧化能力测试结果表明:该类化合物具有较好的降低自由基能力,DPPH的IC50为227.80 μg/mL,ABTS+的IC50为126.63 μg/mL,抗氧化活性优于对照曲酸,但比抗坏血酸弱。
3 抗菌活性
2014年Warren Andrew Andayi等[15]合成了氨基氯喹啉-曲酸杂化物,对恶性疟原虫耐药株(K1)和敏感株(3D7)进行了B-血红素抑制和抗疟原虫活性评价,文中得出对3D7菌株的抗疟原虫活性随亲脂性的增加而增加。化合物8(图7)在两株(IC503D7=0.004 μm;IC50K1=0.03 μm)中均为最强化合物,对B-血红素的抑制活性最好。
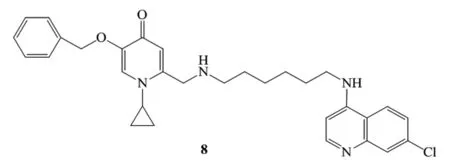
图7 化合物8
2010年Mutlu Dilsiz Aytemir等[16]报道了一系列6-氯甲基-3-羟基-2-取代-4氢-吡喃-4-酮衍生物,并测试了它们的抗菌和抗病毒活性。当浓度为1~2 mg/mL时,部分化合物对枯草芽孢杆菌和金黄色葡萄球菌活性有抑制作用,另外部分化合物表现出对大肠杆菌、铜绿假单胞菌、肺炎克雷伯菌和鲍曼不动杆菌的活性有显著的抑制作用。此外,当浓度为4~8 mg/mL时,大部分化合物对抗白色念珠菌和准西洛念珠菌也有明显效果。
2015年Chiranjeevi Bingi等[17]对所合成的化合物进行了抗菌和抗生物膜活性评价。其中有对金黄色葡萄球菌、枯草芽孢杆菌和大肠杆菌有很强的抗菌活性的化合物,有对枯草芽孢杆菌和大肠杆菌、对枯草芽孢杆菌和大肠杆菌有很好的抑制作用的化合物。
2017年Mahnaz Saraei等[18]合成了两种新型含曲酸结构的丙烯酸酯单体,化合物[5-(苄氧基)-4-氧-4H-吡喃-2-基]丙烯酸甲酯、5-(苄氧基)-2-{[4-(羟甲基)-1,2,3-三唑-1-基]甲基}-4H-吡喃-4-酮和{1-[(5-(苯氧基)-4-氧代-4H-吡喃-2-基)甲基]-1,2,3-三唑-4-基}丙烯酸甲酯具有良好或显著的抗真菌活性,抑菌区约为9.6~17 mm。这些化合物对抑菌区为8~9 mm的革兰氏阳性菌具有中等的抗菌活性。
2019年Xin-Rui Wang等[19]报道的在Zn-Ti层状双氢氧化物中的插入曲酸的新型纳米杂化物对大肠杆菌、铜绿假单胞菌和金黄色葡萄球菌有较强的抗菌活性。
4 抗炎、抗癌和抗肿瘤活性
2010年Dae Sung Yoo等[20]研究几种新合成的曲酸衍生物,一种化合物具有抗炎、抗增殖和抗氧化特性,能够调节胶质瘤细胞增殖和Toll样受体(TLR)4介导的巨噬细胞活化的肿瘤微环境的功能激活。在所测试的各种衍生物中,化合物9(图8)对C6胶质瘤细胞的增殖抑制作用最强,IC50值为4.7 μmol/L。

图8 化合物9
2016年Miri Lee等[21]研究合成了曲酸与对香豆酸的酯衍生物5-羟基-4-氧代-4h-吡喃-2-基-甲基(e)-3-(3-羟基苯基)丙烯酸酯(化合物10)(图9),并评价了对脂多糖(LPS)刺激的RAW264.7巨噬细胞中抗炎活性。研究表明化合物3在浓度为100 μmol/L时抑制率为60%。而当浓度为25 μmol/L时,化合物10对NF-κB的激活抑制作用约为32% μm,优于曲酸和香豆素。
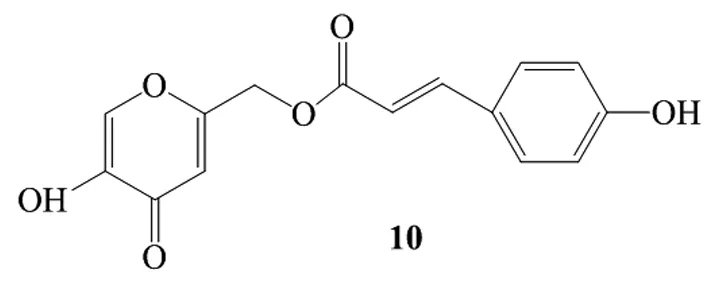
图9 化合物10
2019年Gulsah Karakaya等[22]报道了一系列在抑制A375细胞的细胞毒性方面比KA、CKA、ALM更具有明显效果的曲酸曼尼希碱衍生物,且大多数化合物具有干扰癌细胞增殖的能力,而对健康细胞没有损害,如含有3,4-二氯苄基(化合物11和13)和2,6-二氯苄基(化合物12)(图10)R′基团的化合物明显地显示了这种性质。

图10 化合物11、12和13
2018年Samer Hasan Hussein-Al-Ali等[23]合成的Kj-CH-MNPs 和Kj-PG-MNPs纳米复合型材料,评价了其对皮肤癌细胞(B16-F10黑色素瘤细胞)和正常皮肤细胞(人真皮成纤维细胞鼠)的潜在细胞毒性。当浓度达到50 μg/mL时,游离曲酸的细胞活力曲线不低于50%,而Kj-CH-MNPs和Kj-PG-MNPs纳米复合材料的细胞活力曲线随着浓度的增加而迅速下降。在50 μg/mL浓度下观察到Kj-CH-MnPS和Kj-PG-MnPS纳米复合材料的最大抑制效果,分别显示细胞存活率分别为49.4%和39.2%,IC50分别为47.1 μg/mL和8.4 μg/mL。通过比较曲酸、Kj-CH-MNPs、Kj-PG-MNPs纳米复合材料在66%细胞活力点的浓度值,可以确定纳米材料能降低剂量水平。曲酸在50 μg/mL剂量下显示66%的细胞活力,而Kj-CH-MNPs和Kj-PG-MNPs纳米复合物分别为3.125 μg/mL和1.562 μg/mL以下。
2019年Selin Oncul等[24]研究了曲酸及其10种不同衍生物在肝癌株HEPG2中的抗肿瘤作用,SRB活力测定结果显示,10个衍生物中7个能够在100 μmol/L的IC50浓度下减少HEPG2细胞增殖,这是KA不能达到的效果。化合物14(IC50=37.18 μmol/L)和化合物15(IC50=32.68 μmol/L)(图11)的IC50值最低。化合物14被证明是治疗肝癌细胞的替代剂,它通过增加细胞内ROS浓度而触发固有的p53凋亡途径。
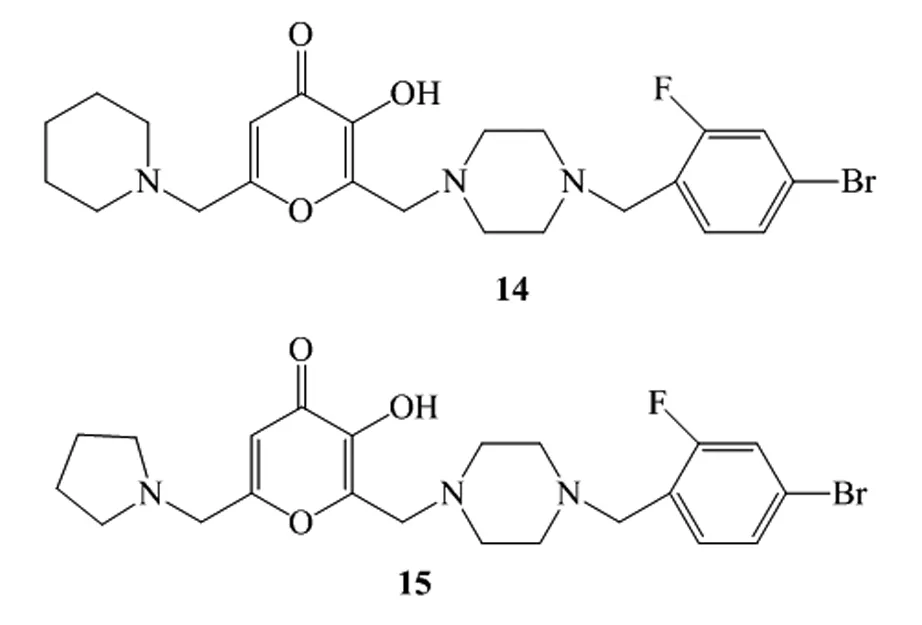
图11 化合物14和15
5 展望
综上所述,曲酸衍生物的曲酸骨架上的吡喃结构2-位甲羟基取代基不同,对酪氨酸酶抑制效果不同,其取代基中有卤素苄氧基一般为有助于酪氨酸酶的抑制。经过对曲酸结构的修饰,与其它具有生物活性的化合物相结合,合成出综合了具有曲酸生物活性和另外一种化合物生物活性的曲酸衍生物,是广大研究者的一个合成思路。根据上述表达,发现曲酸衍生物的抑制酪氨酸酶活性,抗菌性、抗氧化活性、细胞无毒性为我们使其在医药、食品、化妆品等领域广泛运用提供了理论依据。

