一种新型阿莫西林-丙磺舒拼合物在小鼠体内的药代动力学
李 晗,李艳芹,李仲林,陈良柱,方炳虎,*
(1.华南农业大学 兽医学院,广东 广州 510642 ;2.广东温氏大华农生物科技有限公司,广东 云浮 527300)
阿莫西林(amoxicillin,AMO)是一种半合成青霉素类抗生素,兽医临床主要用于尿道、呼吸道、皮肤感染等疾病的治疗。阿莫西林属于时间依赖性药物,但因其在动物体内半衰期短,其在临床应用中需要多次给药。肉鸡内服给药15 mg/kg剂量阿莫西林[1],其消除半衰期为1.8 h,Tmax为0.47 h,Cmax为2.29 mg/L。为减少青霉素类药物在临床使用中的给药次数,开发长效缓释的青霉素类药物成为了新型青霉素药物的研究热点。
丙磺舒(probenecid,PB)又名羧苯磺胺,是苯甲酸的一种衍生物。丙磺舒在体内主要通过肾近曲小管的主动分泌来排泄,又因其脂溶性大,容易被再吸收,故其在体内排泄缓慢。研究表明[2-5],丙磺舒与青霉素类药物联合使用能抑制青霉素类药物在肾小管的排泄,延长青霉素药物的半衰期及其体内作用时间。丙磺舒还会抑制阿莫西林在肝脏和肾脏中的分布[6]。
药物拼合是将2种药物或它们的衍生物通过化学键合的方式形成具有多结合靶点或多重作用机制的药物。药物拼合的方式包括2种:一种是将具有不同作用机制的抗菌药物通过化学键连接,药物在体内被特定酶水解再释放出原化合物而发挥双重抗菌作用(dual-action)[7];一种是将具有不同作用靶点的药物通过化学键连接,这种键合方式不会被体内酶水解,形成的新的杂合分子或杂合药物可作为整体与病原的不同靶标结合发挥其多靶点抗菌作用[8]。被拼合的不同药物在体内药代动力学性质上的差异还可改善其药代动力学性质及降低毒副作用等[7,9]。药物拼合原理的出现大大缩短了新药研发的速度。课题组参考舒他西林[10-11]的合成路线,将丙磺舒和阿莫西林以亚甲基桥连接形成双酯结构,成功合成出一种新型阿莫西林-丙磺舒拼合物(amoxicillin-probenecid twin drug,命名为AB),并对其进行了结构确证及含量检测。拼合物相对分子质量为663.21,为淡黄色固体粉末,易溶于甲醇,微溶于水。
对拼合物进行的的体外模拟代谢试验表明,其能在小肠酯酶的作用下完全分解成阿莫西林和丙磺舒。本试验以阿莫西林、阿莫西林/丙磺舒联合用药为对照,研究阿莫西林-丙磺舒拼合物在小鼠体内的比较药代动力学,为阿莫西林-丙磺舒拼合物的进一步开发应用提供理论基础。
1 材料与方法
1.1 药品与试剂阿莫西林(先秦药业,含量为99.6%);丙磺舒(北京普博欣生物科技有限责任公司生产,含量98.0%);阿莫西林-丙磺舒拼合物(华南农业大学兽医学院兽医药理教研室合成,经前期研究结构确证与含量分析,含量为93.19%);甲醇、甲酸、乙腈均为色谱纯(美国Thermo Fisher公司);磷酸二氢钾、磷酸氢二钾、乙酸乙酯、正己烷均为分析纯(广州化学试剂厂);试验用水由Milli-Q超纯水系统提供。
1.2 主要仪器超高效液相色谱串联质谱仪(UPLC-MS/MS),配有Agilent 1290型液相色谱系统(美国Agilent公司)、AB Triple QuadTM 4500型三重四极杆质谱仪(美国Sciex公司)及Analyst 1.6.3软件(美国应用生物系统公司)。MS 3 basic型多功能振荡器,德国 IKA 公司。Thermo Multifuge X1R型台式高速冷冻离心机,赛默飞世尔科技(中国)有限公司。
1.3 标准储备液的制备
1.3.1阿莫西林标准储备液 精密称取阿莫西林标准品20.08 mg,用超纯水溶解,定容至10 mL,得到质量浓度为 2 g/L的阿莫西林标准溶液。标准储备液于4℃冰箱保存。
1.3.2拼合物溶液 精密称取拼合物71.90 mg,以色谱甲醇溶解,定容至20 mL,得到质量浓度为3.35 g/L 的溶液,现配现用。
1.4 试验动物昆明小鼠(合格证号SYXK(粤)2018-0087),体质量18~22 g,广东省实验动物中心提供。试验前禁食12 h,正常供应饮水。
1.5 UPLC-MS/MS条件
1.5.1液相条件 色谱柱:Luna C18(2)100A(150 mm×2 mm,5 μm);流动相:0.1%甲酸水溶液(A)和乙腈(B);流速为300 μL/min;柱温为40℃;进样量为5 μL,梯度洗脱程序如表1所示。

表1 阿莫西林梯度洗脱程序
1.5.2质谱条件 采用电喷雾离子源(ESI),正离子扫描,多反应监测(MRM)模式对阿莫西林进行定量分析。电喷雾电压(IS)为 5 500 V,离子源温度(TEM)为 500℃,雾化气压力(GS1)为 60 Pa,辅助气流速(GS2)为 60 L/min,气帘气压力(CUR)为 30 Pa,碰撞室压力为(CAD)6 Pa。MRM参数见表2。

表2 阿莫西林及丙磺舒的质谱参数
注:*代表定量离子
1.6 样品前处理方法取100 μL小鼠血浆样品,加入200 μL色谱乙腈,涡旋1 min,10 000 r/min 离心10 min,取上清 150 μL加入 350 μL纯水稀释,混匀,过0.22 μm滤膜,待测。
1.7 方法学评价
1.7.1标准曲线与检测限、定量限 采用空白基质添加法。取空白小鼠血浆按照1.6的方法处理,将阿莫西林储备液稀释,添加至空白基质中,稀释为1,2,5,10,20,50,100,200,500 μg/L的样品,上机检测,以药物峰面积为纵坐标(Y),药物浓度为横坐标(X),对其进行线性回归分析,求标准曲线回归方程及相关系数。在此检测条件下,信噪比S/N≥3定为检测限,信噪比S/N≥10定为定量限。
1.7.2回收率与精密度 将一定质量浓度的阿莫西林标准储备液添加到空白血浆,配制成5,25,500 μg/L 的样品,每个质量浓度5个重复,按照1.6的方法处理后上机,同时制备空白基质添加样品,采用单点定量法进行分析,求得相对回收率。
将阿莫西林标准储备液添加到空白血浆配制成5,25,500 μg/L的样品,每个质量浓度5个重复,连续做3个批次,按照1.6的方法处理上机,计算日内精密度及日间精密度。
1.8 动物试验将体质量为18~22 g的昆明小鼠随机分为3组,每组各72只,将受试样品及参比试剂分别按照药物含量换算给药量,实际给药量均为阿莫西林20 mg/kg,给药方式为灌胃给药。20 mg/kg剂量的阿莫西林,20 mg/kg+13.60 mg/kg剂量的阿莫西林/丙磺舒联合用药(A+B,MA∶MB=1∶1)以及33.36 mg/kg剂量的阿莫西林拼合物(AB)。在给药后0.083 ,0.166,0.25,0.5,0.75,1,1.5,2,3,4,6,8 h进行小鼠眼球摘除采血,每个时间点6个平行。样品采集完,将离心得到的血浆置于-80℃冰箱保存,待测。
1.9 数据处理将试验得到的血浆样品按照1.6中的方法处理分析,得到小鼠血浆中的药物质量浓度。采用winNonlin(Version5.2.1) 软件的非房室模型对药物浓度-时间数据进行拟合并计算药动学参数。
2 结果
2.1 标准曲线在1.5的检测条件下,阿莫西林在谱图上能够呈现较好的峰形(图1)。阿莫西林的标准曲线为:Y=45.7X+390.41,(R2=0.9983)(图2)。检测限为0.05 μg/L,定量限为1 μg/L。
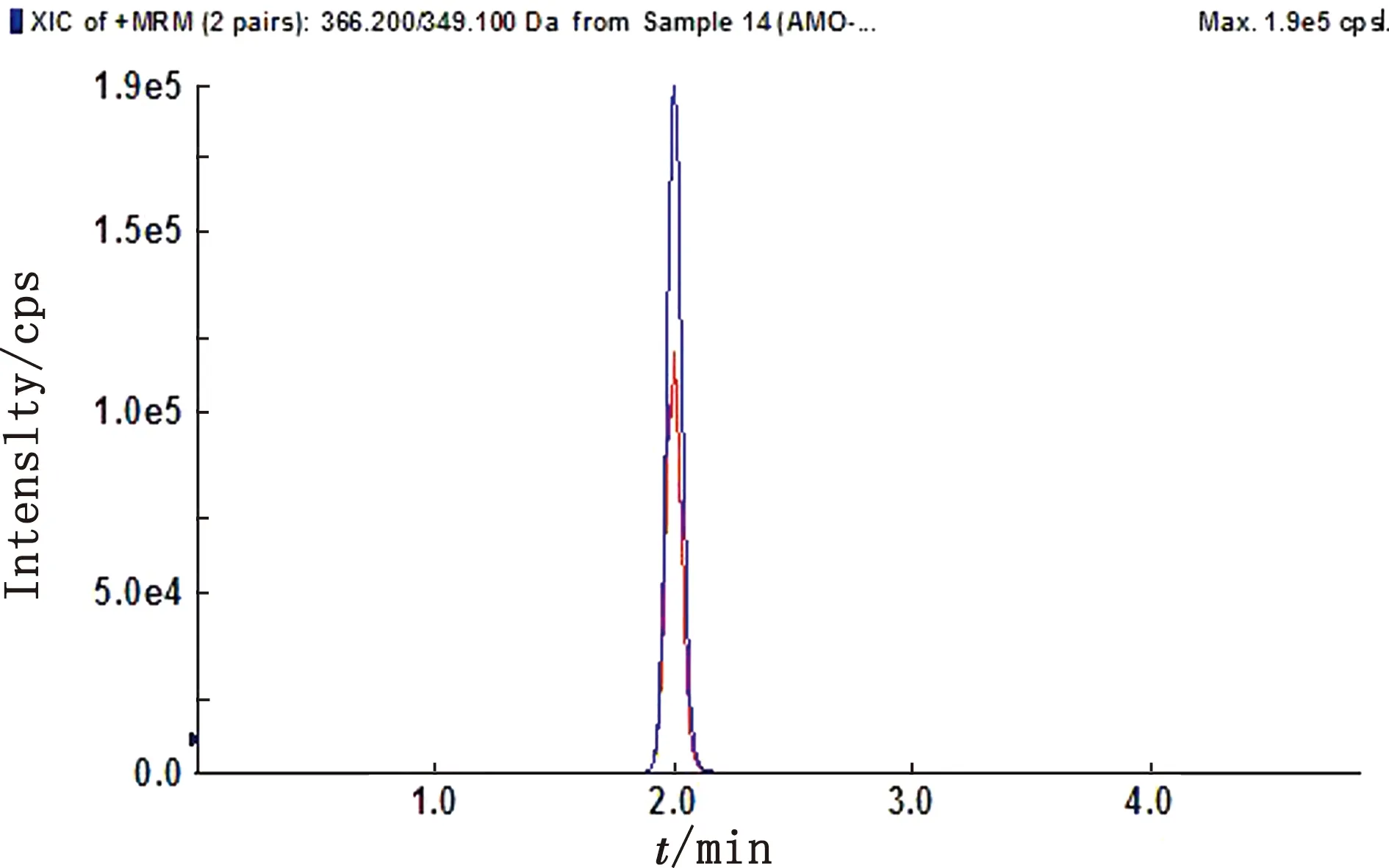
图1 基质加阿莫西林标准液液相-质谱图 图2 阿莫西林标准曲线
2.2 回收率与精密度血浆中阿莫西林添加质量浓度为5,50,500 μg/L时,其平均回收率介于85.32%~97.54%之间,批内精密度介于2.60%~6.09% 之间,批间精密度介于4.81%~7.25%之间,详见表3。表明方法具有较好的回收率和精密度,满足定量分析要求。
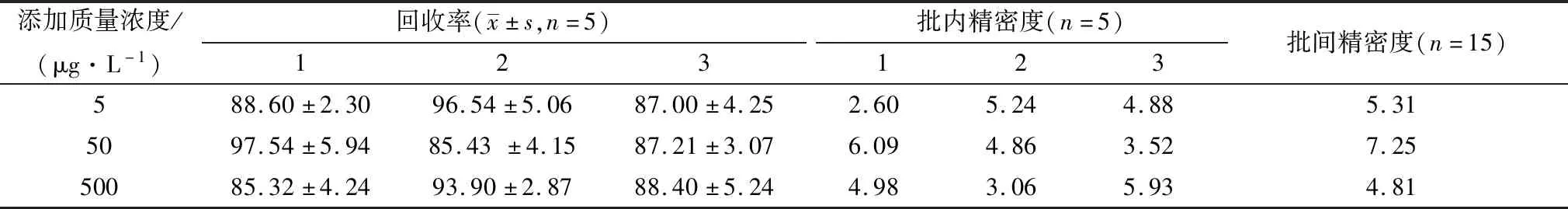
表3 阿莫西林小鼠血浆中的回收率与精密度 %
2.3 阿莫西林(AMO)、阿莫西林/丙磺舒联合用药(A+B)及阿莫西林-丙磺舒拼合物(AB)在小鼠体内药代动力学特征按照 20 mg/kg阿莫西林的有效剂量,分别灌胃给药阿莫西林(AMO)、阿莫西林/丙磺舒(A+B,MA∶MB=1∶1)、以及阿莫西林-丙磺舒拼合物(AB)后,小鼠体内阿莫西林的血药浓度-时间曲线见图3。用药动学软件winNonlin5.2.1的非房室模型对数据进行拟合,其中,阿莫西林-丙磺舒拼合物较联合用药(阿莫西林/丙磺舒)的相对生物利用度(以阿莫西林计)为110.35%。具体药代动力学参数见表4。
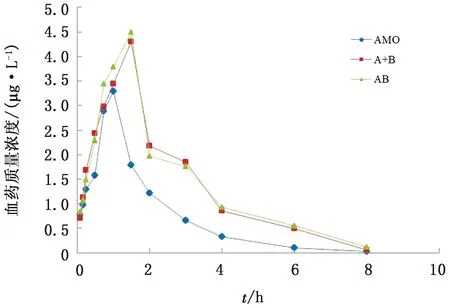
图3 小鼠灌等剂量阿莫西林(20 mg/kg)下,阿莫西林(AMO)、阿莫西林/丙磺舒(A+B)和拼合物(AB)血浆中阿莫西林的药物浓度-时间曲线图
3 讨论
3.1 拼合物与阿莫西林单药的药代动力学比较从表3中数据看出,该研究中所用阿莫西林-丙磺舒拼合物(AB)的达峰浓度(以阿莫西林计)较高,与阿莫西林单药差异显著(P<0.01),说明拼合物在小鼠体内吸收较好;其次拼合物与阿莫西林的消除半衰期(t1 /2ke)分别为(1.77±0.23 ),(1.04±0.21) h,MRTlast分别为(2.64±0.24),(1.81±0.11) h,均差异显著(P<0.01),说明拼合物在小鼠体内消除更慢,驻留时间更长;同时拼合物的AUClast远高于阿莫西林单药,其生物利用度是阿莫西林的198.09%,表明拼合物AB在小鼠体内生物利用度更高。分析原因可能是拼合物在体内慢慢分解为阿莫西林和丙磺舒,丙磺舒通过提高机体对阿莫西林的吸收[12],提高了Cmax和AUClast;同时,丙磺舒对阿莫西林在肾小管分泌过程中存在竞争性抑制[12-13],导致分解出的阿莫西林在小鼠体内消除缓慢,t1 /2ke和MRTlast显著延长。

表4 小鼠灌服等剂量阿莫西林(20 mg/kg)下,阿莫西林单药(AMO)、阿莫西林/丙磺舒(A+B)和拼合物(AB)血浆中阿莫西林的主要药代动力学参数
注:*a,**a表示拼合物与阿莫西林的药代动力参数比较的t检验结果; *b,**b表示拼合物与阿莫西林/丙磺舒的药动参数比较的t检验结果,P<0.01差异极显著(**),0.01
3.2 拼合物与阿莫西林/丙磺舒联用药(A+B)的药代动力学比较由表3可知,拼合物(AB)在小鼠体内的(按阿莫西林计)消除半衰期t1 /2ke为(1.77±0.23) h,AUClast为(11.41±0.75) mg·h/L,比阿莫西林/丙磺舒联合用药(A+B)的t1 /2ke(1.49±0.50) h、AUClast(10.34±0.94 )mg·h/L 显著增加(0.01
本试验对比了阿莫西林林-丙磺舒拼合物、阿莫西林及阿莫西林/丙磺舒联合用药在小鼠体内的药代动力学,试验结果进一步验证了阿莫西林-丙磺舒拼合物在体内可以在酯酶作用下水解成丙磺舒和阿莫西林而共同发挥药效,可充分发挥丙磺舒对阿莫西林的增效作用,显著增加阿莫西林的生物利用度,延长阿莫西林在体内的作用时间,且与联合用药相比更加长效。这为阿莫西林-丙磺舒拼合物的进一步开发应用提供了坚实的理论基础,也为开发新型青霉素类药物提供了新的思路。

