基于线粒体自噬探讨参苓白术散对COPD骨骼肌损伤细胞的保护作用机制
周晓芸,宋雨鸿,薛丹,张丽华,胡涛
(广州医科大学附属市一人民医院,广东 广州 510180)
慢性阻塞性肺部疾病(chronic obstructive pulmonary disease,COPD)的发生与肺部对香烟烟雾(CSE)等有害气体或有害颗粒的异常炎症反应有关[1]。CSE刺激细胞可释放大量活性氧(reactive oxygen species,ROS),引起氧化/抗氧化失衡,导致线粒体的结构和形态改变,使线粒体中受损的蛋白质、DNA 和脂质等含量显著增加,线粒体能量代谢障碍[2-3]。越来越多研究[4]发现线粒体自噬在维持线粒体结构和功能方面具有重要作用。线粒体自噬通过选择性的清除功能障碍的线粒体,降低细胞内ROS水平,维持线粒体的动态和能量代谢平衡,从而下调细胞的凋亡或坏死[5]。骨骼肌是线粒体能量代谢的重要器官,COPD的发生过程中,线粒体动态平衡受到破坏,从而引起骨骼肌功能障碍[6]。中医学认为COPD骨骼肌疲劳的关键病机是“脾虚 (痰)湿盛”。参苓白术散为培土生金的代表方,具有益气健脾功效,临床研究[7-9]发现参苓白术散对治疗COPD 呼吸疲劳有较好的临床疗效,可改善肌肉能量代谢,提高患者生活质量,且降低急性加重次数,但其相关作用机制目前尚不清楚。本文拟采用CSE处理L6大鼠成肌细胞模拟COPD骨骼肌损伤状态,探讨在参苓白术散作用下PINK1/Parkin介导的线粒体自噬对保护COPD骨骼肌细胞的可能作用机制。
1 材料和方法
1.1 材料
L6大鼠成肌细胞(中国科学院细胞库),DMEM 培养基(美国ThermoFisher公司),胎牛血清(美国 Gibco 公司),BCA 蛋白定量试剂盒(美国 Sigma 公司),PINK1、Parkin、LC3B、P62等多克隆抗体(美国 Cell Signaling 公司),抗兔、抗鼠IgG(美国 Cell Signaling 公司),活性氧检测试剂盒、JC-1 线粒体膜电位荧光探针试剂盒、ATP检测试剂盒(均为碧云天试剂公司)。参苓白术散(莲子肉10 g,薏苡仁10 g,砂仁10 g,桔梗10 g,白扁豆15 g,白茯苓20 g,党参20 g,炙甘草20 g,白术20 g,山药20 g),购自康美智慧药房,经广州中医药大学中药中心鉴定合格,采用常规方法煎煮,浓缩后制成冻干粉,放置 -20 ℃冰箱保存备用。酶标仪((美国 Bio-RAD 公司),电泳及转膜装置(美国 Bio-RAD 公司),CO2恒温培养孵箱(美国 Thermo 公司)。
1.2 方法
1.2.1 细胞培养 将L6大鼠成肌细胞置于 37 ℃、50 mL/L CO2培养孵箱中,用DMEM 培养基(5.5 mmol /L 葡萄糖) 培养,每2~3天换液 1 次,待细胞贴壁生长一段时间,光镜下观察其融合度在 75%~85%左右,即可进行种板、传代、冻存等操作。
1.2.2 香烟提取物CSE的制备[10]用市售的过滤嘴香烟(大前门牌香烟,中国上海烟草有限公司)。每次用1支香烟,三通管一头接 50 mL 注射器上,将滤嘴插入 1 mL 移液吸头内,吸头另一端连接在三通管另一头上,形成一个驱动抽吸装置。每次抽取 50 mL 香烟烟雾,将吸入的烟雾通入10 mL DMEM 基础培养基中,形成香烟雾悬液,上下反复摇动注射器 100 次,使烟雾溶解至培养基内,将剩余烟雾排出。上述过程重复 6 次,混匀后用 1 mol/L NaOH 溶液滴定至 pH 7.4 左右,经无菌 0.22 μm微孔过滤装置过滤后备用。
1.2.3 参苓白术散溶液配制 取参苓白术散冻干粉0.5 g(采用常规方法煎煮,浓缩后制成冻干粉),溶于5 mL DMEM基础培养基混匀后形成 100 mg/mL的母液,超声震荡仪 5 min,吸取至注射器针管中,用 0.22 μm过滤器过滤后 1 h 内使用。
1.2.4 实验分组 将L6大鼠成肌细胞随机分为5个组:①control组:用DMEM培养基培养L6大鼠成肌细胞,不作任何处理。②CSE模型组:用含有2.5%CSE的DMEM培养基培养L6大鼠成肌细胞的24 h后换正常DEME培养液继续培养。③SLB-L组:用含有2.5%CSE的DMEM培养基培养L6大鼠成肌细胞,24 h后换含有2.5 mg/mL参苓白术散药液的DMEM培养基继续培养24 h。④SLB-M组:用含有2.5%CSE的DMEM培养基培养L6大鼠成肌细胞,24 h后换含有5 mg/mL参苓白术散药液的DMEM培养基继续培养24 h。⑤SLB-H组:用含有2.5%CSE的DMEM培养基培养L6大鼠成肌细胞,24 h后换含有10 mg/mL参苓白术散药液的DMEM培养基继续培养24 h。
1.2.5 荧光酶标仪检测细胞内的ROS 将各分组的细胞收集后悬浮于稀释好的DCFH-DA中,细胞1×106个/m2,37 ℃细胞培养箱内孵育20 min。用无血清细胞培养液洗涤细胞3次,以充分去除未进入细胞内的DCFH-DA。在荧光酶标仪上使用488 nm激发波长,525 nm发射波长,检测各组细胞的ROS含量。
1.2.6 ATP检测试剂盒检测细胞内线粒体的ATP水平 按实验分组分别处理后,吸除培养液,6孔板每孔加入200 uL裂解液裂解细胞。裂解后4 ℃ 12 000g离心5 min,取上清,冰浴上溶解待用试剂,把ATP标准溶液用ATP检测裂解液稀释成适当的浓度梯度,按照说明配置 ATP检测工作液。取96孔黑板,每孔加100 μL ATP检测工作液,在检测孔内加上80 μL样品或标准品,用luminometer测定RLU值。
1.2.7 JC-1染色试剂盒检测L6大鼠成肌细胞内线粒体膜电位水平 制备L6大鼠成肌细胞悬液,调整细胞密度为5×105个/mL置于流式细胞管。按实验分组分别处理后,按照说明配置 JC-1 染色工作液。流式管中加入0.5 mL 细胞培养液及0.5 mL JC-1 工作液,充分混匀。37 ℃ 避光孵育20 min,600g4 ℃离心3~4 min,沉淀细胞,弃上清。预冷的 JC-1 染色缓冲液(1×)洗涤2次,弃之,加入1 mL JC-1染色缓冲液(1×)重悬后,流式细胞仪检测及记录,Cellquest Pro 软件分析处理数据。
1.2.8 蛋白质印迹法检测各蛋白的表达水平 按实验分组分别处理后,加入细胞裂解液后提取蛋白。以 BCA 法测定蛋白浓度。配置 SDS-聚丙烯酰胺凝胶。组装电泳转膜装置,上样,电泳,转膜,将蛋白转移至聚偏氟乙烯(PVDF) 膜上。脱脂奶粉封闭孵育 1 h。各条带分别孵育兔抗 PINK1 抗体、兔抗LC3B 抗体、兔抗P62抗体、鼠抗Parkin 抗体、鼠抗β-actin 抗体(稀释比例均为1∶1 000,4 ℃ 孵育过夜)。1∶2 000比例稀释抗兔IgG 孵育 1 h。其中需要清洗的步骤均可用 TBST 清洗 3 次。用化学发光法检测目的条带,以β-actin 为内参标化各蛋白表达的水平。
1.3 统计学处理
2 结果
2.1 参苓白术散对CSE诱导的L6大鼠成肌细胞内的ROS水平的影响
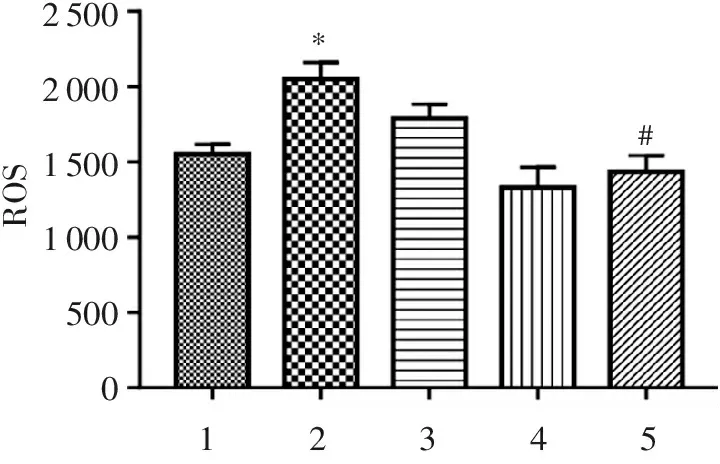
结果显示,与control组相比,CSE模型组细胞内ROS水平上升(P<0.05);与CSE模型组比较,中药组各组细胞内ROS水平下降,其中SLB-M、SLB-H组(P<0.05)具有统计学意义。见图1。
1234525002000150010005000ROS*#
1. control; 2. 2.5%CSE; 3.SLB-L; 4.SLB-M; 5.SLB-H(下图同)。 与正常组相比:*P<0.05; 与模型组相比:#P<0.05。
图1不同浓度SLB对CSE诱导的L6细胞内的ROS水平的影响
Figure1Effect of different SLB concentrations on ROS level in CSE-induced L6 cells
2.2 各组细胞的线粒体ATP水平的检测
结果显示,与control组相比,CSE模型组线粒体膜ATP水平下降(P<0.05),与CSE模型组比较,SLB-M组细胞ATP水平上升(P<0.05)。见图2。

151050ATP*#12345
与正常组相比:*P<0.05; 与模型组相比:#P<0.05。
图2不同浓度SLB对CSE诱导的L6细胞的线粒体ATP水平的影响
Figure2Effect of different SLB concentrations on mitochon-drial ATP levels in CSE-induced L6 cells
2.3 各组细胞内线粒体膜电位变化的 JC-1检测
结果显示,与control组相比,CSE组线粒体膜电位水平下降(P<0.05),SLB-H组细胞内线粒体膜电位下降(P<0.05); 与 CSE模型组比较,SLB-L、SLB-M组细胞线粒体膜电位水平上升(P<0.05)。见图3。
2.4 参苓白术散对CSE诱导的L6大鼠成肌细胞线粒体自噬相关蛋白表达水平的影响
采用 Western blot 法检测各组细胞中蛋白表达水平结果显示,与control组比较,CSE模型组LC3B、p62、PINK1蛋白表达水平升高(P<0.05),Parkin表达水平下降(P<0.05),各中药组LC3B蛋白表达均升高(P<0.05); SLB-L组PINK1蛋白表达水平明显升高(P<0.05) ; 与CSE模型组比较,SLB-M、SLB-H组LC3B、Parkin蛋白水平显著升高(P<0.05),而各中药组p62蛋白表达水平下降(P<0.05),SLB-H组PINK1蛋白表达下降(P<0.05)。见图4。

与正常组相比:*P<0.05; 与模型组相比:#P<0.05。
图3不同浓度SLB对CSE诱导的L6细胞的线粒体膜电位的影响
Figure3Effect of different SLB concentrations on mitochondrial membrane potential in CSE-induced L6 cells

LC3Bp62Pink1Parkinβ-actin160001400052000600006600042000123453.02.01.00.02.01.51.00.50.0LC3B/β-actinParkin/β-actinP62/β-actinPink1/β-actin3.02.01.00.01.51.00.50.0123451234512345*#**#**###*##**#
与正常组相比:*P<0.05; 与模型组相比:#P<0.05。
图4不同浓度SLB对CSE诱导的L6大鼠成肌细胞线粒体自噬相关蛋白LC3B、PINK1、Parkin、P62 蛋白表达
Figure4Effect of different SLB concentrations on the expression of LC3B,PINK1,Parkin and p62 in CSE-induced L6 cells
3 讨论
COPD患者由于通气功能障碍,呼吸阻力升高,耗能增加,使呼吸肌长期超负荷运动,导致呼吸肌顺应性下降、肌力和耐力显著降低[11]。呼吸肌属于横纹肌的范畴,从胚胎学与形态学的角度分属于骨骼肌。研究表明,持续性的呼吸肌功能障碍会引起骨骼肌损伤,骨骼肌损伤是呼吸衰竭发生的重要原因之一[12]。香烟烟雾包含较高浓度的自由基和氧化产物,可刺激机体产生大量的ROS 导致氧化应激,破坏体内的氧化平衡[13]。有研究显示,COPD患者骨骼肌组织的氧化应激明显增加,且发现氧化应激的增加与其活动能力和活动耐力呈负相关[14]。本实验研究发现CSE模型L6大鼠成肌细胞内的ROS含量增加,采用参苓白术散药剂干预治疗后,明显降低细胞内的ROS含量,表明参苓白术散可能是通过调节COPD骨骼肌损伤状态下细胞内氧化/抗氧化系统的平衡,使细胞清除ROS的能力增加,阻断或消除ROS对骨骼肌细胞的过氧化损伤。
线粒体膜电位的稳定是维持线粒体ATP合成和氧化磷酸化的重要条件之一。近年来研究发现,线粒体膜电位是观察细胞早期凋亡以及线粒体膜流动性和通透性功能的直接指标[15]。线粒体膜电位下降可引起线粒体内膜通透性增加,蓄积的Ca2+释放入细胞质,引起电子泄露,产生更多的ROS,使线粒体功能出现障碍,合成的ATP减少,能量代谢失衡,从而引起细胞凋亡甚至坏死[16-17]。本研究结果显示,CSE诱导的L6大鼠成肌细胞线粒体膜电位水平及ATP合成水平显著下降,而参苓白术散组线粒体膜电位水平及ATP水平较CSE模型组均明显升高,提示参苓白术散可通过调节COPD骨骼肌损伤状态下细胞线粒体的能量代谢平衡来维持细胞氧化/抗氧化系统的平衡,在细胞凋亡早期抑制线粒体膜电位的下降,改善线粒体膜的通透性,维持ATP的合成,从而清除细胞内过多的ROS,降低细胞的早期凋亡。
线粒体自噬可通过调控线粒体的融合和分裂清除受损及多余线粒体、减少ROS累积,从而维持线粒体的动态和能量代谢平衡[18]。PINK1是一种丝氨酸/苏氨酸激酶,存在于线粒体外膜的一种蛋白激酶,能够作为受损线粒体的分子感受器;Parkin是由PARK2基因编码的存在于细胞质中的一种E3泛素-蛋白连接酶活性的蛋白,主要介导底物泛素化,调节蛋白降解和信号转导等[19-20]。在生理状态下,PINK1存在于线粒体外膜并很快被蛋白水解酶降解使其维持稳定的低水平状态。CSE诱导L6大鼠成肌细胞使细胞内受损线粒体外膜处于去极化,线粒体膜电位下降,负责降解 PINK1 的蛋白水解酶被抑制,PINK1 在受损线粒体外膜聚集,这一过程可诱导Parkin 转位到受损线粒体,从而介导线粒体自噬的发生。Parkin 转位至受损线粒体后,其 E3 泛素酶被激活,从而线粒体基质蛋白泛素化,泛素化的自噬受体蛋白P62在去极化的线粒体基质上积累,进而与 LC3 结合,介导泛素化的底物进入自噬体,募集受损线粒体到溶酶体上从而完成线粒体自噬[21-23]。本研究发现CSE模型L6大鼠成肌细胞内的自噬蛋白LC3B、P62 、PINK1蛋白表达水平增高,Parkin 表达水平下降,而参苓白术散干预后细胞内自噬相关蛋白Parkin、LC3B表达明显增加,p62表达显著下降,提示参苓白术散可通过激活COPD骨骼肌损伤细胞内PINK1 /Parkin 介导的线粒体自噬途径,清除受损及多余的线粒体,维持细胞内线粒体的动态平衡和能量代谢平衡,提高细胞清除多余ROS的能力,改善细胞内氧化/抗氧化失衡,从而保护骨骼肌细胞的正常结构和功能。
综上所述,本实验在细胞水平证明参苓白术散可激活PINK1/Parkin介导的线粒体自噬通路,提高COPD骨骼肌细胞的线粒体自噬水平,维持体内线粒体动态平衡,减少CSE引起的氧化损伤,提示参苓白术散对改善线粒体功能,改善COPD骨骼肌肌力和耐力状态有重要作用,从而为中药复方在 COPD骨骼肌损伤治疗方面提供了科学的实验依据。

