增施摩西管柄囊霉对甜玉米氮肥增效及土壤丛枝菌根真菌多样性的影响
徐如玉,左明雪,袁银龙,孙 杰,顾文杰,卢钰升,解开治 ,徐培智
(1. 甘肃农业大学资源与环境学院,甘肃 兰州 730070;2. 广东省农业科学院农业资源与环境研究所,广东 广州 510640)
0 引言
【研究意义】丛枝菌根真菌(Arbuscular mycorrhizal fungi,AMF)作为一种分布最为广泛的古老真菌,自然条件下能够与90%以上的陆生植物根系形成菌根共生关系[1-3]。这种共生体形成,一方面能够促进作物对氮、磷、钾等营养元素的吸收,减少化肥施用量[4];另一方面,AM真菌可影响植物根际土壤微生物多样性和群落结构,调节农田生态系统养分循环[5]。【前人研究进展】在前人的研究中,AM真菌对水稻、甘蔗、茶树等作物的化肥减量已有相关报道。张淑娟等[4]通过盆栽试验研究水稻接种摩西管柄囊霉(Funneliformis mosseae)的表现,发现接种AM真菌可以有效促进水稻生长,促进水稻产量的提高,和不接菌相比,每生产100 kg稻谷,氮肥、磷肥、钾肥施用量分别减少3.14 kg、1.88 kg、2.42 kg,对化肥的削减程度高达47%。伍荣冬等[6]、张金莲等[7]在大田甘蔗施用AM真菌,发现接种AM真菌可以增加甘蔗的株高和有效茎数,提高甘蔗产量10%~24%,并减少30%以上的化肥用量。赵青华等[8]采用盆栽方法研究了不同施氮量下接种摩西管柄囊霉对茶树生长、矿质吸收元素及茶业品质的影响,发现当茶树的施氮量为0.53 kg时,接种AM真菌后的茶树,茶叶品质的效果最佳,总干物质量最大,为对照的1.63倍,经计算,此施氮水平下接种AM真菌使氮肥吸收利用率增加了21.57%。但关于AM真菌对玉米上施用化肥减量的研究较少。赵乾旭等[9]在设施盆栽条件下通过接种摩西管柄囊霉发现,与不接种相比较,接种AM真菌提高了间作玉米的菌根侵染率、株高、植株生物量和氮含量,而显著降低了玉米根系土壤中的碱解氮含量,经计算,接种AM真菌使玉米的氮吸收利用效率提高了19.51%。摩西管柄囊霉是球囊霉属的丛枝菌根真菌菌种,具有环境适应力强,应用范围广等特点。刘铭铭等[10]的研究发现,盆栽试验条件下接种摩西管柄囊霉能够更好地促进寄主植物的生长,其菌根侵染率和孢子密度均高于异形根孢囊霉(Rhizophagus intraradices),经计算增施摩西管柄囊霉可使玉米的氮利用率提高27.8%,而增施异形根孢囊霉玉米的氮利用率仅提高9.5%。【本研究切入点】早期关于AM真菌在促进化肥减量的研究主要集中在磷肥减施方面,对氮肥减施增效的研究甚少,且大多数的研究主要局限于盆栽试验。广东省是我国甜玉米的主产区,也是世界上优势产区之一。当前广东省甜玉米复种指数高、氮肥施用集中且施用量大、利用效率低、环境污染严重等问题突出。广东省甜玉米氮肥减施增效技术的创新应用对我国鲜食玉米减肥具有典型性和引领性。在大田上通过增施AM真菌来促进甜玉米氮肥减施增效的研究鲜有报道,严重制约了AM真菌共生体在甜玉米生产中对氮肥减施增效潜力的挖掘。【拟解决的关键问题】本研究以甜玉米为研究对象,采用大田区组试验,利用土壤常规理化指标分析方法和Illumina Hiseq 2500高通量测序平台,研究增施摩西管柄囊霉对甜玉米氮肥减量增效及土壤AM真菌多样性的影响,探索甜玉米根际土壤AM真菌群落结构的变化与氮利用率之间的关系,以期为甜玉米氮肥减量增效以及AM真菌肥在大田作物上的应用提供参考。
1 材料与方法
1.1 试验地概况
定位试验位于广东省惠州市惠阳区农业技术推广中心试验基地(N23°8′46.19″, E113°20′47.84″),于2018年春季开始,一年双季栽培。试验区气候类型为亚热带季风气候,年平均气温为13~22℃,年平均降水量800~1 500 mm,土壤类型为砖红壤,土壤理化性质:碱解氮191.5 mg·kg-1、有效磷 59.1 mg·kg-1、速效钾 224.1 mg·kg-1、pH 值 5.1、有机质21.89 g·kg-1。
1.2 试验材料
供试甜玉米(Zea Mays L.)品种为粤甜28号,由广东省农业科学院作物研究所提供。
供试菌种为摩西管柄囊霉(Funneliformis mosseae,BGC NM04A),购自北京市农林科学院植物营养与资源研究所,摩西管柄囊霉(F. mosseae)菌剂含被侵染的甜玉米植物根段、菌根真菌孢子及根外菌丝的根际砂土混合物,其孢子密度为40个·g-1,参考毕银丽[11]的方法进行室内盆栽扩繁,基质采用风化煤+砂土+蛭石+珍珠岩(1∶1∶1∶1)组合,接种前高压灭菌(121℃,30 min)备用;甜玉米种子经过10 min的10% H2O2消毒,洗净置于培养箱28℃催芽备用,75%酒精盆钵消毒备用;将2.0 kg灭菌基质放入盆钵中,浇水至土壤持水量75%,15 g菌剂平铺,放入催芽后的甜玉米种子6粒,最后覆盖约0.5 g基质;出苗后7 d定苗4株·盆-1,采用自然光照、空调控温的方式,温度控制在白天为(25±2)℃,夜间(19±2)℃,相对湿度保持在65%。在播种后45 d每盆分别补施100 mL的Hoagland营养液。最后收获测定孢子含量备用。
1.3 试验设计
根据当地高产栽培方式优化最佳施肥量为:氮肥(N)330 kg·hm-2、磷肥(以 P2O5计)150 kg·hm-2、钾肥(以K2O计)225 kg·hm-2。试验共设4个施氮水平:(1)N0,不施氮肥;(2)N17.6,施氮肥264 kg·hm-2;(3)N19.8,施氮肥 297 kg·hm-2;(4)N22,施氮肥330 kg·hm-2;同一施氮水平下设增施摩西管柄囊霉(AMF+)315 kg·hm-2和不施(AMF-)2个裂区,共8个处理,每个处理3个重复,各小区面积67.5 m2(4.5 m×15 m),随机区组排列。
各小区磷、钾肥施用量相同,施磷肥(以P2O5计)150 kg·hm-2、钾肥(以 K2O 计)225 kg·hm-2,磷肥品种为过磷酸钙(P2O512%),钾肥品种为硫酸钾(K2O 50%)。氮肥使用尿素(N 46%),在基肥、苗期、拔节期分别以2∶3∶5的比例施入,磷肥一次性基施,钾肥在基肥和拔节期分别以5∶5的比例施入。所有基肥按试验设计施用量起垄撒施旋耕。甜玉米幼苗移栽时接摩西管柄囊霉(F. mosseae)菌剂,每个定植穴接种7 g。甜玉米种植密度为45 000株·hm-2,起垄种植,其他栽培管理措施与当地习惯相同。
1.4 样品采集方法
供试土壤样品采集于2019年秋季甜玉米生长时期的成熟期,参照Zhao等[12]的根际土采集方法在每个小区采集4株长势均匀的植株根际土壤,然后把采集的根际土壤均匀混合,分成2份,1份约2 000 g室温保存带回用于土壤理化性质和孢子含量的测定;1份约500 g放入无菌密封袋密封后用冰盒带回实验室后-80℃保存,用于检测AM真菌群落的多样性。
供试植株根系样品采集于成熟期的甜玉米根系,用细流量的清水冲洗干净后,置于FAA固定液(70%的酒精、甲醛、冰醋酸按照体积比90∶5∶5的比例混合而成)中固定24 h以上,4℃冰箱中保存备用。
甜玉米鲜苞产量采用全小区实收测产的方式进行。
1.5 理化性质的测定方法
土壤pH值采用酸度计,全氮采用凯氏定氮法,全磷和全钾经消煮后,采用钼锑抗比色法和火焰光度法,有机质采用重铬酸钾容量法[13];土壤呼吸采用室内密闭培养法等进行测定[14];碱解氮采用碱解扩散法,土壤速效磷采用氟化铵浸提(酸性土)钼锑抗比色法,速效钾采用乙酸铵浸提火焰光度法,硝态氮、铵态氮采用氯化钾浸提流动注射分析法进行测定[15]。
1.6 菌根侵染率和孢子含量测定方法
菌根侵染率采用台盼蓝染色法进行染色、脱色、制片、镜检[16]。采用湿筛倾注蔗糖离心法检测甜玉米根际土壤中孢子含量[17-18]。
1.7 扩增子试验分析方法
采用土壤DNA提取试剂盒(MinkaGene Soil DNA Kit)对土壤样品进行总DNA的提取,利用NanoDrop One检测DNA的完整性、纯度和浓度。利用AM真菌特异性引物对24个样品AM真菌的DNA扩增采用巢式PCR。两轮扩增引物为:第一轮包括AML1F(5 ′-ATCAACTTTCGATGGTAGGATAGA-3 ′)和AML2R(5′-GAACCCAAACACTTTGGTTTCC-3′),第二轮包括 AMV4.5NF(5′-AAGCTCGTAGTTGAA TTTCG-3′)和 AMDGR(5′-CCCAACTATCCCTAT TAATCAT-3′)[19],利用上述引物对AM真菌进行目标片段扩增。第一轮PCR反应体系为:2×PCR Mix 25 μL,50 ng DNA 模板,10 μmol·L-1正、反向引物各1 μL,加ddH2O至50 μL;第二轮PCR反应体系为:2×PCR Mix 10 μL,50 ng DNA模板,10 μmol·L-1正、反向引物各 0.4 μL,加 ddH2O 至 20 μL。两轮PCR扩增程序为:95℃预变性5 min;95℃变性30 s,50℃退火 30 s,72℃延伸30 s(第一轮重复20个循环,第二轮重复36个循环);72℃延伸8 min,4℃保存。用1%琼脂糖凝胶电泳检测PCR产物的片段和浓度,Pooling及切胶纯化,制备文库后,委托广东美格基因科技有限公司应用Illumina Hiseq 2500平台对构建的扩增子文库进行测序。
1.8 参数计算方法
1.8.1 氮素利用效率相关参数的计算方法[20-22]
氮肥农学效率(NAE,kg籽粒·kg-1N)=(施氮区产量-对照区产量)/施氮量
氮肥偏生产力(PFP,kg籽粒·kg-1N)=施氮区鲜苞产量/施氮量
氮肥吸收利用率(NRE,%)=(施氮区地上部分吸氮量-对照区地上部分吸氮量)×100/施氮量
氮素生理利用率(NPE,kg籽粒·kg-1N)=(施氮区鲜苞产量-对照区鲜苞产量)/(施氮区地上部吸氮量-对照区地上部吸氮量)
1.8.2 菌根侵染率计算方法[23]
菌根侵染率/%=有菌根根段数/总根段数×100
根系中的菌根侵染强度/%=(95×侵染率90%以上根段数+70×侵染率50%至90%的根段数+30×侵染率10%至50%的根段数+5×侵染率10%以下1%以上根段数+侵染率1%以下根段数)/总根段数×100
1.8.3 Alpha多样性指数计算方法[24-26]
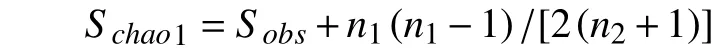
其中,Schao1为估计的OUT数,Sobs为实际观测到的OTU数,n1为只含有一条序列的OTU数目,n2为只含有两条序列的OTU数目,以此类推。
Dominance=,其中,pi为OTUi在全部OTU中的比例。
其中,ni为含有i条序列的OTU数目,N为所有的序列数。
1.9 数据分析与处理
本试验图表制作和统计分析采用Excel 2010和SPSS 20.0,施菌处理和施氮水平及其交互作用的差异显著性采用双因素方差分析(two-way ANOVA)进行检验,不同处理之间的差异显著性采用Duncan’s多重检验法进行检验(P<0.05)。Alpha多样性指数和Anosim分析使用R软件(R-3.2.2)进行分析绘图;Observed-species指数稀释曲线数据计算采用QIIME软件;冗余分析(RDA)首先使用R软件进行去趋势对应分析,然后使用进行cca或rda分析并绘图。
2 结果与分析
2.1 不同处理对甜玉米侵染率、侵染强度、土壤孢子密度的影响
甜玉米收获期侵染率测定结果表明(表1),甜玉米根系AM真菌的侵染率随着施氮水平的提高呈现先升高后降低的趋势。在N19.8时侵染率最高,N22时侵染率下降,表明施氮量过高会不利于AM真菌对甜玉米根系的侵染。在AMF-裂区中,侵染率最大为78.67%,最小为58.00%,各处理间差异显著(P<0.05);在AMF+裂区中,侵染率最大为93.00%,最小为81.00%,N19.8AM处理的侵染率最大,其他3个处理之间并无显著差异。侵染强度在各处理间差异显著(P<0.05),其中,在N22AM处理中侵染强度最大,其次是N0AM处理。孢子密度和侵染率的变化规律一致,随着施氮水平的提高呈现先升高后降低的趋势,N19.8时孢子密度最高,N22时孢子密度下降。
2.2 不同处理对甜玉米鲜苞产量和氮素养分吸收利用的影响
施菌和施氮水平及其交互作用的双因素方差分析结果发现,施氮和施菌的交互作用对鲜苞产量的影响显著(P=0.024<0.05)。由图1可见,在N22、N19.8、N17.6和N0施氮水平下,增施摩西管柄囊霉剂后,甜玉米的鲜苞产量均有所增加,分别较不施菌裂区组增加了0.8%、8.0%、16.7%和32.6%;在N22施氮水平下,增施摩西管柄囊霉剂后甜玉米的鲜苞产量与不施菌裂区组相比无显著性差异(P>0.05),在其他施氮水平下,增施摩西管柄囊霉剂后甜玉米的鲜苞产量差异显著(P<0.05)。总体而言,在高氮水平下增施摩西管柄囊霉剂效果不显著,在低氮水平下效果显著。
由表2可见,在AMF-裂区中,各处理的氮肥农学效率(NAE)、氮肥偏生产力(PFP)、氮肥吸收利用率(NRE)、氮素生理利用率(NPE)均随着施氮量的增加而增加。NPE在N22和N19.8处理之间并无显著差异,但与N17.6处理差异显著(P<0.05)。在AMF+裂区中,N22AM处理的NAE、NPE均高于其他处理,PFP在3个施氮水平之间并无显著差异。增施摩西管柄囊霉剂不同施氮水平的NAE、PFP、NRE和NPE均有所增加。在N17.6施氮水平时,NAE、PFP和NRE相比不施菌处理增加幅度最大,分别增加6.84%、6.85%和11.49%;在N22施氮水平时,增施摩西管柄囊霉剂NPE增加了6.19%;NRE以N17.6 AM处理最高,达到48.26%。
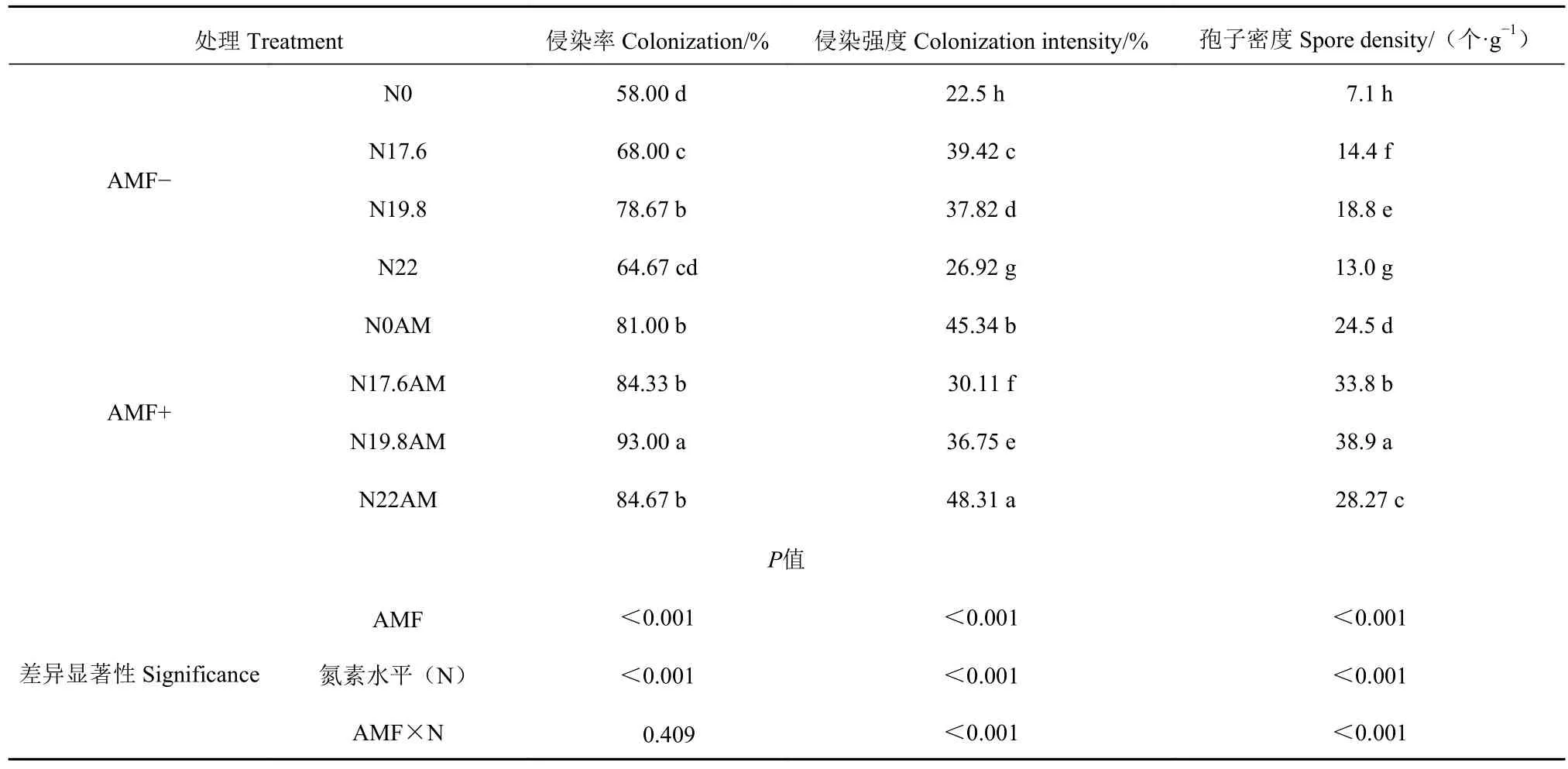
表1 不同处理甜玉米的侵染率、侵染强度和土壤孢子密度Table1 Infection rate and intensity of sweet corn plants and spore density in soil under various treatments
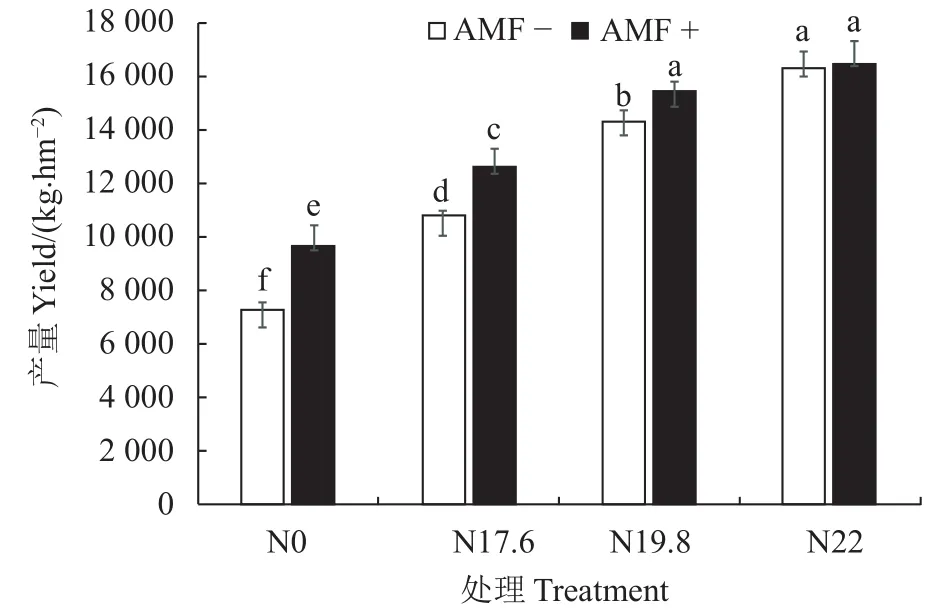
图1 不同处理对甜玉米鲜苞产量的影响Fig.1 Yield of sweet corn as affected by various treatments
2.3 稀释性曲线(Observed-species)分析
通过Illumina Hiseq 2500测序平台,对24个样品进行测序,共获得1 558 461条高质量序列,样品内的AM真菌全部为球囊菌纲(Glomeromycetes)。以97%的一致性将序列聚类成为15 771个AM真菌的OTUs,绘制成图2的稀释曲线。当测序深度达到80 000条序列时,各处理的Observed-species指数上升速度缓慢,曲线逐渐趋向平缓,说明测序深度可以反映样品中绝大多数的AM真菌多样性信息。
2.4 Alpha多样性指数分析
Alpha多样性参数值见表3,N22AM处理的Chao1指数和Richness指数显著高于其他处理(P<0.05),表明N22AM处理的AM真菌菌群的丰富度最高,其次是N19.8、N19.8AM和N17.6AM处理;增施摩西管柄囊霉剂后,各施氮水平的Dominance指数较不施菌裂区均有所增加,说明增施摩西管柄囊霉剂后各处理的AM真菌物种分布较不施菌裂区更为集中;各处理的Shannon指数和Simpson指数在增施摩西管柄囊霉剂后均有所降低,这说明增施摩西管柄囊霉剂,各处理的AM真菌群落组成的优势菌属相对集中。其中,N0AM处理的Dominance指数显著高于其他处理,Shannon指数和Simpson指数显著低于其他处理(P<0.05),说明N0AM处理的AM真菌群落组成的优势菌种相对集中。
2.5 AM真菌群落结构组成分析
各处理相对丰度≥1%的AM真菌属组成情况如图3所示。各处理中AM真菌群落主要由球囊霉属(Glomus)、近明球囊霉属(Claroideoglomus)和类球囊霉属(Paraglomus)组成,占各处理AM真菌总丰度的38.51%以上,而这3个菌属在N0AM处理中所占比例最大,达到了74.22%;增施摩西管柄囊霉剂后,球囊霉属在N17.6AM处理增加了9.18%,与其他处理差异显著(P<0.05);近明球囊霉属在N0AM处理增加了17.85%,与其他处理差异显著(P<0.05);类球囊霉属在增施摩西管柄囊霉剂后在N0AM、N17.6AM和N22AM处理中均有所下降,在N17.6AM下降幅度最大,下降了12.62%,但无显著差异(P>0.05);无梗囊霉属(Acaulospora)在N22处理中所占的比例最大;原囊霉属(Archaeospora)在各处理之间无显著差异。

表2 不同处理的甜玉米氮素利用效率Table2 N utilization efficiencies of sweet corn plants grown under various treatments
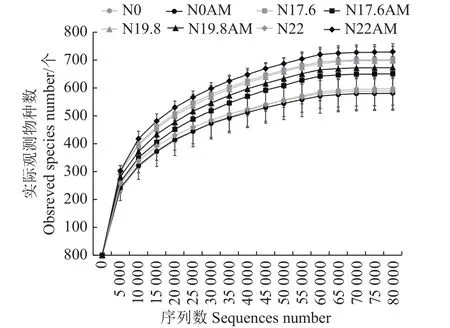
图2 Observed-species的稀释曲线Fig.2 Rarefaction curves of observed species
2.6 AM真菌群落结构与根际土壤环境因子的冗余分析(RDA)
冗余分析可综合反应土壤理化因子与AM真菌群落间的关系及相关程度。由图4所示,图4(a)第一排序轴和第二排序轴分别解释了91.59%和5.20%,图4(b)第一排序轴和第二排序轴分别解释了83.35%和12.35%,都较好地解释了AM真菌群落特征与根际土壤理化性质间的关系。不同的环境因子对AM真菌属的影响不同,在AMF-裂区中,球囊霉属相对丰度与全钾(Total potassium)、速效钾(Available potassium)、pH、铵态氮(Ammonium nitrogen)、硝态氮(Nitrate nitrogen)、碱解氮(Alkaline nitrogen)、速效磷(Available phosphorus)呈正相关,与其他理化指标呈负相关;原囊霉属、无梗囊霉属、类球囊霉属、近明球囊霉属相对丰度与全钾含量和速效钾含量呈正相关,与其他理化指标呈负相关。其中,土壤呼吸(Soil respiration)、碱解氮、pH、速效钾与AM真菌群落特征的相关性较大。在AMF+裂区中,球囊霉属相对丰度与全钾、速效磷、碱解氮、全氮(Total nitrogen)、铵态氮、硝态氮、土壤呼吸和有机质(Organic matter)呈正相关,与其他理化指标呈负相关;原囊霉属、无梗囊霉属、类球囊霉属和近明球囊霉属相对丰度与pH、速效钾、全钾、速效磷和全磷(Total phosphorus)呈正相关,与其他理化指标呈负相关,其中,pH、全磷、速效磷、速效钾、碱解氮、铵态氮、硝态氮和土壤呼吸与AM真菌群落特征的相关性较大。
2.7 AM真菌多样性指数与菌根侵染率、侵染强度、土壤孢子密度和氮素利用率之间的关系
由表4可知,Shannon指数和Simpson指数与菌根侵染率、孢子密度和4种氮素利用率之间均有一定的相关性。特别是增施摩西管柄囊霉剂后,Shannon指数、Simpson指数与菌根侵染率、孢子密度、氮肥农学效率(NAE)、氮肥偏生产力(PFP)、氮肥吸收利用率(NRE)和氮素生理利用率(NPE)呈显著或者极显著正相关关系(P<0.05或P<0.01)。增施摩西管柄囊霉剂显著增加了AM菌多样性指数与菌根侵染率、土壤孢子密度和氮素利用率之间的相关性。

表3 土壤样品的AM真菌α多样性指数分析Table3 Diversity indices of AM fungi in soil samples
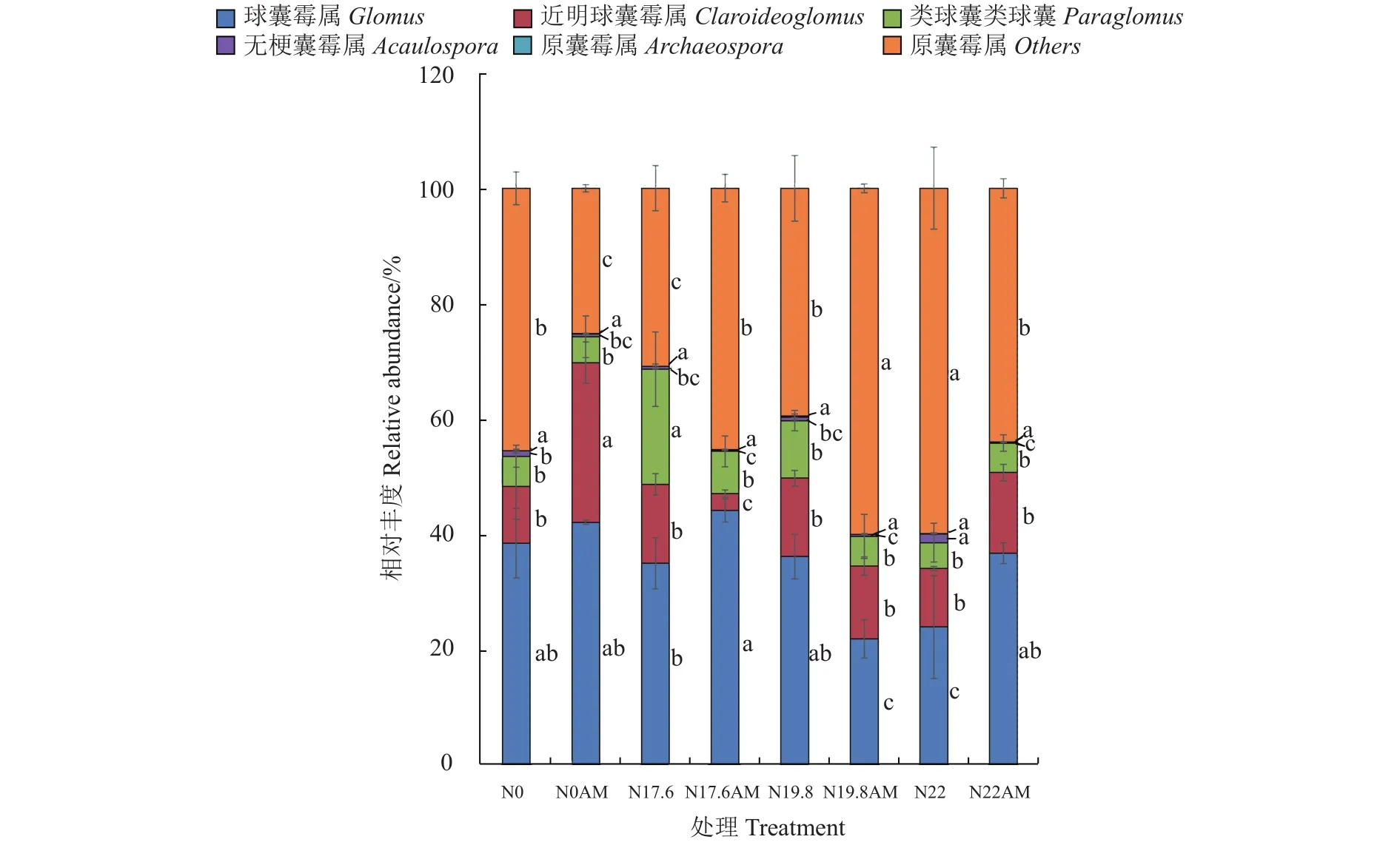
图3 属水平上相对丰度≥1%的物种组成Fig.3 Relative abundances of microbial genera with relative abundance ≥1%

图4 土壤样品AM真菌群落与土壤理化因子的RDA分析Fig.4 RDA analyses on AM fungal community in and chemical properties of soil samples
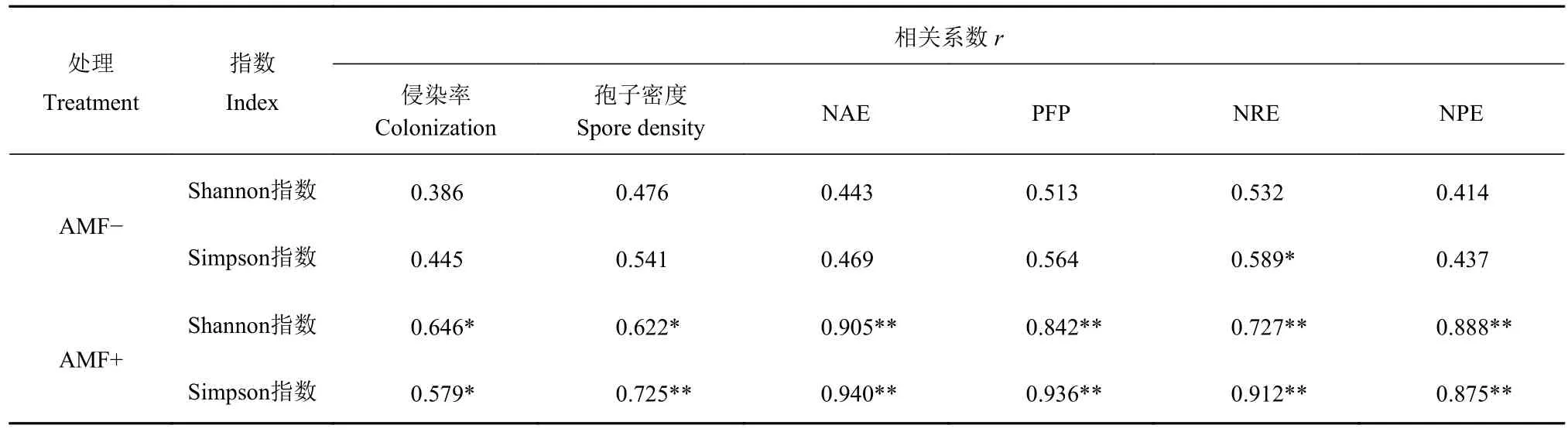
表4 AM真菌多样性指数与菌根侵染率、土壤孢子密度和氮素利用率之间的关系Table4 Relationship between AM fungal diversity index and mycorrhizal infection rate, spore density, and N utilization rate of soil
2.8 增施摩西管柄囊霉剂对甜玉米化学氮肥减施增效的机理
通过对增施摩西管柄囊霉剂和不增施两个裂区甜玉米生长指标的影响比较发现(图5),4个施氮水平的N0、N17.6和N19.8水平,在增施摩西管柄囊霉剂后侵染率、侵染强度、孢子密度、氮利用率(NAE、PFP、NRE和 NPE)、真菌多样性指数(Shannon和Simpson)、鲜苞产量和收获期地上部分氮积累量均和不施菌裂区有显著或极显著的差异,孢子密度分别与氮肥农学效率和甜玉米鲜苞产量呈极显著正相关关系,相关系数分别为0.991、0.977。说明增施摩西管柄囊霉剂能极显著提高N0、N17.6和N19.8施氮水平的AMF侵染率、侵染强度和孢子密度,进而影响氮利用率指标(NAE、PFP、NRE和NPE)的显著提高,改善甜玉米根际土壤AMF群落结构,实现化学氮肥减施增效,甜玉米稳产增产与品质提升。
3 讨论
AM真菌作为一种古老的共生真菌对甜玉米根系土壤中氮素的吸收利用产生了重要的影响,反之不同的施氮量也影响了甜玉米根系土壤AM真菌群落结构的组成,进而影响甜玉米植株氮素代谢。
3.1 增施AM真菌对菌根侵染率、侵染强度、孢子密度、玉米产量和氮素吸收利用的影响
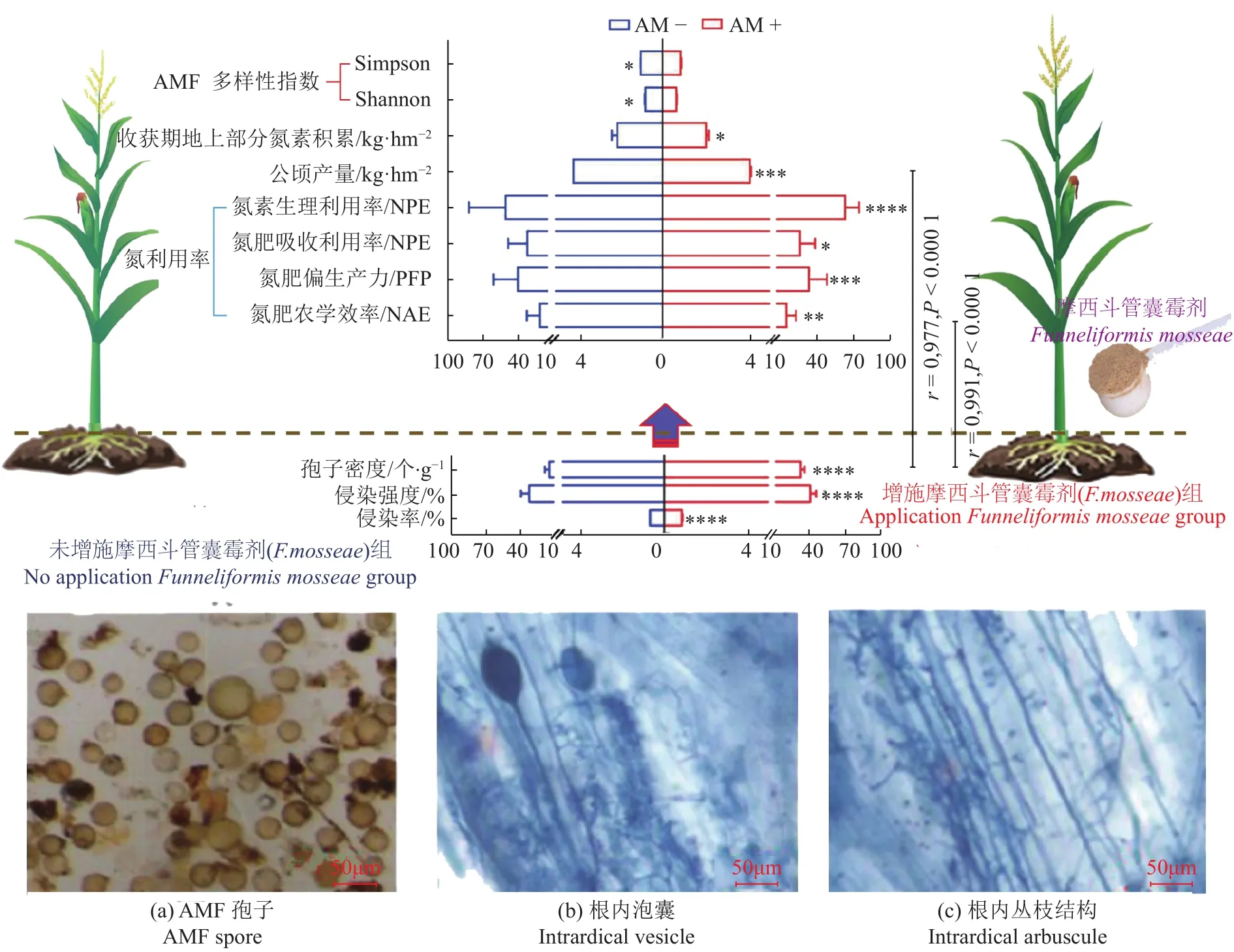
图5 增施摩西管柄囊霉剂对甜玉米化学氮肥减施增效机理Fig.5 Mechanism of F. mosseae on N utilization by sweet corn plants
已有研究结果表明,土壤中氮素含量过高将会降低AM真菌对寄主植物的侵染率,反之在氮含量较少的土壤中更有利于其对寄主植物的侵染[27-29],这与本研究结果一致。甜玉米根系的侵染率在一定范围内随着施氮水平的升高而升高,当在N19.8时侵染率最高,N22施氮水平时,侵染率下降,表明施氮量过高不利于AM真菌对甜玉米根系的侵染;土壤孢子密度和菌根侵染率规律一致,孢子密度随着施氮水平的升高而增加,当在N19.8时孢子密度最高,N22施氮水平时孢子密度下降,这说明土壤中氮素含量丰富时,AM真菌的孢子密度将会降低,原因可能是氮丰富的土壤中存在大量的硝酸根离子,会影响土壤pH的变化,从而刺激或者抑制AM真菌的产孢性能,这与Delowarn K[30]和任爱天[31]的研究结果一致。
增施AM真菌能促进玉米的生长和氮素利用率的提高。姜德锋等[32]研究发现,在不施P肥的条件下,接种AM真菌可使玉米增产23%。罗广宁等[33]研究发现,AM真菌对玉米增产起重要作用,增产率达18.02%~26.6%。赵乾旭等[9]研究发现,接种AM真菌能更好地促进玉米的生长及氮肥利用效率的提高,接种AM真菌使玉米的氮吸收利用效率提高了19.51%。李芳等[34]研究结果表明,玉米接种AM菌后,可以显著提高籽粒产量和养分含量。江彬等[35]研究发现土壤缺氮条件下,增施AM真菌更能促进植株对养分的吸收。本研究结果表明增施摩西管柄囊霉剂后,4个施氮水平的甜玉米鲜苞产量均有所增加。在N0、N17.6和N19.8施氮水平下,裂区间甜玉米的鲜苞产量差异显著(P<0.05),相比不增施摩西管柄囊霉剂的处理,甜玉米鲜苞产量分别增加了32.6%、16.7%和8.0%,与前人研究结果一致。但在N22施氮水平下,裂区间甜玉米的鲜苞产量无显著性差异。本研究中,增施摩西管柄囊霉剂后,不同施氮水平的氮肥农学效率、氮肥偏生产力和氮素生理利用率均有所增加,且在N17.6施氮水平时,氮肥农学效率、氮肥偏生产力和氮肥吸收利用率增加幅度最大,分别较不施菌裂区增加6.84%、6.85%和11.49%。这说明增施AM真菌能促进植物对氮素的吸收和利用[36-38]。但增施摩西管柄囊霉剂对甜玉米产量和氮素养分吸收利用效率的具体贡献值尚需结合供试菌株基因标记和同位素示踪等方法进行进一步探讨。
3.2 不同施肥量对植物根际土壤微AM真菌多样性和群落结构的影响
施肥能够显著影响土壤微生物的多样性[39-41]。蒋雨含[42]在研究不同施肥处理对设施番茄生长及丛枝菌根真菌群落的影响表明,在不同施肥处理下,番茄根际土壤中的丛枝菌根真菌群落多样性差异显著。李冬冬等[43]研究发现,长期定位施肥能够改变土壤的理化性质,从而改变了AM真菌生长的环境,进而对AM真菌群落结构产生了影响。在本研究中,N22AM处理的Chao1和Richness指数最高,说明优化施肥增施摩西管柄囊霉剂后甜玉米根际土壤的AM真菌菌群的丰富度最高;各处理的Shannon指数和Simpson指数在增施AM真菌后均有所下降,说明增施摩西管柄囊霉剂后,各处理的AM真菌群落组成的优势菌属相对集中。
已有研究表明,农田生态系统中,肥料的使用会影响AM真菌群落结构的组成,尤其是氮素的过量投入,会改变AM真菌群落的组成[44-45]。但在不同的生境条件下,AM真菌同属的丰度差异明显。郝杰等[46]在研究施氮对黄土高原旱地小麦根际AM真菌群落结构的影响中发现,不同施氮处理下,类球囊属(Paraglomus)、球囊霉属(Glomus)、近明球囊霉属(Claroideoglomus)为黄土高原小麦根际土壤中AM真菌群落的优势属,相对丰度占到总菌群的95%以上。宋福强等[47]在研究黑土农田中施加AM菌剂对大豆根际菌群结构的影响中发现,施加AM真菌后,从大豆根际土壤中共分离获得3种无梗囊霉属(Acaulospora)和7种球囊霉属的AM真菌。王庆峰等[48]在分析长期施用氮肥和磷肥对东北黑土丛枝菌根真菌群落组成的影响中表明,长期施用氮肥以及氮、磷肥混施显著改变AM真菌群落的组成,在属水平上,球囊霉属、近明球囊霉属、类球囊霉属和巨孢囊霉属(Gigaspora)相对丰度在各处理间具有显著差异。本研究对AM真菌群落结构的分析发现,球囊霉属、近明球囊霉属、类球囊霉属、无梗球囊霉属和原囊霉属是8个处理共有的5个AM真菌属,球囊霉属、近明球囊霉属和类球囊霉属是8个处理共有的优势AM真菌属,其中,球囊霉属在N17.6AM处理中所占的比重最高,为44.14%。不同生境下AM真菌属水平的丰度差异可能主要是由宿主的种类、土壤理化性质和气候条件等因素导致的。
3.3 AM真菌群落结构与环境因子之间的相关性
冗余分析结果显示,增施摩西管柄囊霉剂和不增施裂区各解释了96.79%和95.7%的AM真菌群落与环境变量之间的关系,说明所选理化性质能够较好地分析AM真菌群落结构与环境因子的相关程度。Monte Carlo检验显示,在不增施摩西管柄囊霉剂的处理中,土壤呼吸(P=0.044,解释量为47.84%)对AM真菌群落组成的影响最为显著;在增施摩西管柄囊霉剂的处理中,土壤全磷(P=0.026,解释量为57.84%)、速效钾(P=0.004,解释量为69.70%)和土壤呼吸(P=0.018,解释量为62.18%)对AM真菌群落组成的影响最为显著。胡从从等[49]和刘佳[50]研究表明AM真菌多样性与有效磷存在正相关关系,这与本文研究结果一致。土壤呼吸反映了土壤微生物的活性[51],在增施摩西管柄囊霉剂的处理中土壤呼吸的解释量远大于不增施处理,这说明增施摩西管柄囊霉剂后增加了土壤AM真菌的微生物活性。肖龙敏[52]研究发现AM真菌物种丰度与速效钾呈显著正相关,这与本文的研究结果一致。
不同种类的AM真菌对土壤酸碱度的耐受性不同,张美庆等[53]和Verena S等[54]研究发现,球囊霉属在pH为5~9的土壤中分布广泛,与pH呈正相关关系;蔡晓布等[55]研究发现球囊霉属与pH呈正相关关系,无梗球囊霉属与pH呈负相关关系,无梗球囊霉属在有机质含量为0.9~19.6 g·kg-1时,与有机质含量呈正相关关系,球囊霉属和无梗球囊霉属与有效磷含量呈正相关,与本研究结果基本一致。不同的是本研究无梗球囊霉属与pH呈正相关关系。
3.4 AM真菌多样性与菌根侵染率、侵染强度、孢子密度、氮素生理利用率的相关性
在增施摩西管柄囊霉剂后,显著增加了Shannon指数和Simpson指数与菌根侵染率、孢子密度、4种氮利用率(NAE、PFP、NRE和NPE)之间的相关性。这说明,增施摩西管柄囊霉剂后,改善了AM真菌群落结构,各处理的AM真菌群落组成的优势菌属相对集中,显著增加了孢子密度、侵染率的相关性。增施摩西管柄囊霉剂后,各施氮水平上的Dominance指数均有所上升,Shannon指数和Simpson指数均有所下降,这说明增施摩西管柄囊霉剂后的处理,AM真菌群落组成的优势菌属分布更为集中。摩西管柄囊霉剂能促进植株对土壤氮素养分的吸收,从而提高了氮素利用率,这与赵青华等[8]和赵乾旭[9]研究结果一致。
4 结论
(1)增施摩西管柄囊霉剂可提高甜玉米的鲜苞产量。N19.8水平AM真菌侵染率、孢子密度最高,且与增施摩西管柄囊霉剂存在正交互效应(P<0.001)。N19.8AM处理田间鲜苞产量与N22处理无显著差异,可作为甜玉米氮肥减施的推荐施肥方式。
(2)增施摩西管柄囊霉剂能在一定程度上改善植物的氮素营养状况,促进植物对氮素的吸收和利用。在N17.6施氮水平时,氮肥农学效率、氮肥偏生产力和氮肥吸收利用率增加幅度最大,分别较未增施裂区增加6.84%、6.85%和11.49%。
(3)增施摩西管柄囊霉剂后各处理的AM真菌群落组成的优势菌属相对集中,球囊霉属在N17.6AM处理增加了9.18%,与其他处理差异显著(P<0.05)。增施摩西管柄囊霉剂后,显著增加了Shannon指数、Simpson指数与侵染率、孢子密度和4种氮素利用率(NAE、PFP、NRE和NPE)之间的相关性(P<0.05)。

