蒙药三味阿拉坦其其格散的急性毒性试验
特日格乐 苏龙嘎 齐和日玛

【摘 要】 目的:通过观察蒙药方剂三味阿拉坦其其格对小鼠的急性毒性反应和动物死亡情况,对三味阿拉坦其其格进行安全性评价,力求为其临床用药提供安全范围。方法:按照经典急性毒性实验方法进行,观察小鼠中毒反应及计算出半数致死量(LD50),给药后连续观察7 d,实验结束后处死小鼠,观察重要器官是否存在病理改变。结果:蒙药方剂三味阿拉坦其其格 LD50为16.03 g·kg-1,95 %置信区间(CI)为11.38 ~22.60 g·kg-1。实验过程中小鼠体质量在给药3 d后恢复正常,组织病理切片显示,肝脏空泡变性、椭圆形细胞增生病变、脾脏淋巴细胞凋亡等病变可能与药物使用有关。结论:实验表明蒙药方剂三味阿拉坦其其格具有一定的急性毒性,但在一定剂量范围内使用是安全的。
【关键词】 蒙药方剂三味阿拉坦其其格;小鼠;急性毒性实验
【中图分类号】R285.1 【文献标志码】 A 【文章编号】1007-8517(2020)10-0036-05
Abstract:Objective By observing the acute toxicity and animal death of Mongolian medicine Alatanqiqige-3 to mice, to evaluate the safety of Alatanqiqige-3 in order to provide a safe range for its clinical use.Methods According to the classical acute toxicity experiment method, observe the toxic reaction of mice and calculate the Median lethal dose(LD50). After administration, the mice were observed for 7 days continuously. After the experiment, the mice were killed and the pathological changes of important organs were observed. Results Mongolian medicine Alatanqiqige-3s LD50 was 16.03 g · kg-1 and 95% confidence interval (CI) was 11.38-22.60 g·kg-1. During the experiment, the body mass of mice returned to normal after three days of administration. The histopathological sections showed that the liver vacuolar degeneration, oval cell hyperplasia, spleen lymphocyte apoptosis and other lesions may be related to the use of drugs. Conclusion The experiment shows that the Mongolian medicine Alatangqige-3 has certain acute toxicity, but it is safe to use in a certain dose range.
Keywords:Alatanqiqige-3; Mice;Acute Toxicity
蒙药经典方剂三味阿拉坦其其格散,别名三味木鳖散、日来那木吉乐。有消除“希拉”,镇“赫依”功能,主治综合性“希拉”病,由木鱉子(炮制)、玫瑰花、金色诃子组成的传统蒙药。相关研究表明,木鳖子具有毒性,皂苷和木鳖子素为其主要毒性成分[1-4],一般炮制后才用于临床[5]。木鳖子有多种炮制方法,不同方法炮制的木鳖子含油量均不同,且其他有效成分的相对含量也随之不同,因而影响其毒性和药理作用[6-7]。传统蒙药木鳖子的炮制方法大多采取砂炒法。目前,国内外对木鳖子的化学成分、毒性以及药理作用均进行了一定程度的探索研究,但尚缺乏对含木鳖子复方药的安全性评价。
三味阿拉坦其其格散最早在蒙医古籍《兰塔布》[8]中记载,又相继在《蒙医金匮》[9]《蒙医方剂选编》[10]等中记载,“炮制木鳖子5 g、金色诃子12.5 g、玫瑰花25 g比例制成散剂,有清希拉之效,主治有口苦、目黄、发烧、头疼等症状的综合性希拉病”。由于方剂当中含有木鳖子,且安全性评价和药理作用方面的研究至今空白,导致临床使用率越来越低。因此,三味阿拉坦其其格散的临床安全应用以及新型成药的研发都急切需要安全性评价研究。笔者通过开展三味阿拉坦其其格散急性毒性实验研究,力求为其临床用药提供安全范围。
1 材料与方法
1.1 药材 蒙药方剂三味阿拉坦其其格散的3种单药:木鳖子仁(批号1510001)、诃子(批号171101313)均购自内蒙古天盛蒙中医药有限公司,玫瑰花(批号170201335)购自河北济鑫堂药业有限公司,药材由内蒙古医科大学蒙药学教研室鉴定为正品。
1.2 动物 SPF级昆明种小鼠140只,雌雄各半,雌雄分笼饲养,体重18~22 g,由北京科宇动物养殖中心提供,许可证号:SCXK(京)2018-0010。
1.3 试剂 羧甲基纤维素钠(CMC-Na)(批号: 20180223)购自天津永晟精细化工有限公司;水合氯醛(批号:20180110)购自天津市科密欧化学试剂有限公司;甲醛溶液(批号:20181013)、无水乙醇(批号:20190322)购自天津市津东天正精细化学试剂厂;伊红染液、苏木素染液(批号:20190105)购自南京建成科技有限公司;Leica石蜡(德国Leica公司,批号39601006)。
1.4 仪器 灌胃针、手术剪、电磁炉、炒锅、AK-1000A型500 g摇摆式中药粉碎机(温岭市奥力中药机械有限公司)、RM2016病理切片机(上海徕卡仪器有限公司);NIKON ECLIPSE CI正置光学显微镜(日本尼康)。
1.5 实验方法
1.5.1 受试药物制备
1.5.1.1 木鳖子的炮制以及脂肪油含量测定 本研究炮制方法和脂肪油含量测定均按照《内蒙古蒙药炮制规范》(2015年版)[11]进行。取净木鳖子,照砂烫法炮制后剥去外壳并刮净绿色种皮。炮制品粗粉用乙醚回流提取脂肪油,计算得知脂肪油含量为27.35%,在木鳖子炮制品的脂肪油含量范围内(25%~30%)。
1.5.1.2 三味阿拉坦其其格散配制 称取炮制木鳖子5 g,金色诃子12.5 g,玫瑰花25 g,严格按照《内蒙古蒙药制剂规范》(2007年版)[12]散剂制作法配制,再称取适量三味阿拉坦其其格散粉末,加入1%CMC-Na溶液制成0.43 g/mL(小鼠12号灌胃针头刚好能过的浓度)的药品混悬液,于 4℃保存备用。
1.5.2 预实验方法 取健康SPF小鼠60只,雌雄各半,试验前小鼠禁食不禁水16 h,随机分为10组,每组6只。设能通过小鼠12号灌胃针头的最大浓度为最大浓度,再以1:0.85的组间剂量比稀释,得出单次给药剂量分别为17.2 g/kg、14.62 g/kg、12.42 g/kg、10.56 g/kg、8.98 g/kg、7.63 g/kg、6.49 g/kg、5.51 g/kg、4.69 g/kg、3.98 g/kg。以0.4 mL/10g体积灌胃给药2次/d,给药间隔6 h,连续观察7 d,记录动物死亡情况。根据小鼠死亡情况找出最大致死量Dmax和最小致死量Dmin。
1.5.3 正式试验方法 取健康SPF小鼠80只,雌雄各半,试验前小鼠禁食不禁水16 h,随机分为7组给药组和1组空白对照组,每组10只。根据预实验结果,单次给药最大致死量Dmax为12.42 g/kg,最小致死量Dmin为4.69 g/kg,按K值计算出各组单次给药剂量分别为12.42 g/kg、10.56 g/kg、8.98 g/kg、7.63 g/kg、6.49 g/kg、5.51 g/kg、4.69 g/kg,从高剂量到低剂量依次为A-G组,空白对照组为H组。给药组(A-G组)以0.4 mL/10g体积灌胃给药,2次/d,给药间隔6 h,空白对照组(H组)以0.4 mL/10g体积灌胃1%CMC-Na溶液,2次/d,灌胃间隔6h。连续观察7d,记录动物死亡情况,最终计算半数致死量(LD50值)。
1.5.4 观察指标 给药后观察小鼠的眼、口、鼻等有无异常分泌物,观察小鼠的中毒表现及记录死亡情况;给药当天4 h内,每小时观察临床体征及死亡率,共4次。以后每天观察并称重。实验期间对死亡动物及时进行大体解剖。其他动物在实验结束后进行大体解剖,肉眼观察重要脏器(心、肝、脾、肺、肾) 是否发生体积、颜色、质地等改变[13]。再选取各脏器进行HE染色,显微镜下观察病理改变。
1.5.5 计算半数致死剂量 采用改良寇氏法[13]进行半数致死剂量计算。lgLD50=Xm-i(∑p-0.5) ,LD50的 95%置信区间计算公式为: Log-1(logLD50±1.96×Sx50),式中Xm为最大剂量组对数值;i为相邻两组对数剂量的差值;∑p为各组动物反应率之总和;Sx50:logLD50的标准误。
1.6 统计学分析 采用SPSS 22.0统计软件分析,各组间比较用方差分析。所得数据以(x±s)表示,P<0.05表示差异有统计学意义。
2 结果
2.1 预实验结果 0% 和100%估计致死剂量(Dmax 、Dmin)分别为2×12.42 g/kg和2×4.69 g/kg。見表1。
2.2 正式试验结果
2.2.1 中毒体征观察 给药后4 h内部分小鼠出现自发活动减少、静伏、卷缩、所有小鼠出现饮食饮水量减少等表现,但无小鼠死亡。第2次给药6 h后出现小鼠死亡,76 h后再无小鼠死亡。观察2 d后幸存小鼠摄食饮水基本恢复正常,状态良好,观察7 d无其他异常现象发生。
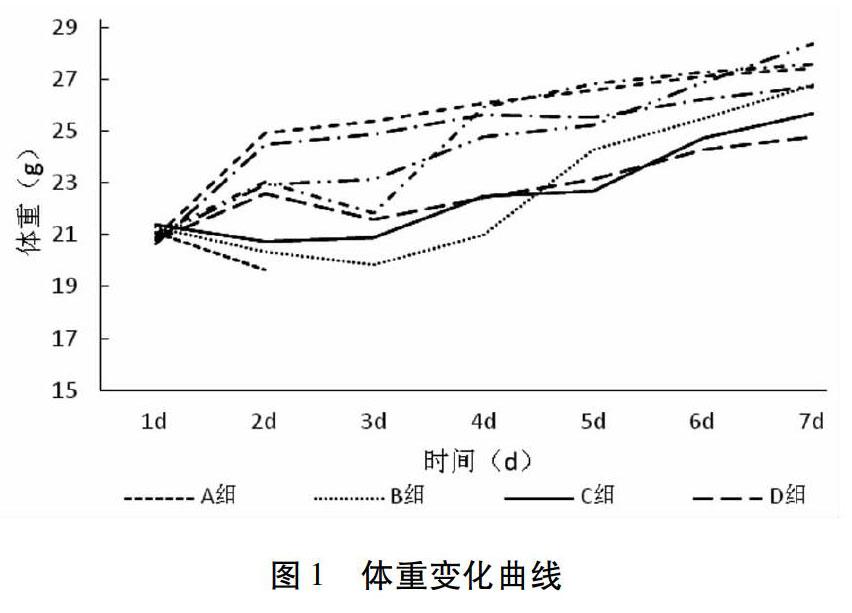
2.2.2 体重变化 如图表1所示,最高剂量组(A组)在第2次给药后体重减轻,并在76 h内全部死亡。给药组(B-G组)小鼠跟空白组(H组)比较,在第2次给药后3 d内出现体重增加减慢、不稳定甚至体重减轻情况,第3天后开始稳定且正常增长。
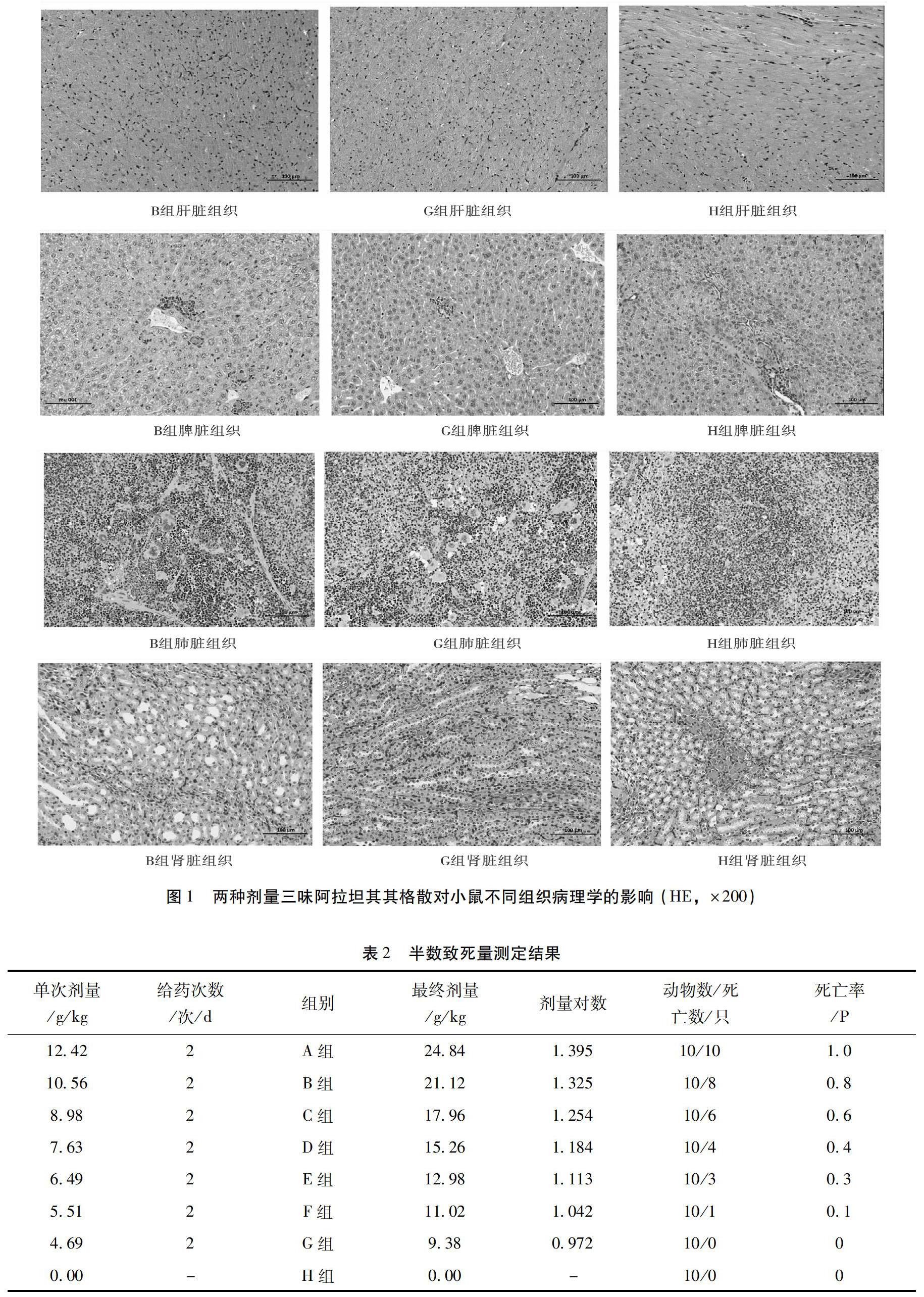
2.2.3 组织病理学观察 死亡小鼠即刻解剖,常规饲养 7d 后所有小鼠处死解剖,心、肝、脾、肺、肾形态、颜色、质地均正常,肉眼未观察到明显病变。组织病理学观察结果如图1所示。
给药组:高剂量给药组(B组)和低剂量给药组(G组)肝脏小叶内均可见少量炎性细胞灶性浸润,大量肝细胞轻度空泡变性,胞质内可见微小空泡。B组肝脏伴少量色素沉着,G组肝脏汇管区少量椭圆形细胞增生。脾脏均可见生发中心及少量凋亡小体,红髓内可见大量髓外造血细胞,且多核巨细胞增生。B组脾脏少量细胞点状坏死,胞核碎裂。肺脏、肾脏、心脏、未见明显病理变化。
空白对照组:(H组)肝脏小叶内可见少量炎性细胞灶性浸润,肝细胞轻度空泡变性,胞质内可见微小空泡。脾脏:红髓内可见少量髓外造血细胞和多核巨细胞增生。肺脏、肾脏、心脏、未见明显病理变化。
以上除环境等原因所致的各组肝脏少量炎性细胞浸润和轻度空泡变性、脾脏少量髓外造血细胞和多核巨细胞少量增生病变外,两种不同剂量给药组(B组、G组)肝脏均发生大量空泡变性,脾脏淋巴细胞均发生凋亡病变。且两种剂量对于肝脏和脾脏的影响在程度上有一定的不同:G组肝脏汇管区出现少量椭圆形细胞增生,而B组肝脏出现少量色素沉着,脾脏出现少量细胞点状坏死,胞核碎裂等病变。所以以上肝脏和脾脏的病变可能与药物使用有关,且随着浓度的增加毒性作用更大。但对小鼠心、肺、肾组织无明显影响。
2.2.4 半数致死量的测定 半数致死量测定实验结果如表2所示,结果按改良寇氏法公式计算得出LD50为16.03 g·kg-1,95 % CI为11.38 ~22.60 g·kg-1。
3 讨论
三味阿拉坦其其格散作为蒙医传统方剂,始载于17世纪的著作《兰塔布》[8]中,相续在多个蒙医学文献中记载,是治疗综合性“希拉”病经典方剂。由于临床应用安全性的缺乏,导致临床使用率和生产率逐年降低。笔者通过观察蒙药三味阿拉坦其其格散对小鼠的急性毒性表现,改良寇氏法计算LD50,初步对其安全性进行了探索与评价。结果表明:三味阿拉坦其其格散第2次给药6 h后小鼠出现死亡,76 h后再无小鼠死亡,观察3 d后摄食量及体重基本恢复正常,说明三味阿拉坦其其格散具有一定毒性。组织病理学观察结果显示:三味阿拉坦其其格散两种不同剂量均对小鼠肝及脾组织产生一定程度的影响,如肝脏大量空泡变性、椭圆形细胞增生等病变,以及脾脏淋巴细胞凋亡、细胞点状坏死,胞核碎裂等病变,且毒性作用随着给药浓度的增加而增加。对心、肺、肾等脏器组织无明显影响。可初步推测三味阿拉坦其其格散毒性靶器官为肝脏和脾脏。
此外,本研究得出三味阿拉坦其其格散的LD50为16.03 g·kg-1,是木鳖子提取物口服LD50[14]的4倍。小鼠体重以 20 g 计,成人体重以70 kg 计,小鼠与人的计量折算系数为0.0026,即小鼠剂量/成人剂量 = 9.1,体重为70 kg的成人临床用量为16.03 g·kg-1/9.1×70 kg =72.15 g 。此用量为三味阿拉坦其其格散在文献上记载的[15-16]临床最大日用量(6 g)的12倍,成人日用量达到72.15 g才会出现急性毒性反应。现实中单次用药量基本达不到如此大的剂量,因此,临床使用中通常不会出现急性中毒情况。但三味阿拉坦其其格散的慢性毒性方面至今无实验研究,无法确定是否存在慢性毒性,所以长期使用需注意对肝、脾功能的影响。
目前蒙医多种方剂中经常用其他药效相似的药材代替木鳖子入药,比如与三味阿拉坦其其格散药效相似的藏药三味蔷薇散中用波棱瓜子代替木鳖子入药[17]。为了保证临床药效及安全性,对三味阿拉坦其其格散进行进一步的慢性毒性研究或毒性成分的探讨,以及筛选出与君药木鳖子药效相似并且毒性更低的药材代替入药是值得进一步深入研究的。参考文献
[1]姜仁輝,林慧彬,林建强.木鳖子皂苷提取分离工艺研究[J].山东师范大学学报(自然科学版),2009,24(1):82-84.
[2]王秀琴,李檀,白宗利,等.木鳖子素的分离与纯化[J].辽宁中医杂志,2007,34(1):78-79.
[3]林慧彬,安芸,路俊仙,等.中药木鳖子的研究进展[J].时珍国医国药,2009,20(4):785-787.
[4]石军飞,闫超.木鳖子炮制前后毒性对比研究[J].北方药学,2013,10(1):52-53.
[5]领小,博·格日勒图,苏日娜.木鳖子研究进展[J].中药材,2007,30(11):1475-1478.
[6]路俊仙,崔璐,陈慧慧,等.不同含油量木鳖子霜毒效关系研究[J].辽宁中医杂志,2010,37(5):946-948.
[7]张振凌,王一硕.木鳖子制霜前后脂肪油含量的比较[J].时珍国医国药,2007,18(11):2779-2780.
[8]第司·桑杰嘉措.兰塔布[M].赤峰:内蒙古科学技术出版社,2013:38-39.
[9]赞巴拉朝吉丹金彭日来.蒙医金匮[M].呼和浩特:内蒙古人民出版社,2014:20-21.
[10]乌力吉.蒙医方剂选编[M].赤峰:内蒙古科学技术出版社,2015:33-34.
[11]那生桑等.内蒙古蒙药炮制规范(2015年版)[M].呼和浩特:内蒙古人民出社,2016:20-21.
[12]内蒙古自治区食品药品监督管理局.内蒙古蒙药制剂规范(2007年版)[M].呼和浩特:内蒙古人民出社,2007:附录8.
[13]陈奇.中药药理研究方法学[M].北京:人民卫生出版社,2011:111-112.
[14]郑蕾,杨若飞,杨甫,等.木鳖子提取物对小鼠急性毒性实验研究[J].中国药师,2017,20(12):2242-2290.
[15]奥·乌力吉,布和巴特尔.传统蒙药与方剂[M].赤峰:内蒙古科学技术出版社,2013:194-195,50-51.
[16]蒙医学编辑委员会.中国医学百科全书·蒙医学[M].上海:上海科学技术出版社,243-244.
[17]国家药典委员会.中华人民共和国卫生部药品标准:藏药(第一册)[M].北京:人民卫生出版社,1995:217.
(收稿日期:2020-02-20 编辑:陶希睿)

