多环咪唑啉缓蚀剂的合成及其缓蚀作用
张晨峰,扈俊颖,钟显康
(西南石油大学 石油与天然气工程学院,成都610500)
在油气田开采过程中,地层水矿化度高、p H低等因素会对井筒、管道等造成较为严重的腐蚀[1]。为抑制管道腐蚀,最常用的方法是加入缓蚀剂。目前的研究主要针对咪唑啉缓蚀剂、酰胺类缓蚀剂、喹啉类缓蚀剂和季铵盐类缓蚀剂等,这些缓蚀剂多为有机缓蚀剂[2-4]。大多数有机物缓蚀剂含有O、N、P、S等元素,起到吸附在金属表面的作用。基于目前的研究进展,发现咪唑啉衍生物在CO2环境中具有良好的缓蚀作用,普遍认为咪唑啉环上N原子可以与铁轨道上的空d轨道结合,增强缓蚀剂分子在钢表面的吸附,从而提高缓蚀率。咪唑啉缓蚀剂作为绿色缓蚀剂,经济高效,安全低毒,在管道防腐蚀方面应用广泛[5-6]。
本工作主要通过引入多个咪唑啉环增强吸附性能,改善缓蚀剂的缓蚀性。首先合成双子咪唑啉和具有四个环的咪唑啉缓蚀剂,采用失重法、电化学法,形貌观察等评价了自制缓蚀剂的性能,以期为其推广应用提供理论基础。
1 试验
1.1 缓蚀剂的合成与表征
将0.1 mol月桂酸和50 mL二甲苯加入四口烧瓶中,采用加热套加热至90℃时,用恒压分液漏斗滴入0.06 mol四乙烯五胺,继续升温至140℃,直至分水器中没有明显的水产生,表明酰胺化反应完成,再采用梯度升温法升温至240℃进行环化反应,反应6~8 h,合成双环月桂酸咪唑啉缓蚀剂(SAI),SAI呈深棕色粘稠状液体,易溶于有机溶剂。
将0.05 mol癸二酸,0.06 mol四乙烯五胺和50 mL二甲苯加入四口烧瓶中,升温至140℃至分水器中没有明显的水产生,停止加热后加入0.1 mol月桂酸至烧瓶中,重新升温至140℃,反应时间为2~4 h,采用梯度升温法升温至240℃,反应时间为6~8 h,合成四环月桂酸咪唑啉缓蚀剂(LAI)。LAI为深黄色粘稠状液体,易溶于有机溶剂。2种缓蚀剂的结构式见图1。
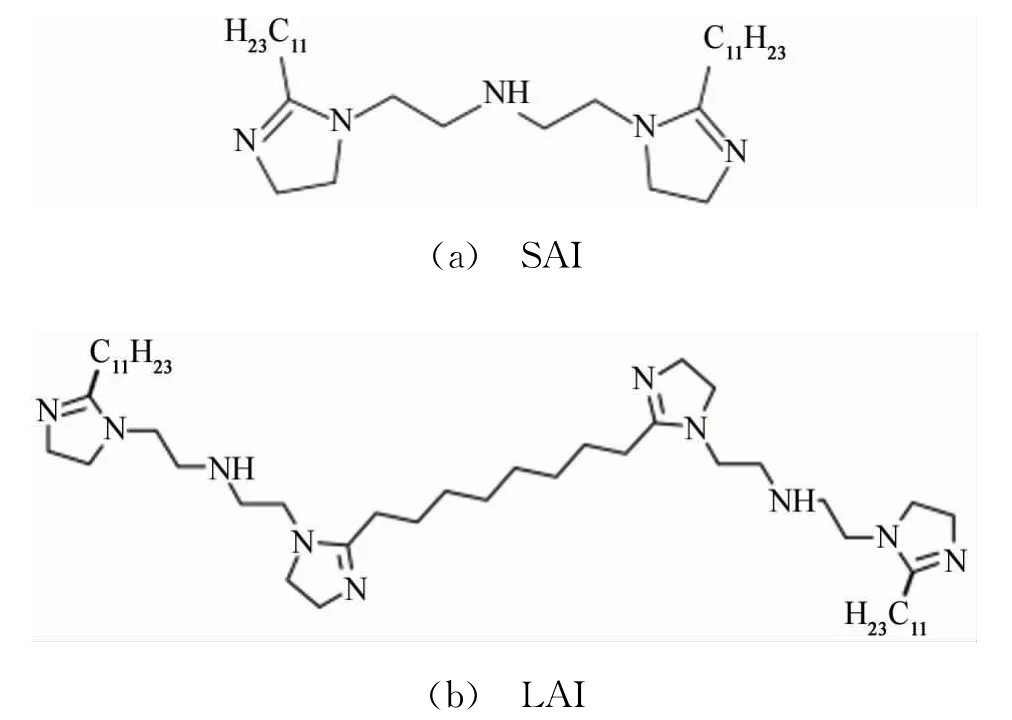
图1 SAI和LAI的结构式Fig.1 Structural for mula of SAI(a)and LAI(b)
采用红外光谱对SAI和LAI这2种缓蚀剂进行表征,结果见图2。由图2(a)可见,3 286 c m-1处为N-H伸缩振动峰;2 925 c m-1和2 852 c m-1处分别为CH3-和CH2-的伸缩振动峰;1 647 c m-1处为C=N双键伸缩振动吸收峰;1 544 c m-1处为CN单键伸缩振动峰。由图2(b)可见,3 303 c m-1处为N-H伸缩振动峰;2 925 c m-1和2 852 c m-1处分别为CH3-和CH2-的伸缩振动峰;1 647 c m-1处为C=N双键伸缩振动吸收峰;1 550 c m-1处为C-N单键伸缩振动峰,这与之前的文献报道一致[17],证明本工作合成的是咪唑啉衍生物SAI和LAI。

图2 SAI(a)和LAI(b)的红外光谱图Fig.2 Infrared spectrums of SAI(a)and LAI(b)
1.2 缓蚀剂的性能评价
1.2.1失重法
试验材料为L360钢(下同),将其加工成40 mm×13 mm×2.5 mm的试片,试验前用丙酮和乙醇去除试片表面油污,用N2吹干后称量并测量尺寸,每组试验用3个平行试样。试验溶液为含不同量缓蚀剂的模拟地层水溶液,试验温度为60℃,试验时间为72 h。试验前,向试验溶液中通入N2以去除溶液中的O2,试验过程中,持续通入CO2。试验结束后,使用去膜液去除试片表面腐蚀产物,用乙醇清洗干净后,吹干称量,并按式(1)计算腐蚀速率[7]。模拟地层水的离子含量见表1。
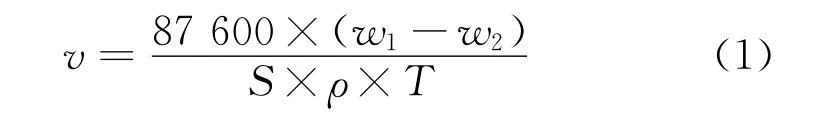
式中:w1和w2分别为试验前后试片的质量;S为试片浸入溶液中的总表面积;ρ为试片密度;T为试验时间。用式(2)计算缓蚀率:

式中:v0和v1分别为试片在未添加和添加缓蚀剂试验溶液中的腐蚀速率。

表1 模拟地层水的化学成分Tab.1 Chemical composition of simulated for mation water mg/L
1.2.2电化学法
电化学试验在CS310 H电化学工作站上完成。采用三电极体系,试样工作面积为1 c m2,非工作面用环氧树脂封装,辅助电极为铂电极,参比电极为饱和甘汞电极(SCE),试验前试样工作面用砂纸(600~1 200号)逐级打磨。电化学阻抗频率为10-2~105Hz,交流幅值为10 mV,采用式(3)计算由电化学阻抗谱法测得的缓蚀率[8]。极化曲线扫描范围为-0.15~0.2 V,扫描速率为20 mV/min,采用式(4)计算由极化曲线法测得的缓蚀率。
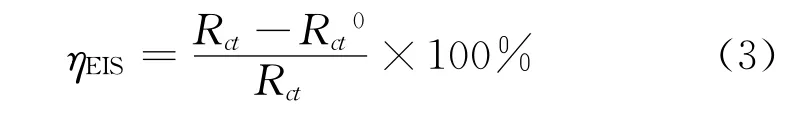
式中:Rct0和Rct分别为加入缓蚀剂前后的电荷转移电阻。

式中:J0和J分别为加入缓蚀剂前后的腐蚀电流密度。
1.2.3形貌观察和成分分析
利用扫描电子显微镜(SEM)观察试片在不含和含缓蚀剂试验溶液中腐蚀后的表面形貌,以判断不同的腐蚀类型。通过EDS分析腐蚀产物组成和缓蚀剂的吸附情况。
2 结果与讨论
2.1 失重法
由表2可见:在不含缓蚀剂的试验溶液中,试片腐蚀速率高达0.473 mm/a,试片出现严重腐蚀。随着缓蚀剂的加入,试片的腐蚀速率明显降低,基本控制在0.1 mm/a以内,这说明SAI和LAI都具有良好的缓蚀效果。当缓蚀剂的加入量为400 mg/L时,SAI与LAI达到最高缓蚀率,分别为88.58%和93.87%。在加注量相同的条件下,相比SAI缓蚀剂,LAI缓蚀剂的抑制腐蚀效果更好。

表2 试样在含不同量缓蚀剂的CO2模拟地层水环境中的腐蚀速率及SAI和LAI的缓蚀率Tab.2 Corrosion rates of samples in simulated for mation water containing different content of inhibitor under saturated CO2 condition and the inhibition rates of SAI and LAI
2.2 电化学阻抗谱
由图3可见,Nyquist图谱中,容抗弧呈现扁平的半圆形,这主要是因为电极表面的不均匀性和电极表面活性位点分布。试验结果显示,在未加缓蚀剂的试验溶液中,容抗弧半径最小,电极受CO2腐蚀严重。根据相关文献报道,容抗弧半径越大,缓蚀剂的缓蚀作用越好[9-10]。加入SAI和LAI后,容抗弧半径随缓蚀剂量的增加而增大,且都在缓蚀剂加入量为400 mg/L时达到最大。
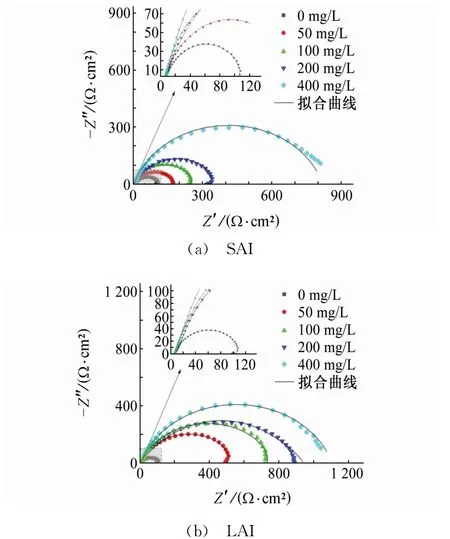
图3 试样在含不同量缓蚀剂试验溶液中的电化学阻抗谱Fig.3 EISof samples in simulated for mation water containing different content of SAI(a)and LAI(b)
图4为电化学阻抗谱的等效拟合电路,其中图4(a)为不含和含高浓度缓蚀剂条件下的阻抗谱拟合电路,图4(b)为含低浓度缓蚀剂条件下的阻抗谱拟合电路。图4中,Rs为溶液电阻,Rct为电荷转移电阻,CPE为常相位角元件,RL为电阻,L为电感元件。由于弥散效应的存在,常用CPE代替理想电容[11]。
由表3可见:随着SAI和LAI量的增加,电荷转移电阻增大,说明缓蚀剂主要通过控制电荷转移电阻的方式来抑制金属腐蚀,缓蚀剂分子取代水分子在钢表面形成了一层吸附膜。当缓蚀剂加入量为4 00 mg/L时,SAI和LAI的缓蚀率达到最大,分别为86.32%和89.94%,LAI的缓蚀性能比SAI的更好。

图4 不同条件下电化学阻抗谱的等效电路图Fig.4 Equivalent circuit diagrams of EISunder different conditions:(a)without or containing high concentrations of inhibitor;(b)containing low concentrations of inhibitor

表3 电化学阻抗谱的拟合结果Tab.3 Fitting results of EIS
2.3 极化曲线
由图5和表4可见:相比于不含缓蚀剂的空白溶液,加入缓蚀剂后,阳极和阴极塔菲尔斜率ba和bc明显减小,这表明缓蚀剂同时抑制了电极表面的阳极和阴极反应,腐蚀电流密度也相应降低。此外,加入缓蚀剂后,自腐蚀电位有所上升,但电位变化小于±85 mV,说明这两种缓蚀剂都为混合型缓蚀剂,且以抑制阳极反应为主[12]。
加入缓蚀剂后,SAI和LAI在试样表面形成了膜,随着缓蚀剂量的增加,膜层变得更加致密,使试样的腐蚀速率下降,缓蚀率上升,且在缓蚀剂加入量为400 mg/L时达到最大值。LAI与SAI的主要区别为咪唑啉环数不同,可以推测随咪唑啉环数的增加,缓蚀剂的吸附性增大。同时较长的碳链起到疏水基的作用,综合影响下,膜的致密性和吸附性得到增强。
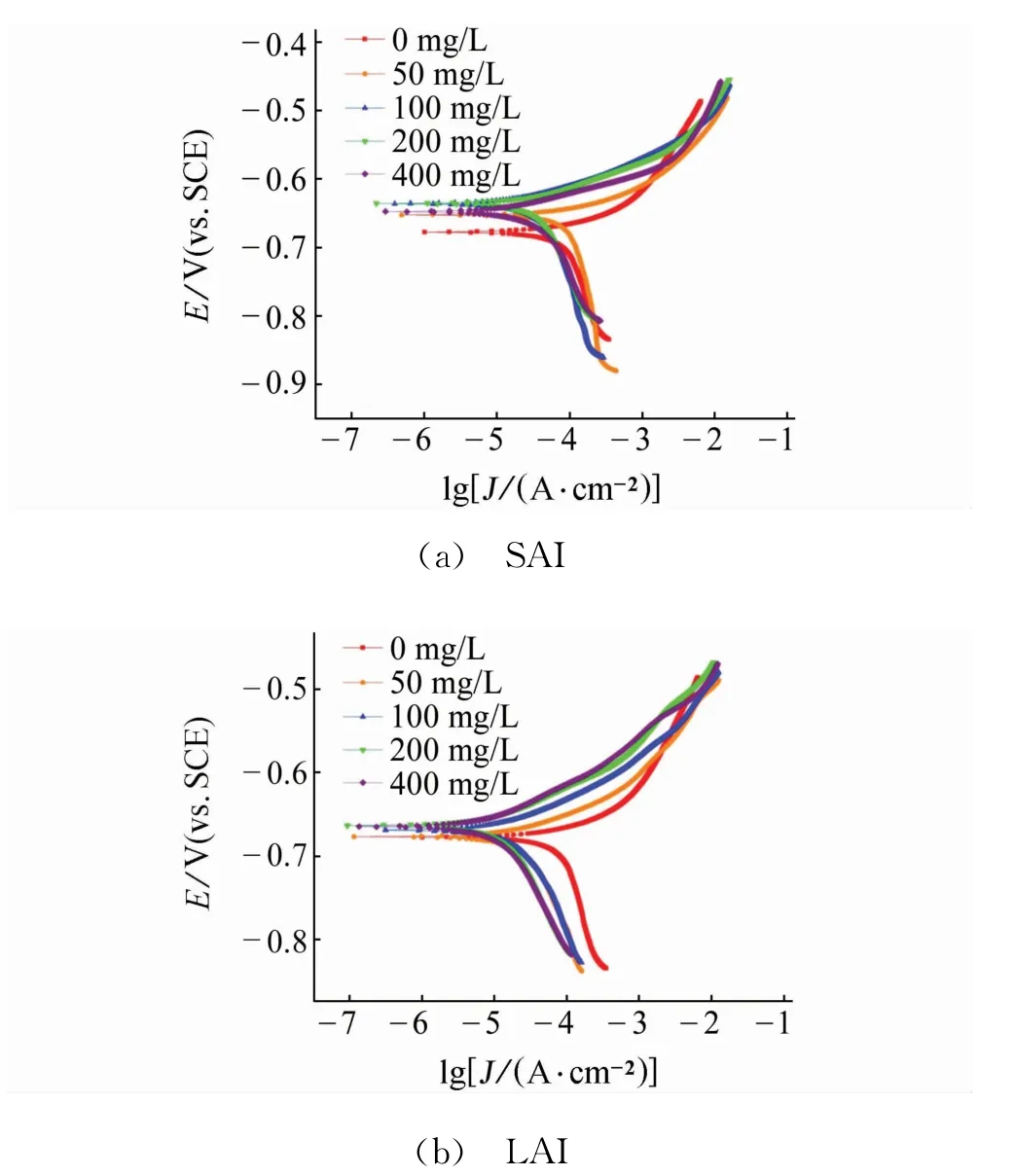
图5 试样在含不同量缓蚀剂试验溶液中的极化曲线Fig.5 Polarization curves of samples in simulated for mation water containing different content of SAI(a)and LAI(b)
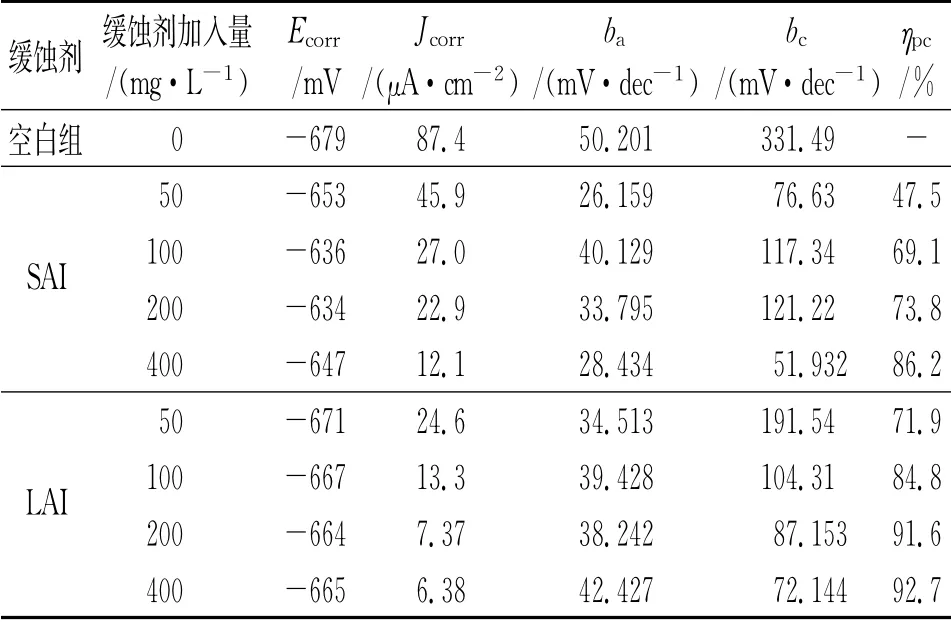
表4 极化曲线拟合结果Tab.4 Fitting results of polarization curves
2.4 吸附等温曲线
大部分有机缓蚀剂都是吸附型缓蚀剂,主要的吸附类型有物理吸附、化学吸附和两者共同作用。利用吸附等温模型,可以研究缓蚀剂的吸附方式,Freundlich,Langmuir和sips isother m都是常见的吸附模型[13]。
通过对两种缓蚀剂的试验数据进行等温吸附曲线拟合,发现Langmuir吸附等温模型的拟合结果较好,见图6。Langmuir等温吸附公式为[14]
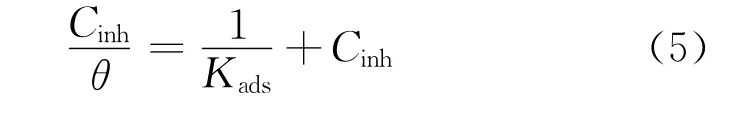
式中:Cinh为缓蚀剂浓度,mol·L-1;θ为覆盖率,%;Kads为吸附平衡常数。由上式可以计算出吸附平衡常数Kads,再通过公式(6)可以计算得到吉布斯自由能ΔGads。
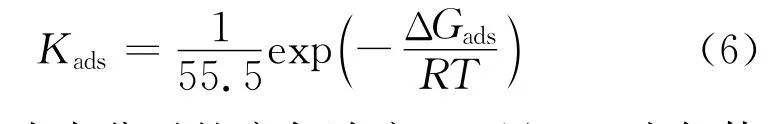
式中:55.5为水分子的摩尔浓度,mol/L;R为气体常数,8.314 J/(mol·K);T为温度,K。
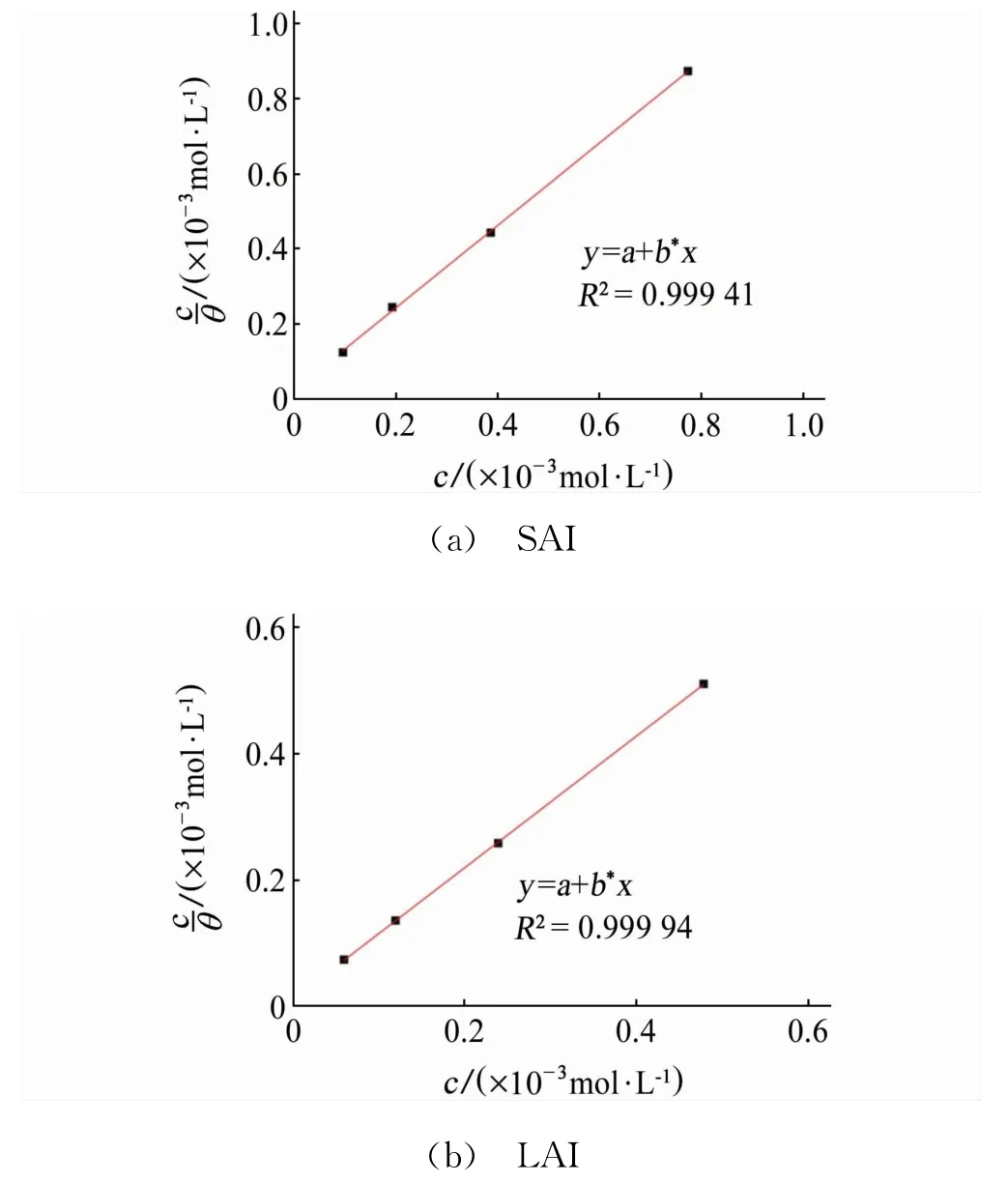
图6 SAI和LAI的Langmuir等温吸附拟合结果Fig.6 Langmuir isother mal adsorption fitting results of SAI(a)and LAI(b)

图7 试样在不含和含缓蚀剂的饱和CO2模拟地层水中腐蚀后的表面SEM形貌Fig.7 Surface SEM morphology of samples after corrosion in saturated CO2 si mulated for mation water without(a)and with(b,c)inhibitors
由表5可见:SAI和LAI的ΔGads都为负值,表明SAI和LAI都能自发吸附在试样表面。一般来说,当ΔGads<-40 kJ·mol-1时,吸附方式以化学吸附为主;当ΔGads>-20 kJ·mol-1时,吸附方式以物理吸附为主;当-20 kJ·mol-1<ΔGads<-40 kJ·mol-1时,缓蚀剂在钢的表面吸附既有物理 吸 附 也 有 化 学 吸 附[15-16]。SAI的ΔGads为-53.53 kJ·mol-1,LAI的ΔGads为-55.46 kJ·mol-1,所以都是以化学吸附作用为主且吸附作用较强。另外,LAI的吉布斯自由能比SAI的更负,说明LAI缓蚀剂的吸附作用更强,这与之前的试验结果相符。
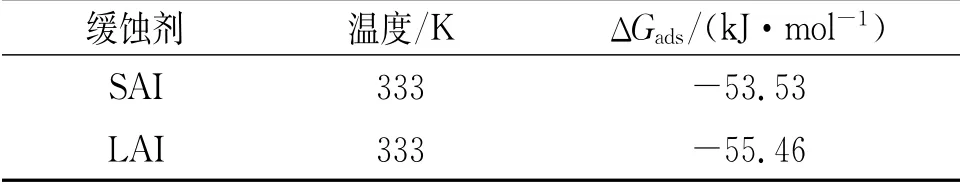
表5 SAI和LAI的ΔG ads计算结果Tab.5 ΔG ads calculation results of SAI and LAI
2.5 SEM和EDS分析
由图7可见:在不含缓蚀剂的试验溶液中腐蚀后,试样表面沉积物裂痕明显较多,腐蚀非常严重,而加入400 mg/L缓蚀剂后,试样表面沉积物裂痕减少,说明缓蚀剂已经吸附在试样表面形成一层吸附膜。由图7还可见:相比于SAI,加入LAI后,试样表面沉积物更加致密。
CO2腐蚀环境复杂,形成的腐蚀产物多样,结合能谱图分析结果,发现空白组试样表面的C和Fe含量较高,当没有缓蚀剂保护时,试样表面腐蚀的反应加剧。加入缓蚀剂后,N含量增多,说明缓蚀剂已经吸附在钢的表面,阻碍腐蚀产物的生成,起到保护金属的作用,见表6。
LAI和SAI具有相同碳链长度的疏水基团,可以有效阻隔水与钢表面的接触,减缓金属表面的腐蚀。另一方面,根据文献报道[4,6],咪唑啉环可以增强缓蚀剂在钢表面的吸附能力,主要依靠咪唑啉上的N原子和C=N双键为Fe的空d轨道提供电子。LAI拥有四个咪唑啉环,吸附的活性位点更多,使其吸附能力比SAI的更强。
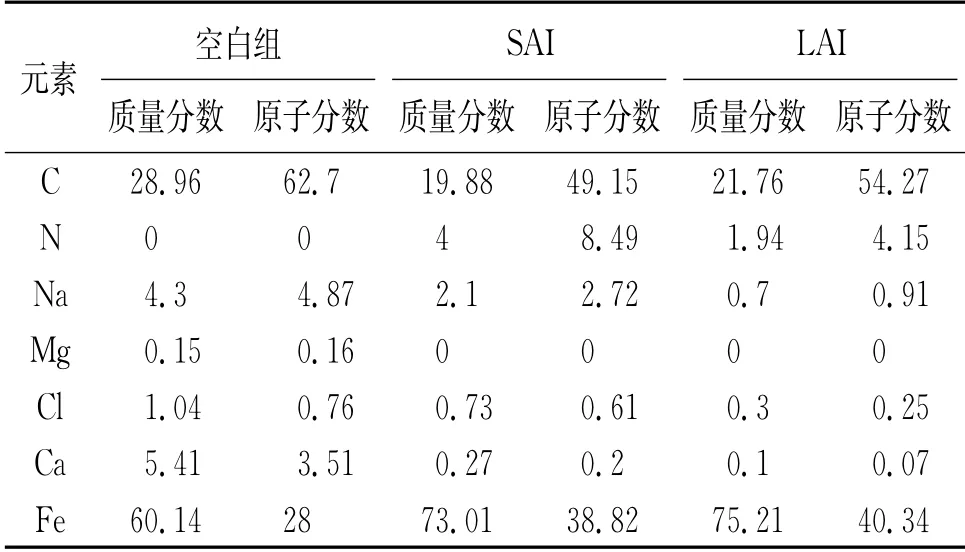
表6 试样在不含和含缓蚀剂的饱和CO2模拟地层水中腐蚀后的表面EDS分析结果Tab.6 EDSanalysis results of samples after corrosion in saturated CO2 simulated for mation water without and with inhibitors %
3 结论
(1)SAI和LAI缓蚀剂在饱和CO2的模拟地层水环境中对L360钢具有良好的缓蚀作用。通过失重法和电化学方法评价了这两种缓蚀剂,结果表明,合成的LAI具有更好的缓蚀效果,加入量为400 mg/L时,最高缓蚀率达93.87%。SAI和LAI均为混合型缓蚀剂,主要抑制阳极反应。
(2)SAI和LAI符合Langmuir吸附等温式,吸附类型以化学吸附为主,形成一层吸附膜,抑制金属的腐蚀。
(3)没有缓蚀剂情况下,试样表面腐蚀产物主要由Fe、C元素组成,加入缓蚀剂后腐蚀产物减少,表面的腐蚀减缓。

