五种人新型冠状病毒研究进展
陈荔萍 周峰
摘 要 冠状病毒是引起人类呼吸道感染的常见病原体。2003年的严重急性呼吸综合征(SARS)、2012年的中东呼吸综合征(MERS)以及新型冠状病毒肺炎(COVID-19)的暴发流行已经引起了全球对于冠状病毒的广泛关注。本文就新发现的5种人新型冠状病毒从病原学、流行病学、致病性、临床特点、病原学检测和防治等方面进行综述。
关键词 呼吸道疾病;人冠状病毒;研究进展
中图分类号:R563.1 文献标志码:A 文章编号:1006-1533(2020)20-0009-04
Research progress of five novel corona viruses
CHEN Liping1, ZHOU Feng2
(1. Department of General Practice of Dapuqiao Community Health Service Center of Huangpu District, Shanghai 200023,China; 2. Center for Disease Prevention and Control of Huangpu District, Shanghai 200023, China)
ABSTRACT Corona virus is a common pathogen that causes human respiratory tract infection. The outbreaks of severe acute respiratory syndrome(SARS) in 2003, Middle East respiratory syndrome(MERS) in 2012 and the pneumonia caused by novel corona virus infection(COVID-19) have attracted worldwide concern about corona virus. This article reviews the newly discovered five new human corona viruses in terms of etiology, epidemiology, pathogenicity, clinical characteristics, pathogenic detection and prevention and treatment.
KEY WORDS respiratory disease; human corona virus; research progress
冠状病毒在自然界中广泛存在,主要感染脊椎动物,被认为是对人类相对无害的一类病毒。但2003年严重急性呼吸综合征冠状病毒(severe acute respiratory syndrome coronavirus,SARS-CoV)的暴发流行,颠覆了人类对冠状病毒的已有认识,意识到其高致病潜能。2004年和2005年又相继发现人冠狀病毒NL63(human coronavirus NL63,HCoV-NL63)和人冠状病毒HKU1(human coronavirus HKU1,HCoV-HKU1)。而2012年9月发现的中东呼吸综合征冠状病毒(middle east respiratory syndrome coronavirus,MERS-CoV),其高病死率再次警示冠状病毒可对人类产生严重致病性。2019年12月又出现了一种新型冠状病毒——严重急性呼吸综合征冠状病毒2(SARS-CoV-2),感染疫情目前已构成全球性大流行。现就自SARS以来全球新发现的5种人新型冠状病毒的研究进展进行综述。
1 冠状病毒简介
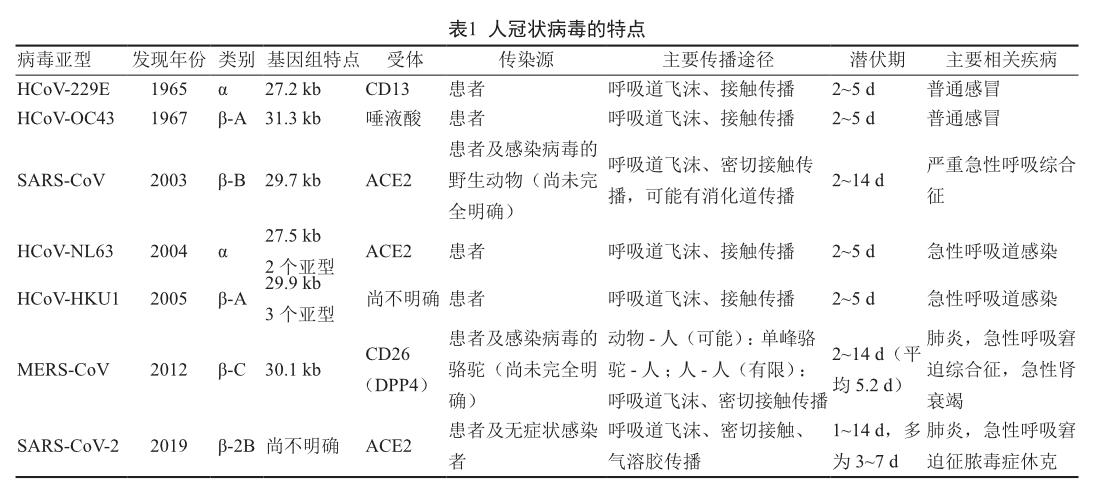
冠状病毒于1937年首次从禽类分离,是一种具有包膜的单股正链RNA病毒,直径约80~200 nm,包膜上有棘突,是已知最大的RNA病毒。1965年Tyrrell等将人鼻冲洗液接种人胚气管细胞,发现有病毒增殖,1968年被鉴定为人冠状病毒。1975年,国际病毒命名委员会正式将其命名为“冠状病毒科(coronaviridae)”,分为α、β、γ、δ 4组,其中β冠状病毒又分A、B、C、D 4个亚组[1]。目前发现能感染人的冠状病毒主要为α、β两大组。经典人冠状病毒包括2个血清型:人冠状病毒229E(human coronavirus 229E,HCoV-229E)和人冠状病毒OC43(human coronavirus OC43,HCoV-OC43)。7种人冠状病毒的特点总结见表1。
2 近年发现的5种人新型冠状病毒
2.1 SARS-CoV
2002年11月严重急性呼吸综合征(SARS)始于广东省佛山市,之后在全球32个国家和地区流行,全球累计报告发病8 422例,死亡916例,病死率近11%。SARS-CoV传染性较强,具有家庭、医院和社区聚集性感染特征,超级传播现象是SARS疫情早期的一大特点,北京市的1例患者在发病后产生四代病例,累计76例感染[2]。SARS-CoV感染常以发热为首发症状,体温一般高于38℃,可伴有畏寒、乏力、干咳、胸闷、气促,严重者发展为急性呼吸窘迫综合征(ARDS),呼吸困难和低氧血症常在发病6~12 d后出现,部分患者有腹泻等胃肠炎症状。SARS患者外周血白细胞计数通常正常,淋巴细胞减少,部分病例血小板减少。影像学检查主要表现为磨玻璃样或网格样改变的间质性炎症和斑片状阴影的实质性渗出。
SARS-CoV常用检测方法包括核酸检测和血清学检测。核酸检测主要通过逆转录-聚合酶链反应(RT-PCR)检测患者呼吸道分泌物、粪便等标本中的病毒RNA。血清学常采用酶联免疫吸附法(ELISA)和间接免疫荧光法(IFA)检测血清中特异性IgM、IgG或总抗体,其中一种抗体阳性或有4倍及以上升高具有病原学诊断意义,由于抗体出现时间较晚,故不能用作早期诊断。国内外研究者还尝试将基因芯片技术应用在病毒检测上,以提高检测的灵敏性和特异性,并可适应冠状病毒种类多且快速变异的特性,实现高通量检测[3]。
目前尚无针对SARS-CoV感染的特异性药物和疫苗,临床治疗以对症支持治疗和针对并发症的治疗为主。纪晓光等[4]在体外实验中证实干扰素α、γ均有抗SARS-CoV作用,Carbajo-Lozoya等[5]在细胞实验中发现低浓度、非细胞毒性的他克莫司(FK506)能强抑制SARS-CoV,这些研究为临床治疗SARS-CoV感染提供了实验依据。
2.2 HCoV-NL63
HCoV-NL63是2004年荷兰学者首先从1例患毛细支气管炎、结膜炎的7月龄婴儿身上分离获得。在基因进化树中,HCoV-NL63和HCoV-229E关系密切[6]。HCoV-NL63是引起上呼吸道感染的常见原因,在世界范围内广泛流行。感染者以婴幼儿居多,感染率在2%左右。HCoV-NL63感染的高峰期一般认为是在冬春季节,但不同地区存在差异。HCoV-NL63感染引起的临床症状一般比较温和,主要为发热、咳嗽、咽痛等普通感冒症状,但在婴幼儿、老年人、合并基础疾病或免疫力低下的人群中也可引起较严重的呼吸道症状。婴幼儿可引发支气管肺炎和毛细支气管炎,部分患者可伴有腹痛、腹泻等消化道症状。另外,HCoV-NL63感染与喉炎的发生相关[7-8],并可导致哮喘加剧、高热惊厥[9-10]。HCoV-NL63感染常合并其他呼吸道病毒混合感染,包括呼吸道合胞病毒、副流感病毒、甲型和乙型流感病毒等[11]。2018年广州的一项研究[12]报告了23例由HCoV-NL63引起的严重下呼吸道感染患儿,其中一半是由新亚型C3引起的,提示HCoV-NL63在持续突变,并可导致严重下呼吸道疾病。
目前,HCoV-NL63感染的实验室诊断多采用RTPCR技术,主要针对HCoV-NL63 1a、1b基因的保守片段进行检测。对HCoV-NL63感染尚无特效药物和疫苗。Pyrc等[13]设计针对HCoV-NL63棘突S基因保守序列的两个小干扰RNA(siRNA)可以抑制病毒复制,静脉注射免疫球蛋白、6-氮尿苷等有一定的抑制HCoV-NL63感染的作用。有研究发现免疫抑制剂FK506亦可抑制HCoV-NL63复制[7]。
2.3 HCoV-HKU1
HCoV-HKU1首次于2005年从1例71岁香港肺炎患者体内分离所得,有A、B、C 3种基因型,其中C型是由A、B型基因重组而成。HCoV-HKU1感染全球均有报道,发生率在0%~4.4%,中位发生率0.9%[14]。我国HCoV-HKU1感染高发于冬春季,但病毒检出率受季节和检测方法等影响,其流行趋势尚须更多研究证实。HCoV-HKU1引起上呼吸道感染主要表现为发热、流涕、咳嗽,下呼吸道感染主要引起细支气管炎和肺炎。HCoV-HKUI感染症状相对较轻,大都为自限性,但合并有基础疾病或免疫抑制的患者感染后会出现较重症状,甚至引起ARDS。有研究发现幼儿HCoV-HKU1感染与热惊厥、胃肠道疾病及急性哮喘发作有关[15-16]。
HCoV-HKU1感染的診断方法多采用RT-PCR法检测呼吸道标本中的病毒核酸。周为民等[17]构建S、N蛋白真核表达质粒转染细胞,并建立IFA血清学检测,结合RT-PCR检查可降低假阴性率。
2.4 MERS-CoV
MERS-CoV于2012年9月首次在沙特被发现,之后在全球27个国家传播。MERS-CoV是继SARS-CoV之后又一可引起严重呼吸系统疾病并有高致死率的冠状病毒。截至2019年11月底,全球共报告MERS病例2 494例,其中死亡858例,病死率为34.4%[18]。
MERS常见临床表现是发热伴寒战、咳嗽、气短、肌肉酸痛,部分有腹痛腹泻、恶心呕吐等胃肠道症状,重症病例可在一周内迅速进展为呼吸衰竭或多器官功能衰竭,特别是肾功能衰竭而危及生命[19]。老年人、免疫缺陷者和慢性病患者在感染后更易出现严重症状。实验室检查主要表现为淋巴细胞和血小板计数减少,乳酸脱氢酶、谷草转氨酶、肌酸激酶升高[20]。MERS肺炎CT特征以双侧胸膜下和基底部肺组织受累为主的广泛磨玻璃样密度影,实变影较少见,呈机化性肺炎的表现倾向[21]。
对MERS-CoV的实验室诊断主要是用RT-PCR法检测病毒RNA,以及采用ELISA、IFA、中和试验(neutralization test,NT)等方法检测血清中病毒抗体。
目前尚无针对MERS的特效药,临床上以对症支持治疗、防止并发症发生为主。恒河猴试验发现利巴韦林和干扰素α 2b联合治疗能显著改善MERS-CoV感染预后[22]。Chan等[23]发现在绒猴模型中单独或联合使用洛匹那韦/利托那韦和干扰素-b 1b均能减轻MERS-CoV感染。另有研究将MERS-CoV免疫的骆驼血清样本输注给受感染小鼠,小鼠肺组织病理学改变有减轻,提示康复者血清有治疗潜力[24]。复旦大学与美国国立卫生院合作开发了对MERS-CoV具有高抑制活性的全人源单克隆抗体(m336),与MERS-CoV的结合亲和力常数达到“皮摩尔”(picomolar)级别[25]。我国学者[26]还从MERS-CoV感染治愈者血清中分离出一种全人源中和抗体MCA1,该抗体在狨猴模型中能完全抑制MERS-CoV复制。目前针对MERS-CoV的疫苗尚处于实验室研究阶段。
2.5 SARS-CoV-2
2019年12月,湖北省武汉市陆续出现不明原因肺炎病例,从患者支气管肺泡灌洗液中发现一种新型冠状病毒,国际病毒分类委员会将其命名为SARSCoV-2[27]。研究显示SARS-CoV-2与蝙蝠SARS样冠状病毒(bat-SL-CoVZC45)同源性达85%以上,其基因特征与SARS-CoV和MERS-CoV有明显区别[28]。世界卫生组织将SARS-CoV-2感染的疾病命名为2019冠状病毒病(COVID-19)。SARS-CoV-2短时间内迅速在全球流行,截至2020年5月20日,国内累计确诊84 505例,死亡4 645例,国外累计确诊4 890 010例,死亡320 659例。
COVID-19以发热、乏力、干咳为主要临床表现,少数患者伴有腹泻等胃肠道症状。轻型患者仅表现为低热、轻微乏力等,无肺炎表现。重症患者多在发病一周后出现呼吸困难和(或)低氧血症,严重者快速进展为ARDS、脓毒症休克、难以纠正的代谢性酸中毒和凝血功能障碍等。重型、危重型患者病程中可为中低热,甚至无明显发热。发病早期外周血白细胞总数正常或减少,淋巴细胞计数减少,部分患者可出现肝酶、乳酸脱氢酶、肌酶和肌红蛋白水平增高;部分危重者可见肌钙蛋白水平增高。多数患者C反应蛋白水平和血沉速率升高,降钙素原水平正常。胸部CT早期呈现多发小斑片影及间质改变,肺外带明显,进而发展为双肺多发磨玻璃影、浸润影,严重者可出现肺实变,胸腔积液少见。
中国疾病预防控制中心对国内72 314例SARSCoV-2感染病例进行总结发现,81%为轻症,14%为重症,5%是危重。有既往合并癥的患者病死率较高,其中合并心血管疾病患者病死率为10.5%,糖尿病者为7.3%,慢性呼吸系统疾病者为6.3%,高血压者为6.0%,癌症者为5.6%。COVID-19目前的粗病死率为2.6%,确切的病死率尚需更多流行病学数据[29]。
对SARS-CoV-2感染的检测主要通过对呼吸道标本或血液标本进行实时荧光RT-PCR检测、病毒基因测序,以及血清特异性IgM和IgG检测。
尚未发现有针对SARS-CoV-2特效的抗病毒治疗方法和疫苗。治疗上以对症支持治疗、氧疗、循环支持为主。《新型冠状病毒感染的肺炎诊疗方案(试行第七版)》中推荐了可能有效的抗病毒药物,包括a-干扰素、洛匹那韦/利托那韦、利巴韦林、磷酸氯喹、阿比多尔等。腺苷类似物瑞德西韦在体外实验中被证实对SARS-CoV-2有抑制作用,在美国首例COVID-19患者的诊疗过程中表现出较好疗效[30],但其治疗有效性还需进一步的临床试验评估验证。其他有治疗前景的抗病毒药物还有达芦那韦、法匹拉韦、单克隆抗体等。康复者血浆主要用于病情进展较快、重型和危重型患者。此外,中医药治疗发挥了中医扶正祛邪和多靶点治疗的特点,协同西医治疗手段,取得了良好临床疗效。
3 总结
5种人新型冠状病毒中,HCoV-NL63、HCoV-HKU1致病性相对较弱,免疫功能低下的人群如婴幼儿和老年人为主要感染对象。SARS-CoV、MERS-CoV和SARSCoV-2在种属进化上均与蝙蝠冠状病毒关系密切,具有人际传播能力,可引起重症呼吸道综合征,老年人和有慢性基础疾病者感染后更易出现严重症状和较高病死率。目前对于冠状病毒在病源动物和人之间的传播途径、病毒变异、抗病毒药物及疫苗的研制等问题上仍有待更多深入研究。同时,必须对未来可能出现的其他新型冠状病毒进行密切监测。
参考文献
[1] 沈军, 俞蕙, 朱启镕. 人冠状病毒与人类呼吸道感染[J].中国循证儿科杂志, 2013, 8(2): 149-153.
[2] Shen Z, Ning F, Zhou W, et al. Superspreading SARS events, Beijing, 2003[J]. Infect Dis, 2004, 10(2): 256-260.
[3] 周琦, 赖平安, 汪琳, 等. 基因芯片技术快速检测SARS病毒[J]. 检验检疫科学, 2005, 15(6): 20-22.
[4] 纪晓光, 赵艳红, 张敏, 等. α干扰素和γ干扰素以及联合作用体外抗SARS-CoV试验研究[J]. 解放军药学学报, 2008, 24(3): 268-269.
[5] Carbajo-Lozoya J, Müller MA, Kallies S, et al. Replication of human coronaviruses SARS-CoV, HCoV-NL63 and HCoV-229E is inhibited by the drug FK506[J]. Virus Res, 2012, 165(1): 112-117.
[6] Pyrc K, Dijkman K, Deng L, et al. Mosaic structure of human coronavirus NL63, one thousand years of evolution[J]. J Mol Biol, 2006, 364(5): 964-973.
[7] vander Hock L, Sure K, Ihorst G, et al. Croup is associated with the novel coronavirus NL63[J]. PLoS Med, 2005, 2(8): e240.
[8] Sung JY, Lee HJ, Eun BW, et al. Role of human coronavirus NL63 in hospitalized children with croup[J]. Pediatr Infect Dis J, 2010, 29(9): 822-826.
[9] Leung TF, Li CY, Lam WY, et al. Epidemiology and clinical presentations of human coronavirus NL63 infections in Hong Kong children[J]. J Clin Microbiol, 2009, 47(11): 3486-3492.
[10] Chiu SS, ChanKH, Chu KW, et al. Human coronavirus NL63 infection and other coronavirus infections in children hospitalized with acute respiratory disease in Hong Kong, China[J]. Clin Infect Dis, 2005, 40(12): 1721-1729.
[11] Debiaggi M, Canducci F, Ceresola ER, et al. The role of infections and coinfections with newly identified and emerging respiratory viruses in children[J]. Virol J, 2012, 9: 247.
[12] Wang Y, Li X, Liu W, et al. Discovery of a subgenotype of human coronavirus NL63 associated with severe lower respiratory tract infection in China, 2018[J]. Emerg Microbes Infect, 2020, 9(1): 246-255.
[13] Pyrc K, Bosch BJ, Berkhout B, et al. Inhibition of human coronavirus NL63 infection at early stages of the replication cycle[J]. Antimicrob Agents Chemother, 2006, 50(6): 2000-2008.
[14] Woo PC, Lau SK, Yip CC, et al. More and more coronaviruses: human coronavirus HKU1[J]. Viruses, 2009, 1(1): 57-71.
[15] Woo PC, Yuen KY, Lau SK, et al. Epidemiology of coronavirus-associated respiratory tract infections and the role of rapid diagnostic tests: a prospective study[J]. Hong Kong Med J, 2012, 18 Suppl 2: 22-24.
[16] Amini R, Jahanshiri F, Amini Y, et al. Detection of human coronavirus strain HKU1 in a 2 years old girl with asthma exacerbation caused by acute pharyngitis[J]. Virol J, 2012, 9: 142.
[17] 周為民, 王文玲, 谭文杰, 等. 人冠状病毒HKU1 血清学检测方法的建立及其初步应用[J]. 中华实验和临床病毒学杂志, 2010, 24(5): 376-379.
[18] World Heath Organization. MERS situation update, November 2019[EB/OL]. (2019-11)[2020-02-08]. https://www.who.int/ emergencies/mers-cov/en/.
[19] 中华人民共和国国家卫生和计划生育委员会. 中东呼吸综合征病例诊疗方案[EB/OL]. (2013-09-05)[2020-02-08]. http://www.nhc.gov.cn/yzygj/s3594r/201309/ d38acc2225bb42fcad5c9f60bdb7cfd6.shtml.
[20] Al-Tawfiq JA, Assiri A, Memish ZA. Middle East respiratory syndrome novel corona MERS-CoV infection. Epidemiology and outcome update[J]. Saudi Med J, 2013, 34(10): 991-994.
[21] Ajlan AM, Ahyad RA, Jamjoom LG, et al. Middle East respiratory syndrome coronavirus(MERS-CoV)infection: chest CT findings[J]. AJR Am J Roentgenol, 2014, 203(4): 782-787.
[22] Falzarano D, de Wit E, Rasmussen AL, et al. Treatment with interferon-α2b and ribavirin improves outcome in MERSCoV-infected rhesus macaques[J]. Nat Med, 2013, 19(10): 1313-1317.
[23] Chan JF, Yao Y, Yeung ML, et al. Treatment with lopinavir/ ritonavir or interferon-β1b improves outcome of MERSCoV infection in a nonhuman primate model of common marmoset[J]. J Infect Dis, 2015, 212(12): 1904-1913.
[24] Zhao J, Perera RA, Kayali G, et al. Passive immunotherapy with dromedary immune serum in an experimental animal model for Middle East respiratory syndrome coronavirus infection[J]. J Virol, 2015, 89(11): 6117-6120.
[25] Ying T, Du L, Ju TW, et al. Exceptionally potent neutralization of Middle East respiratory syndrome corona virus by human monoclonal antibodies[J]. J Virol, 2014, 88(14): 7796-7805.
[26] Chen Z, Bao L, Chen C, et al. Human neutralizing monoclonal antibody inhibition of Middle East respiratory syndrome coronavirus replication in the common marmoset[J]. J Infect Dis, 2017, 215(12): 1807-1815.
[27] Xu X, Chen P, Wang J, et al. Evolution of the novel coronavirus from the ongoing Wuhan outbreak and modeling of its spike protein for risk of human transmission[J]. SCI China Life Sci, 2020, 63(3): 457-460.
[28] Zhu N, Zhang D, Wang W, et al. A novel coronavirus from patients with pneumonia in China, 2019[J]. N Engl J Med, 2020, 382(8): 727-733.
[29] Wu Z, McGoogan JM. Characteristics of and important lessons from the coronavirus disease 2019 (COVID-19) outbreak in China[J]. JAMA, 2020 Feb 24. doi: 10.1001/ jama.2020.2648.
[30] Holshue ML, DeBolt C, Lindquist S, et al. First case of 2019 novel coronavirus in the United States[J]. N Engl J Med, 2020, 382(10): 929-936.

