TETA/AMP复合水基CO2吸收液研究
孙路长,连少翰,王凯亮,王争荣,张士明,韩文荃,宋春风
(1.中国华电科工集团有限公司,北京 100160;2.天津大学 环境科学与工程学院,天津 300354;3.江苏华电句容发电有限公司,江苏 镇江 212000)
0 引 言
近年来,温室效应导致的全球变暖对人类生活产生了不可忽视的影响[1],如海平面升高、阶段性极热天气频发、区域性干旱等。2018年,联合国政府间气候变化专门委员会发布《全球升温1.5 ℃》特别报告,指出人类活动造成的温室气体排放是全球变暖的根源。而温室气体中CO2占比高达60%,因此实现CO2减排是控制温室效应最有效的手段。CO2捕集、利用和封存(CCUS)是实现CO2减排的主要途径。根据《BP世界能源统计年鉴》中的数据,2018年我国一次能源消费中煤炭占比约为58%,我国能源结构仍以煤炭为主。因此燃煤锅炉是国内最主要的CO2集中排放源之一,针对燃煤机组开展CO2捕集对于国内推进CO2减排具有重要意义。常规的燃煤电厂CO2捕集技术分为燃烧前捕集、富氧燃烧和燃烧后捕集3种,其中燃烧后捕集是对煤炭燃烧后产生的烟道气进行CO2捕集,其优点是原理简单,与电厂现有机组匹配性好,升级改造容易,是目前多数燃煤电厂采用的捕集方案。
化学吸收法是CO2燃烧后捕集最成熟的燃烧后CO2捕集工艺之一,已在烟气碳捕集领域得到大规模应用[2-3]。其中单乙醇胺(MEA)是常用的化学吸收液,但单一的MEA作为吸收液有明显的缺点,如溶剂损失大、再生能耗高、腐蚀容器等[4-5]。常见的化学吸收剂还有热碱、离子液体[6]等,但其能耗高、成本昂贵的缺点阻碍了大规模应用推广。因此,为了克服单一吸收液固有的性质缺陷,开发新一代混合吸收剂成为CO2吸收领域的研究重点[7-8]。康顺吉等[9]认为以甲基二乙醇胺(MDEA)为基础的可循环复合胺溶液相比于传统MEA溶液能有效缓解环境压力。陆诗建等[10]认为以烯基胺为主吸收剂的复合胺溶液能有效改善传统MEA工艺对管道与设备腐蚀严重等问题,并筛选出MDEA/TETA(三乙烯四胺)复合胺溶液的最佳配比为质量比5∶20∶75(MDEA/TETA/水),并对其循环吸收-解吸过程进行了测试。朱立宾等[11]对不同配比的二乙烯三胺/哌嗪(DETA/PZ)复配吸收液进行筛选,得到最优配比为5∶1。程毅[12]探究了苄胺分别与DEEA、DMEA混合后的复配吸收液CO2吸收解吸特性,发现其再生性能相比MEA溶液有显著提升。
三乙烯四胺(TETA)的分子结构中具有多个氨基,能提供更多的CO2反应位点[13]。而空间位阻胺具有吸收速率快、腐蚀性低等优点。本文合成了以2-氨基-2-甲基-1-丙醇(AMP)为基础的TETA/AMP复合水基吸收液,并用于燃煤电厂烟气中CO2吸收。采用模拟烟气进行测试,对复合水基吸收液的吸收-解吸性能进行了研究,优选出最佳比例,为工业应用提供理论基础。此外,目前对于新型复合吸收液的研究主要通过小试试验进行复配方案的筛选、参数优化等。然而,由于复配组合的多样性,筛选工作极其复杂繁重。本文拟采用量子化学计算的方式,对复配体系的形成机理与规律进行探究,为复配体系的设计提供指导。
1 试 验
1.1 试验材料
试验药品为:AMP(2-氨基-2-甲基-1-丙醇,分析纯),TETA(三乙烯四胺,分析纯),去离子水。CO2(>99.99%),N2(>99.99%)。
1.2 试验流程
试验装置如图1所示。
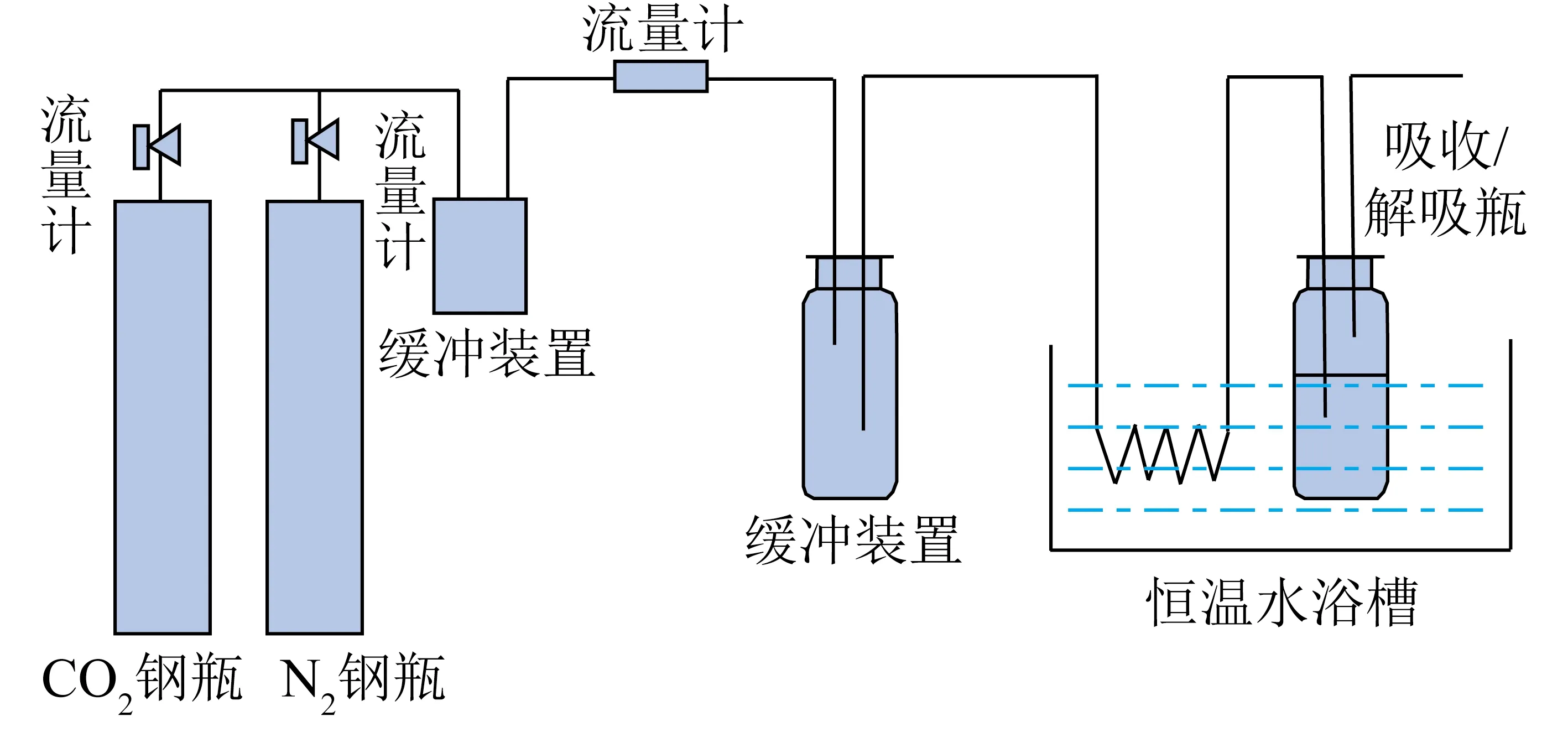
图1 循环吸收试验装置示意
1.2.1吸收试验
吸收试验采用自制装置完成,CO2与N2按比例配气(12% CO2+88% N2,模拟燃煤机组排放的烟气)后,经缓冲瓶充分混匀后进入吸收瓶进行鼓泡吸收,缓冲瓶、吸收瓶及进气管路均置于恒温水浴槽中以确保吸收温度。参照某燃煤电厂CO2吸收塔进气的温度,将吸收过程中体系温度控制为50 ℃。吸收量采用时间间隔法测定。通过测量不同时间吸收瓶质量变化,对比不同吸收液配方的吸收情况。
1.2.2再生试验
再生(解吸)试验与吸收试验条件基本相似,采用纯N2吹脱的方式实现。经过预热后的吹脱气鼓入吸收瓶内进行解吸。解吸时体系温度控制在80 ℃。解吸量采用时间间隔法进行测试。
1.2.3量子化学计算
采用Gaussian 09软件对单个TETA、AMP分子及复合分子团簇进行结构优化,计算过程中基组选择b3lyp/6-31G*,并进行振动分析,计算体系总能量[14]。此外,对分子范德华表面静电势分布进行计算通过绘制填色图的方式实现电势分布可视化,该过程通过GaussView软件实现。常用的范德华表面定义为电子密度为0.001的等值面,因此首先在分子表面利用格点数据产生电子密度为0.001的等值面,再填入不同的颜色实现电子密度可视化区分,最终将颜色格式设置为过度以实现原子位置与电子密度的同步可视化。络合能Ec的计算公式[15]为
Ec=EAB-(EA+EB),
(1)
式中,EA、EB分别为物质A、B的体系总能量;EAB为由物质A、B形成的体系总能量。
2 结果与讨论
2.1 吸收能力
参照某热电厂CO2吸收液浓度,吸收液均为质量分数20%的水基吸收液,复配比例以AMP+TETA总质量占吸收液总质量20%为原则,通过改变复配溶液中AMP与TETA比例(1∶1、2∶1、3∶1),探究复配吸收液的最优配比,配比方案见表1。
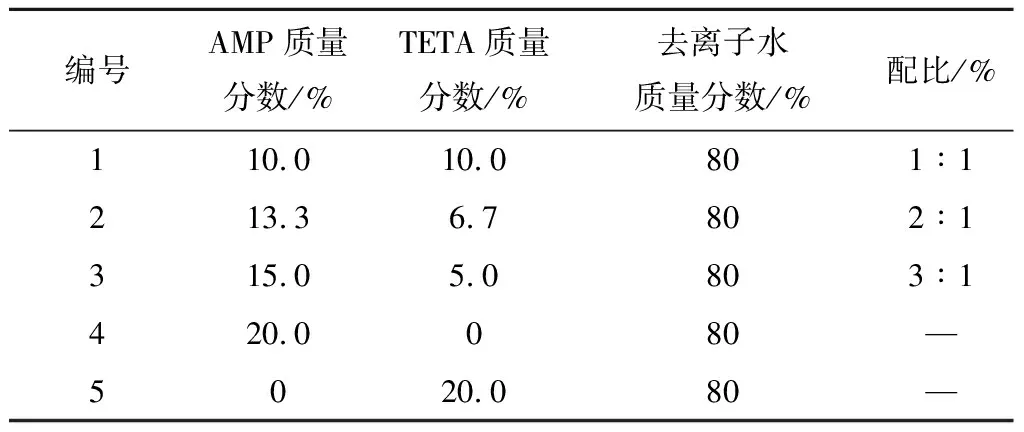
表1 AMP/TETA复配水基吸收液配比
根据时间间隔法测定得到的数据,绘制吸收量-时间曲线,如图2所示。随着TETA在吸收液中占比提高,总吸收量逐渐上升。吸收液10%AMP+10%TETA、13%AMP+7%TETA、15%AMP+5%TETA、20%AMP的最高吸收量分别为0.056、0.049、0.047、0.031 g/g。同20% AMP相比,10%AMP+10%TETA的总吸收量高出近1倍。说明TETA的加入大幅提升了复配溶液的吸收能力,在复配体系中起增大吸收容量的作用。这是因为TETA作为一种多聚胺(具有2个伯胺基和2个仲胺基基团),这些胺基基团在吸收过程中作为反应位点与CO2分子相互作用,进而通过化学反应或氢键作用将CO2分子固定在吸收液中,因此复配吸收液体系表现出较高的CO2吸收负荷。
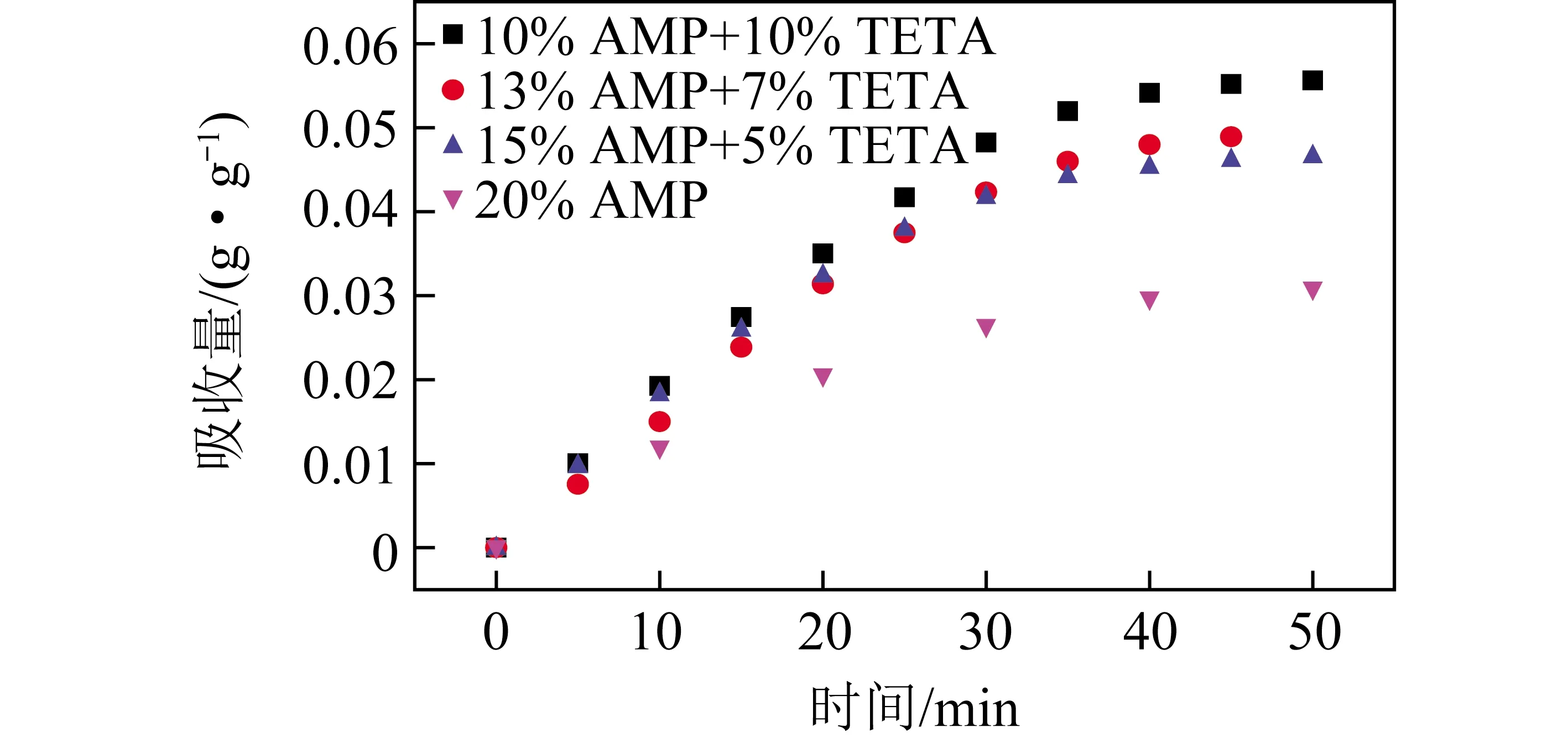
图2 TETA/AMP复合水基吸收液吸收量-时间对比
不同配比吸收液吸收CO2速率对比如图3所示。从整体趋势来看,所有吸收液的吸收速率随着吸收时间延长逐渐降低。在吸收初始阶段,即吸收液处于无CO2状态时,13% AMP+7% TETA的吸收液吸收速率最低;而随着吸收过程的持续进行,其吸收速率与配比为10% AMP+10% TETA的吸收液吸收速率基本一致。在整个吸收过程中,10% AMP+10% TETA吸收液优势明显,说明TETA的加入对提高吸收速率有促进效果。原因为TETA含有较多的亲CO2位点,在吸收过程中,AMP分子借助于空间位阻作用能更快捕获CO2分子,然后将其传递给TETA的反应位点进行储存,通过TETA与AMP分子间协同快速的捕获-转移过程促进了复配吸收液整体吸收速率的大幅提升。

图3 不同配比TETA/AMP复合水基吸收液吸收速率对比
2.2 再生能力
为了考察复合吸收液的再生性能,采用氮气吹脱的方式对其进行了解吸试验测试,结果如图4所示。可知15% AMP+5% TETA的吸收液能最快完成解吸,而10% AMP+10% TETA的吸收液最慢。说明从饱和状态到解吸完成所用时间与AMP在复配体系中的含量呈反相关,AMP在吸收液中的占比越高,复配溶液的解吸耗时越短,证明AMP在氮气吹脱过程中更易解吸,因此将其引入复合吸收液有利于降低解吸能耗。其实质是由于AMP作为一种空间位阻胺,与氮原子相连的碳原子是带有支链的取代基,进而产生明显的空间位阻效应。因此,AMP与CO2的反应产物稳定性较低,可在较低温度下再生,从而具有较高的再生效率和重复利用性。
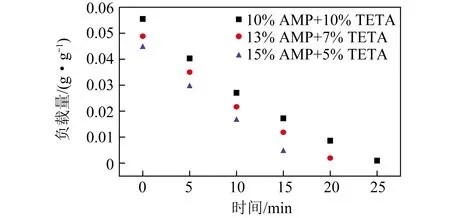
图4 TETA/AMP复合水基吸收液解吸过程负载量对比
不同配比TETA/AMP复合水基吸收液解吸速率对比如图5所示。可知15% AMP+5% TETA的吸收液解吸速率在整个时间尺度上都处于较高水平。在吸收液载荷较高的解吸初期,10% AMP+10% TETA的解吸速率与15% AMP+10% TETA基本相似,而在解吸后期的差距较大,说明AMP对复配溶液的解吸有促进作用。
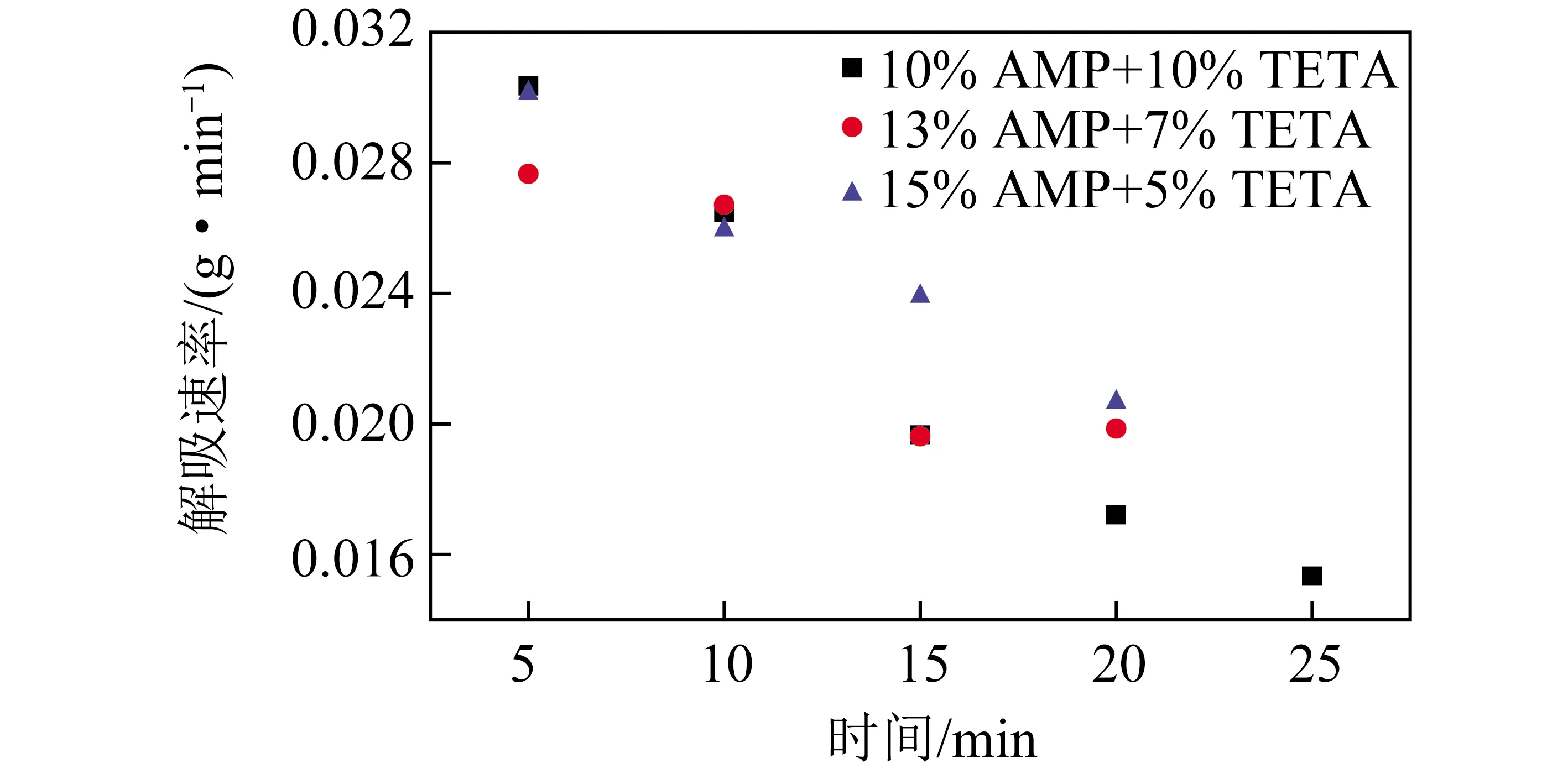
图5 不同配比TETA/AMP复合水基吸收液解吸速率对比
在实际的吸收-解吸工程操作中,为了降低整体工艺能耗,需要富液的吸收量尽可能高。而相同吸收液在CO2负荷量不同时其单位解吸能耗差距较大。随着解吸过程的进行,吸收液负荷量不断降低,而解吸出单位质量CO2所需的能耗持续增高。因此,在解吸工段通常会保留一定量的吸收液负荷,以降低整体工艺能耗。因此,着重考察吸收-解吸过程的前、中间段的吸收液表现。10% AMP+10% TETA配比的复配溶液吸收速率与具有最高吸收速率的复配溶液基本相似,且其在解吸过程中前半段也有不错的表现,因此该配方为此工艺条件下的最优比,更适用于工业化应用。
2.3 复合吸收液吸收CO2机理
TETA分子结构中有2个伯胺基团、2个仲胺基团,大量的胺基基团为高效CO2捕集提供了足够的潜在作用位点;而AMP分子同时存在1个胺基和1个羟基官能团,为2个分子间通过氢键作用构建氢键网络体系提供了可能。为进一步探究2个分子间的相互作用及连接机制,阐明复合体系捕集CO2的作用机理,采用量子化学理论计算方式进行分析。
量子化学计算以量子力学理论方法为基础,采用多种方法探讨分子的内部结构特征。其主要计算方法包含分子轨道理论和密度泛函理论。其中,密度泛函理论计算速度快、精度高、可计算原子数多,且能将能量定义为体系粒子密度函数关系,在量子化学计算领域具有重要地位,本研究采用密度泛函理论进行模拟计算。
为探究该复配体系的形成机理,对其单体分子的表面静电势进行分析,探究了2种物质间的结合方式以及潜在的CO2反应位点。首先,通过密度泛函理论计算对2种分子的单体进行优化,优化后的构型如图6所示,优化过程选择的基组为b3lyp/6-31G*。优化结果显示,TETA分子一侧的链段出现了一定程度的内曲,而另一侧向外延伸。优化后的TETA与AMP分子单体的体系总能量见表2,可知优化后的TETA与AMP分子单体的体系总能量分别为-11.76×105和-7.42×105kJ/mol,未出现虚频。
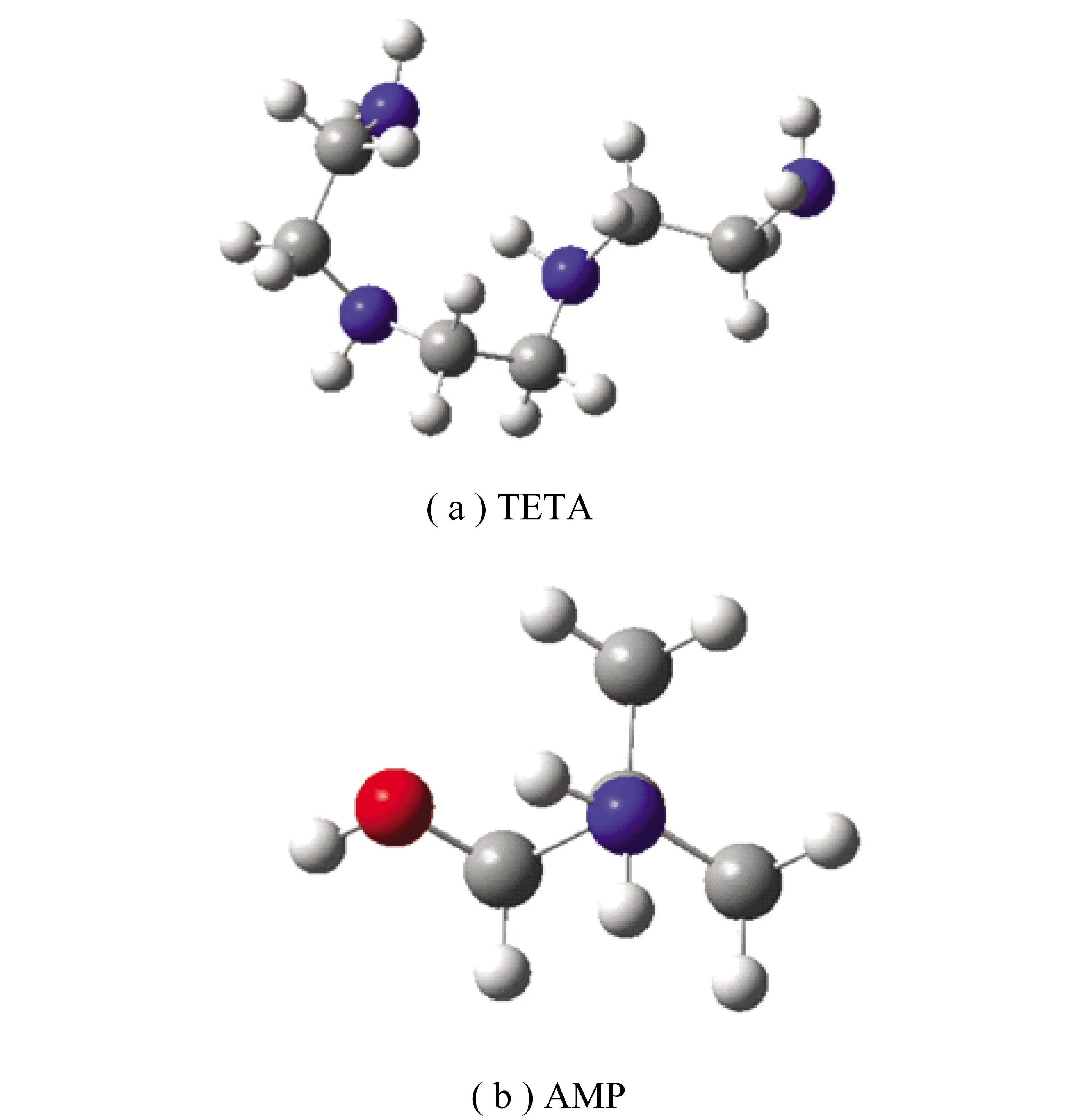
图6 TETA和AMP分子单体优化后的结构
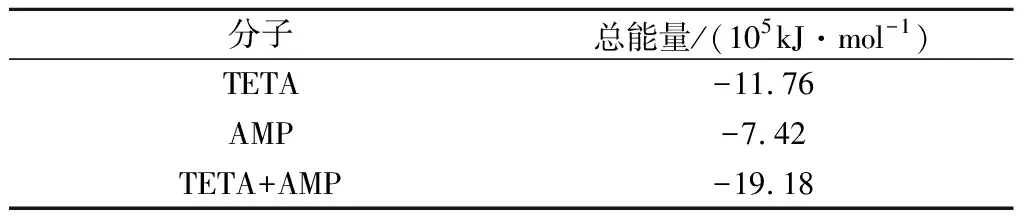
表2 结构优化后的分子体系总能量
在优化后的结构基础上在分子表面利用格点数据产生电子密度为0.001的等值面,从而绘制分子表面静电势等值面,再填入不同颜色实现电子密度可视化区分。其中,红色代表负值,蓝色代表正值。
TETA和AMP分子表面静电势如图7所示,可知TETA分子有4个胺基基团,但具有较强电负性的N原子只出现在分子链段中未内曲的一端,其电负性自内曲的一端向另一端逐渐减弱,内曲一端的N原子电负性最弱。而AMP分子中N原子、O原子均表现出较强的电负性,且羟基末端的H原子处出现较强的正电势,胺基末端的正电势稍弱。这种电势分布为分子间形成氢键网络提供了可能,且TETA中表现出强负电势的点位个数与AMP中表现出强正电势的点位数量比为3∶2,因此,复配体系中单体的组成应为3个AMP分子与2个TETA分子互相连接形成可重复的氢键网络重复单元。值得注意的是,上述试验测试得到的最优复配比例为等质量的TETA与AMP复配,经过换算后的摩尔比约为2∶3,与本节的推测结果一致。

图7 TETA和AMP分子表面静电势
为了探究复配体系设计过程中,引入羟基官能团的必要性,采用密度泛函理论计算方式对复配体系的微观结构进行研究。为明确官能团作用,避免分子之间的相互干扰,在复合体系中只考察一个AMP分子与TETA分子的电子云密度分布。优化后的结构如图8所示,可知两分子的结构无明显改变,其体系总能量为-19.18×105kJ/mol,经计算得到2个分子的络合能约为-65.637 5 kJ/mol。

图8 TETA+AMP优化后的结构
由分子团表面的静电势(图9)可知,AMP分子2个具有明显正电性的位点中,属于羟基的正电性位点同TETA的电子云发生了重叠,且电负性趋于中和。说明在复配体系氢键网络的构建过程中,AMP分子中羟基官能团的作用优先于胺基,更容易与电负性位点形成氢键连接。
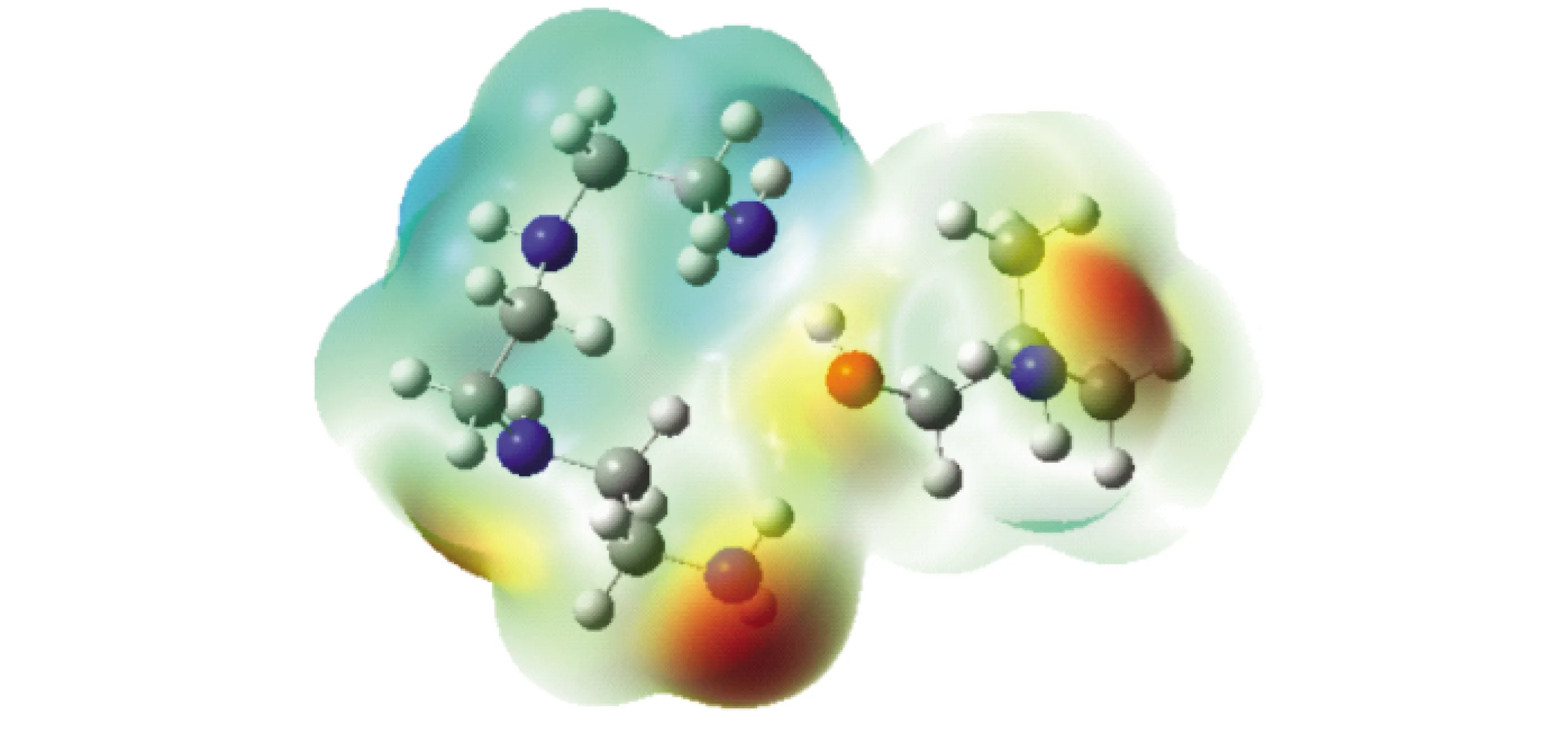
图9 TETA+AMP的表面静电势
3 结 论
1)合成了一系列AMP/TETA复合水基吸收剂用于烟气中CO2吸收。由于TETA含有多个胺基官能团,因此在复合吸收液中主要起增大吸收液载荷的作用;而AMP作为典型的空间位阻胺,其在复合吸收液中主要起降低解吸难度的作用。通过2种物质的复配,将其优点有机结合起来。
2)在复配溶液吸收CO2过程中,具有较快吸收速率的空间位阻胺AMP能快速捕集CO2分子,并将其活化。之后传递给具有较多反应位点的烯基胺TETA,通过快速捕获传递实现整体的大容量吸收过程。而在解吸过程中,空间位阻胺由于其特殊的空间位阻效应,与CO2分子间的连接较弱,导致其极易被从复配溶液中解吸,从而大幅降低解吸难度。
3)通过对不同配比的AMP/TETA复配水基吸收液的吸收-解吸性能测试,优选出最佳配比为10% AMP+10% TETA,为工业化应用奠定了基础。
4)采用密度泛函理论计算方法对复配体系的形成机理进行研究,发现分子表面静电势分布在复配体系形成过程中起重要作用。其静电势表现出较强正/负性的位点即为氢键网络连接点,根据正负位点数对应得到的复配单元组成与实际吸收测试中具有最佳表现的吸收液配比一致。
5)在AMP的2个具有明显正电性的位点中,属于羟基官能团的正电位点更易与TETA相互作用,说明在氢键网络形成过程中,羟基官能团具有优先性,为复配吸收液设计提供了理论指导。
——以高中化学“氢键”的教学为例

