粉煤灰碱熔-水热合成沸石用于水溶液中汞的吸附
燕可翀,李子鹏,李杨敏,王平治
(1.太原城市职业技术学院工程经济系,太原 030027;2.太原理工大学环境科学与工程学院,晋中 030600)
0 引 言
世界卫生组织认为汞是十大危害公众健康的污染物之一。含汞废水的肆意排放会对土壤、沉积物和水体造成不可逆的环境危害,而且若无机汞转变为有机汞,如甲基汞等,其有可能通过食物链富集,进而严重危害到人类健康[1]。基于此,众多科研人员致力于去除水体中的汞。目前,常见的水体除汞技术有吸附、沉淀、共聚、反渗透等,其中吸附法被认为是最为简单易行的方法,故得到了广泛的应用。对于吸附法而言,其关键在于吸附剂的选择。在不同的吸附剂中,活性炭已被广泛应用于去除工业废水中的汞。然而,由于该技术的成本高、制备难、再生难等问题,使得其在大规模吸附系统的应用被限制[2]。
近年来,关于低成本吸附剂制备的研究越来越多。其中,以粉煤灰为原料制备沸石用于吸附废水中重金属污染也有诸多报道[3-5]。粉煤灰作为燃煤电厂产生的固体废弃物,因含有大量的氧化铝和氧化硅,故可用于合成铝硅沸石。目前,粉煤灰合成沸石的主要工艺包括:直接水热法,即直接用碱性溶剂与粉煤灰反应获得沸石;活化-水热法,即对粉煤灰进行机械力活化、碱熔活化等后,再用碱性溶剂与活化粉煤灰反应制得沸石;此外,还包括微波、超声波、模板剂等辅助方法[3-4]。上述方法中特别是以碱熔活化后,再结合水热法合成沸石的转化率最高,得到广泛关注。然而,针对采用该法所合成沸石用于脱除工业废水中汞的研究尚无详尽报道。
本文以粉煤灰为原料,通过碱熔-水热法合成沸石。首先考察了碱熔产物在碱液中的溶解性能及规律;然后利用溶出的铝、硅等,通过水热法合成沸石;对于合成的沸石,进一步考察其对含汞水体中汞的吸附性能和吸附动力学过程。本研究有望为粉煤灰合成沸石用于工业废水中汞的去除提供一定的理论指导。
1 实 验
1.1 实验材料
实验所用粉煤灰取自太原某电厂。经自然晾晒后,在105 ℃下干燥24 h备用。通过X射线荧光光谱分析,粉煤灰原料化学组成(质量分数)见表1,其主要包括氧化铝37%和氧化硅50%,二者质量分数之和可达87%,易合成沸石。

表1 粉煤灰原料的化学组成Table 1 Chemical composition of raw coal fly ash
实验所用其他材料均为分析纯试剂,如碳酸钠、氢氧化钠等;用于配置含汞溶液所用的标液为光谱纯试剂。
1.2 实验过程
(1)粉煤灰合成沸石
将粉煤灰和碳酸钠按照等质量比例加以混合,置于刚玉坩埚内,于程序升温电阻炉内850 ℃下焙烧活化2 h[6];反应样品随炉冷却至室温,粉磨细化后备用,标记为碱熔粉煤灰;将4 mol/L的氢氧化钠溶液(NaOH)与碱熔粉煤灰置于四口烧瓶中,液固比为1∶10,搅拌速度500 r/min,反应温度95 ℃[7];在反应特定时间段内间隔取样,采用电感耦合等离子体发射光谱法测定上清液中硅、铝的含量;根据水热合成沸石的条件[8],添加铝、硅外源,调整SiO2和Al2O3的摩尔比至2,在室温下陈化24 h后,于水热反应釜中100 ℃下晶化8 h,所得产品洗涤干燥研磨后备用。
(2)沸石吸附汞离子
以1 000 mg/mL汞标液为原料,配置初始浓度为10 mg/L汞的模拟废水[9]。吸附实验在恒定室温条件下,连续振动的振动床上进行。向100 mL含汞溶液中添加5 g的粉煤灰基沸石;反应一段时间后,通过真空循环水泵实现固液分离。滤液通过0.45 μm滤膜后,采用电感耦合等离子体发射光谱法测定其中汞的含量。作为对照样品,在没有任何吸收剂的情况下,对配置的含汞模拟废水进行相同的操作,以消除容器壁吸附的影响。所有试验进行三次测量取平均值,以提高准确性、可靠性和再现性。
汞的去除率Rm(%)计算方法如式(1)所示:
(1)
式中:C0和Ce分别表示溶液中汞的初始浓度和平衡浓度,mg/L。
单位质量粉煤灰基沸石的汞吸附量(q)计算方法如下所示:
(2)
(3)
式中:qe为吸附平衡时单位质量粉煤灰基沸石的汞离子量,mg/g;qt为吸附过程中某一时刻单位质量粉煤灰基沸石的汞离子量,mg/g;V为试验溶液体积,L;m为吸附剂重量,g。
1.3 测试表征
利用S8 TIGER型X射线荧光光谱仪(XRF,Bruker,德国),通过硼酸压片法分析粉煤灰样品的化学组成,电压50 kV,电流40 mA,扫描间隔40 s;利用D2 PHASERX射线衍射仪(XRD,Bruker,德国)对粉煤灰、碱熔粉煤灰及沸石进行物相组成分析,Cu Kα靶,电压40 kV,电流40 mA,扫描范围10°~80°,步长为0.02°;电感耦合等离子体原子发射光谱(ICP-AES,Optima-3000 DV系统,Perkinelemer,MA)用于测量溶液中铝、硅、汞的含量,Al、Si、Hg的测定波长分别选定为308.2 nm、251.6 nm和196.164 nm;使用ICP分析软件(Agilent Technologies,CA)通过峰面积积分减去背景计算净强度[9]。
2 结果与讨论
2.1 碱熔预处理粉煤灰
粉煤灰原料的XRD谱如图1所示。粉煤灰中的铝、硅组分主要是以莫来石、石英以及非晶相矿物形式存在。通常情况下,它们的化学反应活性较差,导致沸石合成过程中铝、硅的转化率较低。碱熔预处理可有效激发粉煤灰中铝、硅的反应活性。将粉煤灰和碳酸钠按照等比例质量混合后,在850 ℃下焙烧活化2 h,其XRD谱如图2所示,粉煤灰中莫来石、石英以及非晶相矿物转变为钠铝硅酸盐、硅酸钠和钠霞石等矿物[10]。
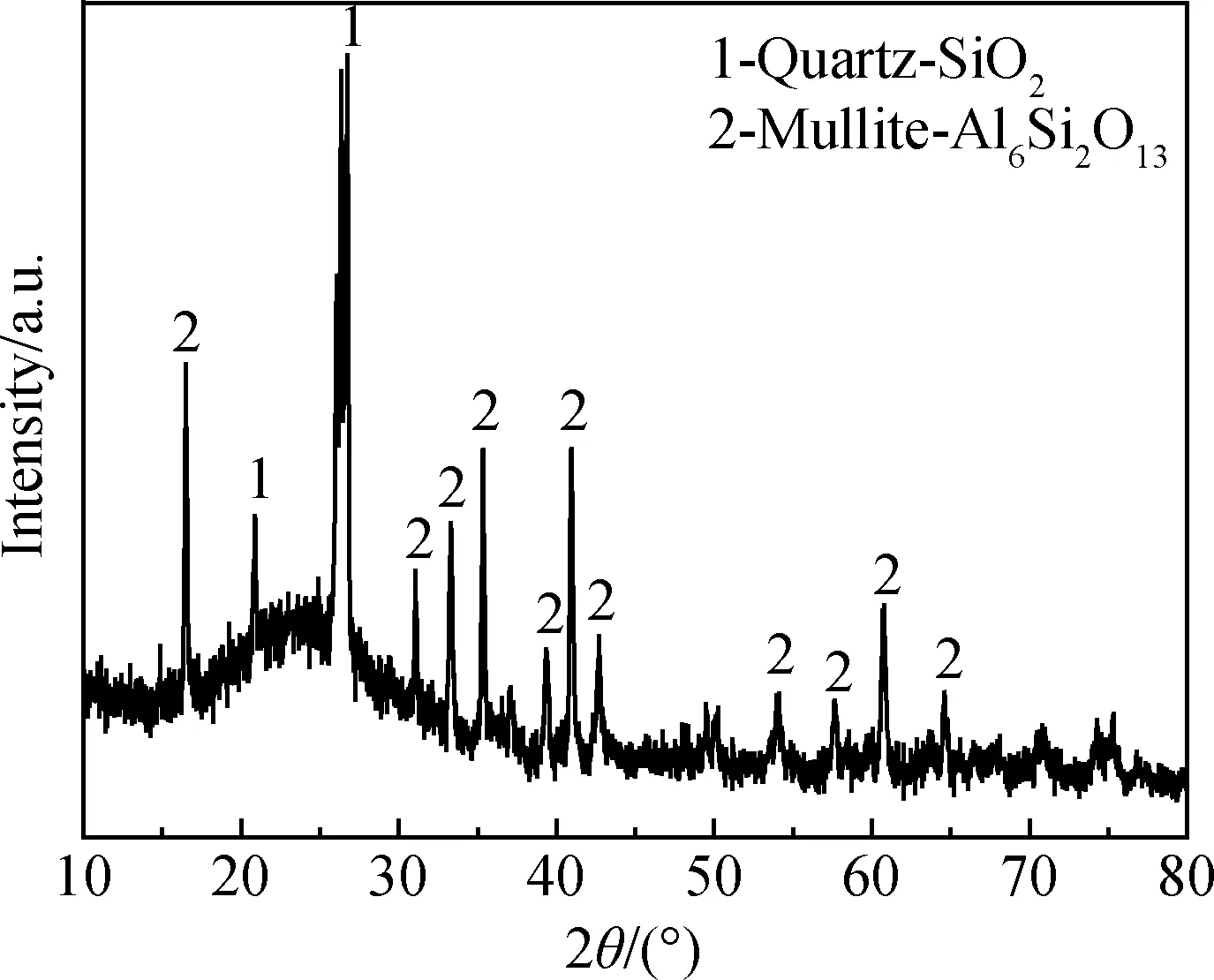
图1 粉煤灰原料的XRD谱Fig.1 XRD pattern of raw coal fly ash
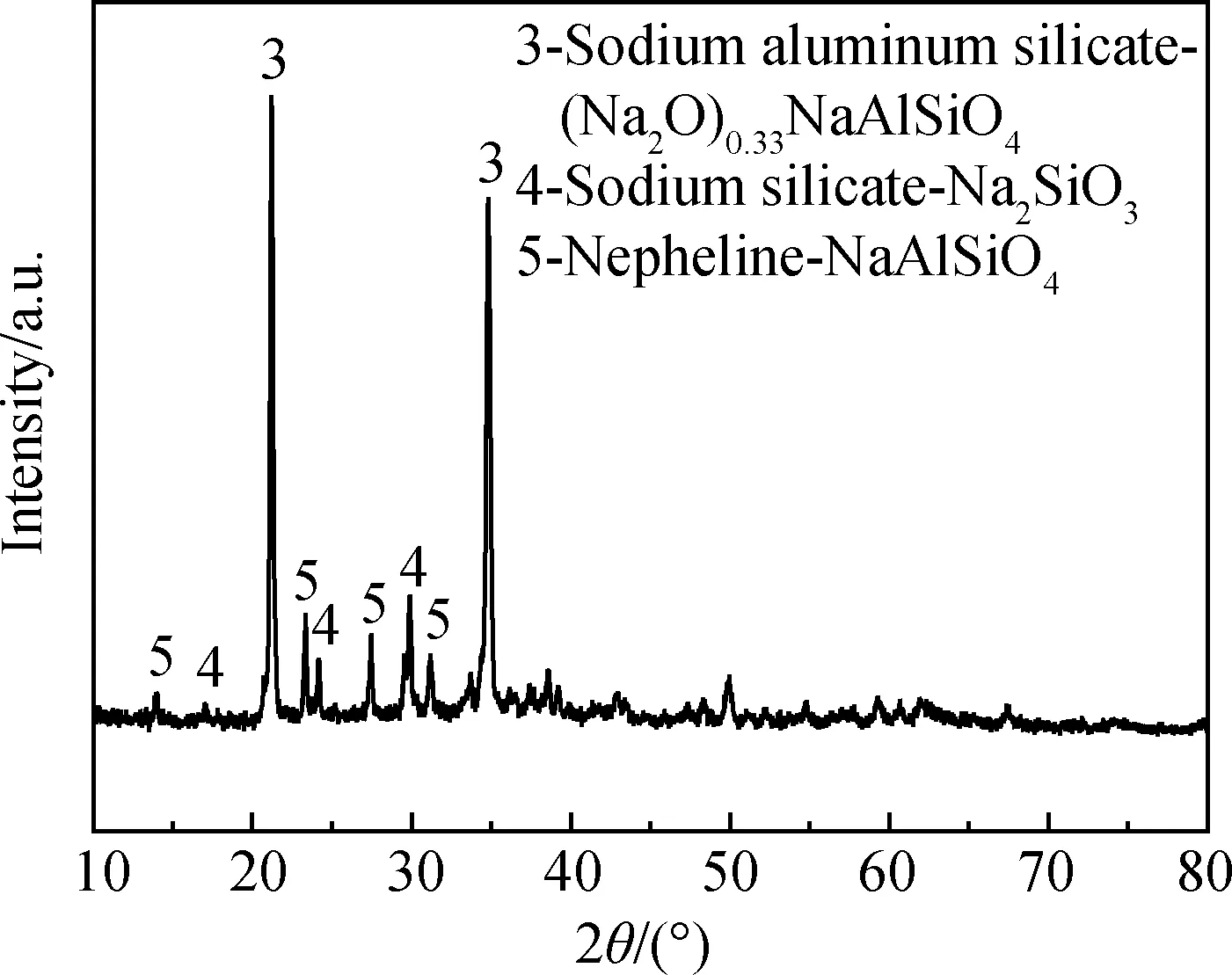
图2 碱熔活化粉煤灰的XRD谱Fig.2 XRD pattern of coal fly ash calcined with alkali
2.2 碱熔活化粉煤灰的溶解
碱熔活化粉煤灰在95 ℃下溶解于4 mol/L的氢氧化钠溶液,溶液中铝离子浓度(CAl)和硅酸根离子浓度(CSi)随时间的变化曲线见图3。从图3中可以看出,随着时间的延长,粉煤灰逐渐溶解,溶液中CAl和CSi相应的升高。反应开始阶段(0~50 min),碱熔活化粉煤灰中铝、硅大量溶出,溶液中CAl和CSi显著提升;当反应时间超过50 min后,铝、硅的溶解速率趋于稳定,反应达到平衡,溶液CAl和CSi不再发生明显变化。碱熔活化粉煤灰在氢氧化钠溶液中溶解平衡时,铝、硅的溶解浓度分别可达10.50 mg/mL和12.78 mg/mL。
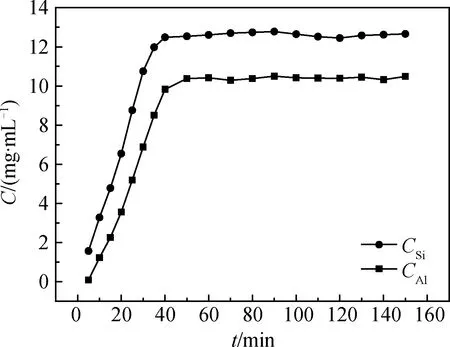
图3 碱熔活化粉煤灰溶解过程中铝离子浓度和硅酸根离子浓度随时间的变化Fig.3 Concentration change of aluminum and silicon during the dissolution of coal fly ash calcined with alkali
2.3 水热合成沸石
在碱熔活化粉煤灰溶解所得溶液中,添加铝、硅外源,调整溶液中SiO2和Al2O3的摩尔比至2;根据水热合成沸石的条件[8],在室温下陈化24 h后,于水热反应釜中100 ℃下晶化8 h制得沸石。图4为碱熔-水热合成粉煤灰基沸石的XRD谱。经XRD分析可知,该法所制得的产物为NaA型分子筛[11];特征峰明显尖锐,说明合成沸石的晶型规则完整。
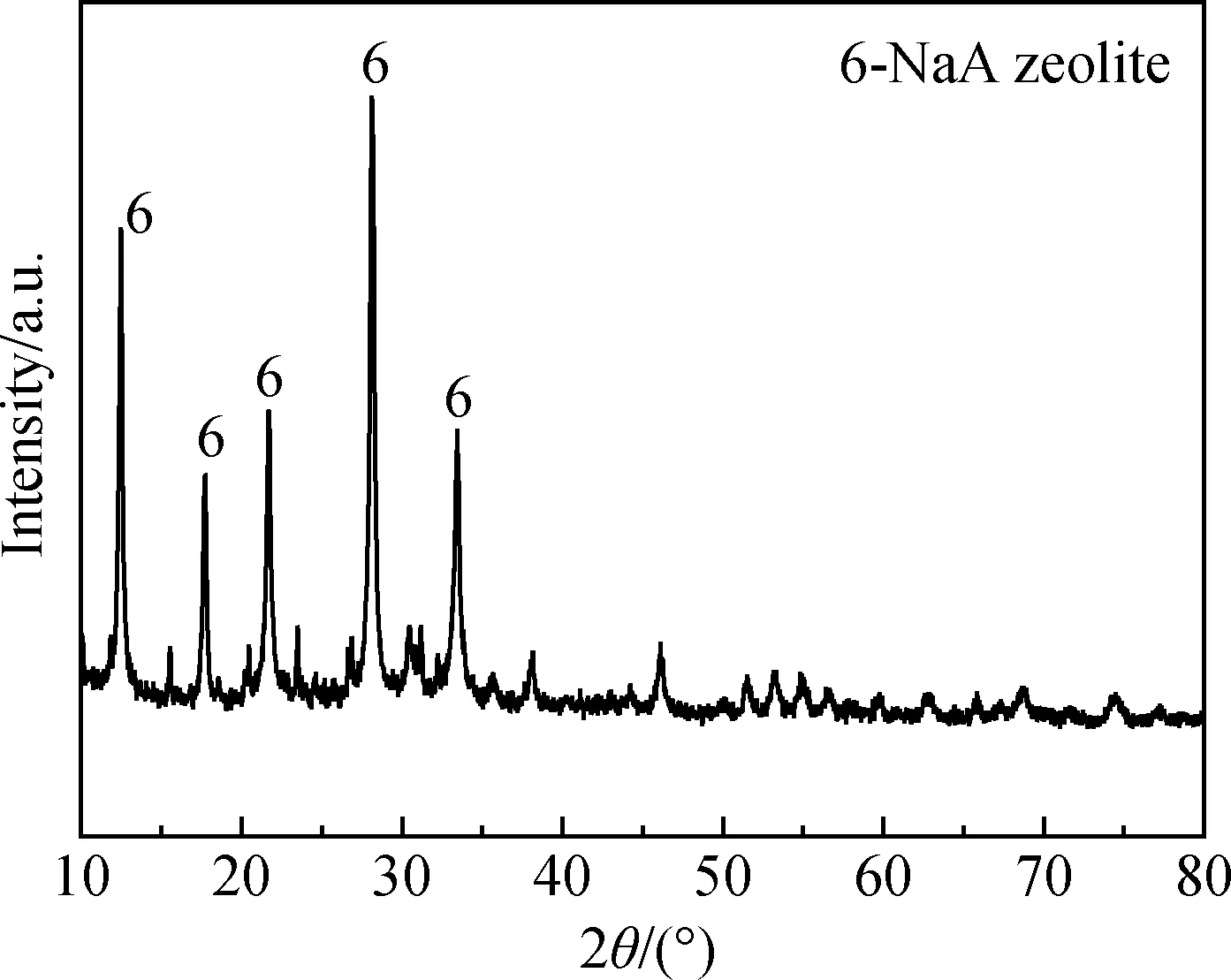
图4 碱熔-水热合成粉煤灰基沸石的XRD谱Fig.4 XRD pattern of zeolite from coal fly ash by alkaline-fusion and hydrothermal method
表2是碱熔-水热合成粉煤灰基沸石经XRF分析所得化学组成结果。从表2可以计算出,产物的分子式为Na1.00Al1.02SiO4.78,沸石产物中NaA型分子筛[12](Na2O·Al2O3·2SiO2·4.5H2O)占总质量的90.32%,是理想的NaA沸石产物。

表2 碱熔-水热合成粉煤灰基沸石的化学组成Table 2 Chemical composition of zeolite from coal fly ash by alkaline-fusion and hydrothermal method
2.4 沸石除汞
以碱熔-水热合成的粉煤灰基沸石为吸附剂,在Hg(II) 10 mg/L、吸附剂50 g/L、pH=2.5、室温条件下,考察其对模拟含汞废水中Hg(II)的吸附能力,结果如图5所示。从图5中可以看出,沸石的初始吸附量较低;随着反应时间延长,吸附能力很快提升至较高水平;在 15 min 左右,模拟废水中Hg(II)的去除率已达92.58%;在15~120 min范围内,Hg(II)的去除率不断提升,增速较缓;在120 min左右,达到吸附平衡, Hg(II)的去除率最高可达95%左右。
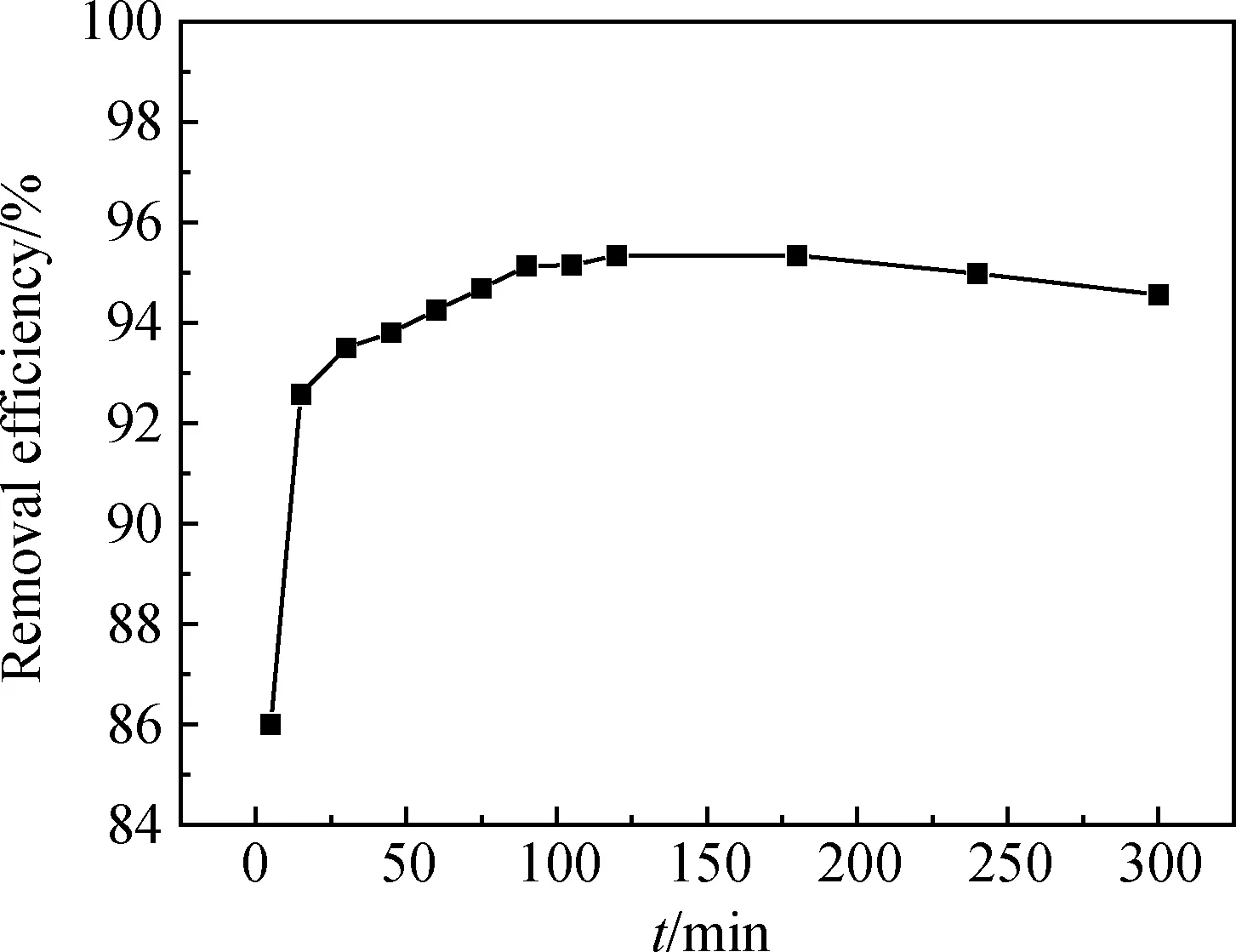
图5 沸石对Hg(II)吸附能力随时间的变化Fig.5 Adsorption capacity of zeolite to Hg(II) as a function of time
以吸附数据为基础,通过比较拟一级动力学模型和拟二级动力学模型的拟合结果,研究碱熔-水热合成粉煤灰基沸石吸附汞(II)的动力学过程[13], 计算结果见表3和图6。拟一级动力学模型采用动力学数据绘制ln(qe-qt)与t的关系图(见图6(a)),实验测得的吸附数据呈现非线性结果,表明Hg(II)在碱熔-水热合成粉煤灰基沸石上的吸附不能使用拟一级动力学模型来描述。相比较而言,根据动力学数据绘制的t/qt值与t的关系图(见图6(b)),则呈现明显的线性关系(R2=0.999 5),表明Hg(II)在碱熔-水热合成粉煤灰基沸石上的吸附更接近于拟二级动力学模型,以化学吸附为主[14]。

表3 拟一级和拟二级吸附动力学拟合参数Table 3 Parameters of pseudo-first-order and pseudo-second-order for the adsorption
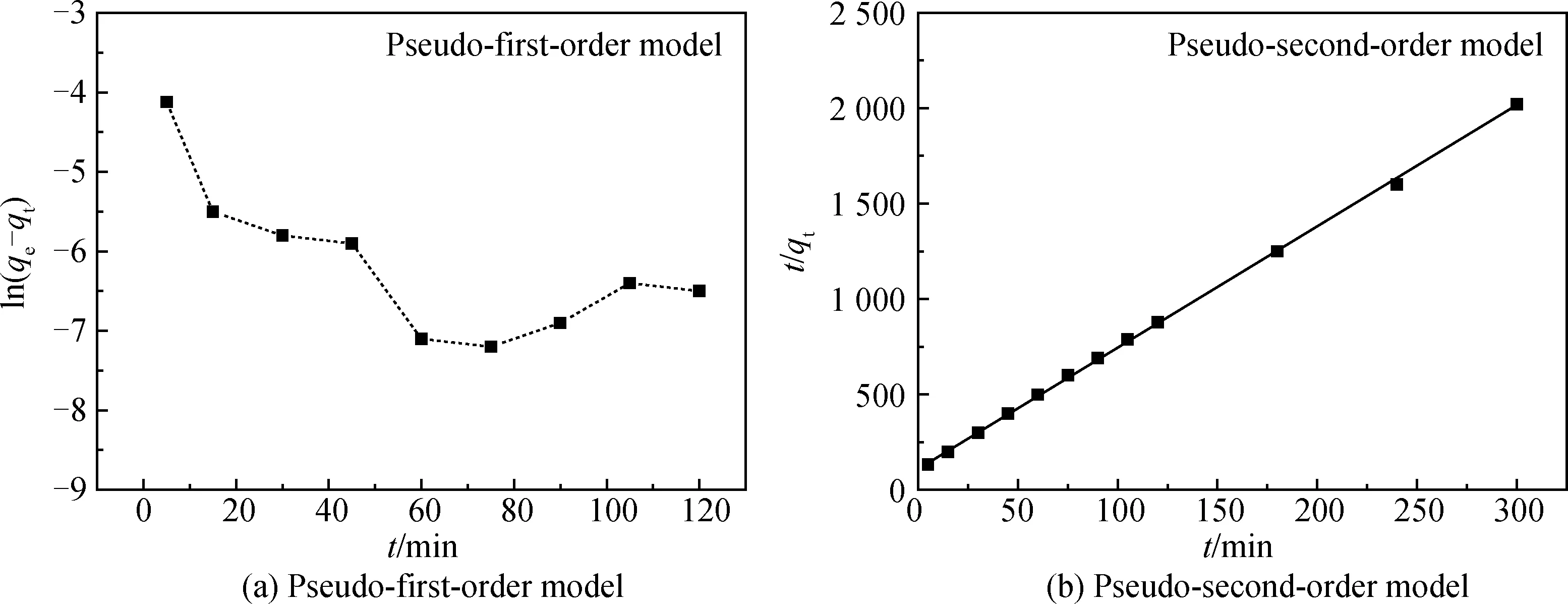
图6 沸石对Hg(II)吸附动力学计算Fig.6 Adsorption kinetic of zeolite to Hg(II) as a function of time
根据经典扩散模型可知,对于Hg(II)在碱熔-水热合成粉煤灰基沸石上的吸附而言,需要经过三个步骤:(1)Hg(II)输送到沸石外表面;(2)沸石外表面吸附Hg(II);(3)Hg(II)在沸石孔道内的迁移和吸附[15]。上述步骤中速度最慢的一步将决定吸附的总速率。颗粒内扩散模型通过绘制t1/2与qt的关系可得,结果见图7。图7的分段线性性质表明吸附过程中存在两个扩散控速步骤,即颗粒内扩散不是唯一的速率限制步骤[15]。图5中Hg(II)从溶液中初始去除速率很高,对应于外部表面吸附或边界层效应;而对于剩余过程,即受到颗粒内扩散控制,直至吸附达到平衡。
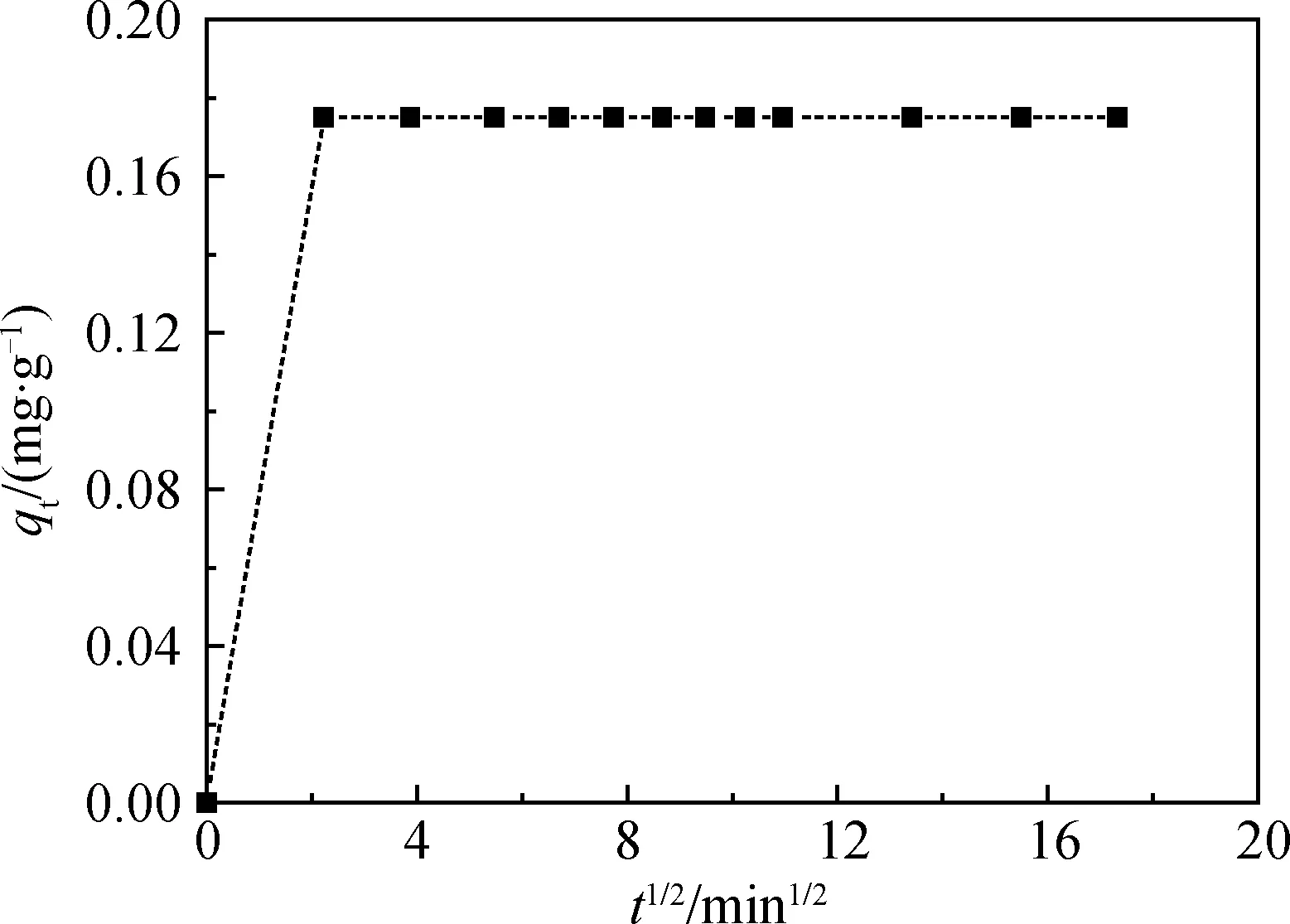
图7 Hg(II)在沸石表面吸附扩散模型计算Fig.7 Application of the diffusion model to the adsorption of zeolite to Hg(II)
3 结 论
(1)碱熔活化可使得粉煤灰中稳定的莫来石、石英及非晶相矿物转变为钠铝硅酸盐、硅酸钠和钠霞石等矿物;这些矿物可溶于氢氧化钠溶液中,形成富含钠、铝、硅的碱性溶液,铝、硅的溶解浓度分别为10.50 mg/mL和12.78 mg/mL;在适宜的水热条件下,富含钠、铝、硅的碱性溶液通过调配铝硅比至2,可合成晶型良好的NaA型沸石,且纯度高达90.32%。
(2)通过碱熔-水热法合成的粉煤灰基沸石可有效吸附水溶液中的Hg(II),去除率可达95%左右,该过程符合拟二级吸附动力学模型(R2=0.999 5),以化学吸附为主;吸附过程中存在两个扩散控速步骤,Hg(II)从溶液中初始去除速率很高,对应于外部表面吸附或边界层效应;而对于剩余过程,则受到颗粒内扩散控制,直至吸附达到平衡。

