泛素化修饰在DNA 损伤修复中的功能研究进展
秦小兵
(武汉大学医学研究院,武汉 430061)
基因组的稳定性时刻遭受到各种各样的损伤威胁,如代谢产物、离子辐射(IR)、紫外线(UV)以及复制错误导致的DNA 损伤[1]。细胞内常见的DNA 损伤类型有DNA 单连断裂、DNA 双链断裂、碱基缺失或错配、DNA-蛋白交联、DNA-DNA 交联等损伤类型。这些DNA 损伤如果不能及时修复,会导致许多疾病的产生,如乳腺癌、卵巢癌、前列腺癌、恶性胶质瘤以及范可尼贫血症等疾病[2]。因此,细胞必须维持基因组的稳定性,为了维持基因组的稳定性,细胞会采取许多措施来修复损伤的DNA。细胞维持基因组稳定性的措施主要有碱基切除修复(BER)、核苷酸切除修复(NER)、同源重组修复(HRR)以及非同源性末端连接(NHEJ)等方式。
在以上DNA 修复过程中,细胞内大量的修复因子参与这些过程,其中许多修复因子在修复过程中会发生翻译后修饰,这些修饰与DNA 损伤修复密切相关,常见的翻译后修饰包括泛素化、甲基化以及乙酰化等。本研究详细阐述了泛素化修饰在DNA 损伤修复过程中的研究现状以及相关进展,从而为相关疾病的治疗和基础研究提供相应的参考和理论依据。
1 泛素化修饰
泛素是一种细胞内普遍存在的由76 个氨基酸组成的小分子,在细胞内可以以游离或者与其他蛋白结合在一起的状态存在[3]。细胞内蛋白质发生泛素化修饰时需要有泛素激活酶(E1)、泛素结合酶(E2)和泛素连接酶(E3)的参与,此外还需要消耗ATP 分子。蛋白质发生泛素化修饰需要3 个步骤:第一步,E1 消耗1 个ATP 分子将泛素连接到自身的半胱氨酸残基上从而将泛素活化;第二步,E1 将活化的泛素分子连接到泛素结合酶E2 上;第三步,泛素结合酶E2 与泛素连接酶E3 结合(图1),从而将泛素分子连接到底物蛋白的赖氨酸残基上[4-6]。泛素分子与底物蛋白的结合方式有多种,目前常见的有K6、K11、K27、K29、K33、K48 和K63 等多种结合方式[7]。

图1 细胞内蛋白质泛素化修饰过程
2 泛素化修饰在碱基切除修复中的作用
泛素化修饰在碱基切除修复(BER)、核苷酸切除修复(NER)、同源重组修复(HRR)以及非同源性末端连接(NHEJ)等修复方式中都扮演着重要角色,下面对泛素化修饰在各种机制中的作用进行讨论。
DNA 复制时会产生大量的DNA 损伤,这些损伤包括碱基错配、缺失等情况,因而碱基切除修复(BER)对于维持基因组稳定性是非常重要的,DNA复制后修复(PRR)能够将DNA 复制过程中产生的大量的DNA 损伤得到修复,从而维持基因组的稳定性。在研究DNA 复制后修复过程中,Rad6(人类细胞中Rad6 对应的蛋白是HR6A∕UBE2A 和HR6B∕UBE2B)是第一个在酵母中发现的与DNA 复制后修复有关的蛋白[8],Rad6 是一个泛素结合酶(E2),它与泛素连接酶Rad18(E3,人类细胞中对应的是RAD18)一起介导PCNA 的单泛素化修饰。当PCNA 的164 赖氨酸发生泛素化之后,它会募集参与DNA 损伤修复的DNA 聚合酶,如DNA 聚合酶η、DNA 聚合酶κ 等蛋白到发生了泛素化修饰的PCNA 上,从而使细胞进行跨损伤合成(TLS)修复途径[9]。而且有报道称,在酵母中Rad5(E3,人类细胞中是SHPRH 和HLTF)会与Ubc13-Mms2(E2)一起介导PCNA 的多泛素化修饰,该修饰会促进染色体的复制,从而使得DNA 损伤能通过复制产生的姐妹染色单体来进行修复,即通过同源重组这条途径来修复损伤的DNA[10](图2)。

图2 泛素化在碱基切除修复中的功能
DNA 在复制或是转录过程中,DNA 的链间会发生一些交联(ICLs),这种交联如果不能得到及时修复,会影响基因的复制和转录等过程,从而引起疾病的发生,这种交联是依赖于碱基切除修复的方式进行修复的。而在范可尼贫血症患者中,由于缺少DNA 交联修复的相关蛋白,因而这些病人的转录和复制过程都会受到影响[2]。目前,发现这些病人中有15 个等位基因会发生突变,这些基因统称为FA,这些基因的产物是在DNA 交联修复的最初3 个步骤中起作用,他们的作用包括链间交联(ICLs)的识别和剪切、跨损伤合成(TLS)以及介导同源重组修复(HRR)[11]。在复制的过程中,当复制叉遇到DNA 交联时,复制叉会停止,进而使得FA 复合体募集到损伤位点。FA 复合体的1 个亚基FANCL 是1个E3 泛素连接酶,该酶可使FANCD2-FANCI 这个复合体发生单泛素化修饰,发生泛素化修饰之后就为后续的修复因子提供了1 个平台[12],而且FANCD2-FANCI 发生泛素化修饰之后可使自身更容易锚定到染色质上并且与其他的一些修复因子结合到一起[13,14],泛素化的FANCD2 会被核酸内切酶FAN1 识别,进而对发生交联损伤的DNA 进行剪切,从而保证受损的DNA 被切除,使得后续DNA 修复过程继续,如同源重组(HR)和跨损伤修复(TLR)等修复方式得以进行(图3)。
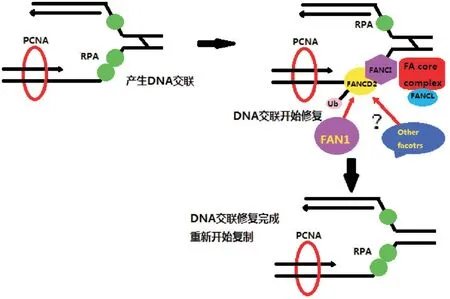
图3 泛素化修饰在DNA 交联修复中的功能
3 泛素化修饰在核苷酸切除修复中的作用
当细胞暴露在紫外线的照射下或其他一些化学药物条件下时,DNA 会产生嘧啶二聚体和环丁烷嘧啶二聚体这2 种常见损伤,此时DNA 损伤需要利用核苷酸切除修复(NER)损伤的DNA。核苷酸切除修复有2 种主要途径:一种是全基因组范围内的修复,这种修复发生在整个基因组中;一种是转录偶联的修复,这种修复方式主要发生在转录的DNA模板链上[15]。
在全基因组碱基切除修复发生的过程中,UVDDB(与UV 引起损伤的DNA 结合非常紧密且特异性很高的结合因子)和XPC-RAD23(全基因组核苷酸切除修复所必须的识别因子)这2 个复合体会检测到DNA 的损伤[10]。该过程首先是当UV-DDB 复合体检测到损伤时,它会募集XPC-RAD23 到损伤位点。而UV-DDB 这个复合体会与CUL4A∕B(一类疏水蛋白家族,可以为E3 泛素连接酶提供支架作用)这个蛋白质形成1 个具有E3 泛素连接酶功能的复合体[15],该复合体使组蛋白发生单泛素化的同时使DDB2 和XPC 发生多泛素化修饰[16]。研究发现,在紫外线损伤DNA 时,泛素化的DDB2 并没有结合DNA 的活性,而且DDB2 的泛素化修饰介导了DDB2 被蛋白酶体的降解[17]。而XPC 发生泛素化修饰后表现出与DNA 结合的活性,特别是当DNA被紫外线损伤之后,结合活性表现出增加的情况,而且XPC 被RAD23(与蛋白酶体发生结合的蛋白)保护而不被降解[18],同时被泛素化的XPC 在DNA损伤位点会募集TFIIH(转录因子2H,核苷酸切除修复因子之一)到损伤位点参与核苷酸切除修复(图4)。
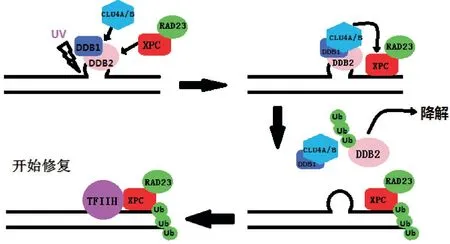
图4 泛素化修饰在全基因组核苷酸切除修复中的功能
在转录偶联的碱基切除修复发生过程中,首先是细胞会激活转录异常引起核苷酸切除修复反应,接着会发生泛素化修饰、RNA 聚合酶2 的降解等事件。转录偶联的碱基切除修复主要依赖于科凯恩综合征蛋白B(CSB,与RNA 聚合酶2 结合的蛋白)。该蛋白除了在碱基切除修复中引起DNA 重塑之外,它还会募集科凯恩综合征蛋白A(CSA)到损伤位点,接着这2 个蛋白和DDB1 与CUL4 一起组成1 个具有E3 泛素连接酶活性的复合体,该复合体形成后会使ATF3 发生泛素化修饰,ATF3 发生泛素化修饰之后,会被蛋白酶体降解,该过程会使RNA 聚合酶2 重新开始转录过程[19,20]。接着在后续招募的蛋白中,有部分蛋白是参与DNA 修复的关键因子,而其中1 个蛋白Rsp5 是E3 泛素连接酶(哺乳动物中是NEDD4),它会与Uba1(E1)、Ubc5(E2)一起介导RNA 聚合酶2 发生K-63 的泛素化从而导致其降解[21],RNA 聚合酶2 降解之后转录终止,DNA 开始后续修复机制(图5)。

图5 泛素化修饰在转录偶联的碱基切除修复中的功能
另外,E3 泛素连接酶RNF8 也是一个在DNA损伤扮演着重要功能的蛋白。有研究指出,RNF8与Ube2S∕Ube2C 介导的组蛋白的K11 位泛素化修饰对于DNA 损伤修复很重要。该泛素化修饰同样是在DNA 损伤发生后,对终止正在转录的RNA 聚合酶2 介导的RNA 转录是必须的[7],这样在DNA损伤位点,细胞就能将RNA 聚合酶2 从损伤位点解离下来,以便于DNA 损伤修复因子参与损伤DNA 的修复。
4 泛素化修饰在DNA 双链断裂修复中的作用
DNA 双链断裂(DSB)是细胞内最严重的DNA损伤,DNA 双链断裂有同源重组修复(HRR)和非同源性末端连接(NHEJ),同源重组修复(HRR)是一种精确的修复机制,而非同源性末端连接(NHEJ)则是一种易错的修复机制。在DNA 双链断裂修复过程中,当细胞检测到DNA 发生损伤时,组蛋白H2AX会 发 生 磷 酸 化 而 形 成γH2AX[22],MDC1 会 识 别γH2AX 并被募集到损伤位点,当MDC1 被募集到损伤位点时,ATM 将MDC1 磷酸化,磷酸化的MDC1会被E3 泛素连接酶RNF8 所识别[23]。接着E3 泛素连接酶RNF168 也被募集到该位点,当RNF8 和RNF168 都被募集到损伤位点后,会引起H2A 发生K13∕K15 泛素化修饰,K13∕K15 泛素化修饰发生之后DNA 双链断裂修复的相关因子,如53BP1、RAD18、BRCA1、RAP80 复合体(也称作BRCA1-A)以及EXPAND(EXPAND 在DNA 修复中的作用可使DNA 处于松散状态)等因子会被募集到DNA 损伤位点[24],当53BP1 被募集到该位点并且被RAD18进行泛素化修饰后,53BP1 与染色质的结合更加紧密,有助于DNA 损伤的修复。紧接着这些因子会参与到DNA 损伤修复,而这些不同因子之间的相互作用会使细胞决定选择使用非同源性末端连接(NHEJ)还是同源重组(HR)来进行修复,如53BP1募集到DNA 损伤位点时会使细胞用非同源性末端连接(NHEJ)进行修复,而当BRCA1 募集到损伤位点时,细胞会倾向于使用同源重组(HR)这条修复途径(图6)。
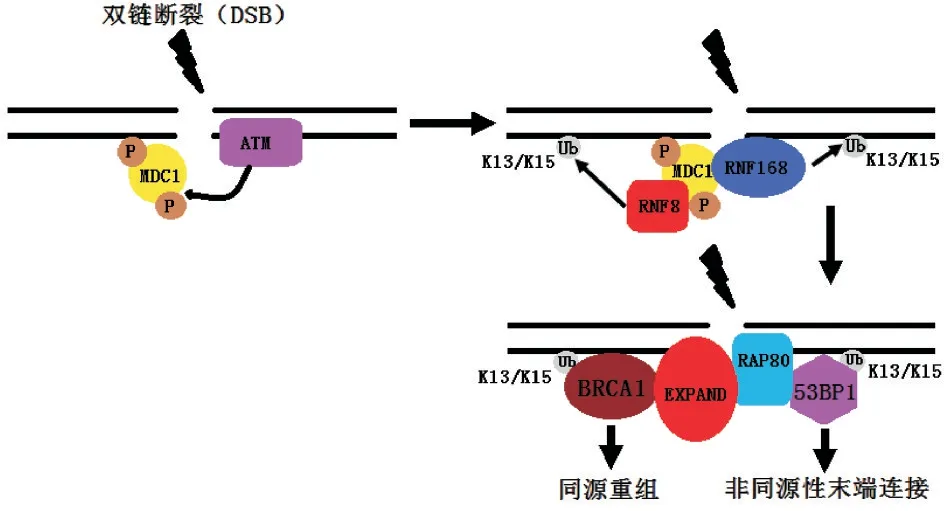
图6 泛素化修饰在DNA 双链断裂修复中的功能(一)
在DNA 双链断裂修复过程中,除了RNF8 和RNF168 这2 个E3 泛素连接酶被募集到损伤位点之外,RNF20 和RNF40 这2 个蛋白也会以ATM 依赖的方式募集到DNA 损伤位点,RNF20 和RNF40会 引 起 组 蛋 白H2B 的K120 泛 素 化 修 饰[25]。当RNF20 和RNF40 引起H2B 的K120 泛素化修饰之后,该修饰会促进染色质的解聚,从而为修复因子提供接近损伤染色质的空间[26,27],这些修复因子包含了参与同源重组修复(HRR)和非同源性末端连接(NHEJ)这2 种修复方式的修复因子[28]。在修复过程中,除了RNF20 和RNF40 会引起H2B K120 的泛素化修饰外,E3 泛素连接酶BMI1∕RING2 在DNA双链断裂位点会依赖于NBS1(MRN 复合体中的蛋白之一)而被募集到损伤位点,该过程接着会引起H2A∕H2AX 的K119 泛 素 化 修 饰,H2A∕H2AX 的K119 泛素化修饰产生之后会使E3 泛素连接酶RNF168 更容易定位到损伤位点,但是RNF168 到该位点之后是否会对BMI1∕RING2 催化产生的泛素化修饰起加强作用并不清晰[29],RNF168 会使组蛋白H2A 的13 位和15 位赖氨酸发生泛素化修饰,此外,RNF168 还会使H2A 发生K63 泛素化修饰,因此,当RNF168 被募集到损伤位点之后会催化H2A产生K63 泛素化修饰,该修饰会帮助RAP80 也被募集到损伤位点,而RAP80 会帮助其他的DNA 损伤修复因子进入损伤位点参与DNA 损伤修复[30](图7)。
此外,BRCA1 在同源重组(HR)修复途径中会和BARD1 形成1 个异源二聚体来泛素化H2A 的127 位和129 位赖氨酸,K127∕129 的泛素化修饰会在同源重组修复过程中促进损伤DNA 的末端进行切割而形成黏性末端[31],从而保证链侵入过程顺利发生,使得损伤的DNA 能够从姐妹染色单体上找到互补序列进行修复。BRCA1 参与修复过程会受到许多机制的调节,Baranes-Bachar 等[32]研究中提到 了UBE4A 这 个E3∕E4 泛 素 连 接 酶,UBE4A 以53BP1 依赖的方式被募集到DNA 双链断裂的位点,接着使组蛋白发生K48 和K63 连接的泛素化修饰,紧接着RAP80 会被募集到发生K63 修饰的这个位点,之后它会募集BRCA1,从而组成BRCA1-A 复合体(包括BRCA1、RAP80、ABRAXAS 和MERIT40等蛋白)。UBE4A 也会帮助BRCA1-A 向BRCC 复合体(包括BRCA1、BRCA2、PALB2、RAD51 等蛋白)转化,当BRCA1-A 转化成BRCC 复合体之后,BRCC 复合体会促进RAD51 在DNA 双链断裂位点的结合,从而使得同源重组修复继续进行[7]。

图7 泛素化修饰在DNA 双链断裂修复中的功能(二)
5 小结与展望
DNA 作为细胞的遗传物质,控制着细胞的每一个生理过程,同时DNA 也是细胞内每个生理过程的基础,如果DNA 发生损伤,对于细胞来说将是致命的。DNA 损伤会造成DNA 的突变,而产生的这些突变会导致机体产生癌症等各种疾病。因而,准确理解DNA 损伤以及DNA 损伤的修复机制对于相关疾病的治疗具有重要的指导意义,目前通过靶向DNA 损伤相关蛋白来治疗疾病的药物已经有部分得以应用。而泛素化修饰在DNA 损伤修复过程中的作用暗示着许多泛素化修饰相关的蛋白可能是潜在的治疗靶点,因此,对近几十年来报道过的DNA 损伤修复过程中起关键作用的泛素化修饰过程和相关蛋白进行总结,可以为相关疾病的治疗和基础研究提供相应的理论依据。

