13例肾上腺畸胎瘤临床诊疗分析并文献复习
杨过 孟庆军 田雨冬 崔林刚 徐鹏超 杨涛
郑州大学第一附属医院泌尿外科 郑州 450052
畸胎瘤是一种来源于全能细胞的生殖细胞肿瘤,常见于睾丸、卵巢,较少发生于纵隔、骶尾部、腹膜后等部位,而肾上腺畸胎瘤(adrenal teratoma,AT)更为罕见[1-2]。国内外文献对于该病的报道较少,多为个案。本研究通过回顾性分析2012-10—2019-03间郑州大学第一附属医院收治的13例AT患者的临床及随访资料,并进行相关文献复习,探讨AT的临床特征及外科诊疗方法,旨在提高对AT的认识。
1 材料与方法
1.1 研究对象选取2012-10—2019-03间就诊于郑州大学第一附属医院术后病理诊断为AT的患者为研究对象。病理诊断皆由我院病理科两位高级职称医生进行独立诊断,排除同时罹患肾上腺外的畸胎瘤者。共13例。
1.2 分析方法(1)收集并详细记录患者病历资料(包括性别、年龄、现病史、既往史、体格检查等),术前实验室检查及影像学检查结果等。(2)记录手术方式、手术时间、肿物的特征,以及术中生命体征、出血量和术后恢复情况。(3)记录大体病理形态及组织病理检查结果。(4)通过电话或门诊复查随访。随访内容包括术后是否行放、化疗和相关内科治疗,症状缓解与否,以及进行内分泌、肿瘤标记物和腹部CT等检查。
1.3 一般资料及术前检查13例患者中位年龄31岁,其中男1例(7.7%)、女12例(92.3%);均为单侧发病,其中左侧8例、右侧5例。3例因腹部不适或胀痛就诊,10例为体检发现。均无高血压、糖尿病病史。所有患者入院后均完善血常规、肝肾功能、电解质、肾上腺相关激素检查,及肿瘤标记物等检查。其中1例上午8时促肾上腺皮质激素(adrenocorticotropic hormone,ACTH)为78.4 pg/dl(正常7.2~63.3 pg/dl),1例下午4时皮质醇为511 g/L(正常64~327(g/L),其余患者未见异常。术前腹部CT显示肿瘤最小为25 mm×20 mm×15 mm,最大为152 mm×103 mm×99.7 mm。2例(15.4%)考虑肾上腺髓样脂肪瘤,11例(84.6%)考虑AT。见图1。
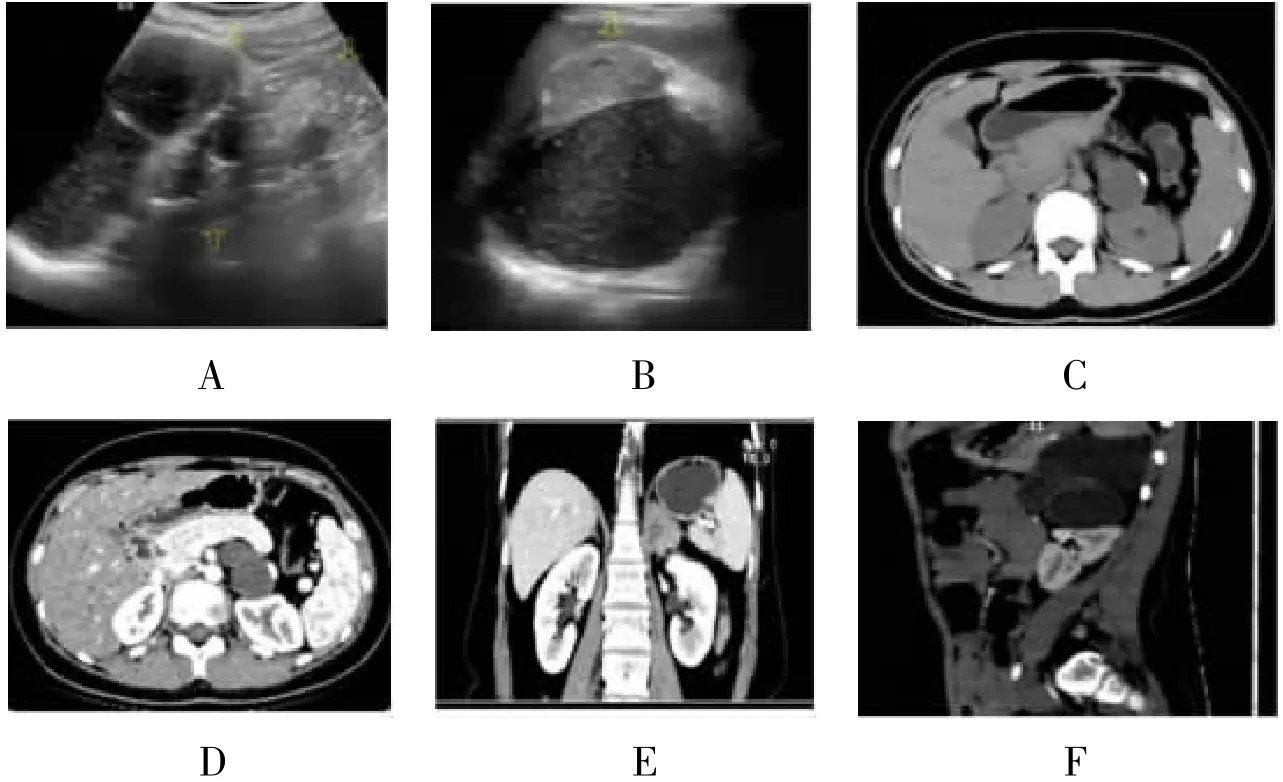
图1 AT的彩超、平扫及增强CT影像图
1.4 手术方法10例行腹腔镜肾上腺切除术(9例经腹腔入路,1例经腹膜后入路),3例行开腹肾上腺切除术。术中见肿瘤与周围脏器粘连,小心分离肿物,可见肿物形状规则,呈卵圆形,质地中等,未见肿物破裂出血及周围浸润。术中均无明显血压波动,出血量少,未予输血。完整切除肿物后术区均留置引流管。
1.5 统计学方法数据采用SPSS 22.0统计学软件进行处理。计量资料以(±s)表示,行t检验;计数资料用n(%)表示,采用χ2检验。P<0.05表示差异有统计学意义。
2 结果
2.1 手术时间等指标腹腔镜组的手术时间、拔除引流管时间、肠胃功能恢复时间及术后住院日均短于开放手术组,术中出血量少于开放手术组,差异有统计学意义(P<0.05)。见表1。所有患者切口均愈合良好,无围手术期并发症。
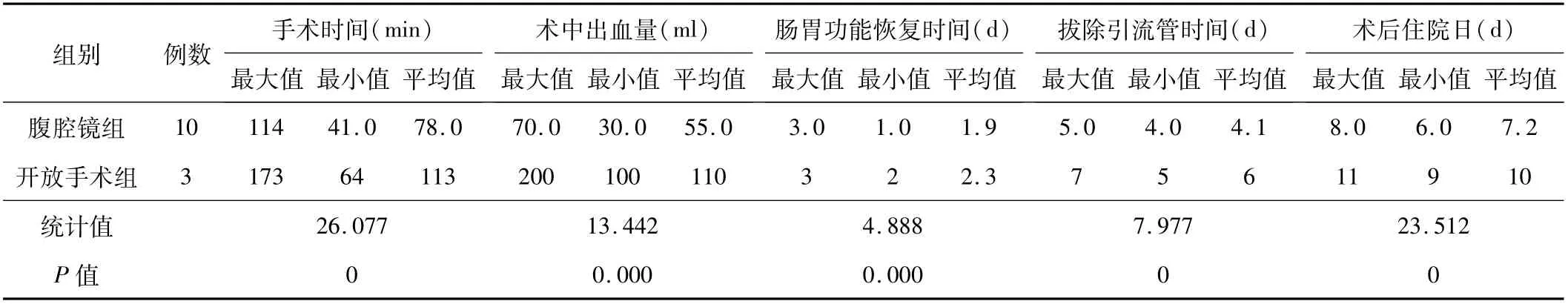
表1 2组患者手术时间等指标比较
2.2 术后病理结果大体病理:标本呈卵圆状,切开后呈囊性,可见淡黄色或褐色黏稠样液体流出,组织间隙可见油脂样物及少量毛发。组织病理:肾上腺成熟性畸胎瘤,其中1例行免疫组化后明确其为肾上腺成熟性畸胎瘤。见图2。免疫组化结果:AE1/AE3[CK(上皮+)],CD56(56C04)×(-),SYN(+),NSE(-)。

图2 AT大体病理及光镜下病理
2.3 临床特征及术后随访13例患者均获5~81个月随访。其间均未行放、化疗及相关内科治疗。其中3例因腹部不适就诊者症状消失,2例ACTH和皮质醇异常者恢复正常。血甲胎蛋白(AFP)、人绒毛膜促性腺激素(HCG)和癌胚抗原(CEA)未见异常。腹部CT均未见复发或癌变。见表2。
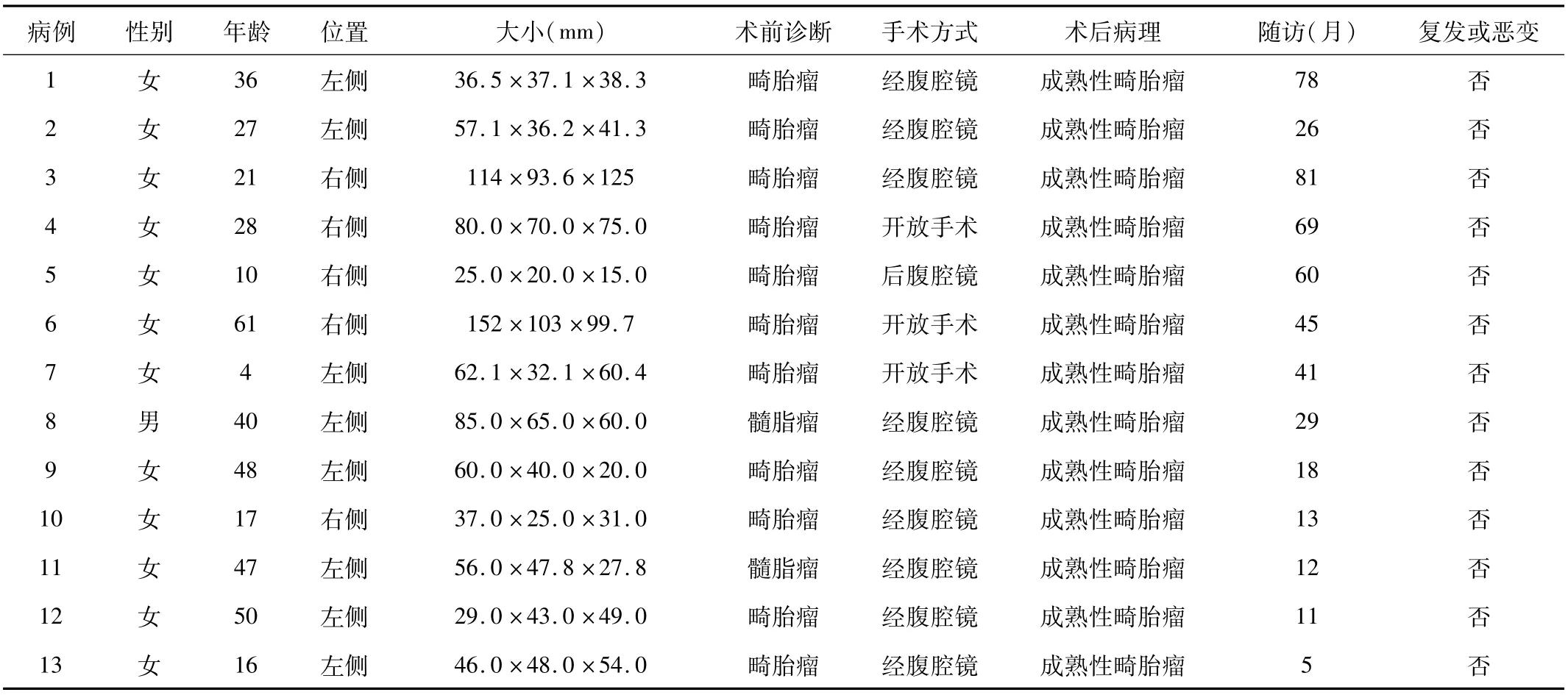
表2 2组患者的临床资料与随访结果
3 讨论
畸胎瘤是一种起源于全能细胞的生殖细胞肿瘤,并具备向不同体细胞多向分化的潜能。常发生于人体的生殖腺内,较少发生于骶尾部、腹膜后等部位,AT更为罕见[1-2]。按分化程度畸胎瘤可分为成熟性畸胎瘤和未成熟性畸胎瘤,成熟性畸胎瘤约占95%,又称为皮样囊肿。囊壁由鳞状上皮、骨组织、毛发及牙齿等构成,囊内可见淡黄色黏稠样液体[3-4]。AT以女性多见,往往单侧发病,至今未见国内外文献报道双侧发病者[5]。其临床症状不典型,多由体检发现,较少因肿瘤较大压迫周围脏器或破裂出血引起腰痛、腹痛等症状[6-7]。本组男性1例,女性12例,全部为单侧成熟性畸胎瘤,仅有3例出现腹部不适等症状,与上述文献相符。
AT无典型临床特征,主要靠超声、CT及MRI检查诊断,并为术前评估及术式选择提供依据。超声多显示为钙化、骨化高回声,以及脂肪、囊性低回声影。CT多见低密度的囊性和脂肪性区域以及高密度钙化,可明确肿瘤的生长部位及与周围脏器的关系,便于手术方式的确定[8]。MRI显示畸胎瘤周围血管及浸润方面有明显优势,多表现为T1和T2加权图像均显示混合信号,其中脂肪含量高[9]。
AT通常表现为无内分泌功能的“偶发瘤”,可行内分泌检查与肾上腺来源的其他肿瘤进行鉴别,如皮质醇增多症、原发性醛固酮增多症以及肾上腺嗜铬细胞瘤。然而AT易与含脂肪成分的其他肾上腺肿瘤相混淆,因此术前仍需影像学检查与以下几种疾病进行鉴别:(1)髓样脂肪瘤:是一种少见的肾上腺肿瘤,多为良性,大部分患者无自觉症状,肾上腺内分泌相关检查均为阴性,CT通常表现为圆形或类圆形的以脂肪密度为主的低密度影,CT值为-150 HU~-40 HU,可呈条索状以及不规则云絮状等,增强扫描通常无强化或轻微强化。如肿瘤合并出血和钙化,则两者鉴别困难,应结合超声、MRI检查信号特点综合分析。(2)肾上腺囊肿:大多无临床症状,体检发现居多。肾上腺内分泌检查多为阴性。CT常提示囊肿壁薄而均匀,增强扫描囊内未见强化。(3)脂肪肉瘤:起病隐匿,发现时肿瘤往往已经很大。CT表现为脂肪密度肿块内包含软组织成分,或软组织成分内包含脂肪密度肿块。(4)腹膜后血管平滑肌脂肪瘤:一般体积较大,CT显示边缘不清晰,其内密度不均匀,含有大量的脂肪和软组织密度影。增强后轻度不均匀强化。(5)神经鞘瘤:大都包膜完整,界线清楚,肿瘤增大时可有坏死、囊性变等。CT显示内部钙化灶往往为散在的斑点样,而畸胎瘤的钙化灶常常为碎片状或是凝固状。
本组患者中,有11例术前CT诊断为AT,2例术前CT诊断与术后病理诊断不相符。可见术前CT并不能完全确诊。有学者认为,CT引导下穿刺活检可用来术前诊断,因有穿刺失败,肿瘤破裂等风险,故有一定局限性。如术前评估能完整切除肿瘤,不建议穿刺活检。但对于术前或其他相关治疗前需要明确诊断的患者,应选择穿刺活检[10-11]。术后病理检查是AT诊断的“金标准”。成熟性畸胎瘤肉眼下多呈囊性,组织间隙可见油脂样物,镜下可见来自三个胚层的成熟组织,如皮肤、皮肤附属器、骨及软骨等。未成熟畸胎瘤肉眼下多呈实性肿块。镜下可见原始神经上皮管等未成熟成分。成熟性畸胎瘤完全由来自三个胚层的成熟组织构成,必须对肿瘤进行充分取材和彻底检查,因为含有未成熟成分会完全改变肿瘤的预后。对普通病理鉴别诊断困难者,可行免疫组化进行鉴别诊断。有学者对3例肾上腺畸胎瘤免疫表型分析,其中2例成熟性畸胎瘤WT-l、Syn、CK、CgA、MyoDl、desmin、CD34血管呈阳性,CD56、S-100、CD99均呈阴性。成熟性畸胎瘤Ki67增殖指数5%,未成熟性畸胎瘤Ki67增殖指数70%[12]。
AT大多数为成熟性畸胎瘤,虽为良性肿瘤,但仍有恶变的可能,而且随着肿瘤的增大可出现周围脏器压迫症状,甚至有破裂出血和感染的可能。因此一经诊断,应尽快手术治疗[13]。腹腔镜手术因具有效果好、切口小、术后恢复快,已成为治疗小于6 cm肾上腺肿瘤的“金标准”[14]。腹腔镜手术有经腹腔和经腹膜后两种入路,根据术者的经验和个人习惯,无明显优劣之分[15]。对大于6 cm的AT,开放手术是切除肿瘤的主要方法。但有学者指出,对肾上腺良性肿瘤,只要术前影像学上或术中无局部侵犯,腹腔镜手术是安全、可行的[5]。长期以来,针对大于6 cm的肾上腺肿瘤,是采用腹腔镜手术还是开放手术,一直存在争议,主要是出于肿瘤控制和手术难度的考虑。近年来,随着医疗技术水平提高,腹腔镜治疗大于6 cm的肾上腺肿瘤已经成为可能[16]。本组有2例大于6 cm的AT患者采用腹腔镜手术,均获良好预后。结合相关文献和我们的体会,AT治疗的关键是完整切除肿瘤,术者可结合患者的具体病情及自身经验,选择合适的手术方式[15]。围术期需特别注意以下几点:(1)由于肿瘤与腹腔脏器、血管关系密切,术前应充分做好胃肠道准备及备血。(2)术中应在不损伤周围脏器的情况下完整切除肿瘤[17]。由于AT往往与肾动脉、肾静脉、肝脏,胰腺及下腔静脉等粘连较重,术中应小心钝性分离。若畸胎瘤表面有明显凹陷,应仔细查看周围有无血管包绕等[18]。若术中发现肿瘤血管丰富或周围浸润,应当考虑恶变的可能,必要时结合术中快速病理检查,适当扩大手术范围[18]。(3)术后及时肌注肾上腺皮质激素,以免出现肾上腺皮质功能不全。本组13例患者术后全部补充肾上腺皮质激素,均未见围手术期及远期并发症。(4)肾上腺成熟性畸胎瘤多为囊性畸胎瘤,术中因粘连易导致囊壁破裂,且术中无法明确其生物学行为。因此应小心分离囊壁周围组织,如有囊壁破裂及内容物流出,建议及时用蒸馏水冲洗术区,以防止肿瘤残留或扩散[4,19]。
有报道称约1.46%成熟性畸胎瘤会发生恶性转归,而肾上腺成熟性囊性畸胎瘤分化程度高,且对于放化疗不敏感,因此术后不必行放化疗,只需定期随访[20]。本组13例均行手术完整切除肿瘤,术后未行放、化疗及相关内科治疗,长期随访未见肿瘤复发或癌变。对未成熟畸胎瘤,其复发及转移率较高,术后仍然需放、化疗并且终身随访[21]。某些未成熟畸胎瘤常伴有AFP、HCG和CEA升高,这些对于术前诊断及预后判断具有重要意义[22]。对肾上腺未成熟性畸胎瘤,应在切除的基础上辅以化疗,目前尚无标准的化疗方案。Leandros等[20]报道了1例采用BEP方案(博来霉素、依托泊苷、顺铂)化疗的案例,术后随访13个月未见复发及转移。Nishioka等[12]认为对于成熟性和未成熟性畸胎瘤的预后和随访都应该详细检查和治疗,且仍需进一步探讨其具体的放疗、化疗方案。
综上所述,AT是一种罕见的生殖细胞来源肿瘤,发病年龄跨度大,临床表现缺乏特异性,术前诊断主要依靠影像学检查,病理检查是确诊的根本依据。完整切除肿瘤是AT治疗的关键。成熟性畸胎瘤切除术后预后良好,因其具有恶性转归风险,术后定期随访是必要的。未成熟畸胎瘤术后易复发,需辅助放、化疗,且终身随访。术后定期复查有利于监测肿瘤复发情况,基于以往研究,AFP水平与畸胎瘤的复发情况具有相关性,其可作为观察疗效的预测指标[11]。然而由于本组案例数量有限,目前的结果并不全面,今后还需要更进一步的研究和长期跟踪随访。

