超声诊断肝细胞肝癌术后5年复发情况的预测指数模型
阿曼·玛克沙提,庄国梅,杨小萍,邹 媛,刘 涛,王淑霞
新疆医科大学健康管理院健康体检部,新疆 乌鲁木齐830011
肝细胞肝癌(HCC)为全球第五大常见恶性肿瘤,目前肝癌根治术以及肝移植术仍是HCC最有效的治疗方法,但肝癌极易侵犯血管导致肝内复发和肝外转移[1-2]。研究表明HCC患者术后1、3、5年累计肝内复发率分别为44.66%、73.79%、89.32%,肝癌术后复发极大影响了肝癌切除术后的远期疗效[3-5],而影响HCC术后复发有诸多因素。甲胎蛋白(AFP)、Child-Pugh分级、肿瘤大小、肿瘤数目、分化程度以及微血管侵犯等均被认为是影响HCC患者术后无病生存时间和总生存时间的独立预测因素[6-8]。但目前还没有一种有效的方法对影响HCC术后复发的危险因素进行全面的评估及预测HCC术后肿瘤复发。彩色多普勒超声具有无创、可重复、实时动态监测等优点,是诊断肝癌以及监测HCC术后复发转移的重要影像学检查,有研究认为肝癌患者术后的肝动脉血流量明显增加及肝动脉比门静脉流量的骤然增加提示肝癌患者术后复发的可能,并且把肝动脉流量大于900 mL/min、肝动脉比门静脉流量大于0.33作为诊断肝癌术后复发的参考值[9]。但是目前还没有研究通过术前多普勒超声影像学表现来全面地评估和预测HCC复发转移的风险。本研究主要应用超声检查观察HCC的声像图特征,了解其与术后复发的关系,在此基础上建立超声诊断预测HCC术后5年复发情况的预测指数(PI)模型,评价超声诊断在预测HCC术后复发中的应用价值。
1 资料与方法
1.1 一般资料
本研究基于新疆医科大学第一附属医院病案信息科的原始资料以及肝癌二级预防的随访数据的临床研究,收集2011~2013年新疆医科大学第一附属医院术前超声科诊断并经术后病理证实为HCC的患者的病例资料共178例。纳入标准:所有患者均为初次确诊肝癌并在我院行肝癌切除术患者;肝功能储备分级为A级或B级;肿瘤≤10 cm;肿瘤数目≤3个;门脉内无癌栓、无肝内肝外转移、无淋巴结转移;病历资料完整。排除标准:肝功能储备分级为C级;严重心肺肝肾功能障碍者;合并有其他恶性肿瘤者;术后大出血死亡、失访、意外死亡的患者。所有患者术后均随访5年,随访终点为术后5年内肝癌复发或转移。178例患者术前行常规超声检查,术后经病理诊断为HCC。其中男性123例(69.1%),女性55例(30.9%),年龄36~65岁(52.7±2.8岁)。全组患者HCC术后1、2、3、5年累计复发率为36.5%、44.3%、55.2%、63.8%,中位复发时间25.8±3.2月。本研究经我院伦理委员会批准,所有患者均知情同意。
1.2 研究方法
1.2.1 仪器与方法 采用GELOGIC9、GES6等彩色超声诊断仪,探头频率3.5~5 MHz,患者取平卧位及左侧卧位,位于肝区进行多切面扫查。记录原发病灶的部位、大小、边界及血供等声像图特征;超声发现复发病灶后,经再次术后病理及腹部CT血管成像等联合确诊[4]。
1.2.2 超声诊断肿瘤部位 依据Couinaud分段法,将肝脏分成5叶、8段,肿瘤位于肝第Ⅱ、Ⅲ、Ⅵ、Ⅶ段者称为外周型;肿瘤位于肝第Ⅰ、Ⅳ、Ⅴ、Ⅷ段者称为中央型,若肿瘤同时位于外周及中央型肝段,则将其归于中央型组[3]。肿瘤大小:单发肿瘤取肿瘤最大横截面直径,多发肿瘤取所有肿瘤最大横截面直径之和。彩色多普勒血流信号分级:参照乳腺癌Adler分级[3],共分为0~Ⅲ级:肿块内无血流为0级;有1~2个点状血流为I级;3~4个点状血流、1~2条血管为Ⅱ级;>4个点状血流或>2条以上血管为Ⅲ级。将上述0~I级定性为少血供型,Ⅱ~Ⅲ级定性为富血供型。
1.2.3 术后超声观察随访 术后1年内每2月复查1次,第2~4年每3月复查1次,第5年每半年复查1次。复查指标包括肝脏超声、AFP、肝功能等。
1.3 统计学方法
采用IBM SPSS19.0软件进行处理,将178例患者的基本资料和超声诊断结果分组,应用Kaplan-Meier生存分析中的寿命表法计算1、2、3、5年累积复发率,采用Log-rank法检验各组间差异,将单因素分析所有指标代入Cox风险回归模型进行多因素分析,采用最大似然比前进法,以P<0.05为差异有统计学意义,得出独立预测因子以及回归系数。根据预测因子以及回归系数建立超声诊断预测HCC术后5年复发情况的PI模型,对PI模型进行有效性检验和多因素校正,绘制PI模型预测此类患者术后5年复发情况的ROC曲线,取约登指数(敏感度+特异度-1)最大时所对应的最佳分界点为界值,结合阳性预测值,阴性预测值和灵敏度、特异度等评价PI模型对HCC术后5年复发情况的预测价值。
2 结果
2.1 Kaplan-Meier和Log-rank单因素分析
Kaplan-Meier 生存分析和Log-rank 检验结果显示,肿瘤边界、肿瘤部位、肿瘤大小、肿瘤数目与HCC术后5年复发情况明显相关(P<0.05,表1),而年龄、性别、肝硬化、肿块回声、肿瘤血供与复发无相关性(P>0.05)。
2.2 多因素Cox回归分析
将单因素分析中的所有指标代入多因素Cox风险回归模型进行分析,校正和控制混杂变量后,筛选出对此类患者术后5年复发情况有显著性影响的独立预测因子有4个:肿瘤边界(β=0.14,OR=1.23)、肿瘤部位(β=0.36,OR=1.58)、肿瘤大小(β=0.59,OR=2.42)、肿瘤数目(β=0.41,OR=1.79)是增加HCC术后5年复发风险的独立危险因素(P<0.05,表2)。
2.3 PI模型的建立以及有效性检验
采用向前逐步回归LR法建立回归模型,经3步回归,肿瘤边界、肿瘤部位、肿瘤大小、肿瘤数目依次被选为预测因子。根据以上预测因子结合β值建立超声诊断预测HCC术后5年复发情况的PI模型:PI=0.14×X1(边界清=0,边界不清=1)+0.36×X2(周围型=0,中央型=1)+0.59×X3(cm)+0.41×X4(单发=0,多发=1),方程中的变量X1、X2、X3、X4分别对应肿瘤边界、肿瘤部位、肿瘤大小、肿瘤数目,PI值范围为0.76~5.42,PI值越大,预测HCC术后5年内复发的风险越大,反之风险越小。模型有效性检验:χ2=12.43,P<0.05。
2.4 PI模型的多因素校正
将PI值代入Cox回归模型进行单因素和多因素分析,多因素校正的指标为所有相关影响因素,在校正相关影响因素后,PI模型成为独立预测因子(β=1.08,OR=2.91),PI值每增加1个单位,此类患者5年内复发的风险将增加1.91倍(P<0.05,表3)。
2.5 PI模型预测价值的验证
PI模型及肿瘤大小预测HCC术后5年复发情况的ROC曲线显示(图1),PI模型的受试者工作特征曲线下面积(AUROC)为0.812(0.765~0.957)(P<0.05),提示预测模型的分类能力达81.2%,预测水平达中等以上,取约登指数最大时(0.883~0.124=0.759)所对应的最佳分界点为界值,界值为1.66,以PI≥1.66作为判断HCC术后5年内复发的标志,PI<1.66作为判断HCC术后5年内未复发的标志。本研究在PI≥1.66的105例患者中有90例5年内复发,可根据PI值正确判断出,阳性预测值为85.7%,灵敏度为79.6%;在PI<1.66的73例患者中有50例5年内未复发,阴性预测值为68.5%,特异度为76.9%,总体准确度为78.7%(表4)。

表1 超声诊断预测HCC术后5年复发情况的Kaplan-Meier单因素分析Tab.1 Kaplan-Meier univariate analysis of ultrasound diagnosis to predict the recurrence of HCC after 5 years

表2 超声诊断预测HCC术后5年复发情况的Cox多因素分析Tab.2 Cox multivariate analysis of ultrasound diagnosis to predict the recurrence of HCC after 5 years

表3 PI模型预测HCC术后5年复发情况的Cox回归分析Tab.3 Cox regression analysis of PI model to predict the recurrence of HCC after 5 years

表4 PI模型预测价值的验证Tab.4 Verification of PI model predictive value
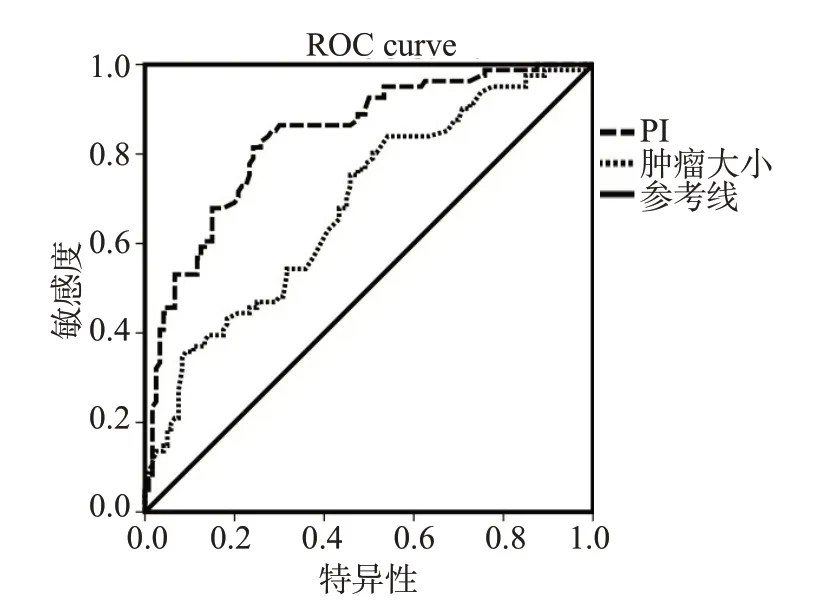
图1 I 模型预测HCC 术后5 年复发情况的ROC曲线Fig.1 The ROC curve of PI model to predict the recurrence of HCC after 5 years.
3 讨论
由于传统超声对于HCC的诊断主要集中于对肿瘤本身的形态学及血流动力学信息进行描述,可以直接或间接反映肿瘤负荷和固有生物学特性[10-11],因此推测某些超声影像学诊断指标可能在预测HCC切除术后复发中具有潜在价值。本研究从超声声像图方面研究与肿瘤术后复发的相关性,可在术前辅助判断患者术后复发的危险性,从而指导临床早期预防HCC术后复发。
既往研究发现位于不同部位的肝癌术后复发率差异显著,外周型明显低于中央型[12-13]。而我们的多因素分析结果也显示中央型肝癌术后复发的风险是周围型肝癌的1.58倍,再次证实了以上结论,其可能原因为,从肝脏解剖的角度,中央型肿瘤距离第一、第二肝门较近,肿瘤周围是重要的、较粗大的门静脉,术中的挤压和损伤易引起癌细胞从门静脉的转移,致使癌瘤于术后短期内复发[14]。
肿瘤大小和肿瘤数目是影响HCC术后复发的主要因素之一[15-16]。一项Logistic多因素分析显示肿瘤直径是预测肝癌微血管侵犯的独立因素,肿瘤直径越大越容易出现微血管侵犯[17];且肿瘤越大复发时间就越早,另有研究发现微血管侵犯、肿瘤最大径≥5 cm、多发性肿瘤是肝癌术后早期复发最主要的原因,因为它们往往提示患者具有较大的肿瘤负荷和较强的肿瘤血管侵袭能力[18]。我们的单因素分析显示,肿瘤直径5~10 cm组以及多发肿瘤组术后各阶段累计复发率显著高于肿瘤直径<5 cm组和单发肿瘤组,多因素分析也提示其为影响肝癌术后复发的独立危险因素,这与既往研究报道一致。
肿瘤形态不规则、边界不清晰,往往提示肿瘤包膜不完整或缺如或肿瘤浸润性生长有研究认为肝癌术后复发影响最大的是肿瘤包膜不完整或缺如,其次为微血管侵犯、病灶大小和病理切缘阳性[19-20]。我们的单因素和多因素分析结果也显示肿瘤边界不清晰术后复发率明显高于形态规则、边界清晰的病变。但用众多的因素评估肝癌术后的复发情况需要一个客观、统一的评估标准,因此基于多因素分析结果我们建立了超声诊断预测HCC术后5年复发情况的PI模型,经多因素校正,PI模型进入最后的回归模型中,也成为独立预测因子,OR值为2.91,复发风险值最大,预测能力最强,且PI值每增加1个单位,此类患者5年内复发的风险将增加1.91倍。以PI=1.66作为作为最佳诊断截点来预测肝癌术后5内复发的灵敏度和特异度分别为79.6%和76.9%,AUROC为0.812,提示此模型具有良好的区分度和诊断效能。因此,相较既往研究得出的单个因子去预测将来某结局事件的发生风险,我们将HCC的各个超声学声像图特征以及它们各自的量化权重均体现于模型中,综合反映了肿瘤负荷以及其生物学特性和侵袭潜能,其预测水平以及预测价值比单个因子更高更强,具有前瞻性。
综上所述,我们的研究首次提出了超声诊断预测肝细胞肝癌术后5年复发情况的PI模型,并结合有效性检验,多因素校正及ROC曲线验证此模型具有良好的区分度和预测价值,为临床HCC术后复发情况的精准评估提供依据。对于被模型判断为术后5年内复发风险极高的患者,临床医生可根据超声提供的资料,采取对应的治疗及措施,安排相应的术后随访的时间、频率,及时早期的发现HCC肝内转移复发,进而提高患者的术后生存率。