壳聚糖基碳量子点的制备、表征及其对过氧化氢的荧光检测研究
满华盛 吕霞敏 黄建颖
(浙江工商大学食品与生物工程学院/浙江省食品安全重点实验室,浙江 杭州 310018)
碳量子点(carbon dots,CDs),也称碳点或碳纳米点,是一类新兴的准球形荧光碳纳米材料。CDs 于2004年由Xu 等[1]在钝化单壁碳纳米管过程中首次发现,由于其具有优良的水溶性,光致发光性,良好的生物相容性和低毒性以及表面功能的可调性而逐渐引起关注[2]。CDs 具有普遍的共性,如紫外荧光特性就是被广泛研究和报道的重要特性之一[3-4]。CDs 在制备过程中因其原料的不同,表面会形成不同的亲水性官能团,如羟基、氨基和羧基等,被认为是造成其独特光学性质的重要原因[5]。此外,CDs 的表面易于修饰,掺杂氮、硫或金属离子都可能会进一步改进其光学特性,甚至增加新的功能[6]。在过去十几年里,CDs 已被广泛应用于传感器[7]方面,而良好的生物相容性和低毒性[8-9]将它与传统的基于过渡金属的量子点和有机染料[10-11]区分开来,非常适用于生物或食品体系。
壳聚糖是自然界中资源丰富且廉价易得的阳离子多糖,有着丰富的氮含量及表面基团,但其难溶于水,在很大程度上限制了自身的应用范围,因此将其应用于高性能氮掺杂CDs 的制备,无疑是制备环境友好型CDs 的极佳选择。另外作为一种氮含量丰富的天然可再生资源,壳聚糖基新型氮掺杂CDs 的制备有助于拓宽CDs 和壳聚糖在各领域的应用范围。
过氧化氢(H2O2)是一种强氧化剂,主要应用于化工、医药和环境等领域[12],同时H2O2在许多国家被用作漂白剂、食品包装抗菌剂和贮存用杀菌剂,如应用于小麦粉、食用油和鸡蛋等。但是,为保障H2O2处理后食品的安全性,H2O2溶液浓度应小于3%[13]。对于食品加工来说,控制H2O2的残留极其重要。目前,已报道多种H2O2的检测方法,如高效液相色谱[14]、分光光度[15-16]、荧光[17-19]、化学发光[20]以及电化学[21-22]法。然而这些方法通常存在分析时间长,维护费用高,非现场检测等缺点,另外在绿色CDs 未被开发关注前,为使绝大多数的CDs 获得更好的性能,会使用有毒有害的反应原料或掺杂具有毒性的金属离子,不利于环境保护,且限制了其在很多方面的应用。H2O2作为生活中常用的氧化消毒剂,具有一定的毒性,尤其在食品当中,若残留超标必然会对人体健康产生不良影响。因此,开发新型准确快速检测H2O2的方法至关重要。本研究采用壳聚糖与DL-酒石酸为反应前体,采用水热法制备新型CDs,并对其进行表征测定,通过荧光响应的手段实现对H2O2的快速检测,以期为高效快速检测食品中的H2O2提供一定的理论依据。
1 材料与方法
1.1 材料与试剂
壳聚糖[Chitosan,CH,脱乙酰度91%,粘度60 mPa·s (1%,20℃)],青岛弘海生物技术有限公司;DL-酒石酸(分析纯)、溴化钾(光谱纯),上海麦克林生物化学有限公司;浓硫酸、30%双氧水、硫酸亚铁、磷酸盐缓冲液(phosphate buffer saline,PBS,pH 值4.0)均为分析纯,国药集团化学试剂有限公司。
1.2 仪器与设备
RCT 型加热磁力搅拌器,德国IKA 公司;TDW 温度控制仪,余姚市长江温度仪表厂;2-16KL 高速冷冻离心机,德国西格玛公司;-80℃超低温冰箱,上海汗诺仪器有限公司;Labconco FreeZone 立式冷冻干燥机,美国LABCONCO 公司;EL 204-IC 电子天平,梅特勒-托利多仪器有限公司;UV-2600 紫外-可见分光光度计,RF-5301 PC 荧光分光光度计,日本SHIMADZU 公司;JEM-1010 透射电子显微镜,日本JEOL 公司;Nicolet Nexus 870 傅里叶变换红外光谱仪,德国Thermo 公司;PHS-3C 型pH 计,上海仪电科学仪器股份有限公司;Smart 系列纯水/超纯水仪,美国默克密理博。
1.3 试验方法
1.3.1 壳聚糖基碳量子点的制备 参照文献[23]的方法并略作改动。准确称取3.9 g 壳聚糖分别溶解于50 mL 0.35 mol·L-1DL-酒石酸溶液中,60℃搅拌至胶状,将混合物放入装有四氟乙烯内衬的不锈钢高压反应釜中,200℃水热处理5 h。自然冷却至室温后,将得到的混合物于10 000 r·min-1离心30 min,上清液用0.22 μm 滤膜过滤,再参照Wen 等[24]的方法并适当修改,在2 L 超纯水中用透析袋(截留率为100~500 Da)透析纯化48 h,所得样品水溶液进行冷冻干燥,得到浅黄色粉末,于干燥器中保存备用。
1.3.2 碳量子点的表征
1)紫外吸收光谱的测定。使用紫外-可见分光光度计测定CDs 溶液的紫外吸收光谱,扫描范围为200~800 nm,每个样品测定3 次。
2)荧光发射光谱的测定。使用荧光分光光度计测定CDs 溶液的荧光发射光谱,激发波长为290 ~360 nm,扫描范围为220~900 nm,狭缝宽度为10.0 nm,每个样品测定3 次。
3) 透射电子显微镜( transmission electron microscope,TEM)测定。使用TEM 观察CDs 的表面形态。
4)傅立叶变化红外光谱(fourier transform infrared spectroscopy,FT-IR)测定。采用KBr 压片法制样,使用红外光谱仪在400~4 000 cm-1的波数范围内进行测定,分辨率为4 cm-1。
5)荧光量子产率(fluorescence quantum yield,QY)测定。以硫酸奎宁(量子产率为0.54)作为标准物质分散于0.1 mol·L-1H2SO4溶液中[24],用来测定所制备CDs 的荧光量子产率。分别记录CDs 溶液和硫酸奎宁的相应吸光度以及在相同激发波长(320 nm)下的发射峰面积。根据公式计算量子产率:

式中,Q 表示QY;Ⅰ表示荧光积分面积;n 表示溶剂的折射率,nCDs为水的折射率(1.33),ns为0.1 mol·L-1H2SO4的折射率(1.33);A 表示相应的吸光度。下标“s”指硫酸奎宁,下标“CDs”指CDs 溶液。
1.3.3 不同浓度铁离子对0.5 mg·mL-1CDs 荧光强度影响以及H2O2标准曲线的绘制 将不同浓度0.5 mL Fe3+溶液添加到4.5 mL CDs 溶液中,使得5 mL 混合溶液中CDs 浓度为0.5 mg·mL-1,Fe3+浓度分别为0、10、15、20、25、30、40、50、60、75、90、130、150、170、200、300…900、1 000 μmol·L-1,测量320 nm 波长处的荧光发射图。再将0.5 mL Fe2+溶液添加到4.0 mL 的CDs 溶液中,然后将提前配制好的不同浓度的H2O2溶液各0.5 mL 分别添加至4.5 mL 上述混合溶液中,至溶液的最终体积为5.0 mL,添加得到的H2O2浓度分别为0、10、15、20、25、30、40、50、60、75、90、130、150、170、200、300…900、1 000 μmol·L-1,其中Fe2+浓度为1 mmol·L-1,CDs 浓度为0.5 mg·mL-1,充分反应一段时间后,在室温下记录320 nm 激发波长下每个混合溶液的荧光发射图谱,根据不同浓度混合溶液的荧光强度绘制CDs 溶液的荧光恢复图谱。以H2O2浓度为横坐标,混合溶液的相对荧光强度作为纵坐标绘制标准曲线。
1.4 数据统计与分析
每组试验进行3 次平行,采用Excel 2010 软件进行数据统计分析,Origin 8.0 软件绘图。
2 结果与分析
2.1 紫外吸收光谱分析
CDs 溶液(0.1 mg·mL-1)的紫外吸收光谱如图1所示。样品水溶液在紫外-可见光谱中的宽吸收峰出现在285 nm 处,该处的吸收峰属于氮掺杂CDs 的特征吸收峰,这是由于存在sp2域(π→π*和n→π*跃迁)[25]。插图为CDs 溶液(1.0 mg·mL-1)在日光和紫外灯波长(365 nm)照射下的光学图片,可以清楚看到,透明的淡黄色CDs 溶液在365 nm 波长的紫外光照射下显示出较强的蓝色荧光,表明其具有良好的光致发光性。
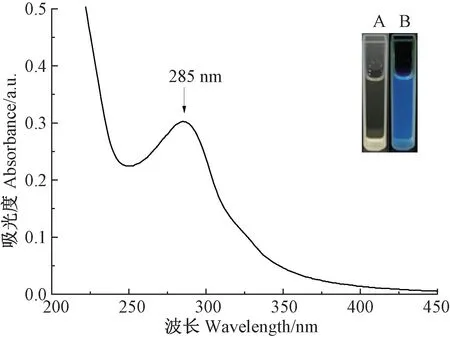
图1 CDs 溶液的紫外吸收光谱Fig.1 UV-vis spectra of CDs in aqueous solutions
2.2 荧光发射图谱分析
由图2 可知,当激发波长介于290 ~320 nm 时,CDs 溶液(0.1 mg·mL-1)的荧光发射强度明显增强,在激发波长为320 nm 时达到最大。由于CDs 具有较为均匀的尺寸,发射波长并未出现明显的蓝移或红移[26]。当激发波长从320 nm 增加到360 nm 时,发射波长随着荧光发射强度的减弱出现红移,说明制备的CDs 具有随激发波长而改变发射峰位置的特性[27]。样品溶液在不同激发波长下的发射光谱证明了其多色发射的特性,这种激发依赖行为可能是因为CDs 在水热碳化过程中表面上形成的羧基和氨基等官能团充当了激发能阱从而导致不同的光致发光特性[28]。
2.3 TEM 分析

图2 CDs 溶液在不同激发波长下的荧光发射光谱Fig.2 Fluorescence emission spectra of CDs solution under the excitations with different wavelengths
TEM 是观察纳米级荧光CDs 形态的重要工具之一。由图3 可知,透析处理所得CDs 的平均粒径约为20 nm,且具有较宽的尺寸分布,大多数CDs 呈现近似圆形或椭圆形,并有少许聚集,这与前人报道一致[28]。

图3 CDs 的透射电子显微镜微观图Fig.3 TEM images of CDs
2.4 傅立叶变化红外光谱分析
为了研究氮掺杂CDs 中存在的官能团,使用FTIR 来表征其结构。由图4 可知,对壳聚糖粉末而言,3 430 cm-1处为胺基的O-H 和N-H 的伸缩振动峰,2 878 cm-1处为C-H 特征峰[23],1 654 cm-1和1 599 cm-1处为壳聚糖(酰胺Ⅰ)谱带的乙酰化氨基[29]。壳聚糖水热处理形成CDs 后,原本3 430 cm-1处胺基的特征吸收峰变为3 380 和3 205 cm-1处的两个峰,而属于C-H 的2 878 cm-1处的吸收峰几乎消失。壳聚糖乙酰化氨基的C =O 伸缩振动峰从1 654 cm-1移至1 719 cm-1处,Sahu 等[30]研究认为是形成羟基和羧基所致,归因于羧酸基团的C =O 伸缩振动,即CDs 的表面存在羧酸基团[31]。在1 600 和1 400 cm-1处的吸收峰为C=C、C-OH 的伸缩振动和C-N 的弯曲振动,与前人报道相一致[32],而1 000 ~1 200 cm-1处的其他尖峰则为C-O 和C-N 伸缩振动以及-OH 弯曲振动。虽然水热碳化的机理有待进一步研究,但从红外光谱图的分析可以进一步证实CDs 中含有羟基、羰基和羧基等官能团,这些功能性亲水基团的存在可以大大改善所制备的荧光CDs 的水溶性及稳定性[33]。另外,CDs 的红外光谱中显示出多个与壳聚糖不同的振动峰,表明壳聚糖经过水热碳化形成了石墨结构。

图4 壳聚糖和CDs 的红外光谱图Fig.4 FT-IR spectra of chitosan and CDs

图5 Fe3+浓度对0.5 mg˙mL-1CDs 溶液荧光强度的影响Fig.5 Effect of Fe3+concentration on fluorescence intensity of 0.5 mg˙mL-1 CDs solution

图6 H2O2 浓度对CDs-Fe2+混合溶液荧光强度(A)和相对荧光强度(B)的影响Fig.6 Effect of H2O2 concentration on fluorescence intensity (A) and relative fluorescence intensity of CDs-Fe2+solution (B)
2.5 荧光量子产率分析
以硫酸奎宁(0.1 mol·L-1H2SO4为溶剂;QY =0.54)为标准物质,测定CDs 溶液和硫酸奎宁溶液相应的吸光度以及在320 nm 激发波长下两者的发射峰面积,根据公式(1)计算得出所制备CDs 的QY 为5.22%。
2.6 不同浓度Fe3+对0.5 mg˙mL-1 CDs 荧光强度的影响以及H2O2 标准曲线的绘制
由图5 可知,Fe3+对于CDs 溶液的荧光有着猝灭作用,当Fe3+浓度到达1 000 μmol·L-1时荧光几乎完全消失。另外,由图6 可知,Fe2+与CDs 溶液混合后荧光依旧较强,当添加不同浓度的H2O2时,CDs-Fe2+混合溶液的荧光发射光谱如图6-A 所示,随着H2O2浓度的增加,CDs-Fe2+混合溶液的荧光强度逐渐降低,当添加的H2O2浓度达到1 000 μmol·L-1时,荧光几乎完全猝灭。研究进一步揭示了CDs-Fe2+混合溶液的荧光强度与H2O2浓度在0 ~60 μmol·L-1范围内具有良好的线性关系(图6-B),可作为标准曲线,回归方程为F/F0=-3.614 4×C(H2O2)+0.995 3,相关系数(R2)约为0.990 0,其中F0和F分别是不存在和存在H2O2时CDs-Fe2+混合溶液在320 nm 激发波长处的荧光强度,根据公式3S/k(其中S 表示标准偏差,k 是线性回归方程的斜率),预估检测限为0.65 μmol·L-1。
3 讨论
本研究以壳聚糖和酒石酸为反应前体,水热处理制备了荧光量子产率为5.22%的新型氮掺杂CDs,经透射电镜测得其粒径约为20 nm,TEM 图中颗粒稳定性较好,并采用傅里叶变换红外光谱等对其进行结构表征,证明形成了石墨烯结构且其表面存在丰富的含氧和氮的功能性官能团,荧光效应较好并能用于检测。
本研究结果表明,Fe3+可以淬灭壳聚糖衍生的氮掺杂CDs 的荧光,而同等浓度Fe2+对其影响不大,由此推断,H2O2将Fe2+氧化为Fe3+,Fe3+与CDs 产生配位,同时它可以转移到Fe3+的空d 轨道,从而导致混合溶液的荧光猝灭,这是一个静态猝灭过程,与前人的报道一致[34]。因此CDs-Fe2+氧化还原型荧光开关传感器可以成为检测H2O2的理想传感器。这种新型荧光传感器,对比已报道的其他方法,如Pradeep 等[35]利用 3,3′,5,5′-四甲基联苯胺( 3,3′,5,5′-tetramethylbenzidine,TMB)与其自制的绿色CDs 混合来检验H2O2,其检测限为35 μmol·L-1,而本研究采用更易获得且环保的Fe2+与CDs 混合,无需昂贵的设备,也不用复杂的操作步骤或苛刻的试验条件,响应范围类似,且检测限更低,灵敏度更高。但本研究制备的荧光传感器偏向于定量监测食品中H2O2或氧化自由基的含量,对于成分定性的研究有待进一步深入。
4 结论
本研究以氮含量丰富的壳聚糖及酒石酸作为反应前体,通过温和的水热处理制备得一种新型氮掺杂CDs,并利用Fe2+和H2O2之间的氧化反应构建了可用于分析H2O2的荧光传感器,可定量检测低浓度下的H2O2,具有易于操作,安全环保,线性范围宽,检测限低,灵敏度高和响应速度快等优点,在食品和生物系统中具有巨大的应用潜力。

